Con el avance en el tratamiento de los diversos tipos de neoplasias malignas pediátricas, la supervivencia de los niños que cursan con este padecimiento es cada vez mayor. Se estima que en nuestro país, en los próximos años, 1 de cada 1,000 habitantes menores de 25 años será un sobreviviente de cáncer. Debido a esto, ha surgido la necesidad de mejorar el cuidado de la salud de esta población. Algunos aspectos para considerar son la vigilancia y el tratamiento oportuno de las alteraciones endocrinológicas. Tanto la neoplasia en sí como la quimioterapia, la radioterapia y los procedimientos ablativos pueden dañar estructuras relacionadas con el sistema endocrino. En estos pacientes son frecuentes las alteraciones del crecimiento por diversos mecanismos, las alteraciones tiroideas primarias o secundarias, las alteraciones de la función sexual y reproductiva, el daño a la salud ósea y el aumento del riesgo cardiovascular. Los efectos secundarios endocrinológicos pueden presentarse a corto plazo o hasta 10 años o más después de concluido el tratamiento. En este trabajo se propone una guía para vigilancia y referencia oportuna al especialista.
Advances in treatment of childhood cancer have increased the rate of cure and survival in these patients. It is believed that in the near future 1/1,000 inhabitants <25 years of age will be a cancer survivor. Because of this, it is necessary to improve health care in this population, with endocrinologic disorders being one of the affected systems needing special attention. Both the neoplasm and its treatment including radiotherapy, chemotherapy and ablative procedures may injure endocrine system-related structures. Growth disorders are frequent in these patients so are primary or secondary thyroid disorders, sexual and reproductive dysfunction, bone health problems and increased cardiovascular risk. Endocrinologic side effects may present in the short term or >10 years after conclusion of treatment. In this paper we propose a guideline for surveillance and timely referral to a specialist for these patients.
1. Introducción
La incidencia anual de cáncer en menores de 14 años es de entre 70 y 160 casos por millón1. En México se documentaron 2,039 casos nuevos de cáncer en este grupo de edad en el 2008 —que corresponde aproximadamente a 64 casos por millón— con el 65% de las neoplasias hematológicas y el 10% del sistema nervioso central2. Es muy probable que esta cifra refleje un subrregistro, ya que en distintos estudios epidemiológicos se ha informado de una alta incidencia de leucemia en población hispánica. En la Ciudad de México se ha registrado una incidencia de 57.6 casos por millón al año tan solo de leucemia3.
La mejoría en el tratamiento del cáncer en la edad pediátrica ha aumentado la sobrevida a largo plazo (del 20% en 1954 al 83% en 2006) a más del 70% en el caso de leucemias linfoblásticas agudas (LLA) y a más del 90% en los linfomas de Hodgkin4. Según esta cifra, en nuestro país se espera que cada año se recuperen y sanen de cáncer más de 1,500 niños. Con esta cifras se estimaría que, en los años siguientes, aproximadamente uno de cada mil habitantes menores de 25 años sería un sobreviviente de una neoplasia maligna en la infancia.
Los niños sobrevivientes de cáncer pueden volver a ser saludables y tener un crecimiento y desarrollo normales. Pero también pueden experimentar efectos tardíos del cáncer o del tratamiento que les permitió sobrevivir. Es por esto que se ha vuelto una necesidad que el médico de primer contacto esté capacitado para identificar los efectos tardíos de la neoplasia y de la quimioterapia, la radioterapia y los procedimientos quirúrgicos a los que fue sometido el paciente durante su tratamiento5.
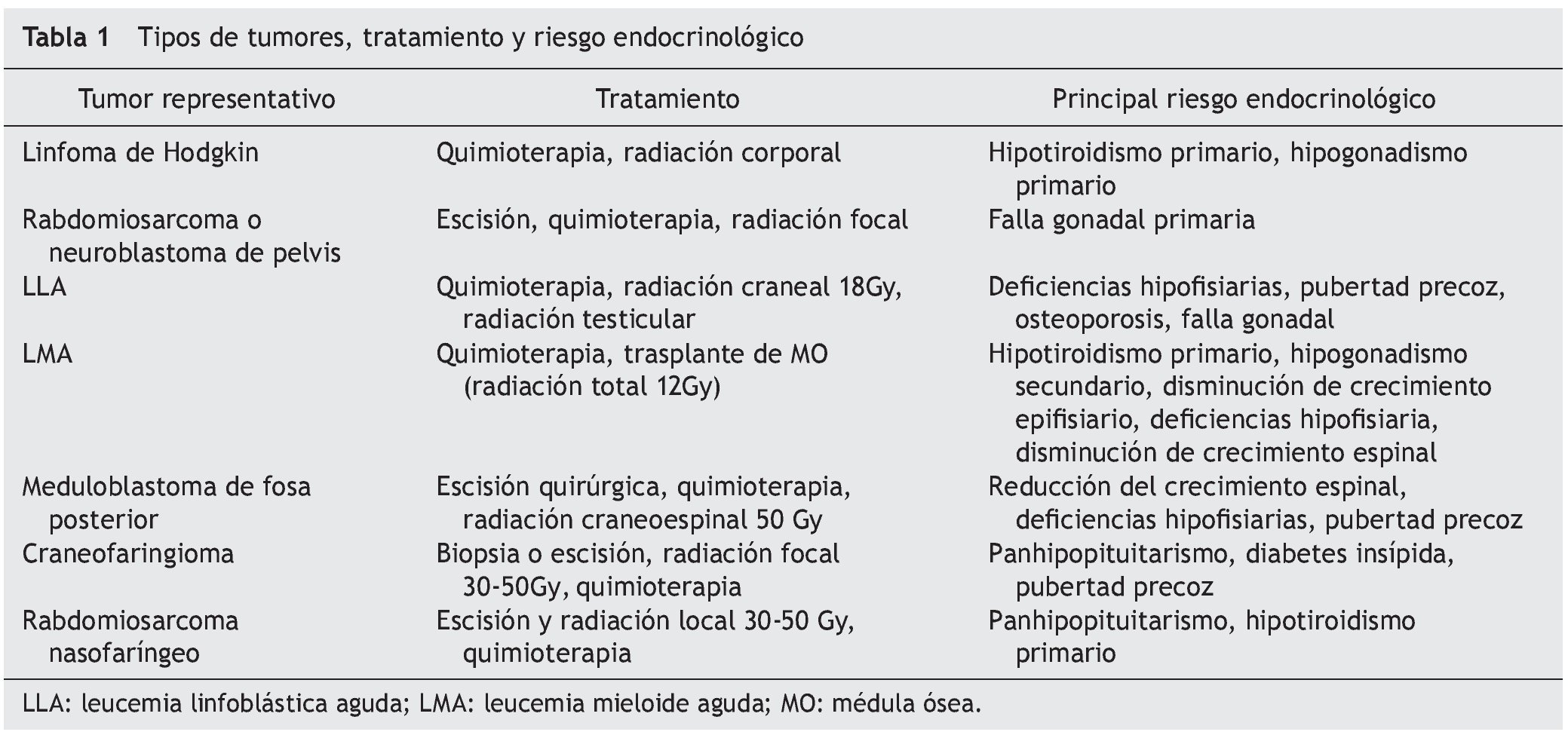
El sistema endócrino es particularmente susceptible de sufrir secuelas a largo plazo después de haberse resuelto el cáncer. El 57% de los sobrevivientes presenta al menos un trastorno endocrinológico y el 23% presenta más de uno. Los pacientes de mayor riesgo son los que han recibido trasplante de células madre hematopoyéticas, debido a las altas dosis de radiación y quimioterapia a las que son sometidos6. Las alteraciones mejor descritas son las hipotálamo-hipofisiarias, las tiroideas y las gonadales. Las afecciones a estas estructuras aunadas al daño multisistémico por el cáncer y su tratamiento predisponen a problemas endocrinológicos, entre los que se encuentran la limitación del crecimiento, las alteraciones de la pubertad, la infertilidad , el hipotiroidismo y neoplasias tiroideas, el aumento de factores de riesgo cardiometabólicos y la disminución de la densidad mineral ósea (tabla 1). El pediatra debe vigilar y monitorizar el desarrollo de nuevas endocrinopatías, esperadas e inesperadas, durante los 10 a 15 años siguientes, o incluso más, después de terminado el tratamiento antineoplásico7,8.
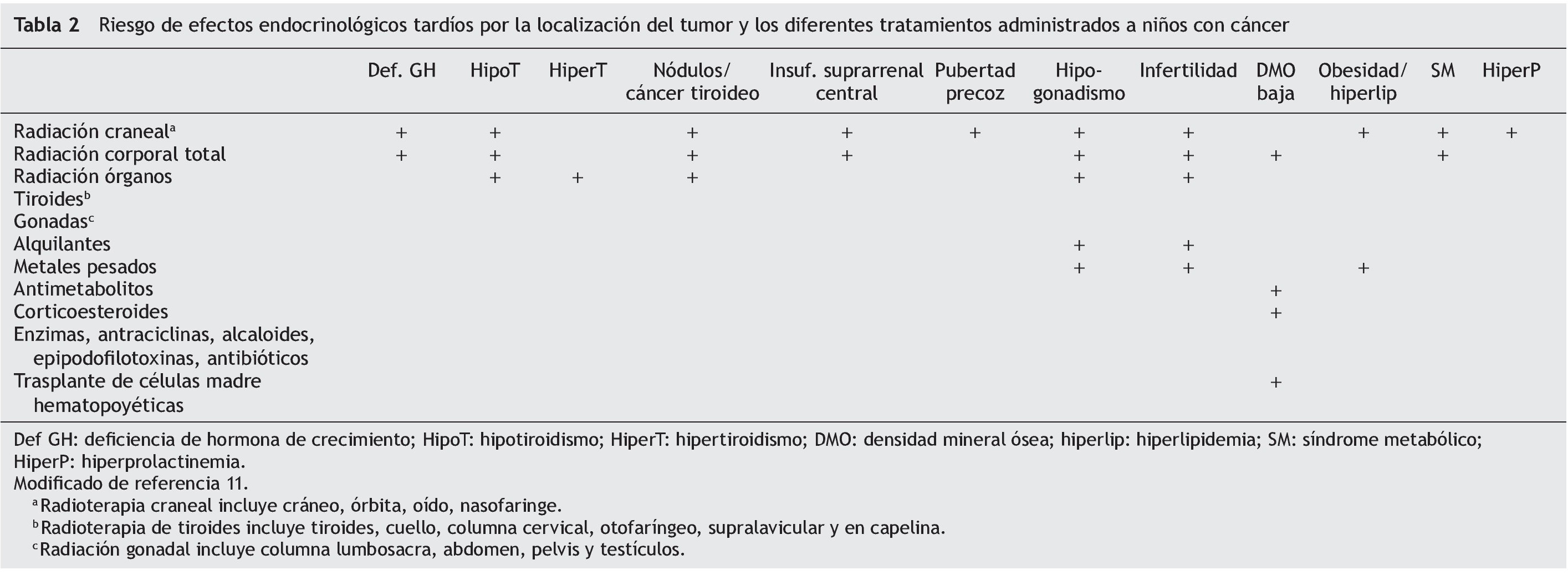
El riesgo de efectos endocrinológicos tardíos particulares depende de la localización del tumor y de las modalidades terapéuticas que se utilizaron (tabla 2). Por otra parte, tanto el tumor como los procedimientos quirúrgicos pueden requerir la resección o la lesión de estructuras fundamentales para el funcionamiento endócrino.
2. Radioterapia
El impacto de la radioterapia depende del campo involucrado, de la dosis total, del esquema de administración y de la edad del paciente al recibirla. Como regla general, cualquier estructura dentro del campo radiado puede sufrir alteraciones en su función. Por ejemplo, la radiación por linfoma de Hodgkin afecta directamente la función de la tiroides y de las gónadas si se aplicó en cuello o en abdomen, respectivamente. La radiación craneoespinal para el meduloblastoma afecta la función del hipotálamo, la tiroides y el crecimiento vertebral. Además, existe una relación bien establecida entre la dosis de radioterapia craneal y el desarrollo de deficiencia de hormonas hipofisiarias. El eje de hormona de crecimiento (GH) es el más sensible, llegando a lesionarse con dosis desde 18 Gy, seguido por el eje de gonadotropinas, el de tirotropina y, por último, el de corticotropina9.
3. Quimioterapia
Los agentes alquilantes y los metales pesados causan disfunción gonadal femenina y masculina relacionada con la dosis. El busulfán, la procarbazina y la mecloretamina son particularmente gonadotóxicos. La ciclofosfamida es uno de los agentes alquilantes más frecuentemente utilizados. Los pacientes que recibieron dosis mayores de 7.5 g/m2 presentan el mayor riesgo de toxicidad gonadal. Al igual que con la radioterapia, las células germinales se lesionan a dosis más bajas que las de Leydig. Además, la combinación de quimioterapia con radioterapia aumenta el riesgo. La disfunción gonadal en mujeres por el uso de alquilantes puede resultar en pubertad retrasada o detenida, menopausia prematura o infertilidad.
4. Crecimiento en sobrevivientes de cáncer
Se espera que la velocidad de crecimiento disminuya durante el trascurso de una enfermedad activa moderada o grave como es el cáncer. Lo óptimo resulta cuando, al resolverse esta, exista un crecimiento de recuperación que lleve al paciente de regreso a su carril de crecimiento familiar para que pueda alcanzar su potencial genético de estatura. Existen múltiples factores que limitan este crecimiento en un niño que ha padecido cáncer. Está, en primer lugar, la falta de ganancia de talla ocasionada por el déficit nutricional, por el estado inflamatorio, por la afección psicológica generada por la neoplasia en sí y por las enfermedades intercurrentes; su magnitud puede ser tal que ya no sea recuperable. En segundo lugar se encuentran los efectos tóxicos de la quimioterapia y de la radiación en hueso. Por último, se encuentra el daño en las glándulas secretoras de hormonas directamente involucradas con el crecimiento.
4.1. Disminución del crecimiento por efectos directos en el hueso
La radiación a las placas epifisiarias limita el crecimiento óseo. La radioterapia al neuroeje causa disminución del crecimiento vertebral y, por tanto, un segmento superior desproporcionadamente corto, mientras que los pacientes sometidos a radiación corporal total, como los receptores de trasplante de médula ósea, pueden sufrir daño generalizado a los centros de crecimiento.
En cuanto a la quimioterapia, se ha observado que el metotrexato a altas dosis lesiona la placa de crecimiento ocasionando una disminución en el crecimiento longitudinal de los huesos largos10.
Los glucocorticoides, por su parte, disminuyen la producción de IGF-1 e inducen resistencia a esta hormona en la placa de crecimiento. Además, disminuyen el péptido natriurético tipo C, lo cual resulta en la reducción de la proliferación e hipertrofia de condrocitos, de la síntesis de matriz, y como consecuencia un crecimiento lineal disminuido. Estos fenómenos afectan directamente al hueso, independientemente de la inhibición de la secreción de GH y gonadotropinas por estos fármacos11.
4.2. Disminución del crecimiento por efectos directos en glándulas endocrinas
La deficiencia de GH es el problema endocrinológico más frecuente que ocurre después de la radioterapia de cráneo. Se recomienda que se vigile el crecimiento de los pacientes que recibieron esta modalidad de tratamiento cada seis meses11 y, en caso de detectar talla baja o velocidad de crecimiento por debajo del percentil 10 para la edad y sexo, se deben realizar pruebas específicas para identificar deficiencia de GH, además de excluir otras condicionantes hormonales y sistémicas de crecimiento disminuido. Siempre que se detecte una deficiencia de GH o de alguna otra hormona hipofisiaria, es necesario valorar la suficiencia del resto de los ejes endocrinos.
El hipotiroidismo en conjunto (primario, secundario y terciario) es tan frecuente o más que la deficiencia de GH y por sí solo puede condicionar una limitación del crecimiento.
En cuanto a la función gonadal, la producción insuficiente de hormonas sexuales (andrógenos y estrógenos) causa, además del retraso o falta de desarrollo de caracteres sexuales, una falta de la aceleración puberal del crecimiento, lo que resulta en un déficit de talla aún más notorio a partir de la segunda década de la vida. Por otro lado, la pubertad adelantada, que también puede ocurrir como resultado de una neoplasia o intervención intracraneal, causa cierre temprano de las placas epifisiarias y una talla final menor a la esperada por su potencial genético.
4.2.1. La tiroides en sobrevivientes de cáncer
La radiación al cuello con más de 10 Gy puede inducir hipotiroidismo o, muy raramente, hipertiroidismo. Dosis mayores de 25 Gy predisponen al desarrollo de nódulos tiroideos. El riesgo de cáncer aumenta progresivamente hasta la dosis de 30 Gy, a partir de la cual disminuye con dosis más altas12.
4.2.1.1. Hipotiroidismo
Se estima que el 24% de los sobrevivientes de cáncer presentan alteraciones tiroideas asociadas principalmente con radiación, ya sea de cuello o cráneo. Los pacientes sometidos a radiación corporal total tienen una prevalencia de hipotiroidismo de cualquier tipo de hasta el 34%13-16. El hipotiroidismo primario por daño directo a la tiroides es frecuente después de recibir radioterapia para un linfoma de Hodgkin o un carcinoma nasofaríngeo. La tiroides suele ser pequeña y aumentada de consistencia, con niveles elevados de hormona estimulante de tiroides (TSH) y bajos de tiroxina libre17 (T4L). El antecedente de radioterapia de cuello aumenta 17 veces el riesgo de hipotiroidismo primario respecto de la población general18. La prevalencia aumenta con el tiempo, por lo que es necesario revisar periódicamente las pruebas de función tiroidea en los sobrevivientes que han recibido radioterapia de cuello, aunque hayan pasado muchos años desde este evento19.
Hipotiroidismo primario. El hipotiroidismo primario subclínico se define con niveles de T4L normales y TSH levemente elevada. Si bien el manejo de esta condición es controversial, se ha observado que los pacientes con este perfil que han recibido radioterapia de cuello y tienen limitación del crecimiento, mejoran la velocidad de este, el perfil de lípidos y el vigor si reciben tratamiento sustitutivo con hormona tiroidea para llevar las concentraciones de TSH a 1-2 mU/l20,21.
Hipotiroidismo secundario. El hipotiroidismo secundario, o por daño a los tirotropos hipofisiarios, puede ocurrir después de recibir radiación craneal. Puesto que en esta forma de hipotiroidismo no ocurre elevación de los niveles de TSH —que es un marcador muy sensible de insuficiencia sutil de hormonas tiroideas—, el diagnóstico bioquímico de certeza se hace hasta que la T4L se encuentra por debajo de los valores de referencia, sin una elevación concomitante de TSH. Sin embargo, los pacientes con deficiencia parcial de TSH pueden cursar con niveles de T4L en el tercio inferior del rango de referencia, lo que puede retrasar el diagnóstico de hipotiroidismo secundario. Este retardo en el diagnóstico pude ser trivial para un adulto, pero para un niño puede significar pérdida de oportunidad de crecimiento y, potencialmente, implicaciones funcionales. La deficiencia leve de TSH puede preceder a la aparición de otras deficiencias hipotálamo-hipofisiarias y se puede detectar con una prueba de estimulación con hormona liberadora de tirotropina (TRH) antes de que haya evidencia manifiesta clínica o bioquímica de otro tipo.
Hipotiroidismo terciario. El hipotiroidismo terciario ocurre por lesión hipotalámica. Es difícil diferenciarlo de un hipotiroidismo secundario, y frecuentemente coexisten. Bioquímicamente puede presentarse con el mismo perfil tiroideo que el hipotiroidismo secundario, o bien puede observarse una concentración de TSH ligeramente elevada que, sin embargo, posee bioactividad disminuida por patrones alterados de glucosilación. Es posible diagnosticarla con una prueba de estimulación con TRH en la que se observa buena respuesta de TSH aunque, por lo general, no es necesario ni práctico hacer el diagnóstico diferencial.
Por último, es posible que un paciente que ha recibido radioterapia tanto de cabeza como de cuello presente un hipotiroidismo mixto, primario y central.
Para diagnosticar hipotiroidismo de manera oportuna se recomienda vigilar el crecimiento y las concentraciones de la TSH y la T4L anualmente. El diagnóstico se basa en una concentración de T4L persistentemente baja, o en el tercio inferior de los rangos de referencia, además de signos y síntomas compatibles. El tratamiento es con levotiroxina una vez que se ha descartado insuficiencia adrenal ya que, de lo contrario, la administración de hormonas tiroideas puede precipitar una crisis suprarrenal en un paciente deficiente de hormona adenocorticotropa (ACTH).
Nódulos y cáncer tiroideo. Los pacientes que recibieron radioterapia de cuello presentan mayor riesgo de desarrollar nódulos y cáncer tiroideo. Hasta el 27% de los pacientes que recibieron radioterapia de cuello desarrollan nódulos tiroideos en un seguimiento a 20 años; de estos, hasta el 38% pueden ser malignos22.
5. Pubertad y función reproductiva en sobrevivientes de cáncer
Las alteraciones del proceso de pubertad normal en sobrevivientes de cáncer pueden ser de tres tipos: pubertad precoz o rápidamente progresiva, pubertad retrasada, detenida o ausente, e infertilidad.
5.1. Pubertad precoz
La pubertad precoz ocurre en pacientes que perdieron la inhibición hipotalámica de la secreción de hormona liberadora de gonadotropinas (GnRH) como resultado de la presencia del tumor (por ejemplo, un glioma hipotalámico o de la vía óptica), de presión intracraneal elevada, cirugía o radiación intracraneal11,23,24. La pubertad precoz se asocia con dosis de radiación craneal de 18 a 30 Gy, mientras que dosis mayores a 30 a 40 Gy generalmente causan deficiencia de GnRH y, por lo tanto, retraso puberal. El crecimiento mamario en niñas menores de 8 años o el crecimiento testicular en varones menores de 9 años deben abordarse como pubertad precoz. Algunos niños pueden desarrollar crecimiento transitorio del botón mamario debido a la recuperación nutricional. Estos niños deben revisarse cada tres a seis meses. Si el crecimiento del botón mamario persiste por más de 12 meses, puede significar el inicio de la pubertad11. El tratamiento de pubertad precoz con análogos de GnRH debe ser indicado y supervisado por un endocrinólogo pediatra.
5.2. Pubertad retrasada, interrumpida o ausente
El retraso en el desarrollo puberal, es decir, la falta de desarrollo mamario en niñas mayores de 13 años y de crecimiento testicular en varones mayores de 14, puede ser funcional o secundario a una lesión hipotálamo-hipofisiaria o una gonadal. El retraso puberal de tipo funcional puede ser una variante de la normalidad (no patológica), o bien deberse a desnutrición, enfermedad crónica, depresión, ansiedad o hipotiroidismo, y no se diferencia bioquímicamente de un hipogonadismo de origen hipotálamo-hipofisiario (hipogonadotrópico). El diagnóstico certero lo determina la evolución y la progresión puberal al mejorar el problema funcional que le dio origen.
La radiación craneal frecuentemente causa hipogonadismo hipogonadotrópico por lesión del hipotálamo, con disminución de la secreción de GnRH, o por lesión de los gonadotropos hipofisiarios, con disminución de la secreción de las hormonas luteinizante (LH) y folículo estimulante (FSH). Por su parte, el hipogonadismo hipergonadotrópico, que es secundario a lesión de la gónada —testículo u ovario—, generalmente es causado por quimioterapia altamente citotóxica o radiación a gónadas. Los quimioterapéuticos más gonadotóxicos son los alquilantes, como la ciclofosfamida, la mecloretamina y la procarbazina. La forma de presentación del daño gonadal en los varones es, frecuentemente, como una pubertad retrasada, mientras que en las mujeres es una falla ovárica prematura o menopausia temprana.
La radiación corporal total, abdominal, pélvica y lumbosacra, particularmente en mujeres pospuberales, puede comprometer la función ovárica, en especial si recibieron dosis mayores de 10 Gy prepuberales o 5 Gy pospuberales, o bien altas dosis de agentes alquilantes. Los testículos son particularmente sensibles a la radiación, con azoospermia reversible observable con dosis desde 1 a 3 Gy, azoospermia permanente a partir de 6 Gy y daño de células de Leydig con dosis mayores de 20 Gy25.
El tratamiento de los niños y niñas con hipogonadismo incluye el tratamiento de reemplazo con testosterona o estrógenos, respectivamente, por un endocrinólogo pediatra, con precaución de no ensombrecer el pronóstico de talla por una fusión acelerada de las placas de crecimiento por las hormonas sexuales.
5.3. Infertilidad
La infertilidad puede ser secundaria a hipogonadismo de origen central (hipogonadotrópico) o gonadal (hipergonadotrópico), o bien a lesiones del epitelio germinal, que es el responsable de mantener las células germinales (ovocitos y espermatozoides). Esta lesión puede ser provocada por radioterapia o quimioterapia. Los quimioterapéuticos asociados con la infertilidad incluyen la mecloretamina, clorambucil, melfalán, busulfán, ciclofosfamida, ifosfamida, procarbazina, nitrosoureas y platino. Las dosis de radiación mayores a 250 cGy a los testículos o mayores a 1000 cGy a ovarios pueden ocasionar infertilidad. Los espermatozoides son más sensibles al daño por quimioterapia y radioterapia que los ovocitos y que las células de Leydig, lo que explica que los varones sufran con mayor frecuencia de infertilidad que las mujeres y que sufran con mayor frecuencia infertilidad que hipogonadismo. La elevación de niveles de FSH y de inhibina B son marcadores de daño al epitelio germinal en varones. Es importante informar al adolescente, de una manera sensible, sobre su pronóstico reproductivo, las opciones de reproducción asistida con las que se cuenta y ofrecer la realización de espermatobioscopia a los pacientes interesados.
6. Función córtico-suprarrenal en sobrevivientes de cáncer
Los corticotropos hipofisiarios son menos sensibles a la radioterapia, comparados con los somatotropos, gonadotropos y tirotropos. Sin embargo, la deficiencia de ACTH tiene consecuencias más serias si no se detecta a tiempo. Es poco frecuente si no se recibió radioterapia craneal mayor a 24 Gy, pero debe sospecharse siempre que haya existido un tumor intracraneal, independientemente de si recibió radioterapia o si se documenta deficiencia de otras hormonas hipofisiarias. La vigilancia de deficiencia de esta hormona debe continuarse de 10 a 15 años después de resuelta la neoplasia, ya que el daño a los corticotropos se manifiesta progresivamente a lo largo de varios años. La vigilancia se lleva a cabo anualmente, con interrogatorio de síntomas (falla de medro, anorexia, deshidratación, hipoglucemia, letargia, hipotensión) y con determinación de cortisol a las 8 a.m., con evaluación por el endocrinólogo pediatra si este es menor a 10-18 μg/dl26. La deficiencia más severa se manifiesta por hipoglucemia y crisis adrenal precipitada por una enfermedad intercurrente. Pueden cursar con hiponatremia leve o moderada; la hiponatremia severa y la hiperkalemia no se presentan ya que está preservada la función mineralocorticoide. Es importante valorar la suficiencia del eje de corticotropina antes de iniciar sustitución con hormonas tiroideas, para no precipitar una crisis suprarrenal.
7. Riesgo cardiometabólico en sobrevivientes de cáncer
Los sobrevivientes de cáncer en la infancia tienen un alto riesgo de presentar enfermedad cardiovascular comparado con la población general, por lo menos hasta 45 años después del diagnóstico original de la neoplasia. El daño vascular inducido por la quimioterapia y la radioterapia es, en parte, responsable del aumento de riesgo cardiovascular temprano, aunque las anormalidades endocrinológicas y metabólicas pueden ser responsables de una gran proporción de este riesgo conforme la sobrevida se alarga. Se ha descrito una mayor prevalencia de obesidad en los sobrevivientes de cáncer con respecto a la población general, así como niveles más bajos de colesterol, de lipoproteínas de alta densidad (HDL) y niveles mayores de glucosa, asociados principalmente con el antecedente de radiación craneal y deficiencia de hormona de crecimiento. También está relacionado con factores conductuales, como la inactividad física, que es más frecuente en sobrevivientes de cáncer, resaltando la necesidad de promover enfáticamente el estilo de vida saludable en estos pacientes.
La radiación craneal produce problemas de control de peso, frecuentemente exacerbados por la deficiencia concurrente de GH e hipotiroidismo. En las niñas y los pacientes que recibieron dosis de radioterapia mayores a 18 Gy el riesgo es mayor. Se recomienda medir los niveles de glucosa, de insulina y el perfil de lípidos en ayuno cada dos años en pacientes con sobrepeso u obesidad y cada 5 años en pacientes con peso normal.
Los metales pesados, como carboplatino y el cisplatino, pueden causar dislipidemia. Para los pacientes con antecedentes familiares de dislipidemias, con sobrepeso u obesidad o con deficiencia de GH, el riesgo aumenta27.
Por otra parte, la radiación induce cambios anatomopatológicos en las coronarias, similares a aquellos observados en la aterosclerosis espontánea. Posiblemente, este fenómeno se deba a la lesión endotelial secundaria a la generación de especies reactivas de oxígeno por la radiación ionizante y a la inflamación en respuesta a ella. Se ha encontrado enfermedad arterial coronaria sintomática en el 10% de los pacientes 9 años después de la radiación mediastinal, y se ha descrito un riesgo de aterosclerosis prematura y de eventos vasculares cerebrales 10 veces mayor en pacientes sobrevivientes de leucemia y tumores intracraneales que recibieron radioterapia en cráneo y cuello comparado con la población general, particularmente con dosis mayores de 20 Gy28.
8. El hueso en sobrevivientes de cáncer
Se ha estimado un riesgo de fracturas durante los 5 años posteriores al diagnóstico de leucemia dos veces mayor al de la población general29, y una prevalencia del 24% de densidad mineral ósea baja en pacientes en la tercera y cuarta década de la vida que padecieron LLA en la edad pediátrica, comparado con el 15% de riesgo en la población general30.
La etiología del déficit de masa ósea en los pacientes que sufrieron cáncer en la niñez es multifactorial, e incluye tanto los efectos directos como los indirectos del cáncer y los de su tratamiento, lo que resulta en pérdida de hueso, disminución del crecimiento óseo y acreción mineral disminuida. La infiltración maligna, los glucocorticoides y el metotrexato pueden interferir directamente con el metabolismo óseo. La nutrición subóptima, la falta de exposición a radiación solar y la actividad física disminuida son factores que también limitan la mineralización del hueso. Por otra parte, las endocrinopatías prevalentes en sobrevivientes de cáncer, como la deficiencia de GH, de hormonas sexuales y de vitamina D, contribuyen a este déficit. No se conocen con precisión los efectos directos de la radioterapia en la densidad mineral ósea (DMO) pero se cree que son lesivos por daño a la matriz ósea.
Los glucocorticoides a dosis farmacológicas afectan el hueso por varios mecanismos incluyendo una actividad osteoblástica disminuida, mayor resorción ósea, interferencia con la GH/IGF, menor fuerza muscular, y trastorno del balance de calcio a nivel intestinal y renal. Particularmente, las dosis acumuladas mayores a 9,000 mg/m2 de prednisona tienen mayor riesgo de desarrollar baja DMO y no recuperarla.
El metotrexato tiene efecto citotóxico en los osteoblastos que da como resultado en volumen óseo disminuido y menor formación de hueso nuevo. Dosis acumuladas mayores de 40,000 mg/m2 se asocian con un mayor riesgo de osteopenia y falla para recuperar una masa ósea normal después del tratamiento.
Los estrógenos juegan un papel crucial para alcanzar y mantener el pico de masa ósea, ya que previenen su resorción y estimulan el crecimiento de hueso, tanto en varones como en mujeres. Los andrógenos tienen un papel importante en la aposición ósea del periostio, que agrega fuerza al hueso. Los agentes alquilantes conllevan un riesgo dosis-dependiente de falla gonadal que impacta directamente en la densidad mineral ósea, ya que producen deficiencia de hormonas sexuales. El riesgo de hipogonadismo primario o secundario es incluso mayor si se combina con radioterapia a gónadas o a hipotálamo-hipófisis.
Se desconoce hasta qué punto la pérdida o falta de ganancia de masa ósea durante el periodo de la enfermedad y tratamiento sea recuperable si se corrigen las deficiencias hormonales y se optimiza la nutrición y la actividad física31.
En cuanto a la prevención y tratamiento de la deficiencia de masa ósea en niños, se recomienda aumentar el ejercicio de resistencia (con peso o fuerza) conforme se tolere, garantizar un aporte de 1,500 mg diarios de calcio elemental y de 400 a 1,000 UI de vitamina D, así como desalentar el tabaquismo, el consumo de alcohol y de cafeína. También es indispensable sustituir con hormonas sexuales a los pacientes hipogonádicos y con GH a los pacientes deficientes de la misma.
Los pacientes con DMO de más de 2.5 DE por debajo de la media pueden beneficiarse de tratamientos más específicos. La calcitonina y los bifosfonatos se reservan para pacientes con fracturas recurrentes y como parte de ensayos clínicos. La investigación de los bifosfonatos en los pacientes pediátricos es limitada; solamente se han probado en pacientes con osteogénesis imperfecta. Es importante no subestimar los potenciales riesgos de usar estos medicamentos a edades tempranas. Se recomienda una evaluación basal de DMO a los 18 años11,31.
9. Hiperprolactinemia en sobrevivientes de cáncer
Las dosis de radioterapia mayores a 40 Gy, la cirugía de mesencéfalo o un tumor en el área hipotalámica pueden predisponer al desarrollo de hiperprolactinemia, que interfiere con la secreción pulsátil de gonadotropinas. En mujeres, la hiperprolactinemia se manifiesta con galactorrea e irregularidades menstruales; en los varones, con galactorrea y disminución de la libido. Se recomienda determinar los niveles de prolactina solamente si se observan signos o síntomas compatibles.
10. Vigilancia endocrinológica en sobrevivientes de cáncer
Los sobrevivientes de cáncer requieren seguimiento continuo:
• Bianual
— Para la medición precisa de peso, talla, segmentos corporales y brazada
— Edad ósea si está creciendo muy rápido o muy despacio
— IGF-1 e IGFBP3 si está creciendo muy despacio
• Anual
— Evaluación de estadio de Tanner e interpretación del estadio y tempo puberal
— LH, FSH, esteroides sexuales, inhibina B (varones) y hormona antimülleriana en niñas si hay pubertad retrasada o interrumpida
— T4L y TSH
— Palpación y USG tiroides si hubo radiación a cuello
— Consejo nutricional para prevenir obesidad y alteraciones metabólicas, y asegurar adecuado aporte de calcio y vitamina D (vigilancia anual o más frecuente si hay alteraciones)
• Densidad mineral ósea a los 18 años, 5 y 10 años después de terminada la quimioterapia, y más frecuentemente si la DMO resulta anormal
Conflicto de intereses
La autora declara no tener ningún conflicto de intereses.
Recibido el 14 de enero de 2014;
aceptado el 14 de febrero de 2014
Correo electrónico:fernandacastillapeon@gmail.com