Aunque la monitorización continua de glucosa a tiempo real (MCG-TR) está disponible desde hace más de 10 años, su incorporación a la práctica clínica es aún escasa. El objetivo de este artículo es revisar la evidencia científica existente en torno a los actuales sistemas de MCG-TR incorporados a la atención de los pacientes con diabetes que pudiera justificar su utilización en determinados perfiles clínicos. Tras una búsqueda bibliográfica seleccionando fundamentalmente estudios controlados aleatorizados que comparan los sistemas MCG-TR con la automonitorización de la glucemia, hay 12 estudios clínicos —dos con sistemas actualmente no comercializados y uno en DM2— y un reciente metaanálisis con 6 de ellos. Además de analizar sus principales ventajas e inconvenientes, se ha recogido información sobre su utilización en situaciones especiales -pacientes en UCI, gestación- y revisado estudios de calidad de vida y de coste-efectividad. También se describe la variable situación administrativa en cuanto a financiación por los sistemas de salud públicos en Europa y América, así como las indicaciones clínicas actualmente reconocidas para su uso.
Real time continuous glucose monitoring (CGM-RT) has been available for ten years, but its clinical use is still limited. The objective of this review is to look at the scientific evidence on the current CGM-RT systems incorporated into the care of patients with diabetes, to justify its use in specific patient profiles. After a systematic search for randomised controlled trials comparing CGM-RT systems with glucose self-monitoring, 12 clinical studies were selected — two with systems currently unavailable on the market currently, and one in type 2 diabetes — and a recent meta-analysis of 6 of them. In addition to analysing their main advantages and disadvantages, information has been collected on their use in special situations such as ICU patients or during pregnancy, reviewing studies of quality of life and cost-effectiveness. We also describe the currently recognised indications and the variable administrative positions in Europe and America.
En el momento actual el grado de control glucémico que reduce el riesgo de complicaciones crónicas en pacientes con diabetes tipo 1 (DM1)1 y tipo 2 (DM2)2 es aún difícil de lograr, y a pesar de la disponibilidad de los análogos de insulina y de los infusores subcutáneos de insulina, alcanzarlo evitando las hipoglucemias1 continúa siendo un reto y solo una minoría de pacientes consigue niveles adecuados de hemoglobina glucosilada (HbA1c)3.
Mientras que los autoanálisis solo proporcionan una medida puntual de glucosa de sangre capilar justo en el momento de la prueba, la monitorización continua de glucosa (MCG) ofrece una información continua de los niveles glucémicos, por lo que está entre los avances recientes más importantes que podrían revolucionar el tratamiento diabetológico.
La aparición de la MCG se produjo en los años noventa con las primeras publicaciones de MCG mediante microdiálisis en 19924,5, y la MCG retrospectiva con la tecnología de sensores-aguja se introdujo con el cambio de siglo6–8. En el momento actual hay comercializados 4 sistemas de MCG a tiempo real (MCG-TR) que miden la glucosa del fluido intersticial y generan un promedio de lecturas de glucosa cada pocos minutos (1-5min) con posibilidades de información a tiempo real y también de dirección, tasa de cambio y tendencias junto con alarmas de hipoglucemia, hiperglucemia y predictivas. Estos sistemas son: Guardian Real-Time® (MedtronicMiniMed, Northridge, CA), Freestyle Navigator® (Abbot Diabetes Care, Alameda, CA), Dexcom SEVEN® (Dexcom, San Diego, CA) y GlucoDay® (Menarini Diagnostics) (tabla 1). Los tres primeros son sistemas de aguja y el último de microdiálisis; todos ellos utilizan la reacción de la glucosa-oxidasa y están comercializados en España, excepto el Freestyle Navigator®.
Sistemas de monitorización continua a tiempo real de glucosa actualmente disponibles
| Catéteres enzimáticos insertados subcutáneamente | |
| • Paradigm Veo® (Medtronic) | Sistema de monitorización a tiempo real; requiere calibración con 2 medidas de glucemia capilar diaria; vida del sensor, 6 días; alarmas en hiper e hipoglucemia; funciones de tendencias y predictivas. |
| • Freestyle Navigator® (Abbott) | Sistema de monitorización a tiempo real; requiere calibración con glucemias capilares a las 10, 12, 24 y 72 h; alarmas en hiper e hipoglucemia funciones de tendencias y predictivas; vida del sensor, 5 días. No comercializado en España. |
| • Dexcom SEVEN® (DexCom) | Sistema de monitorización a tiempo real; requiere calibración con glucemias capilares cada 12 h; alarmas en hiper e hipoglucemia funciones de tendencias y predictivas; vida del sensor, 7 días. No comercializado en España. |
| Sistema de microdiálisis insertado subcutáneamente | |
| • GlucoDay (Menarini)® | Sistema de monitorización a tiempo real; requiere calibración con glucemias capilares al inicio una sola vez; alarmas en hiper e hipoglucemia; vida del sensor, 2 días. |
Aunque estos sistemas pueden alcanzar asumibles valores de median relative absolute diference (MRAD) entre el sensor y las medidas de referencia de glucosa inferiores al 15%9–11, en su manejo es importante reconocer la existencia de un decalaje «fisiológico» sensor independiente entre la glucemia capilar y la intersticial de al menos 10min (entre 5 y 20min). Este decalaje se incrementa cuando los niveles de glucosa cambian rápidamente (>2mg/dl/min) y es dependiente del sistema según las técnicas de procesamiento de los datos. EL CGM DexCom® tiene un retraso de 6min12, y entre 8 y 15min el Freestyle Navigator®13,14 y el ya desaparecido Guardian CGMS®15,16. Las denominadas «tendencias» en la glucosa intersticial son representativas de los cambios en la glucemia sanguínea, pero los «valores absolutos» de la glucosa intersticial no siempre son coincidentes con los niveles de glucemia sanguínea. Pueden existir oscilaciones relacionadas con la pérdida temporal de la señal, aumento de sensibilidad del sensor y perturbaciones de tipo mecánico. Por ello, los valores absolutos deben ser siempre confirmados con una medida de glucemia capilar antes de realizar cualquier cambio terapéutico. Un efecto paralelo «no esperado ni deseable» de la utilización de estos sistemas es el aumento en la frecuencia de realización de glucemias capilares diarias, que a su vez y de forma independiente se correlaciona con el control glucémico17.
Los sistemas de MCG-TR, al igual que generan gran cantidad de datos clínicos, han producido un incremento en las publicaciones científicas y, sobre todo en los últimos años, de estudios aleatorizados sobre la efectividad de esta tecnología en mejorar el control glucémico en DM1 comparando con la automonitorización convencional de la glucosa que han ido definiendo indicaciones y perfiles de pacientes; quedan, sin embargo, muchas cuestiones por resolver, tan importantes como el beneficio aportado en el marco asistencial habitual, a largo plazo y los requerimientos clínicos para su implementación.
VentajasLos primeros estudios llevados a cabo en pacientes con DM1 han sugerido que la información que ofrecen estos sistemas permite a algunos pacientes manejar más eficazmente su diabetes18, con disminución de excursiones glucémicas, menor número de episodios de hipoglucemias19–22, menores tiempos gastados en rangos de hiperglucemia e hipoglucemia23 y, descrito por ahora solo en adolescentes, una mayor respuesta de la adrenalina ante las hipoglucemias que podrían transformarse en una herramienta útil ante las hipoglucemias desapercibidas24.
Sin embargo, han sido estudios recientes los que han efectuado las más importantes aportaciones para testar la eficacia de estos sistemas. En la tabla 225 se resumen todos los estudios aleatorizados20,21,22,23,24,25,26 que se han efectuado en pacientes con DM1 y MCG-TR hasta este momento, en cuanto a HbA1c e incidencia de hipoglucemias severas. Ocho de los 9 estudios efectuados en DM1 muestran un efecto positivo de la MCG-TR en la HbA1c (descenso de 0,3-0,7% o 3-8mmol/ml), y entre las conclusiones de los resultados publicados más importantes se encuentran:
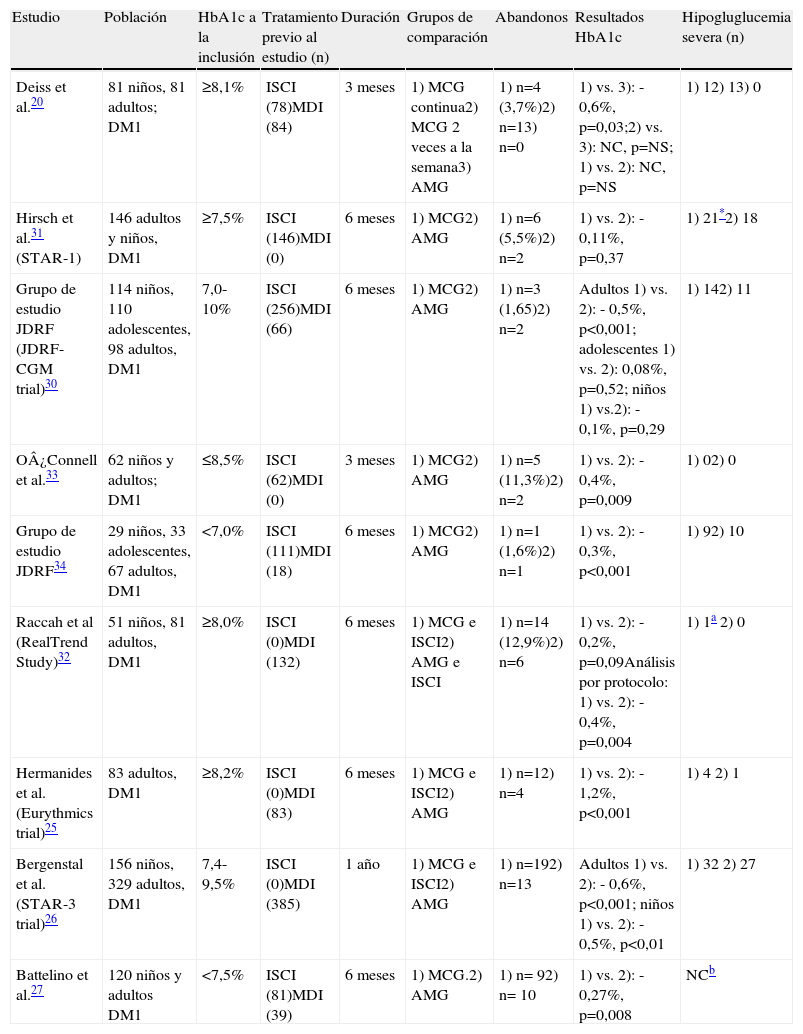
Ensayos clínicos aleatorizados de MCG-TR en diabetes tipo 1 (DM1)
| Estudio | Población | HbA1c a la inclusión | Tratamiento previo al estudio (n) | Duración | Grupos de comparación | Abandonos | Resultados HbA1c | Hipogluglucemia severa (n) |
| Deiss et al.20 | 81 niños, 81 adultos; DM1 | ≥8,1% | ISCI (78)MDI (84) | 3 meses | 1) MCG continua2) MCG 2 veces a la semana3) AMG | 1) n=4 (3,7%)2) n=13) n=0 | 1) vs. 3): -0,6%, p=0,03;2) vs. 3): NC, p=NS; 1) vs. 2): NC, p=NS | 1) 12) 13) 0 |
| Hirsch et al.31 (STAR-1) | 146 adultos y niños, DM1 | ≥7,5% | ISCI (146)MDI (0) | 6 meses | 1) MCG2) AMG | 1) n=6 (5,5%)2) n=2 | 1) vs. 2): -0,11%, p=0,37 | 1) 21*2) 18 |
| Grupo de estudio JDRF (JDRF-CGM trial)30 | 114 niños, 110 adolescentes, 98 adultos, DM1 | 7,0-10% | ISCI (256)MDI (66) | 6 meses | 1) MCG2) AMG | 1) n=3 (1,65)2) n=2 | Adultos 1) vs. 2): - 0,5%, p<0,001; adolescentes 1) vs. 2): 0,08%, p=0,52; niños 1) vs.2): -0,1%, p=0,29 | 1) 142) 11 |
| O¿Connell et al.33 | 62 niños y adultos; DM1 | ≤8,5% | ISCI (62)MDI (0) | 3 meses | 1) MCG2) AMG | 1) n=5 (11,3%)2) n=2 | 1) vs. 2): -0,4%, p=0,009 | 1) 02) 0 |
| Grupo de estudio JDRF34 | 29 niños, 33 adolescentes, 67 adultos, DM1 | <7,0% | ISCI (111)MDI (18) | 6 meses | 1) MCG2) AMG | 1) n=1 (1,6%)2) n=1 | 1) vs. 2): -0,3%, p<0,001 | 1) 92) 10 |
| Raccah et al (RealTrend Study)32 | 51 niños, 81 adultos, DM1 | ≥8,0% | ISCI (0)MDI (132) | 6 meses | 1) MCG e ISCI2) AMG e ISCI | 1) n=14 (12,9%)2) n=6 | 1) vs. 2): -0,2%, p=0,09Análisis por protocolo: 1) vs. 2): -0,4%, p=0,004 | 1) 1a 2) 0 |
| Hermanides et al. (Eurythmics trial)25 | 83 adultos, DM1 | ≥8,2% | ISCI (0)MDI (83) | 6 meses | 1) MCG e ISCI2) AMG | 1) n=12) n=4 | 1) vs. 2): -1,2%, p<0,001 | 1) 4 2) 1 |
| Bergenstal et al. (STAR-3 trial)26 | 156 niños, 329 adultos, DM1 | 7,4-9,5% | ISCI (0)MDI (385) | 1 año | 1) MCG e ISCI2) AMG | 1) n=192) n=13 | Adultos 1) vs. 2): - 0,6%, p<0,001; niños 1) vs. 2): -0,5%, p<0,01 | 1) 32 2) 27 |
| Battelino et al.27 | 120 niños y adultos DM1 | <7,5% | ISCI (81)MDI (39) | 6 meses | 1) MCG.2) AMG | 1) n= 92) n= 10 | 1) vs. 2): -0,27%, p=0,008 | NCb |
AMG: automonitorización de glucosa; DM1: diabetes mellitus tipo 1; ISCI: infusión subcutánea de insulina; JDRF: Juvenile Diabetes Research Foundation; MCG: monitorización continua de glucosa; MDI: múltiples dosis de insulin; NC: no comunicado; NS: no significativo.
Modificado de Hermanides J, Moshe P, Hans de Vries J. Current application of continuous glucose monitoring in the treatment of Diabetes. Diabetes Care. 2011;34 Suppl 2.
En la primera publicación del potente estudio de la Juvenile Diabetes Research Foundation (JDRF)27 que aleatorizó a MCG-TR o automonitorización de glucosa (AMG) a 322 adultos, adolescentes y niños con DM1 y HbA1c de 7-10%, se comunicó que los adultos de más de 25 años que utilizaban la terapia intensiva insulínica con MCG-TR experimentaron un descenso del 0,5% de HbA1c (de 7,6 a 7,1%) respecto al grupo control, sin un aumento de hipoglucemias, asociado todo ello mayor frecuencia de uso del sensor en este grupo de edad. La utilización de estos sistemas en niños, adolescentes y adultos <25 años no redujo valores de HbA1c, sin que hubiera diferencias en hipoglucemias en ningún grupo de edad.
Efecto dependiente de la dosisDesde Deiss et al.20, varios estudios18,26,28,29 han comunicado la importancia de la frecuencia de su uso, esto es, la MCG-TR es efectiva en bajar la HbA1c en pacientes que realmente la utilizan la mayor parte del tiempo. Entre ellos se encuentra un subestudio del JDRF29 en que se demuestra que para todos los grupos de edad hay una reducción significativa de HbA1c en los pacientes que utilizan la MCG-RT ≥6 días a la semana sin aumento de hipoglucemias asociado, siendo los adolescentes los menos adherentes en su utilización.
Buen control metabólico previoTambién puede beneficiar a pacientes con buen control metabólico previo (HbA1c<7%). En un pequeño subgrupo de 129 adultos y niños con HbAc<7% los resultados que combinaban HbA1c e hipoglucemia eran más favorables para el grupo que utilizaba la MCG, sugiriendo que esta tecnología puede ser beneficiosa para los pacientes con DM1 que ya han alcanzado un excelente control27.
Efecto a largo plazoUn subestudio de la serie JDRF ha demostrado el beneficio metabólico mantenido durante 1 año, esto es, la eficacia en adultos para mantener la A1c<7% con menos hipoglucemias que en un grupo control28.
Factores predictores de adherenciaLa propia adherencia previa a la terapia insulínica intensiva evaluada por la realización de glucemia capilar más de 6 veces al día antes de su instalación es un factor predictor de éxito y adherencia a esta tecnología29.
CostesOtro subestudio del JDRF sobre coste-efectividad ha confirmado un inmediato beneficio en calidad de vida en la cohorte a cualquier edad paradójicamente con HbA1c<7%. Esto es, al efectuar el análisis de coste efectividad con la proyección de la reducción de probabilidad de complicaciones microvasculares se ha obtenido en la cohorte de HbA1c<7% una ganancia en QALY de 1,11 y un incremental coste-efectividad ratio (ICER) de 78.943$/QALY. En la cohorte de HbA1c>7% la ganancia de QALY fue menor de 0,60 y el ICER de 98,679$/QALY29. Proyecciones a largo plazo señalan esta tecnología como coste-efectiva en pacientes con DM1 en un umbral en torno a los 100.000$/QUALY, aunque hay carencias de certezas en este área18.
Calidad de vidaJunto a su efecto en la HbA1c, la MCG-TR puede tener un impacto positivo en los resultados «percibidos» por los pacientes. A pesar de verse enfrentados continuamente a su diabetes, a las frecuentes alarmas y a las molestias de la portabilidad de estos sistemas, los resultados publicados de un seguimiento vía internet con 162 pacientes con MCG-TR/ISCI (infusión subcutánea de insulina) versus 142 pacientes solo con ISCI refieren que los pacientes que utilizaban la MCG-TR estaban más satisfechos con su tratamiento y tenían mejor calidad de vida30. En el estudio Eurythmics25, los pacientes asignados a MCG-TR/ISCI experimentaron menos problemas con su diabetes y un aumento en la satisfacción con su tratamiento evaluado por el Diabetes Treatment Satisfaction Questionnaire (DTSQ). En el estudio JDRF se evaluaron en 451 pacientes (casos y controles) (o sus padres), después de las 26 semanas de seguimiento, la calidad de vida y la satisfacción con el sistema MCG-RT (casos) con cuestionarios específicos. Los scores DQOL permanecieron sin cambios significativos en ambos grupos, con una ligera diferencia significativa a favor del grupo de adultos con MCG-TR en algunas subescalas, junto a una sustancial satisfacción con esta tecnología entre los participantes y sus padres31. La insatisfacción con estos sistemas ha sido referida por otros autores como principal causa de abandono de los pacientes32.
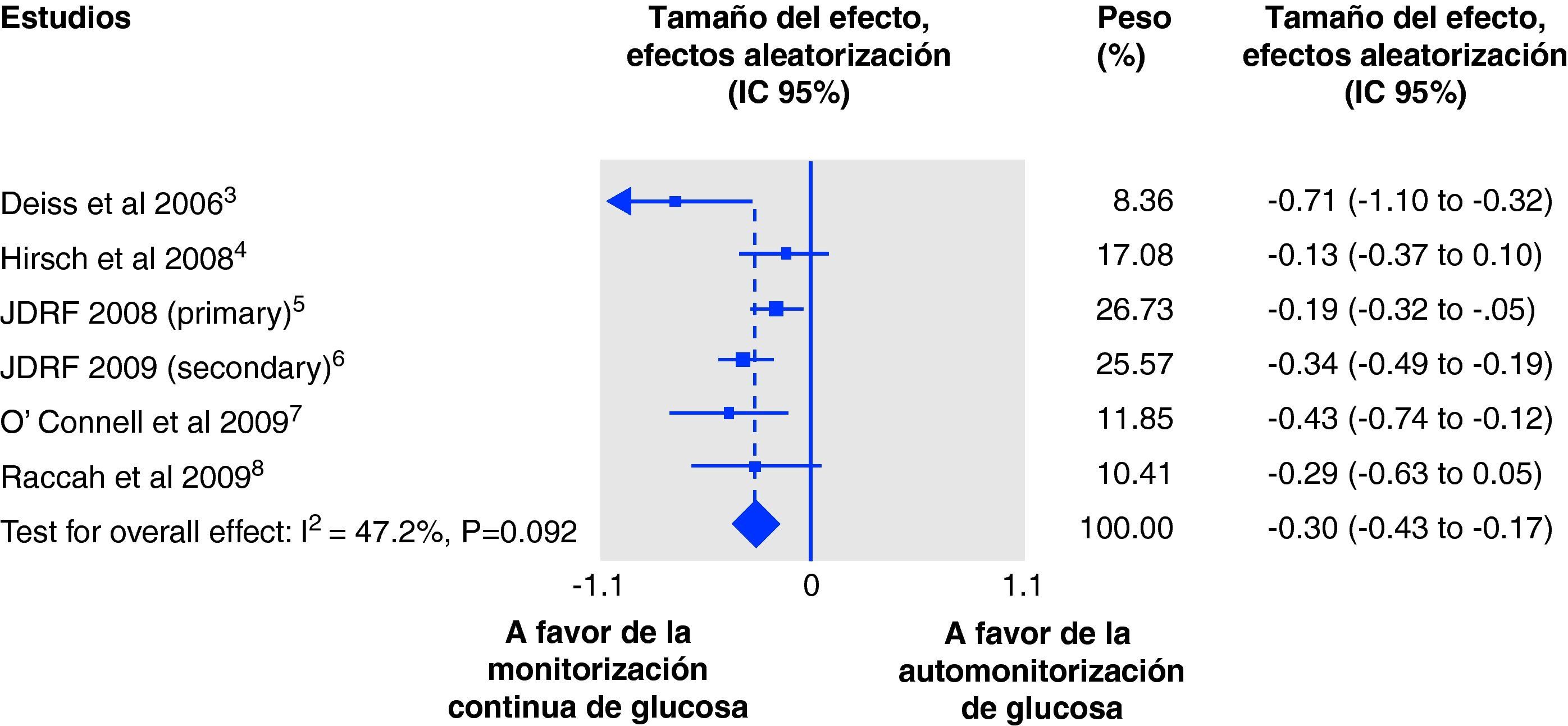
Metaanálisis de ensayos aleatorizados para diabetes tipo 1En un reciente metanálisis publicado por Pickup et al.33 para determinar la efectividad de la MCG-TR comparada con la AMG en DM1 implicando a 6 estudios clínicos aleatorizados18,20,26–29 con más de 892 pacientes (449 en MCG-TR y 443 en AMG) de más de 2 meses de duración, donde la forma de administración de insulina fue similar en ambas ramas, se analizaron como datos primarios la HbA1c y el área bajo la curva de hipoglucemia durante las dos opciones, seguido por una metarregresión exploratoria para evaluar factores determinantes de la HbA1c y de los tiempos en hipoglucemia. Los autores concluyen que la MCG-TR se asocia con una reducción significativa en la HbA1c y de los tiempos en hipoglucemia. El descenso en HbA1c es mayor en pacientes con mayores niveles de inicio y en los que utilizan con más frecuencia los sensores, lo que indica que estos sistemas son más coste-efectivos en pacientes con DM1 con mal control metabólico a pesar de la terapia intensiva insulínica si son capaces de utilizar frecuentemente el sistema.
La diferencia global en HbA1c fue de –0,30% (IC del 95%: −0,43 a −0,17%) (fig. 1). Un modelo de ajuste de determinantes de la HbA1c final mostró que los principales efectos resultaban de la influencias aditivas de la HbA1c basal, el uso del sensor y su interacción con el tipo de tratamiento, teniendo la edad un efecto menor. La reducción global en el área bajo la curva de hipoglucemias fue de –0,28 (−0,46 a −0,09), correspondiendo a una reducción en la exposición a hipoglucemias del 23%.
Metaanálisis para evaluar la diferencia en el porcentaje de HbA1c entre monitorización continua de glucosa y automonitorización de glucosa utilizando un modelo de efecto aleatorio. Globalmente, la diferencia de medias para los 6 estudios fue 0,30% (3 mmol/mol) a favor de la monitorización continua de glucosa. (Tomado de Pickup et al.34.).
La aplicación de la MCG-TR está siendo investigada en pacientes hospitalizados, especialmente en áreas donde es necesario un riguroso control glucémico, como en unidades de cuidados intensivos (UCI)34. Aunque en el pasado existían dudas en cuanto a la precisión de estos sistemas en estos espacios asistenciales35, se han efectuado estudios36–39 en pacientes críticos, y algunos de ellos refieren una mayor precisión y fiabilidad comparados con las glucemias capilares de los «point of care»40,41. Considerada aún como una tecnología inadecuada para guiar la terapia insulínica en la UCI, actualmente está surgiendo evidencia que apoya su utilización en pacientes críticos tanto pediátricos42 como adultos43. En un estudio llevado a cabo en 174 pacientes adultos de UCI en terapia intensiva insulínica con 2.045 medidas pareadas se apreció que las medidas del sistema MCG-TR cumplían criterios ISO junto a adecuadas correlaciones (0,92) y diferencias (diferencia media de 2mg/dl; diferencia absoluta de 8mg/dl) con los niveles de referencia arterial, y un Error Grid Analysis con un 99,1% de los valores de MCG-TR en la zona aceptable para el ajuste terapéutico de insulina43. Además, un reciente estudio ha confirmado que la MCG-TR puede reducir significativamente episodios de hipoglucemias en la UCI44.
MCG-TR en el embarazoLa utilización de MCG-TR durante la gestación tiene similares limitaciones a las que existen en la población con diabetes en general, a lo que hay que añadir la carencia de estudios que hayan evaluado las variaciones fisiológicas entre glucemia intersticial y capilar en el embarazo y de estudios aleatorizados que hayan comunicado evidencia científica de peso para indicar su utilización. La mayor parte de los estudios efectuados de esta tecnología durante la gestación son series cortas y no homogéneas de pacientes con DM1, DM2 y diabetes gestacional y con sistemas no TR45, por lo que sacar conclusiones resulta aún difícil.
Diabetes tipo 2Hasta el momento se han publicado dos estudios sobre la utilidad de la MCG-TR en pacientes con DM2, de 3 meses46 y 18 meses47 de duración, utilizando este último una tecnología ya comercialmente retirada por sus importantes reacciones cutáneas —hasta del 49% de casos— y que provocaba dificultades en su utilización, por lo que los resultados no son valorables.
InconvenientesAunque la MCG-TR consigue bajar la HbA1c en determinados grupos de pacientes, se trata de una tecnología emergente que tiene una serie de barreras limitantes para su utilización más generalizada. Entre ellas podemos citar las siguientes:
- 1.
La MCG-TR en este momento es aceptada solo como complemento a los autoanálisis de glucemia capilar convencional, ya que la precisión de los sistemas aún no es la adecuada y es necesario confirmar los valores altos o bajos con AMG antes de efectuar cualquier cambio terapéutico.
- 2.
Algunos pacientes (5-20%) experimentan molestias, como eritema, edema o irritación de la piel debido al adhesivo del sensor.
- 3.
Una de las claves del uso efectivo de la MCG-TR es la interpretación de los datos. Su uso proporciona abundantes lecturas de glucosa a tiempo real que pueden ser descargadas retrospectivamente tanto por los pacientes en casa como por los profesionales sanitarios, permitiendo incluso su envío por determinadas plataformas de telemedicina y acercándonos a los nuevos paradigmas de una autonomía supervisada. Se trata de una propuesta compleja: implica la interacción de conocimientos, habilidades, actitudes y toma continua de decisiones que precisa un alto nivel de competencia tanto de profesionales como de pacientes, junto a un importante soporte educativo para el manejo adecuado de los datos. Es un avance tecnológico donde paradójicamente el factor humano es vital, requiriendo de importantes tiempos asistenciales y formación de los profesionales implicados para su optimización18, así como de una gran motivación por parte del paciente.
- 4.
Los pacientes mal controlados parecen beneficiarse de estos sistemas cuando su uso es frecuente. Paradójicamente, este perfil de usuario —sobre todo niños y adolescentes— suele ser poco adherente, y por ello la utilidad real de la MCG-TR puede que se vea limitada.
- 5.
Hay algunos pacientes que no toleran estos sistemas con mayor tasa de abandono (del 1,6 al 12, 9%, siempre <15%) en la rama de MCG-TR de la mayor parte de estudios aleatorizados (tabla 2).
- 6.
En la mayoría de los estudios aleatorizados los pacientes o estaban en tratamiento con ISCI antes de la aleatorización o la iniciaron durante el estudio, por lo que habría que ser prudentes para extrapolar los resultados a pacientes con múltiples dosis de insulina (MDI).
- 7.
Estos sistemas no han demostrado, en contra de lo esperado, prevenir o disminuir los episodios de hipoglucemias severas. En el reciente metaanálisis de Pickup et al.33 la tasa de incidencia de hipoglucemia severa durante la MCG-TR no fue significativamente diferente de la correspondiente a la automonitorización. En la tabla 2 se muestran los episodios de hipoglucemias severas; en el STAR-1 hubo incluso más episodios de hipoglucemias severas en el grupo MCG-TR que en el grupo control, aunque con un amplio intervalo de confianza (1,06-22,33).
Los estudios efectuados no han sido diseñados ni en número de pacientes ni en duración para valorar hipoglucemias severas. Son necesarios otros diseños para evaluar este aspecto a fin de justificar el reembolso de estos sistemas en pacientes bien controlados donde el valor de esta tecnología pudiera venir de la mano de la prevención de hipoglucemias.
Indicaciones actuales de MCG-TRAunque en el momento actual los sistemas de MCG-TR tienen unas indicaciones clínicas precisas basadas en la evidencia científica disponible, también existen otras posibles indicaciones avaladas por la experiencia clínica, consensos o grupos de expertos.
Indicaciones clínicas basadas en la evidencia científicaEn el momento actual estas indicaciones parecen limitarse a pacientes con DM1, cuando la HbA1c permanece por encima de los objetivos individualizados a pesar de la optimización de la terapia intensiva (MDI o ISCI)26,27,39.
Otras posibles indicacionesSin embargo hay otras indicaciones que, ante la carencia de evidencias, se han ido reconociendo por consenso48,49. Entre ellas se encuentran:
- •
Optimización de la terapia ISCI cuando la HbA1c no baja por debajo de 7,5% (o de 6% en el embarazo)48.
- •
Protección frente a hipoglucemias incapacitantes; también para pacientes con hipoglucemias desapercibidas y/o miedo a hipoglucemias.
- •
Necesidad de asegurar la prevención de hiperglucemias (p.ej., en embarazo)45.
Entre las principales se encuentran:
NICE 2010Clinical Guideline 15 (2010).Type 1 diabetes: diagnosis and management of type 1 diabetes in children, young people and adults. 2010.
- •
Los niños y jóvenes con DM1 con problemas persistentes de hipoglucemias asintomáticas o hipoglucemias o hiperglucemias de repetición son candidatos a los sistemas de monitorización continua de glucosa (nivel de recomendación B).
- •
Los sistemas de monitorización continua de glucosa tienen un papel en la evaluación de los perfiles de glucosa en adultos con importantes problemas de control glucémico en la terapia con insulina, particularmente en caso de: a) repetidos episodios de hiperglucemias o hipoglucemias en el mismo momento del día, y b) hipoglucemias asintomáticas que no responden a un ajuste convencional de dosis de insulina (nivel de recomendación B).
La importancia que esta tecnología va alcanzando se visualiza entre otros aspectos porque, en el «Executive Summary» de las recomendaciones de la American Diabetes Association (ADA) 2011, de los 7puntos en torno a la «monitorización de la glucosa», tres corresponden a recomendaciones específicas de la MCG-TR, con su correspondiente nivel de evidencia científica.
- •
La MCG-TR, en conjunción con tratamientos intensivos de insulina, puede ser una herramienta útil para descender la A1C en adultos seleccionados (>25 años de edad) con DM1 (A).
- •
A pesar de que la evidencia en la disminución de A1C es menos potente en los niños, adolescentes y adultos jóvenes, la MCG puede ser útil en estos grupos. El éxito se correlaciona con la adherencia al uso continuo del dispositivo (C).
- •
La MCG-TR puede ser una herramienta complementaria a la AMG en los pacientes con hipoglucemia desapercibida o episodios frecuentes de hipoglucemia (E).
Establece que son candidatos a estos sistemas:
- •
Pacientes con DM1 con control inestable y/o que no pueden lograr niveles aceptables de A1c.
- •
La MCG-TR es particularmente valiosa en la detección tanto de hipoglucemias nocturnas y como de la hiperglucemia posprandial.
Recomienda específicamente la monitorización continua de glucosa en tiempo real en:
- •
Pacientes con DM1 bien entrenados y A1c>8,1%, a pesar de adecuada terapia intensiva insulínica con MDI o ISCI.
- •
Después de 3 meses a partir de la utilización de la MCG a tiempo real es obligatorio volver a evaluar a cada paciente y la reducción de la A1c. En caso de fallo, el uso de del sistema TR debe cesar. The Endocrine Society. Un grupo de trabajo de esta sociedad con el consenso de otras sociedades (Diabetes Technology Society y European Society of Endorinology) ha evaluado el uso potencial de MCG-TR en niños, adolescentes y adultos a nivel hospitalario y extrahospitalario. En esta reciente guía de obligada lectura se aportan tanto la fuerza de cada una de las recomendaciones como la calidad de la evidencia científica disponible51.
En general, y a la luz de la evidencia científica aportada, la MCG-TR podría ser coste -efectiva en pacientes con DM1 mal controlados por los beneficios a largo plazo relacionados con el descenso de la HA1c y de los tiempos en hipoglucemia. Sin embargo, su papel en otros perfiles de pacientes o en la prevención hipoglucemias es aún difícil de valorar. Esto se refleja en el estado actual de reembolso de estos sistemas en los distintos sistemas sanitarios. En Estados Unidos, la mayoría de las aseguradoras reembolsan la MCG-TR solo en pacientes con HbA1c elevada o con episodios de hipoglucemias severas de repetición. En Europa, la MCG-TR está cubierta en circunstancias muy precisas en Suecia, Suiza, Holanda, Eslovenia y Francia.
Específicamente en España, en el momento actual y aunque desde al año 2009 existe un documento de consenso elaborado por el Grupo de Trabajo de Nuevas Tecnologías de la Sociedad Española de Diabetes (SED)49, la situación administrativa generalizada es de «alegalidad». Algunas Unidades de Diabetes de referencia han podido disponer de experiencia con estos sistemas en el desarrollo de proyectos de investigación clínica financiados con fondos obtenidos de forma competitiva en las respectivas convocatorias de ayudas a la investigación autonómicas y nacionales; otras lo han conseguido adhiriéndose a proyectos de investigación multicéntricos internacionales promovidos por las respectivas empresas privadas, y de manera casuística, otras han podido conseguir estos sistemas negociando con sus respectivas gerencias para casos muy específicos, previa elaboración de informes justificativos.
La heterogeneidad a nivel nacional e internacional, por tanto, está bien servida. En el anexo 1 se recoge la situación actual de financiación de los sistemas MCG-TR en los principales países del mundo.
Mientras tanto, la incorporación de la MCG-TR a la atención diabetológica coste-efectiva debería hacerse en unidades acreditadas que dispongan de los conocimientos y de la experiencia necesarios para confirmar las indicaciones clínicas de estos sistemas, su seguimiento, su evaluación —tanto de su impacto clínico como de los programas específicos (educativos y tecnológicos) necesarios para su manejo—, junto a las estrategias de retirada. Ante la velocidad del desarrollo tecnológico y la relativa lentitud de aparición de la evidencia científica necesaria para su incorporación, el hecho de trabajar en esta frontera del conocimiento hace recomendable el registro de casos y sistemas en plataformas informáticas de competencia institucional, de obligado cumplimiento, con renovación anual de prescripción, que permita un seguimiento en el ámbito clínico habitual y donde se establezcan los necesarios criterios consensuados de indicación, confirmación de adherencia, renovación anual y retirada.
ConclusionesLa evidencia científica disponible nos permite afirmar que en pacientes con DM1 la MCG-TR desciende significativamente la HbA1c en mayor grado a mayor nivel de HbA1c de inicio, sin incrementar la incidencia de episodios de hipoglucemias severas en pacientes que utilizan el sistema con frecuencia. Además, puede tener un impacto positivo en la calidad de vida de algunos de estos pacientes. La utilidad de estos sistemas en adolescentes y niños requiere atención adicional, en cuanto que estos pacientes suelen ser poco adherentes. Por ahora, la MCG-TR no parece estar indicada para prevenir hipoglucemias severas ni en pacientes con DM2. Aunque los resultados de su aplicación en embarazadas y en la UCI son prometedores, se necesita más investigación en estos escenarios. Finalmente, mientras que la precisión y la portabilidad de estos sistemas deben mejorar, se requiere un amplio trabajo de profesionales y pacientes para trasladar el potencial beneficio a la práctica habitual. Son necesarios más estudios que nos permitan confirmar resultados a largo plazo en el marco asistencial habitual, incluyendo evaluación de adherencia y calidad de vida.
Conflicto de interesesM. Soledad Ruiz de Adana ha recibido honorarios como conferenciante de Medtronic, Roche y Novalab. El resto de autores no presenta conflicto de intereses.
Entre los países que han aprobado el reembolso total de los sistemas RT para una población de pacientes determinada cubriendo el sistema de salud el dispositivo, los fungibles y todo el seguimiento, siempre que cumplan las indicaciones de reembolso aprobadas, se encuentran:
- –
Población:
- •
Los sistemas de MCG personales están en la actualidad cubiertos por la mayoría de los planes de salud de Estados Unidos.
- •
La cobertura generalmente se aplica a los pacientes de DM1 que presenten episodios de hipoglucemia severa o inexplicable y/o que no alcancen los objetivos de HbA1c de la American Diabetes Association (ADA).
- •
El programa federal Medicare están en proceso de aprobación de los sistemas de MCG personales, cubriendo en la actualidad los MCG profesionales.
- •
- –
La evidencia clínica considerada en el proceso se presentó en un dossier con toda la evidencia científica disponible hasta finales del 2008 con la inclusión del estudio JRDF 2008, que era el último disponible en ese momento.
- –
Los sistemas de MCG a tiempo real quedaron incluidos en la Cartera del Servicio Nacional de Israel (National Health Basket) y, por tanto, completamente financiados en sistema público a través de los «Sickness Funds», para la siguiente población de pacientes:
- •
Diabéticos tipo 1 —niños entre 6 y 18 años— con hipoglucemias desapercibidas severas, que hayan sufrido 2 episodios de hipoglucemia severa en los últimos 12 meses y haya sido necesaria su derivación a urgencias o llamar a una ambulancia.
- •
Gestantes con DM1.
- •
De manera reglada en este país:
- –
Una persona cubierta con seguro, capaz de mejorar el control glucémico en base a las automediciones, tiene derecho a un sistema de MCG-TR si él/ella:
- a)
Tiene DM1 y se encuentra en el proceso de desarrollo de su sistema nervioso central (mielinización). El derecho está asegurado hasta que no se haya completado el desarrollo del SNC, hasta los 7 años como máximo (incluidos), o
- b)
Tiene diabetes con episodios de hipoglucemia desapercibida y padece hipoglucemia severa, o
- c)
Está embarazada, tiene DM1 o DM2 y requiere tratamiento intensivo de insulina.
- a)
- –
El sistema de MCG-TR reembolsable incluye los sensores y el transmisor.
- –
La prescripción máxima para los pacientes que se puedan beneficiar será de 1 trasmisor y 40 sensores al año, y la realizará un médico autorizado.
- –
Inicio del reembolso a nivel nacional: 1 de febrero de 2010.
- –
El sistema de MCG personal es reembolsable como sistema integrado para pacientes con DM1 que utilicen un infusor subcutáneo de insulina y cumplan una de las 3 condiciones:
- a)
Dos o más episodios de hipoglucemia severos al año que requieran la ayuda de otra persona, o
- b)
Pacientes con niveles de HbA1c de al menos 9%, en los casos en que el tratamiento optimizado con insulina no haya resultado efectivo, o
- c)
Niños que requieran al menos 10 tests de glucosa plasmática cada 24 h.
- a)
- –
Siempre se debe realizar un acuerdo con el paciente o la familia sobre el uso continuo del sistema por un máximo de 3 meses, estableciendo la indicación del tratamiento y el resultado esperado.
- –
Se debe realizar una evaluación de los resultados en cada paciente concreto; si no se obtuviesen los resultados deseados, se interrumpiría la terapia.
- –
A nivel clínico, el uso del sistema de MCG debe ser monitorizado y quedar registrado a través del registro nacional de diabetes (NDR) y de SWEDIABKIDS.
- –
El inicio del reembolso a nivel nacional data de septiembre de 2009.
El sistema de MCG personal es reembolsable como sistema integrado para pacientes con DM1 que utilicen un infusor subcutáneo de insulina y cumplan una de las siguientes condiciones:
- –
Hipoglucemias severas o diabetes inestable que haya requerido servicios de urgencias u hospitalización. o
- –
HbA1c ≥8%.
- –
Despues de los primeros 6 meses el paciente debe ser reevaluado por el médico a fin de completar la petición administrativa correspondiente.
El sistema de MCG personal es reembolsable en:
- –
Niños con DM1.
- –
Adultos con DM1 y dificultades para alcanzar objetivos. Por ejemplo, HbA1c C(>8% o >64 mmol/mol), o
- –
Gestantes con DM1 y DM2.
Información parcialmente facilitada por Medtronic®.