«La escleroterapia puede mucho más de lo que en general imaginamos. Teóricamente lo puede todo (Mollard 1994)». En esta reflexión, este cirujano vascular, intuye la potencialidad de los esclerosantes en la nueva forma farmacéutica acabada de nacer.
La escleroterapia, procedimiento técnicamente ciego, no evolucionaba, permanecía durante décadas como complemento a la cirugía. No podía progresar porque estaba presa de limitaciones inherentes a la forma líquida de los productos utilizados que impiden hacer suyos los requerimientos básicos de la escleroterapia:
- a)
Conocimiento de la concentración intravascular del esclerosante.
- b)
Homogénea, extensa y manejable distribución sobre las paredes venosas.
- c)
Control del tiempo de contacto esclerosante-endotelio.
La clave de la escleroterapia se encierra en el control de la acción de los fármacos esclerosantes y este control se consigue con la forma farmacéutica de espuma inyectable; con ella la escleroterapia rápidamente evoluciona hasta alcanzar una nueva era.
“Sclerotherapy can be much more than we generally imagine. Theoretically, it can be everything. (Mollard 1994)”. In this reflection, a vascular surgeon sensed the potentiality of sclerosing agents in the recently created new pharmaceutical form.
Sclerotherapy, technically a blind procedure, did not evolve; it remained as a complement to surgery for years. It was unable to progress because it was a prisoner of the limitations adherent to the liquid form of the products used, which that impeded compliance with the basic requirements of sclerotherapy:
- a)
Knowledge of the intravascular concentration of the sclerosing agent.
- b)
Homogeneous, extensive, and manageable distribution of the venous walls.
- c)
Temperature control of the sclerosing agent-endothelium contact.
The key to sclerotherapy involves controlling the action of the sclerosing drugs, and this control is achieved in the pharmaceutical form of an injectable foam, and with this, sclerotherapy rapidly advanced until reaching this new era.
Nowadays, different therapies are used in the treatment of varicose veins, including radiofrequency and laser ablation, stripping, surgery, mechanical-chemical systems, steam, and glue, with very different outcomes.
Sclerotherapy is a minimally invasive technique used for more than a hundred years, and useful for treating tiny little veins, until recently, in 1993, a pharmaceutical grade foam was developed that succeeded in treating large varicose veins, and is imitated by many others. The physical-chemical features of these foams vary considerably among themselves, depending on the production technique, concentration of sclerosing agent, types of gases used, gas/liquid proportion, type of gas/ size of bubble ratio, as well as varying in their safety and therapeutic use.
The optimal liquid/gas proportion is obtained when there is sufficient liquid for the bubbles to be spherical and with the smallest diameter possible, but without introducing excess sclerosing liquid, which is described as kugelschaum (wet foam) or alternatively, it forms polyederschaum (dry foam). A series of experimental and theoretical studies have been conducted with the purpose of investigating the mechanical and rheological properties of the foams. However, to study its dynamic behaviour is a challenging theoretical problem, due to the complex interaction between the physical phenomena that occur in different longitudinal scales (that is to say, from the molecular to the macroscopic).
And, in this interesting time of the evolution of the injection of drugs deposited over bubbles, is where we currently are.
En estos tiempos, diferentes terapias se emplean en el tratamiento de venas varicosas1-4, incluyendo radiofrecuencia y ablación láser5, strippping6, surgery7, sistemas mecano-químicos8, vapor de agua y pegamento9, con muy diferentes resultados.
La escleroterapia es una técnica mínimamente invasiva utilizada desde hace más de cien años y útil para tratar pequeñas venitas10, hasta que recientemente, en 1993, se desarrolla una espuma de grado farmacéutico que logra el tratamiento de grandes varices11,12 y es imitada por muchas otras13–18. Las características físico-químicas de estas espumas varían considerablemente entre sí dependiendo de la técnica de producción, concentración de esclerosante, tipos de gases utilizados, proporción gas/líquido, relación tipo de gas/tamaño de burbuja16,19 y de igual manera varían su seguridad y utilidad terapéutica4,20,21.
La proporción óptima líquido/gas se obtiene cuando hay líquido suficiente para que las burbujas puedan ser esféricas y del menor diámetro posible, pero sin introducir el exceso de líquido esclerosante, que se describe como kugelschaum o su defecto, que forma polyederschaum22. Una serie de estudios experimentales y teóricos se han realizado con el fin de investigar las propiedades mecánicas y reológicas de las espumas23. Sin embargo, estudiar su comportamiento dinámico representa un problema teórico desafiante, debido a la compleja interacción entre los fenómenos físicos que ocurren en diferentes escalas de longitud (es decir, desde la molecular hasta la macroscópica).
Y en este interesante momento de evolución de la inyección de fármacos depositados sobre burbujas, nos encontramos actualmente.
Estado del arte. IndicacionesLa aparición de reflujo y el posterior desarrollo de las venas varicosas requieren una conexión entre la tríada formada por el origen de reflujo, las vías de transmisión y los vasos terminales. Estos tres elementos están presentes en todos los pacientes con venas varicosas: a) el origen de un reflujo identificado mediante Doppler o eco-Doppler color, puede ser eliminado; es el menos importante, porque la ausencia de válvulas funcionantes en un segmento venoso aislado tiene poca importancia si la sangre no tiene dónde ni por dónde refluir. b) Las vías de transmisión, anatómicamente muy variables, son fácilmente identificables a simple vista y con eco-Doppler color. Dotan de significado al origen del reflujo y su eliminación estable debe ser confirmada en las visitas de seguimiento. c) Los vasos finales que conducen el reflujo hacia perforantes de pierna, al tobillo-pie, o al plexo indiferente plantar, son también sencillamente eliminables.
Pero el éxito total sobre las varices de miembros inferiores, padecimiento conceptualmente simple, es inaccesible a la cirugía y los métodos basados en fibras intraluminales (radiofrecuencia, láser, glue, vapor de agua, etc.); usados aislada o conjuntamente, no logran eliminar por completo todas las venas varicosas en una extremidad, no es raro que pequeñas venas incompetentes persistan y estas venas olvidadas suelen ser la base de recurrencias.
La clave para el éxito terapéutico en el tratamiento de la insuficiencia venosa radica en la eliminación completa, rigurosa y confirmada de todas las venas varicosas de pierna, tobillo y pie.
Por primera vez la medicina dispone de una herramienta con esta capacidad.
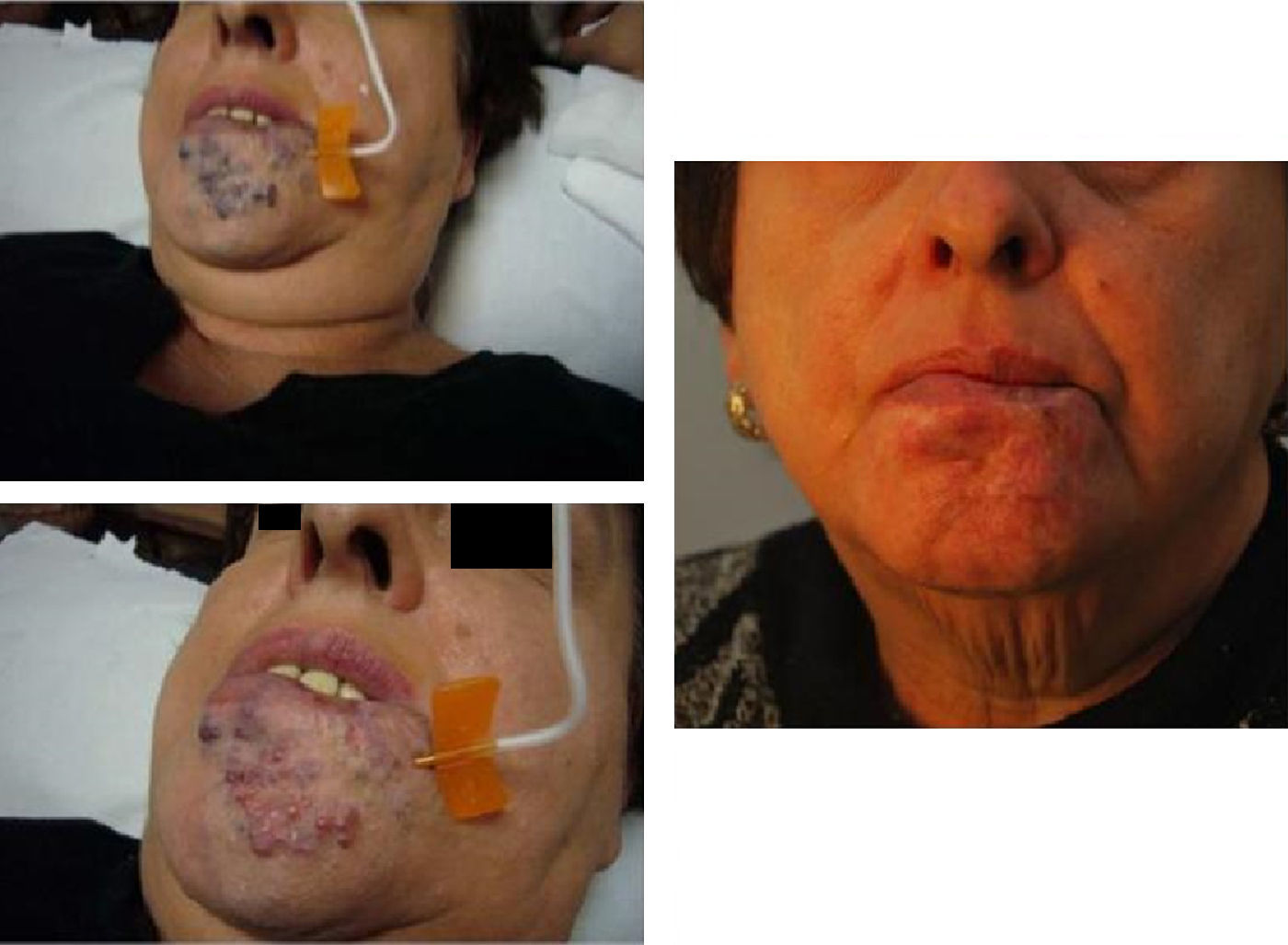
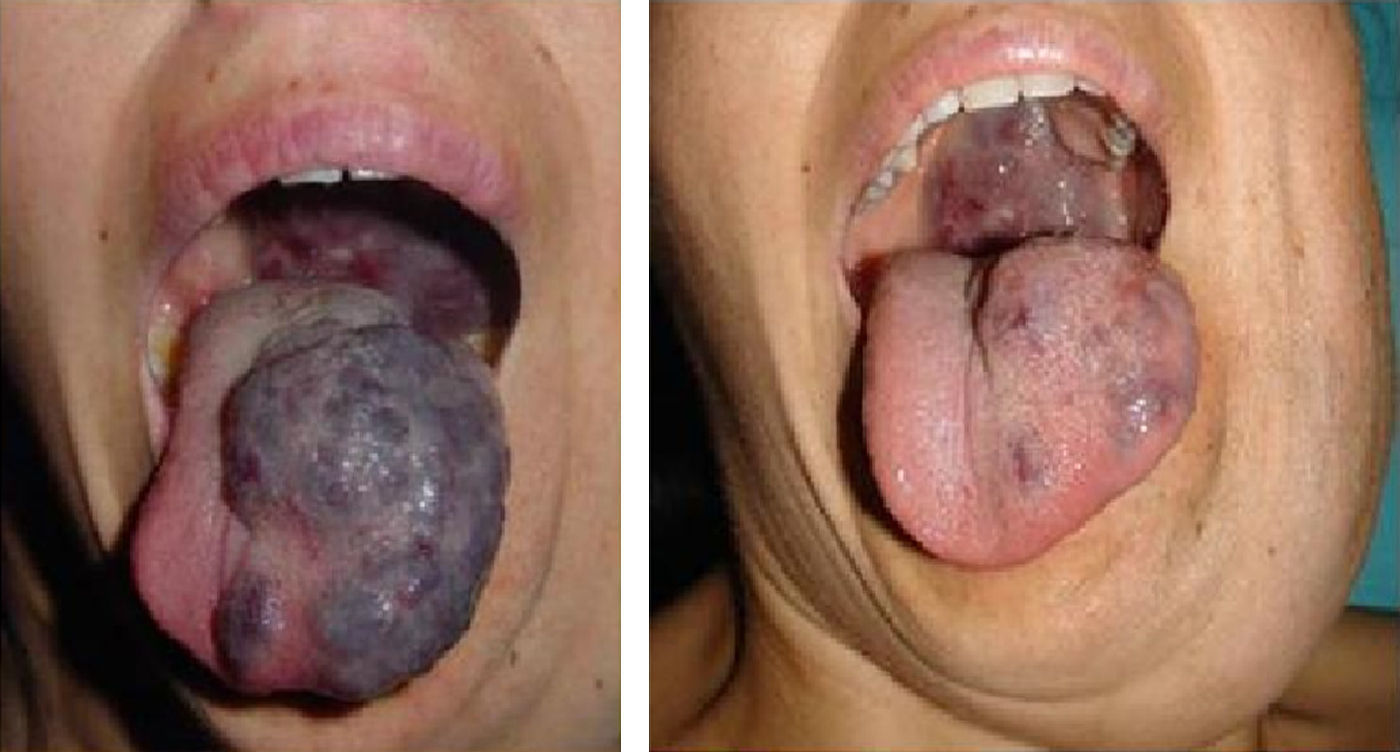
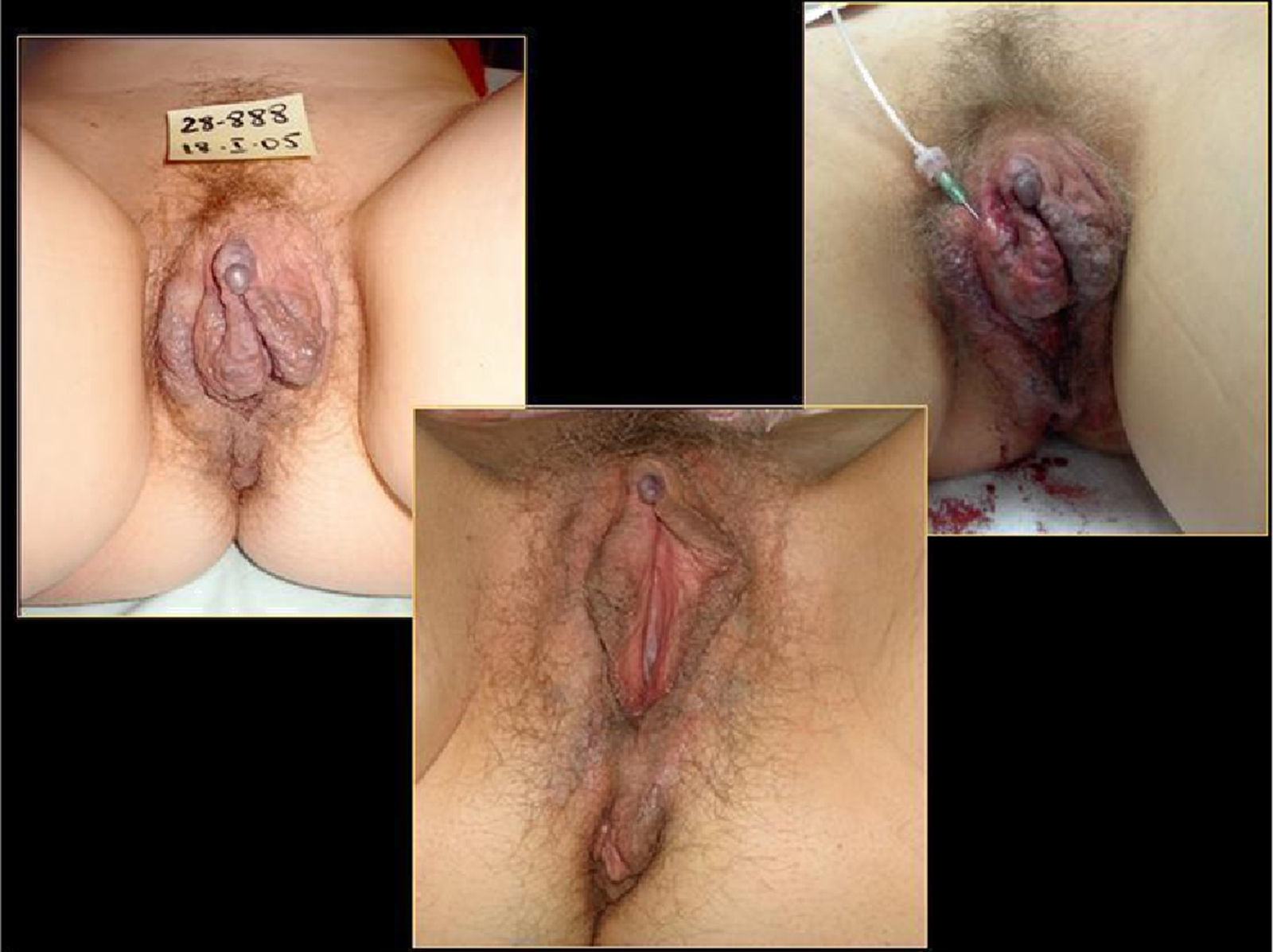
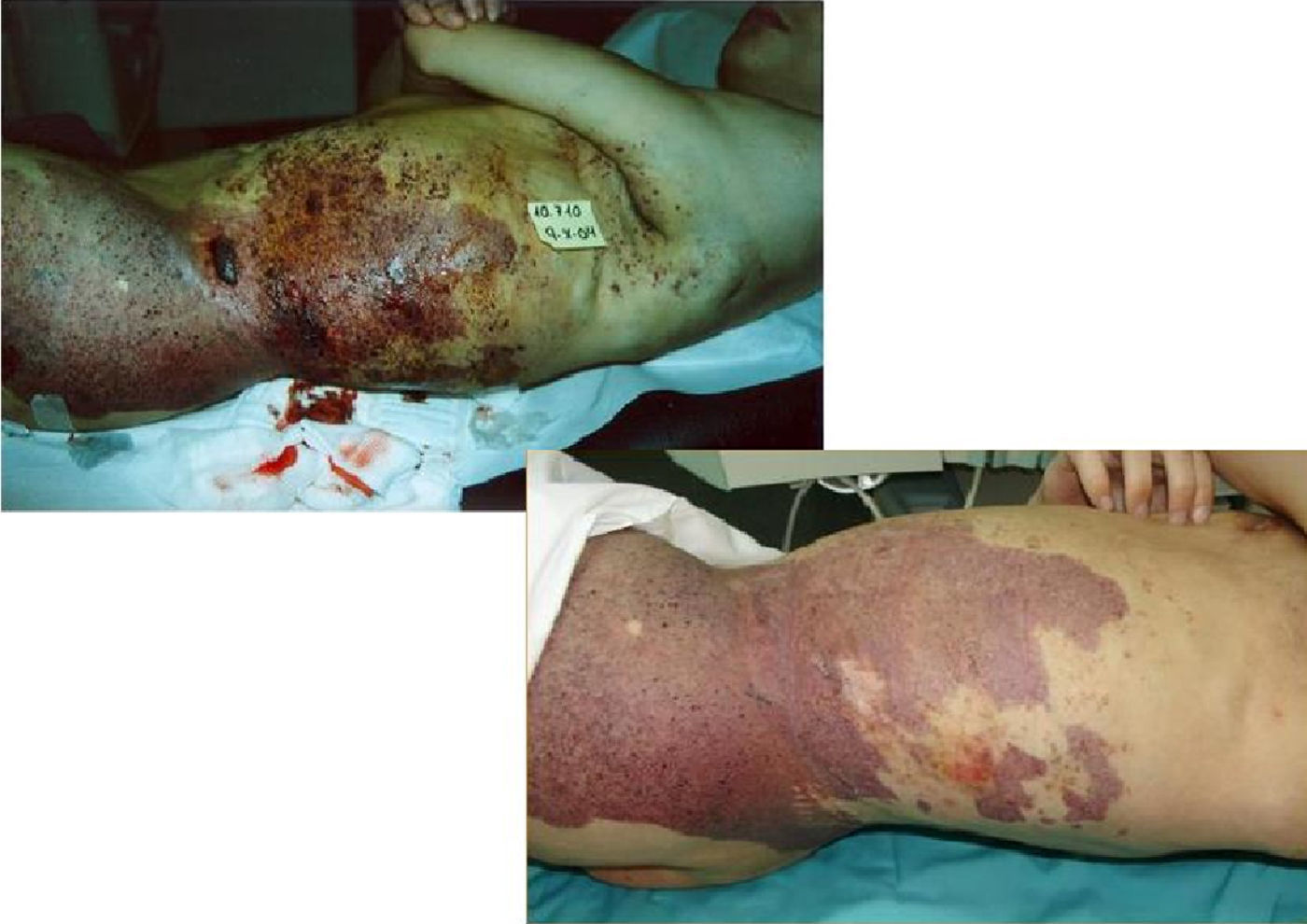
La escleroterapia con líquidos, terapia clásica de reconocido potencial24, pero limitada efectividad, ha entrado en una nueva era4,12. Su limitada utilidad, impuesta por su forma líquida sujeta a dilución e inactivación progresiva en la sangre y el muy difícil control de su acción una vez inyectadas, ha sido superada por el sencillo recurso de colocar estos líquidos en periferia de microburbujas, que desplazan físicamente la sangre contenida en el vaso y le permite actuar sobre el tejido diana. La clave de la escleroterapia que reside en el control de la acción de los productos esclerosantes, lo permite. Desde 1993, nuestra experiencia y la de otros han demostrado la eficacia de la escleroterapia con microespuma guiada por eco-Doppler color. Esta ha sido utilizada con éxito no solo en pacientes con venas varicosas en las piernas de tradicional indicación quirúrgica25,26, sino también en malformaciones venosas inoperables y también en otras situadas en territorios delicados, como lengua, labios, área vulvar, etc. y asimismo en úlceras hipertensivas venosas en las piernas11,27,28. Bergan29 dice en el 50 Congreso de la UIP celebrado en Mónaco 2009, «La escleroterapia con espuma alcanza su más alta cima de éxito en el tratamiento de las úlceras venosas de las piernas». Nuestra microespuma patentada amplió, sin limitaciones aparentes, la capacidad terapéutica de la escleroterapia. Un viejo concepto volvió a la vida.
Sin embargo, la gran facilidad con la que puede ser producida espuma a partir de un surfactante, es la causa de una simplista analogía entre espuma y microespuma.
Los Estados Unidos de Norteamerica (EE. UU.) disponen de una microespuma de grado farmacéutico aprobado por la FDA (Varithena®), evolución de nuestro concepto original, pero su ausencia en Europa da lugar a pluralidad de esfuerzos para conseguir y utilizar espumas «fabricadas en casa» en escleroterapia. Ha habido numerosas publicaciones de resultados obtenidos con heterogéneos tipos de espumas, producidos por desiguales métodos caseros30–33 y utilizando muy variables técnicas de aplicación. Sin embargo, las grandes diferencias físicas y de dinámica intravascular entre las espumas caseras y la específica microespuma, de grado farmacéutico aprobada en EE. UU., sugieren que debe observarse cautelosamente la eficacia y seguridad de uso de estas mudables y tornadizas espumas. La publicación de casos de embolismo aéreo con sintomatología isquémica, cerebrovascular después de la administración de espumas caseras, señalan la preocupación por la seguridad de su empleo sin seguir precauciones estrictas17,34–39. Como mínimo, deben acatarse las recomendaciones del Consenso de Tegernsee40, auspiciado por Kreussler, en cuanto a la obediencia por el moderado volumen máximo recomendado a inyectar.
Los inconvenientes de estas espumas abarcan desde: a) el inadecuado gas o mezcla de gases utilizados en su formación (comúnmente aire atmosférico, de alto contenido de nitrógeno, gas esencialmente insoluble en sangre a presión atmosférica) hasta incluso gases menos solubles aún41; b) el alto grado de coalescencia de sus burbujas; c) su variable cohesión interna; d) la incertidumbre o desconocimiento de la dosis de líquido esclerosante contenido en un volumen determinado de espuma y e) la inexactitud del mínimo y homogéneo diámetro posible de sus burbujas42.
La espuma de grado farmacéutico supera estos inconvenientes aunque adolece de una distribución comercial limitada a EE. UU. y de una normalizada técnica de aplicación que incorpore las cada vez más eficaces y convenientes medidas de seguridad.
Mecanismos de acciónLas burbujas son la estructura óptima para dotar al líquido esclerosante depositado en su periferia de una superficie exponencialmente mayor conforme decrece su diámetro.
Al disponer estos vectores esclerosantes de la adecuada cohesión interna, pueden físicamente desplazar la sangre contenida en el vaso actuando como un ariete neumático y después, progresivamente dispersarse en sus unidades estructurales. De esta manera, el esclerosante es homogéneamente distribuido, a concentración conocida sobre una extensa superficie endotelial y durante un tiempo controlable. La microespuma se fabrica en un rango concreto de diámetro de burbujas, con exacta composición gaseosa, precisa relación gas-líquido y con la más idónea cohesión interna. La combinación correcta de estos factores, junto con la técnica de la aplicación adecuada son, todos, parámetros claves para la seguridad y la eficacia del procedimiento.
Aunque cualquier espuma, comparada con la acción de un esclerosante líquido es más eficaz en la eliminación de venas varicosas, su seguridad no lo es. Las espumas caseras no cumplen los estándares de calidad farmacéutica; su heterogeneidad por: gases utilizados, relación gas/líquido, características físicas (compacidad, cohesión interna, coalescencia, etc.) muy variables entre ellas. Significan el deseo de disponer de manera temprana y antes de la llegada de una registrada y estandarizada especialidad farmacéutica de un elemento al que su éxito precede. Sin embargo, una especialidad farmacéutica de aplicación intravenosa, que incorpora por primera vez la inyección de gases no disueltos en sangre, no es el elemento más adecuado y seguro para ser fabricado por los médicos en nuestras sencillas clínicas.
Tratamiento en venas safenasLa primera etapa en nuestro procedimiento para el tratamiento de la vena safena mayor, consiste en la inyección de 1% de microespuma de polidocanol usando un catéter corto de calibre 20 (51mm longitud) colocado en la vena en la mitad del tercio del muslo en sentido distal. Con la pierna elevada, inyectamos el volumen requerido para llenar totalmente la vena safena mayor en el muslo (volumen de llenado). Cuando, con la sonda de ecografía, la microespuma se ve llegar a la unión safeno-femoral se detiene la inyección. Aproximadamente de 10 a 20 cc se necesitan, dependiendo de las dimensiones de la vena. La microespuma debe confinarse exclusivamente al eje tratado y evitar llenar las colaterales superficiales del muslo o pierna de esta alta concentración. Una acción endotelial moderada impide sobredosis en venas superficiales y una reacción inflamatoria indeseable.
Entonces aspiramos con una jeringa para ver el color del contenido intraluminal, renovando su contenido con un volumen apropiado de microespuma (volumen renovación) uno o dos veces, si es necesario, hasta que se obtiene un aspirado de blanco, lo que indica que el segmento contiene solo microespuma. El volumen de renovación es considerablemente más pequeño que el volumen de relleno porque el segmento de vena ya contiene microespuma, y además ya estamos en la fase de vasoespasmo reflejo que disminuye drásticamente la capacidad del vaso; solo 2 a 3 cc serán necesarios para renovar eficazmente el contenido. El pequeño exceso de microespuma inyectada drena a la vena femoral, pero es prácticamente inactivo, ya que está en el extremo proximal del «ariete neumático» que ha desplazado la sangre de la vena en la primera inyección y ha experimentado dilución e inactivación.
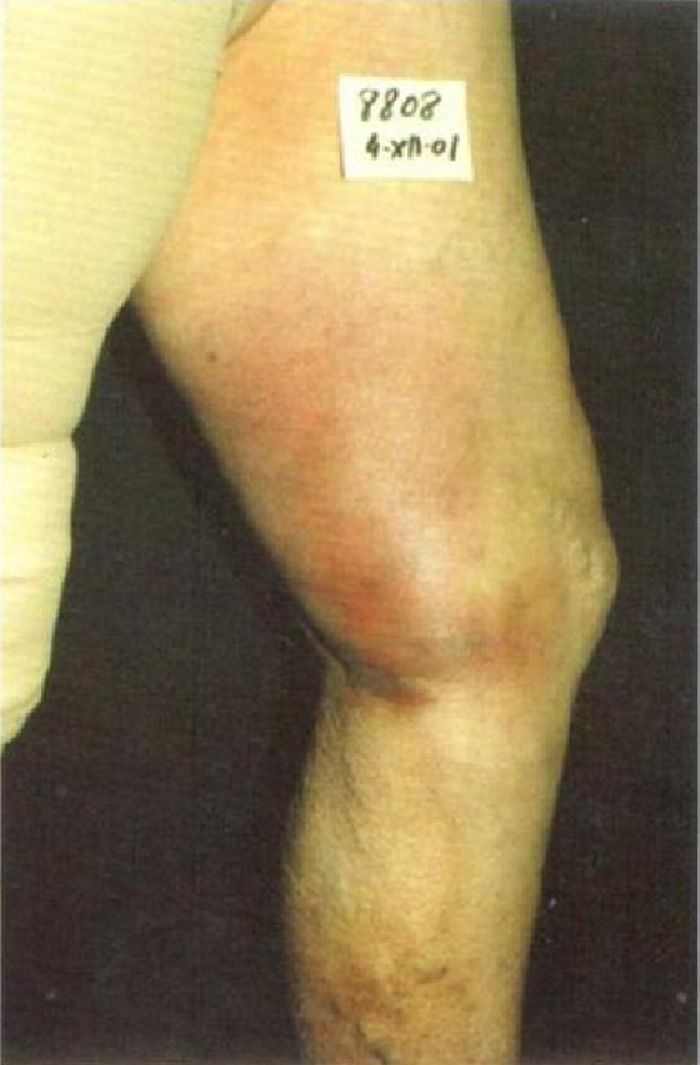
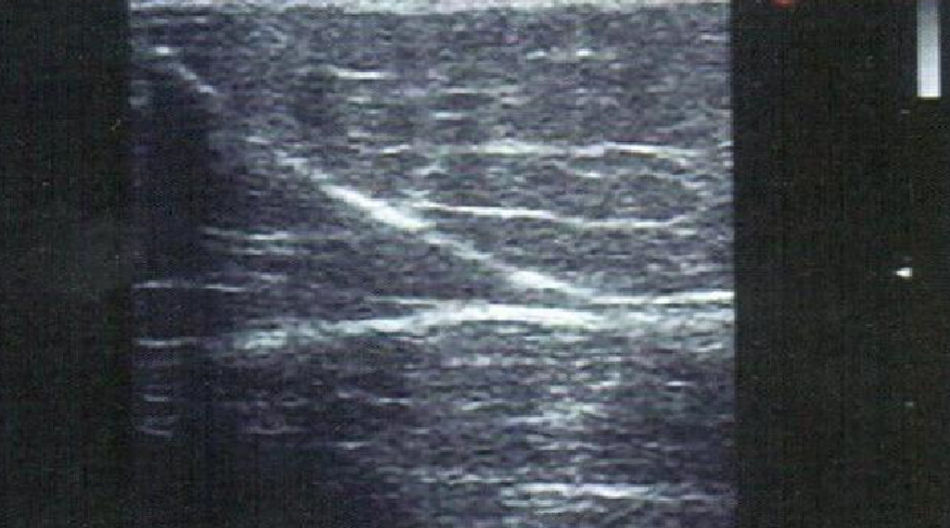
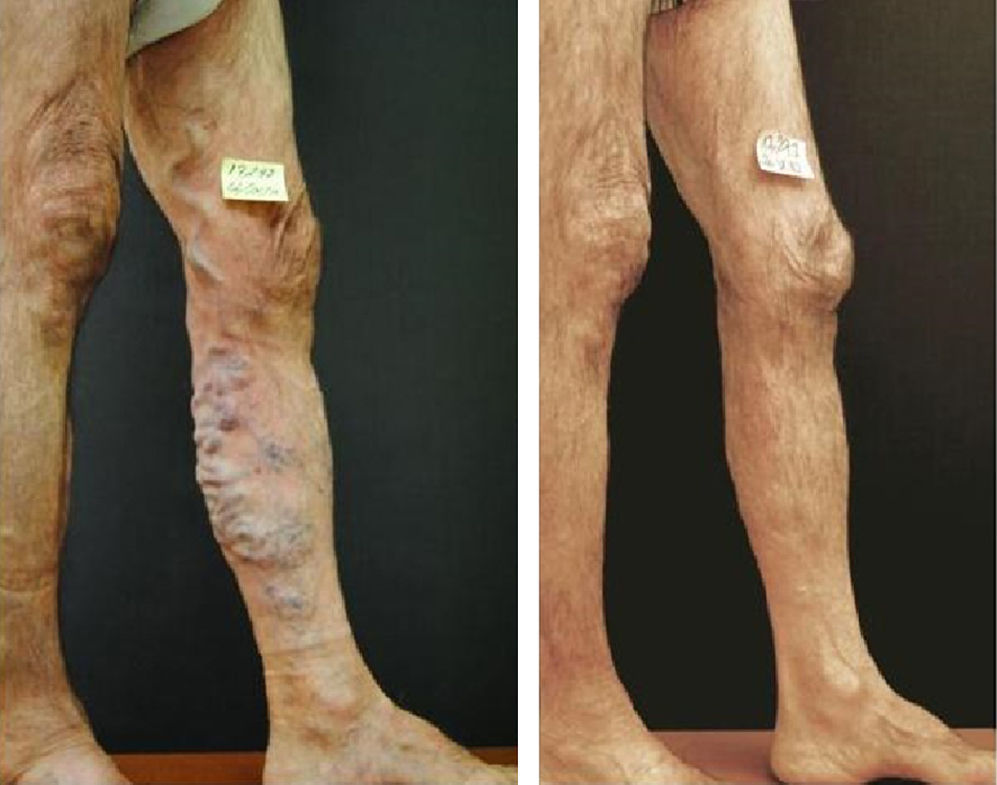
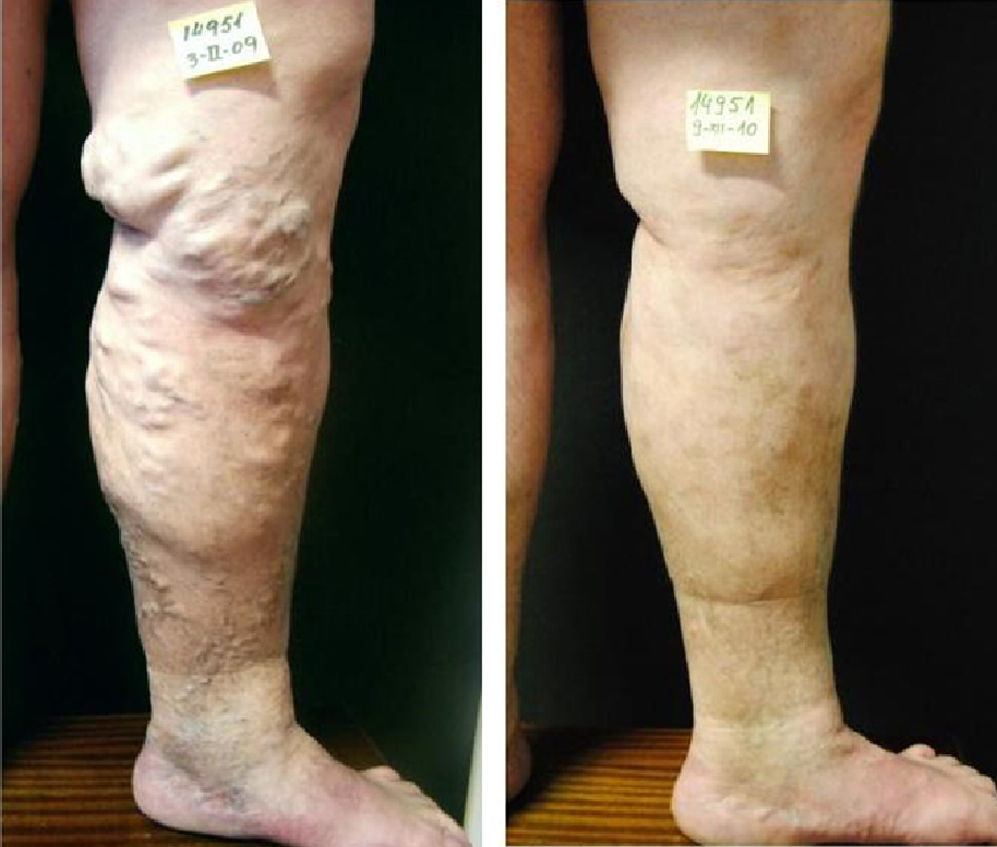
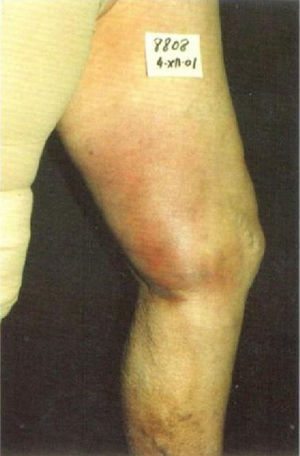
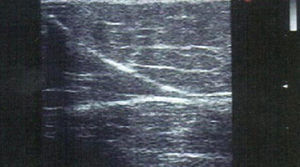
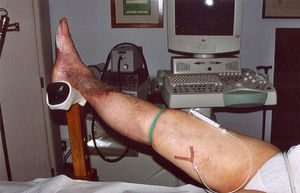
Limitaciones intravasculares de la compresión perimetralSobre la base de nuestras observaciones, utilizando ultrasonidos, las medias de compresión de 35mmHg no tienen ningún efecto sobre la morfología o función de las grandes venas varicosas. Incluso cuando en decúbito, rollos de gasa u otros cilindros no elásticos se colocan sobre el eje safeno y son fuertemente comprimidas por una venda de poca elasticidad (Peha-Haft: Hartmann), no se produce la reducción esperada del diámetro de la vena comprimida en el muslo, comprobable al volver el paciente a la posición en pie. Por lo tanto, la aplicación conjunta de estas medidas de compresión (es decir, la media+vendaje+cilindros no elásticos), no ocluyen ni disminuyen la luz del vaso. Al conservar el eje safeno varicoso sus dimensiones, no se evita la formación de un trombo tras la inyección esclerosante. Por esa razón, nosotros utilizamos el recurso técnico de la «oclusión proximal» como manera de comenzar el tratamiento de ejes dilatados. La involución de las varices situadas bajo este segmento proximal ocluido es muy marcada, evita la reacción inflamatoria secundaria y permite disminuir sensiblemente la dosis a inyectar durante el resto del tratamiento; realmente no existen varices grandes sino varices dilatadas llenas de sangre que fácilmente se cambian por varices prácticamente vacías, más pequeñas (fig. 1).
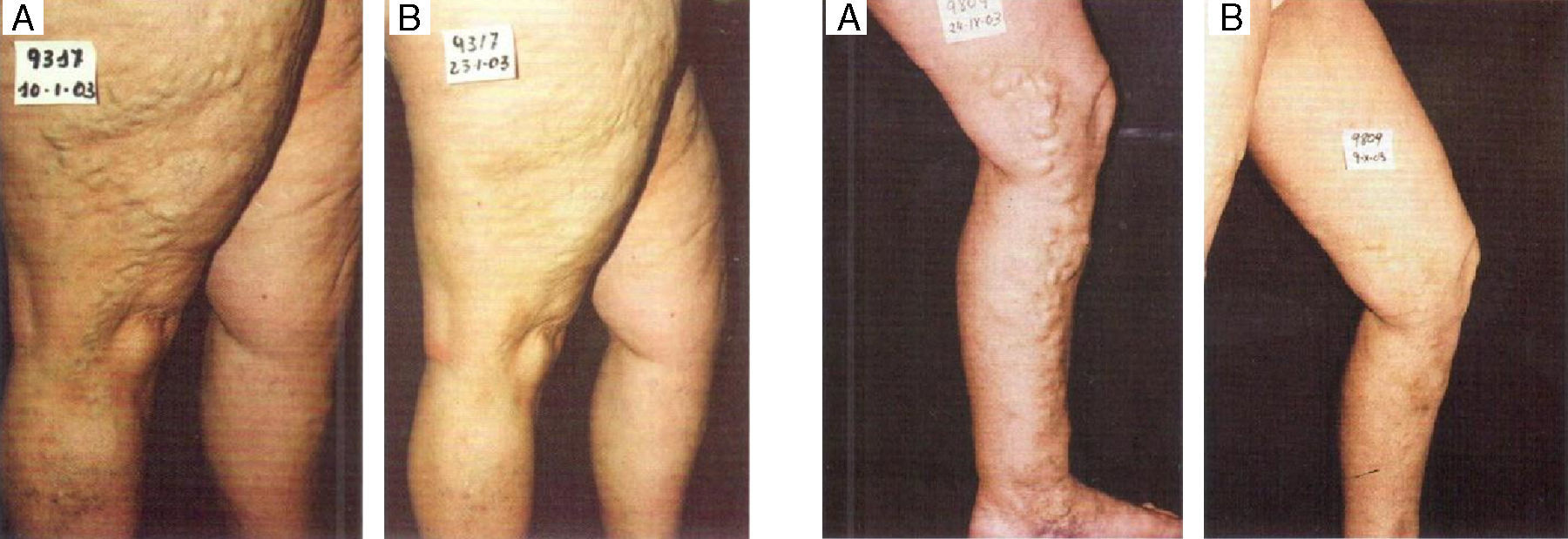
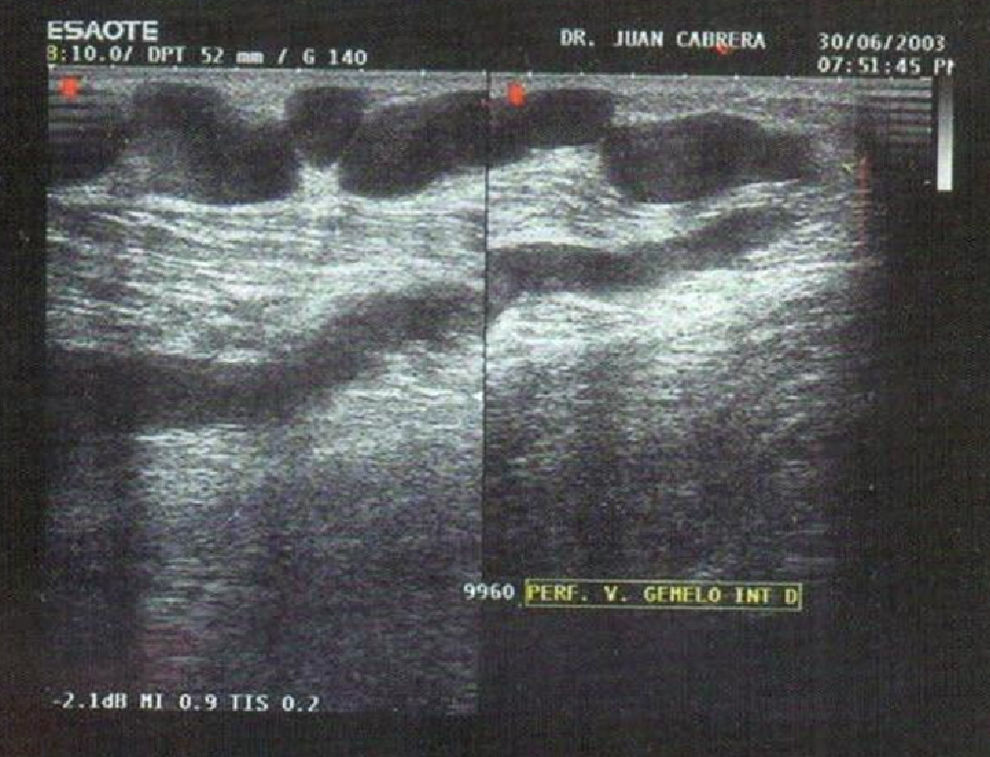
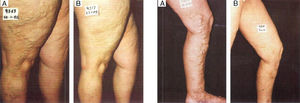
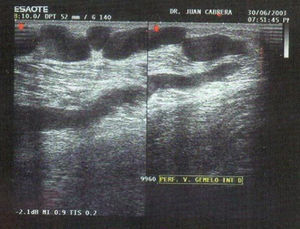
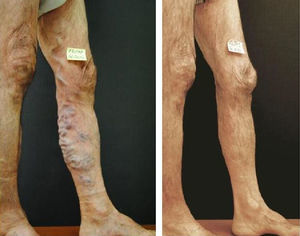
SeguimientoCuando el paciente, todavía con la media de compresión colocada, regresa a la clínica entre 10 a 15 días después del tratamiento, verificamos la oclusión del segmento safeno proximal tratado y comprobamos la involución de las venas varicosas, en muslo y pierna, subyacentes a este segmento (fig. 2A y B). Durante esta segunda sesión de tratamiento, adecuamos la concentración de esclerosante a la localización y reducido tamaño de estas venas. La apropiada concentración de polidocanol que inyectamos en estas varices tronculares involucionadas, con una aguja 25G, oscila entre 0,18 y 0,37%, este pequeño diámetro de aguja limita el flujo a través de la microespuma y resulta adecuada al menor tamaño de las varices inyectadas.
En este punto, el disminuido volumen de las venas involucionadas permite tratar un área mayor utilizando un mismo volumen de microespuma.
Tratamiento de las «venitas» de pielEl tratamiento de pequeñas venas de la piel (tread veins) requiere un especial sistema de abordarlas, usando finas agujas y baja concentración de polidocanol (0,18-0,10%). La menor capacidad espumante de esta baja concentración y el alto «stress» mecánico sufrido por las burbujas a su paso por esta fina aguja, causa disrupción de las burbujas que coalecen en mayor número, de modo que cuando se emplea alguna «espuma casera» se forman burbujas mayores con muy alta relación gas/líquido que drenan rápidamente y retornan al más estable estado de líquido y gas o bien permanecen poco tiempo en un estadio intermedio como emulsión. Si además se utiliza aire atmosférico de alto contenido en nitrógeno muy poco soluble en líquidos corporales, las complicaciones de embolismo cerebral sintomático, en pacientes con PFO, son más frecuentes35–39. La micronización de las burbujas utilizadas en el tratamiento de estas venitas y el empleo de CO2 es especialmente necesario, máxime cuando este sencillo tratamiento con fines estéticos representa el mayor monto en la práctica de muchos profesionales.
Evolución del tratamiento: esclerosis «proximal»Tras ceder el vasoespasmo reflejo, y cuando el paciente abandona la clínica, la sangre vuelve a llenar el vaso y el tamaño del trombo solo depende de las dimensiones de la vena tratada (fig. 1).
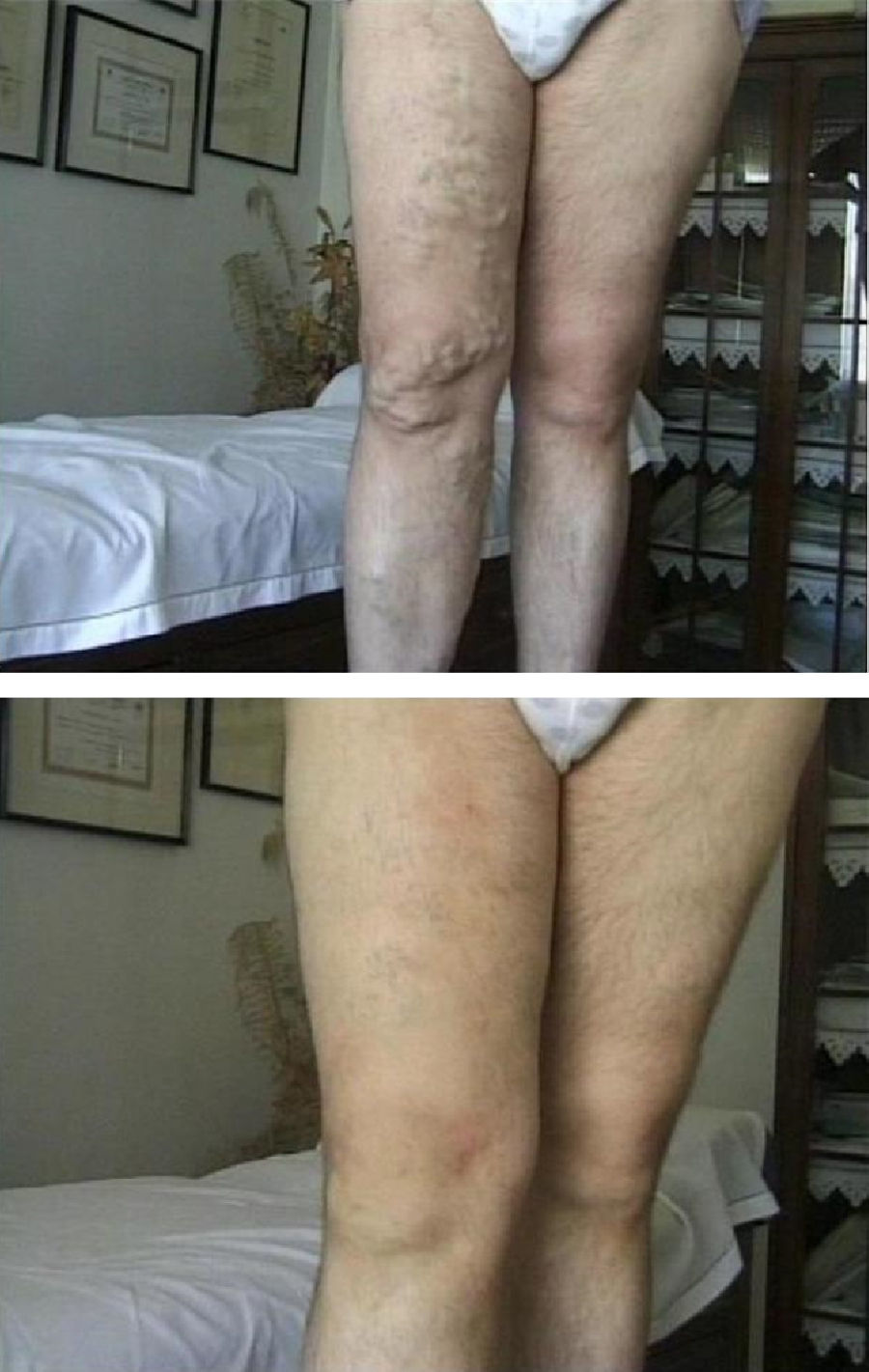
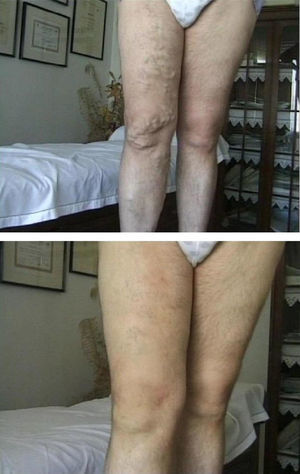
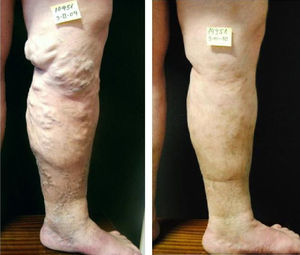
La proximidad de este trombo hemático, rico en trombina, a la piel puede producir una indeseable tromboflebitis y aumento del riesgo de pigmentación de la piel. Estas venas voluminosas deben ser inyectadas con bajas concentraciones y toda vez que su tamaño se haya reducido sobradamente tras el cierre del segmento proximal. El objetivo de esta «esclerosis proximal» no es solo un cierre más estable de la unión safeno-femoral o de la fuente proximal de reflujo sino provocar la involución de venas varicosas distales (fig. 3).
En nuestra opinión, hasta que no haya una solución para las limitaciones de la compresión perimetral, este es el enfoque más adecuado.
En las sesiones siguientes, verificamos por ultrasonidos que el segmento proximal tratado es ocluido y el diámetro de las venas superficiales tributarias, distal de la vena cerrada, ha disminuido significativamente y son tratadas con volúmenes y concentraciones adecuadas a su nuevo «estatus».
Durante los primeros años de nuestra práctica, la oclusión estable de la unión safeno-femoral fue objetivo primordial, vigilando con ecográfica su involución y progresiva fibrosis hasta la reabsorción total.
Hoy en día, prestamos poca atención a estas reminiscencias quirúrgicas; la unión safeno-femoral continúa abierta sin reflujos y con excelentes resultados a largo plazo. Esto es similar a la experiencia reportada con el procedimiento Venefit del tratamiento con láser intravenoso (EVLT) que no persigue, ni consigue (a diferencia de la espuma), la oclusión del confluente safeno-femoral. Distinto es no poder al no querer, aunque en este caso coincidan.
Medidas de seguridad en el tratamiento con microespumaManiobra de puerta cerradaLas complicaciones más temidas de la escleroterapia son la inyección intraarterial y la trombosis venosa profunda (tabla 1). El uso del eco-Doppler color ayuda a evitar la inyección intraarterial y la inyección de la safena interna en el tercio medio del muslo, la impide absolutamente. En otras localizaciones, el uso de la inyección guiada por ultrasonido ha reducido la incidencia de esta complicación, aunque el médico siempre debe estar alerta ante este peligro. La rutina es mala compañera en escleroterapia.
Medidas de seguridad
| - Conocimiento de las limitaciones de la compresión perimetral |
| - Esclerosis proximal previa |
| - Elevación del miembro |
| - Baja concentración de polidocanol |
| . Safena interna: 0,7-1% |
| . Tributarias involucionadas: 0,27-0,37% |
| - Volumen de llenado preciso |
| - Espuma libre de nitrógeno |
| - Maniobra de puerta cerrada |
| - Compresión local (úlceras en piernas) |
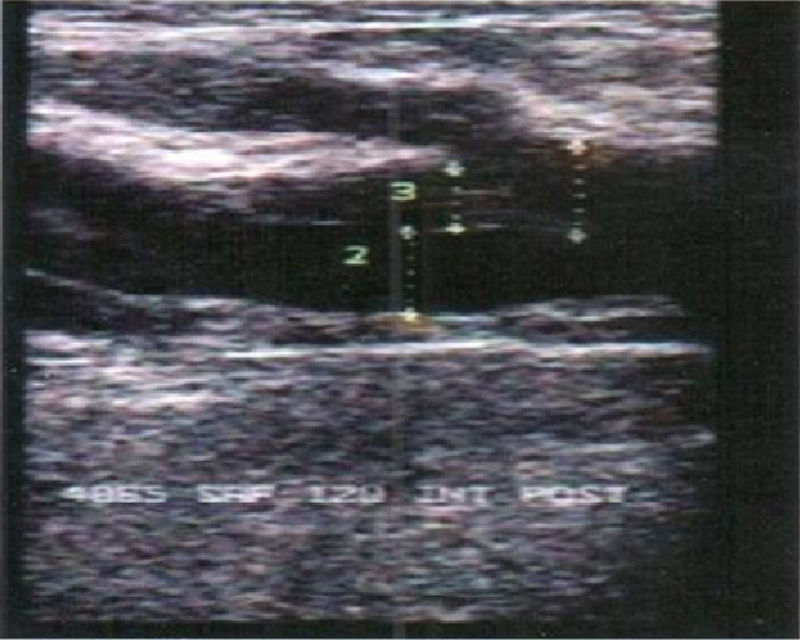
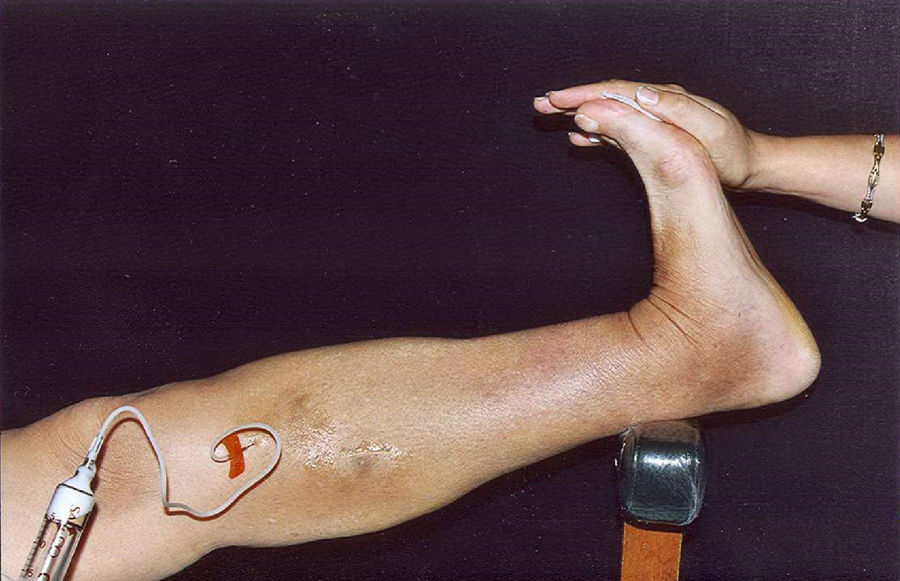
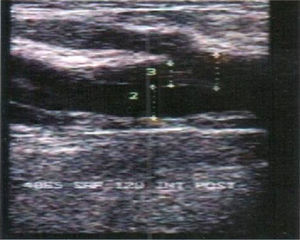
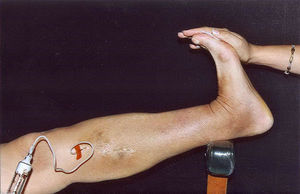
En la escleroterapia de las venas varicosas tronculares, la TVP, siquiera sea el limitado post ablation saphenous trombus extension, generalmente se produce por un trastorno de la coagulación en el paciente o por una inyección demasiado larga (fig. 4). La localización más frecuente de esta complicación es en las venas musculares de la pierna, aunque desde nuestra publicación sobre el empleo rutinario de la maniobra de puerta cerrada, esta trombosis accidental ha desaparecido de nuestra experiencia. Por otro lado en nuestra dilatada experiencia no hemos observado ninguna oclusión de la vena femoral común. Su alto flujo diluye el esclerosante y reduce las consecuencias de eventuales fallos técnicos (fig. 5), como la inyección de altas concentraciones o volúmenes de microespuma superiores a la capacidad del vaso tratado.
El punto potencialmente más controvertido de la escleroterapia en el reflujo del eje safeno son las venas perforantes con conexión directa al sistema venoso profundo: femoral, poplítea y venas gemelo interno (fig. 6). Estos lugares de reinyección muy comunes, conllevan un alto riesgo de extender la trombosis de la vena varicosa a un segmento más o menos extenso de las venas del gemelo que podría extenderse a la poplítea y vena femoral superficial.
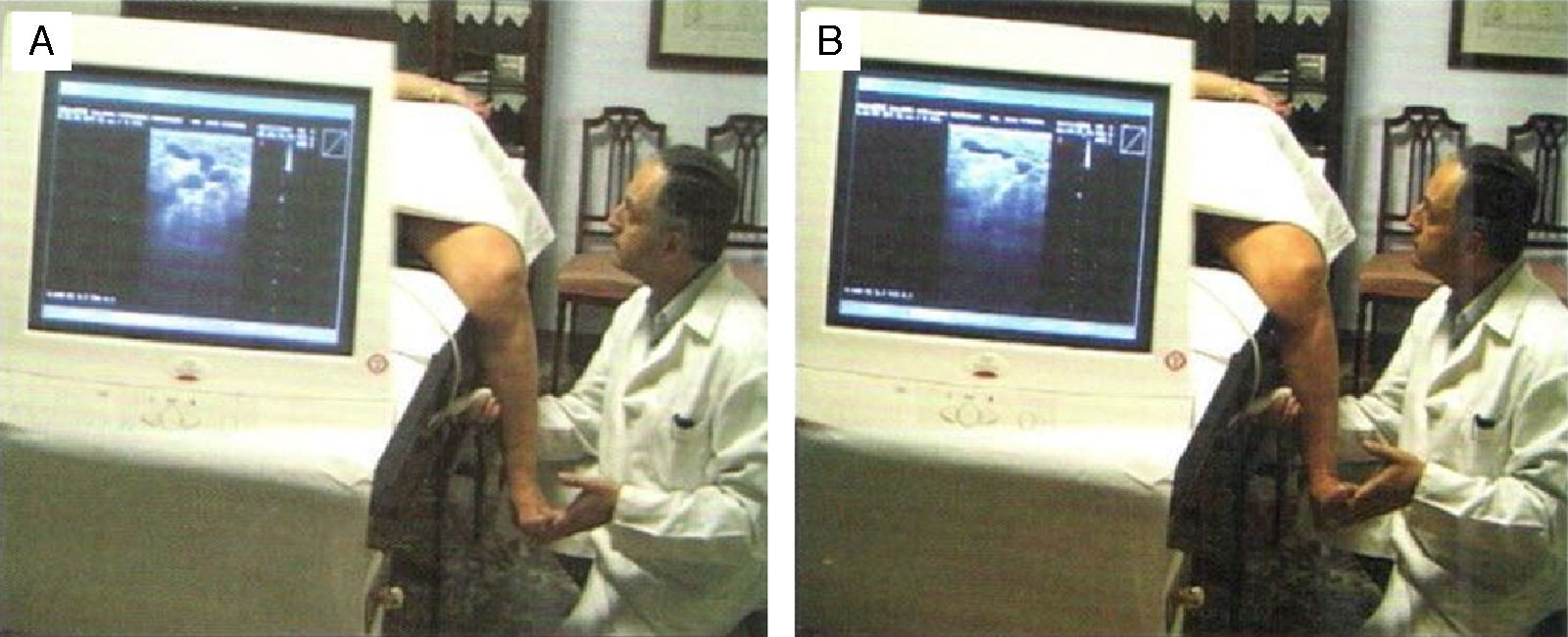
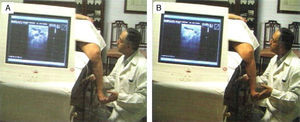
Para evitar la trombosis venosa profunda, disponemos de dos 2 sistemas preventivos. La primera es una doble medida: reducción en la ya baja concentración del esclerosante y estricta limitación del volumen inyectado, siempre adecuado a la capacidad de la vena a tratar. Las inyecciones que superen este volumen y concentraciones mayores de 0,37% son defectos técnicos que suelen pagarse. La segunda medida es cerrar la vena del gemelo durante y después de la inyección utilizando la contracción muscular de la pantorrilla. Los ultrasonidos ofrecen la visión de las venas musculares completamente cerradas cuando el paciente está en pie y así permanecen mientras que la contracción muscular causada por esta posición continúa. En posición supina, los vasos están abiertos pero la flexión dorsal activa del pie produce igual resultado cerrando estas vías de drenaje venoso (fig. 7).
La presión de la mano del médico o de un ayudante realiza la flexión dorsal del pie y se invita al paciente a presionar el pie hacia abajo haciendo flexión plantar. Esta contracción voluntaria activa es la más eficaz y se practica rutinariamente (fig. 8).
La combinación de medidas de seguridad gradualmente desarrolladas y aplicadas en nuestra práctica diaria han proporcionado una dramática reducción de pequeñas complicaciones. En nuestra última revisión sobre 10.000 pacientes con extremidades inferiores tratadas hemos observado 22 casos de TVP de venas musculares. En 10 estaban asociadas a desórdenes de coagulación y tras la incorporación de las «medidas de seguridad» no hemos observado ninguna TVP en venas musculares de las piernas en los últimos 10 años.
Composición gaseosa y tamaño de la burbujaSolubilidad y tamaño de burbujas son elementos clave de seguridad. Eckmann43 en un modelo «in vivo», estudia las diferencias de dinámica intravascular entre espumas caseras y Varisolve® (la patentada microespuma). El autor demuestra que las microburbujas no alteran el flujo de sangre arteriolar mientras que las burbujas mayores causan su completa oclusión. Esto afecta de forma sustantiva al empleo de espuma como vector de fármacos, y aunque la escleroterapia con espuma se está convirtiendo en un procedimiento generalizado, se plantearon preocupaciones cuando fueron publicados síntomas isquémicos por embolismo cerebral aéreo tras su uso en escleroterapia. El riesgo de embolismo cerebral gaseoso se incrementa especialmente en pacientes con comunicación cardiaca derecha-izquierda y tras la petición de la FDA, se estudiaron con especial atención pacientes con foramen ovale y varices tratados con Varisolve® especialmente reformulado para eliminar trazas de nitrógeno en su composición gaseosa. Se demostró que el producto no produce daño cerebral en retina y corazón44, fue demostrado por RNM con perfusión-difusión, pruebas visuales y marcadores de isquemia miocárdica.
Las espumas caseras son corrientemente formadas con la técnica de agitación entre dos jeringas que contienen O2 y CO2 en variables proporciones (tabla 2). Sin embargo la enorme fluidez del CO2 no permite tener seguridad de que permanezca en la jeringa en la que ha sido introducido y en todo caso estas espumas contienen trazas de nitrógeno suficientemente altas para producir embolias sintomáticas de gas y además carecen da las características físicas claves que definen las espuma de grado farmacéutico.
Otras medidas de seguridad: elevación de la pierna, ligadura elástica, preciso volumen de llenadoEn grandes varices, la sangre que contienen es el principal antagonista para un efectivo contacto esclerosante-endotelio, a concentración conocida. Este volumen puede ser significativamente reducido elevando la pierna, disminuyendo asimismo la presión, lo que facilita su total desplazamiento y el homogéneo contacto del esclerosante con la superficie endotelial. Sin embargo, la elevación de la pierna no detiene el flujo aferente y la dilución de la microespuma puede producirse por esas aferencias. Este muy variable flujo proximal se detiene colocando una ligadura elástica sobre cóndilo interno. Esta ligadura también evita el paso del esclerosante a las tributarias de la pierna que serán tratadas en otra sesión con la concentración adecuada a su tamaño y dependiendo del grado de involución que presenten (fig. 9).
Después del procedimiento se coloca una media 23mmHg y el paciente permanece en reposo unos minutos mientras las burbujas inyectadas drenan a la circulación general y se disuelven en la sangre, proceso en el que la enorme superficie vascular pulmonar,(alrededor de 150m2), juega un importante papel.
Cuando un determinado territorio venoso debe ser llenado de microespuma, necesitamos conocer la longitud del segmento a tratar para calcular el volumen necesario para su llenado; si la vena es gruesa y se inyecta a bajo caudal, la espuma flota en la sangre y solo contacta con la pared superior de la vena y no es suficiente, pues el segmento debe ser llenado completamente y el líquido esclerosante contactar con todo su perímetro endotelial. A este fin realizamos aspiración con la jeringa y con este simple acto conocemos su eventual dilución antes de volver a inyectarla de nuevo. La comprobación del contenido intraluminal por aspiración no debe usarse en el tratamiento de perforantes en las piernas pues la aguja está cerca de la perforante y la aspiración obtiene sangre que procede del SVP. Esta situación se resuelve no colocando la aguja sobre la perforante y adaptando el volumen de la microespuma inyectada a la capacidad de las venas tratadas.
El volumen a inyectar de las espumas «off label» es muy reducido por motivos básicos de seguridad y no son adecuadas para el tratamiento de malformaciones venosas inoperables, que suelen precisar de grandes volúmenes en cada sesión. Tras la introducción de las medidas que incrementan la eficacia y seguridad del método, la escleroterapia con microespuma es el tratamiento de elección cuando está indicada la eliminación anatómica y funcional de un extenso y complejo territorio venoso patológico (figs. 10 y 11).
Evolución a largo plazo. Estabilidad de resultadosEl talón de Aquiles de la cirugía en varices es su alto grado de recurrencias45,46 acompañadas de la agresividad e incompletos resultados de este procedimiento. Adicionalmente las venas varicosas reaparecen, ocasionalmente pocos meses después de haber sido aparentemente tratadas con éxito. Es la «herencia varicosa», muy marcada en algunos pacientes en los que estas recurrencias parecen causadas por el desarrollo de venas varicosas no visibles durante el tratamiento. Estas venas incompetentes toman la plaza de aquellas que han sido extirpadas, manteniendo continuidad hemodinámica al conectar con los vasos finales en los músculos de las piernas y así aseguran su progresión.
Salvo un perfecto tratamiento con microespuma, no existe ningún procedimiento terapéutico que pueda eliminar por sí solo todo tipo de varices. Sin embargo, la eliminación de todas las venas varicosas de un área determinada no significa que el éxito total se ha alcanzado. La victoria final puede ser reclamada solo cuando podemos estar razonablemente seguros de que también se han eliminado todas las venas que pueden constituir una fuente de recurrencia. El profundo conocimiento anatómico y funcional que aporta el eco-Doppler es una ayuda inestimable en este objetivo y con él realizamos exhaustivos exámenes en las visitas subsecuentes, entre 3 y 5 meses, después del primer tratamiento. Aquí empieza el tiempo de tratar las venas neoformadas, recanalizadas y otras que también son reveladas en las revisiones de 6, 9 y 12 meses.
Este plan de activo seguimiento proporciona la progresiva, sistemática y completa eliminación de las venas varicosas que podrían producir una recurrencia y cuya supresión a largo plazo es la clave de la estabilidad de los resultados (tabla 3). Este logro no es alcanzable con cirugía o técnicas endoluminales, pues la enfermedad varicosa está considerada un padecimiento esencialmente evolutivo, sin embargo, la aplicación correcta del tratamiento puede reducir acentuadamente su recurrencia.
Nuestro objetivo final es hacer nuestros resultados estables a largo plazo e incorporar a nuestra técnica mejoras que disminuyan el tiempo de tratamiento y que sea más cómodo para el paciente; el tipo de compresión aplicada es de importancia crítica para la comodidad, y puesto que de la aplicación de una compresión fuerte no obtenemos beneficios, usamos medias que ejercen una compresión moderada. Nunca más de 23mmHg.
La disponibilidad de una espuma de grado farmacéutico, micronizada, homogénea, estable a largo tiempo y reproducible, es crucial, ya que permite el desarrollo de un protocolo de tratamiento estándar que facilitaría la comparación de los resultados obtenidos por diferentes grupos (tabla 4).
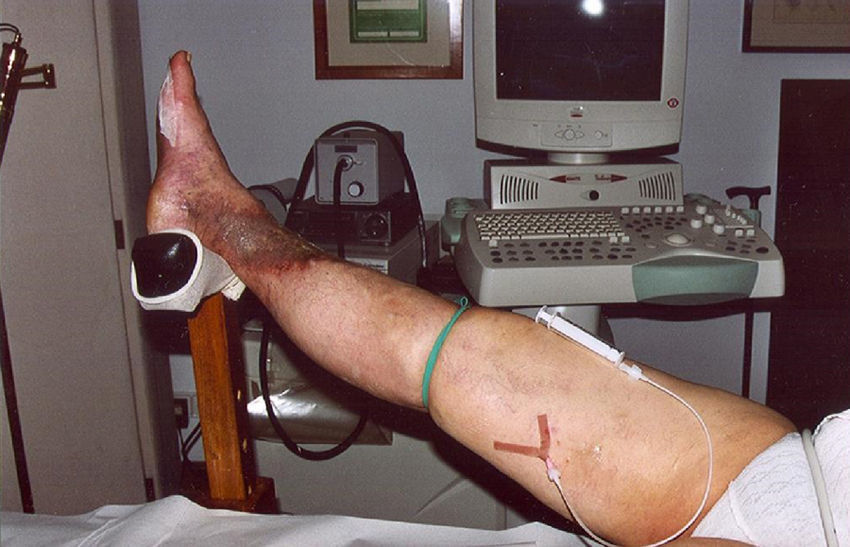
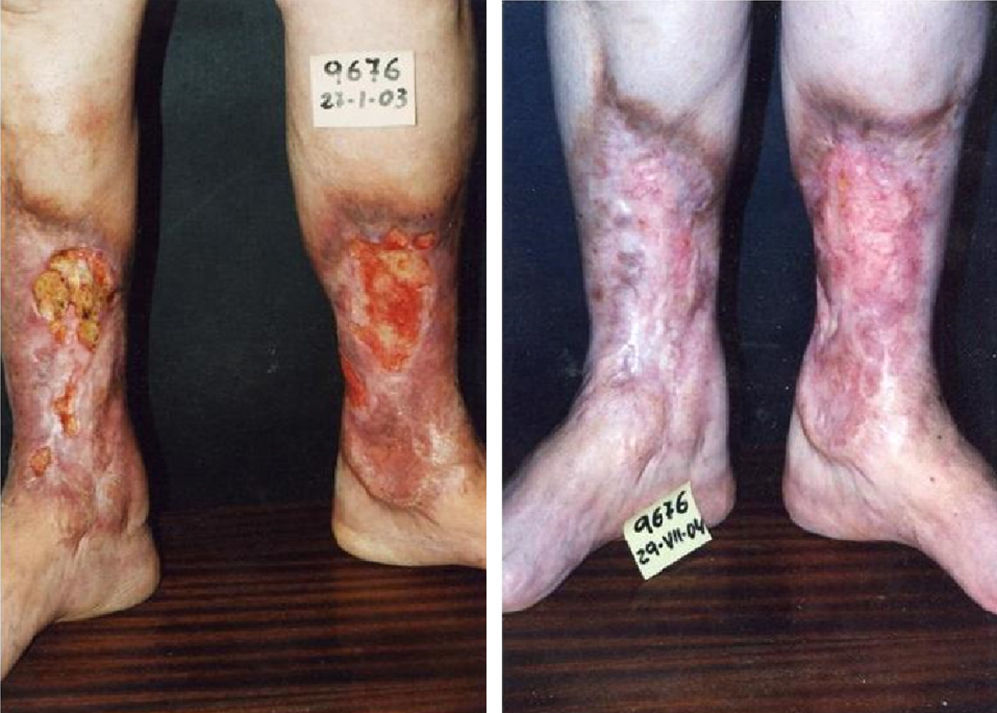
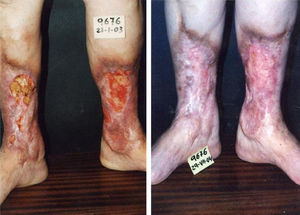
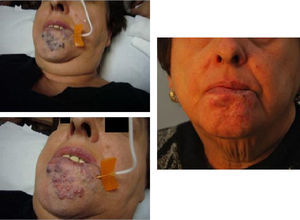
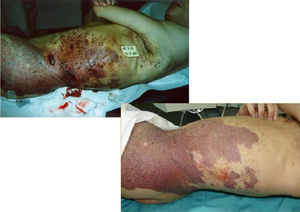
Otras indicaciones de la microespumaÚlceras venosas, malformaciones venosas, varicoceleComo se mencionó antes, la microespuma se ha utilizado también con excelentes resultados en pacientes con úlceras varicosas en las piernas y malformaciones venosas. Nuestros resultados muestran que la escleroterapia con microespuma guiada por ultrasonidos es altamente eficaz y logra el cierre estable de úlceras venosas (fig. 12) en pacientes de incluso edad avanzada28.
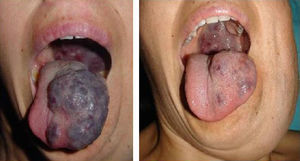
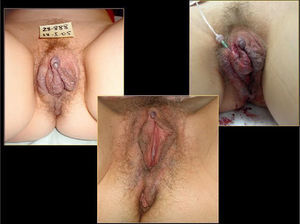
Además, hemos obtenido muy buenos resultados en pacientes con malformaciones venosas11. En las malformaciones venosas de mediano a pequeño tamaño pudimos eliminar completamente la lesión, y en los que presentaron gran malformación venosa logramos una importante mejoría clínica y significativa reducción en el tamaño de la malformación. En estos pacientes es necesario inyectar un volumen de espuma elevado y proporcional al tamaño de la malformación. El excelente equilibrio gas/líquido y el mínimo diámetro de burbuja de nuestra microespuma nos permite inyectar hasta 80cc en estos pacientes en una sesión. Nunca hemos sufrido complicaciones mayores en estos pacientes con malformaciones venosas (figs. 13–16).
En varicocele, a pesar de que tenemos una limitada experiencia, hemos obtenido muy buenos resultados con significativa mejora de la calidad del esperma. El enfoque terapéutico consiste en la inyección de polidocanol 1% con una aguja 21G colocada en la vena espermática en el canal inguinal. La inserción de la aguja y la administración de la microespuma se realiza en decúbito supino mientras el paciente realiza la maniobra de Valsalva. El incremento de presión abdominal hace que la microespuma progrese en sentido distal y al interrumpir el Valsalva, retrocede en sentido proximal al punto de inyección evitando de este modo tromboflebitis del plexo pampiniforme.
En las visitas de control confirmamos la oclusión de varicocele con examen físico y eco-Doppler color.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesEl autor declara no tener ningún conflicto de intereses.