El cambio en el paradigma de tratamiento en la cirugía vascular se ha producido gracias al desarrollo de las técnicas endovasculares, que se han ido posicionado como alternativa de tratamiento respecto a técnicas quirúrgicas tradicionales en múltiples sectores de nuestra especialidad. Pero el sector carotídeo supone una excepción a este hecho, ya que los resultados de las técnicas mínimamente invasivas aún no han conseguido igualar a los de la técnica quirúrgica tradicional, la endarterectomía carotídea. El objetivo de este artículo de opinión es el de defender la adopción de la endarterectomía carotídea quirúrgica como la técnica de elección para el tratamiento de la estenosis carotídea frente al stent carotídeo, mediante una revisión no sistemática de la literatura, de los ensayos clínicos de mayor impacto y de las principales recomendaciones de guías clínicas internacionales.
The paradigm of treatment in vascular surgery is changing, due to the huge advances in endovascular techniques, as well as in the new endovascular skills of the next generations of vascular surgeons. Minimal invasive techniques are becoming the first line of treatment in many vascular sectors, but this assumption is still very controversial in carotid bifurcation disease, where the results of angioplasty plus stenting strategy are not as good at it seems when this technique is compared with carotid endarterectomy.
The aim of this paper is to justify the adoption of the carotid endarterectomy as the first line treatment for carotid bifurcation disease in the endovascular era. This is based on a non-systematic review of the literature, the analisis of the main randomized controlled trials published, and the guidelines of the most relevant scientific committees.
El infarto cerebral/ictus es una de las 5 principales causas de muerte y la primera causa de incapacidad crónica en países desarrollados y la estenosis severa de las arterias carotídeas extracraneales está involucrada en el 20-30% de los infartos cerebrales1. La prevención secundaria del ictus puede realizarse de 2 modos: mediante la optimización del tratamiento médico adecuado al mecanismo subyacente (antiagregación, anticoagulación) y la modificación de los factores de riesgo implicados (cese de hábito tabáquico, control de hipertensión, dislipidemias, etc…) y mediante la identificación y el tratamiento activo de la aterosclerosis carotídea si esta es la causa a la que se atribuye la etiología. En la actualidad, las opciones para el tratamiento activo de la estenosis carotídea son la endarterectomía carotídea quirúrgica (ECA) y la terapia endovascular mediante angioplastia y stenting carotídeo. La ECA se ha considerado tradicionalmente como la técnica gold standard de tratamiento apoyado en los resultados de estudios aleatorizados históricos que demostraron su eficacia en prevención de eventos neurológicos frente al tratamiento médico aislado. Los avances en las técnicas endovasculares en el sector carotídeo en los últimos años han tenido como consecuencia la mejora de resultados, con estudios que han presentado resultados similares a la ECA en algunos subgrupos de pacientes con características específicas. De este modo, el tratamiento endovascular se ha llegado considerar por algunos grupos de especialistas implicados en el tratamiento de esta patología, como radiólogos intervencionistas, neurólogos, cardiólogos y cirujanos vasculares como una posible alternativa de tratamiento a la endarterectomía para pacientes con estenosis carotídea, tanto sintomática como asintomática2. Las nuevas tecnologías y la inversión de la industria se centran en el desarrollo de terapias endovasculares mínimamente invasivas, como observamos en otros sectores de la patología arterial periférica. Pero la cuestión es, si a día de hoy y con los datos disponibles, puede considerarse el tratamiento endovascular como alternativa válida a la endarterectomía carotídea, si entendemos como alternativa una técnica con resultados similares o no inferiores para la mayoría de los pacientes.
Este artículo de opinión está basado en una revisión no sistemática de la literatura, analizando revisiones de la literatura y artículos originales publicados en los últimos 10 años, los más importantes ensayos clínicos aleatorizados y no aleatorizados que comparan los resultados de la ECA y el stenting carotídeo tanto en pacientes sintomáticos como asintomáticos y las recomendaciones de las principales guías clínicas publicadas por prestigiosas sociedades médicas internacionales.
El objetivo de este artículo es el de defender y justificar la posición adoptada por muchos grupos de trabajo, como el nuestro: y es que en la era endovascular, el tratamiento mediante la ECA quirúrgica debería seguir siendo considerado el tratamiento de elección para la mayoría de los pacientes con estenosis carotídea.
Ensayos clínicos aleatorizados que comparan el tratamiento activo en la estenosis carotídea: ¿cómo comparar ensayos clínicos con diseños tan diferentes y con casi 20 años de diferencia entre ellos?Los primeros ensayos clínicos fueron diseñados hace casi 20 años con la idea de evaluar el beneficio del tratamiento activo mediante la endarterectomía carotídea vs. el tratamiento médico aislado (antiagregación simple con AAS 80-325mg). Estos son los conocidos ensayos North American Symptomatic Carotid Endarterectomy Trial (NASCET), European Carotid Surgery Trial (ECST), Asymptomatic Carotid Atherosclerosis Study (ACAS), Asymptomatic Carotid Atherosclerosis Trial (ACST), y Veteran Affairs Cooperative Study Group (VA Cooperative)3-7. Los primeros ensayos, NASCET y ECST estudiaron exclusivamente a pacientes sintomáticos. El NASCET, publicado en 1991, enroló a 2.885 pacientes sintomáticos con grados de estenosis (30-99%); en sus resultados se observó una incidencia de infarto cerebral ipsolateral en el 9,0% de los pacientes que recibieron endarterectomía vs. el 26% en el brazo de tratamiento médico, y demostró una reducción del riesgo absoluto de 17,0 (p<0,001) en la cohorte de pacientes con estenosis (70-99%) sometidos a ECA. También demostró una disminución del riesgo absoluto del 16,5 (p<0,001) en la incidencia de muerte o infarto en el brazo de la ECA (15,8%) vs. la antiagregación aislada (32,3%). En cuanto al efecto del sexo, NASCET demostró que las mujeres tienen menos riesgo de infarto cerebral con tratamiento médico y que el beneficio de la intervención mediante ECA en mujeres sintomáticas no es significativo respecto al tratamiento médico aislado (14% vs. 15%) El ECST, publicado en 1998, enroló a 3.024 pacientes sintomáticos y mostró también una reducción de riesgo absoluto de eventos neurológicos ipsolaterales en la CEA vs. la antiagregación del 18,7 y de infarto o muerte del 21,2, en cohortes de pacientes con estenosis de alto grado (70-99%). Los ensayos ACAS, publicado en 1995 y enrolando a 1.662 pacientes, ACST publicado en 2004, con 3.120 pacientes, y VA Cooperative, en 1992, con 440 pacientes, se diseñaron para estudiar a pacientes asintomáticos con estenosis por encima del 50-60%. Estos ensayos también mostraron reducciones en el riesgo absoluto de infarto ipsolateral, infarto o muerte en el brazo de la endarterectomía, aunque mucho menores que en pacientes sintomáticos. En el ACAS, que fue detenido tempranamente debido al beneficio observado en la ECA a los 2,7 años de seguimiento medio, la reducción de riesgo absoluto fue del 6,3 (p=0,08) en el ACST, del 5,4 (p<0,0001), y en el VA Cooperative de 3,0 (p>0,05). En ambos estudios, ACAS y ACST, se confirmó que el beneficio de la intervención mediante ECA es menor en mujeres; en el ACAS las mujeres presentaron mayor riesgo quirúrgico (3,6% vs. 1,4%) y no beneficio en la reducción de infarto cerebral estimada a 5 años (7,3% vs. 8,7%), y en el ACST la reducción absoluta de infarto no perioperatorio fue menor en mujeres que en hombres (4,1% vs. 8,2%).
Estos ensayos clínicos sirvieron en su momento para demostrar el beneficio de la intervención activa respecto a la opción de solo tratamiento médico (antiagregación con AAS a dosis bajas, 80-325mg) y han sustentado la endarterectomía carotídea como el tratamiento de elección para la mayoría de los pacientes. Resultados que se observaron especialmente beneficiosos en la reducción significativa de ictus ipsolaterales en pacientes sintomáticos con estenosis severas respecto a pacientes asintomáticos en los que la reducción absoluta de eventos fue menor5.
Los ensayos de los últimos años se han diseñado con un objetivo distinto: el de comparar tanto en pacientes sintomáticos como en asintomáticos los resultados de una técnica estandarizada, la endarterectomía carotídea, con los de una técnica endovascular mínimamente invasiva y emergente, la angioplastia y stent carotídeo. Entre los ensayos clínicos más importantes destacamos los aleatorizados Stenting and Angioplasty with Protection in Patients at High Risk for Endarterectomy (SAPPHIRE) trial, el Endarterectomy versus stenting in patients with symptomatic severe carotid stenosis (EVA-3S), el Stent-Protected Angioplasty versus Carotid Endarterectomy (SPACE), el International Carotid Stenting Study (ICSS) y especialmente el estudio Carotid Revascularization Endarterectomy Versus Stenting Trial (CREST)8-12. Deben citarse también otros estudios importantes, aunque no aleatorizados, y registros multicéntricos publicados, como el Protected carotid stenting in high-surgical-risk patients (ARCHeR Study), el Carotid artery revascularization in high surgical risk patients with the NexStent and the Filterwire EX/EZ (CABERNET Study) y los estudios Medtronic AVE Self-expanding CaRotid Stent System with distal protection In the treatment of Carotid stenosis II y II13-15.
El ensayo SAPPHIRE aleatorizó a 334 pacientes, combinando asintomáticos con estenosis>50% y asintomáticos con estenosis >80%. Los considerados de alto riesgo que fueron desestimados para cirugía fueron seleccionados para el brazo de tratamiento endovascular mediante angioplastia y stent con empleo de dispositivo de protección de embolización distal. Aunque este ensayo fue detenido tempranamente por culpa del bajo número de pacientes enrolados, los resultados en mortalidad a 30 días, infarto ipsolateral o muerte fueron no inferiores en el brazo del tratamiento con stent (12,2% vs. 20,1% p=0,053, p=0,004 para no inferioridad). La diferencia numérica a favor del stent carotídeo se explicó por la menor incidencia de infarto de miocardio y muertes tardías, mientras que las frecuencias de infarto ipsolateral (4,3% vs. 5,3%) o cualquier infarto (6,2% vs. 7,9%) fueron similares.
Estos resultados y los de otros estudios no aleatorizados, como el ARCHeR, empleando dispositivos de protección embolígena distal, apoyaron el empleo del stent carotídeo como una alternativa a la endarterectomía en pacientes considerados de alto riesgo quirúrgico, e incluso esta actitud terapéutica la vemos reflejada en las recomendaciones de guías clínicas de sociedades médicas internacionales.
Sin embargo, la interpretación posterior de los datos de los numerosos y tan variados ensayos clínicos ha provocado controversias y la existencia de numerosos dilemas a la hora de generalizar sus resultados en la práctica clínica.
Al hecho de que algunos estudios tuvieron que detenerse precozmente por la baja inclusión de pacientes, como el ya mencionado estudio SAPPHIRE, hay que sumar que en otros ensayos comparando la ECA vs. el stent carotídeo y diseñados con pacientes con riesgo estándar, como el ensayo EVA-3S, los resultados del brazo endovascular obligaron a detener el estudio por cuestiones de seguridad, ya que a los 30 días la incidencia de infarto o muerte fueron significativamente mayores en el brazo del stent (9,6% vs. 3,9%). Aunque para interpretar correctamente estos datos hay que tener en cuenta que en este estudio no se emplearon sistemas de protección embolígena en el primer tercio de los pacientes enrolados, que la experiencia de los operadores de stent carotídeo era muy variada o que el IAM no fue recogido como resultado primario.
El estudio aleatorizado SPACE también tuvo que ser detenido precozmente, tras aleatorizar a solo 1.200 de los 1.900 previstos, debido a la baja potencia estimada del estudio y a problemas de financiación. Este estudio tiene ciertas similitudes con el estudio EVA 3-S en cuanto a que en solo un 27% de los pacientes se emplearon dispositivos de protección de embolización y a la variabilidad de la experiencia de los operadores. A pesar de estas limitaciones, se observaron similares resultados a los 30 días en infarto o muerte en los brazos de ECA (6,8%) vs. stent (6,3%), pero se destaca en el análisis de los resultados de este estudio que en mayores de 75 años (n=225) se observó una importante diferencia a favor de la endarterectomía en infarto o muerte respecto a la técnica endovascular (11,0% vs. 7,5%). Aquí aparece la controversia de que observamos peores resultados en el tratamiento con angioplastia y stent carotídeo en pacientes de edad avanzada, pacientes que normalmente son considerados con un riesgo mayor para cirugía y, por tanto, en los que otros estudios aleatorizados, como el ensayo SAPPHIRE, se recomendaba tratamiento endovascular.
En los resultados internos del estudio aleatorizado ICSS, que enroló a 1.713 pacientes sintomáticos con riesgo quirúrgico estándar, se observaron similares resultados en muerte o infarto incapacitante en los brazos stent y endarterectomía (4,0% vs. 3,2%, p=0,34) pero mayor incidencia de muerte, infarto cerebral o infarto de miocardio periprocedimiento (8,5% vs. 5,2%, p=0,006) en el brazo de tratamiento endovascular. Este estudio también destaca por sus importantes limitaciones, entre otras el empleo de un sistema de protección embolígena en solo el 72% de los pacientes, e incluso la exclusión de 2 centros que participaban en ensayo debido a su alta incidencia de infartos cerebrales y muerte en el brazo del stent carotídeo.
Hasta la fecha, el mayor ensayo aleatorizado que ha comparado la ECA vs. el stent es el CREST, con 2.502 pacientes aleatorizados y con importantes diferencias en diseño respecto a los 3 ensayos anteriores: EVA 3-S, SPACE e ICSS. En primer lugar, los investigadores del brazo del stent carotídeo presentaron un riguroso proceso de selección y acreditación, además de demostrar experiencia clínica y análisis de sus resultados en un preestudio monitorizado, de modo que solo un 52% de los investigadores del grupo de stent carotídeo que aplicaron a participar en este ensayo fueron aceptados. En segundo lugar, el sistema de protección embolígena distal fue requerido en el CREST por protocolo de estudio y empleado en el 96% de los pacientes. Y en tercer lugar, la importancia del infarto de miocardio fue reconocida y se incluyó como end point primario del estudio. Aunque el CREST fue diseñado inicialmente como estudio de pacientes sintomáticos debido al bajo enrolamiento y a los cambios en las prácticas clínicas a lo largo del tiempo, se incluyó a pacientes asintomáticos tardíamente, de modo que finalmente representan el 47% de la población del estudio. En sus resultados, no se observó diferencia en los eventos primarios: muerte, infarto, infarto de miocardio a 30 días o infarto ipsolateral a 4 años (7,2% vs. 6,8%, p=0,51) entre el tratamiento con stent o la ECA. Las diferencias residen en que se observó un mayor número de eventos tipo infarto miocardio tras la ECA (1,1% vs. 2,3%, p=0,01) y un mayor número de infartos cerebrales tras el stent carotídeo (4,1% vs. 2,3%, p=0,01). Es interesante destacar que los análisis de calidad de vida realizados en este aspecto estiman un mayor impacto en calidad de vida tras el infarto cerebral que tras el infarto de miocardio, pero sin embargo la aparición de un evento isquémico coronario se asocia a un mayor incremento en el riesgo de mortalidad que el evento neurológico. En el ensayo CREST también se demostró una interacción significativa entre el tratamiento asignado y la edad, como en el EVA-3S, con un mayor riesgo de infarto cerebral asociado al stent carotídeo en mayores de 70 años.
Tras considerar todos estos ensayos, realizados a lo largo de los últimos 20 años, y tan diferentes entre sí unos de otros, es difícil la comparación de resultados y la obtención de conclusiones claras. En pacientes con riesgo quirúrgico estándar, la evidencia disponible indica un ligero mayor riesgo de infarto periprocedimiento en el tratamiento con stent carotídeo, especialmente en pacientes de edad avanzada. Pero este riesgo de presentar eventos neurológicos es inferior en operadores con experiencia y con el empleo de rutina de sistemas de protección cerebral, por lo que debe ser valorado el empleo de stent carotídeo en casos de pacientes con mayor riesgo de evento coronario isquémico y complicaciones cardiacas, ya que estas provocan un mayor impacto largo plazo en la mortalidad y son inferiores que en los pacientes sometidos a endarterectomía carotídea. En pacientes asintomáticos las lecciones obtenidas de estos ensayos es que los beneficios de la intervención, ya sea mediante endarterectomía o stent, son claramente inferiores respecto a los sintomáticos.
Los resultados de estos ensayos han comparado la ECA vs. el tratamiento médico o la ECA vs. el stent carotídeo, pero pueden ponerse en cuestión actualmente ya que la mejora en el tratamiento médico también ha sido exponencial en los últimos años. Gracias a una mejor y más continuada estrategia de antiagregación plaquetaria, a la confirmación de los beneficios de la terapia antilipidemiante con estatinas, y el control estricto de la presión arterial, es de esperar la mejora de los resultados en pacientes que adoptan la mejor terapia médica posible (best medical treatment [BMT]).
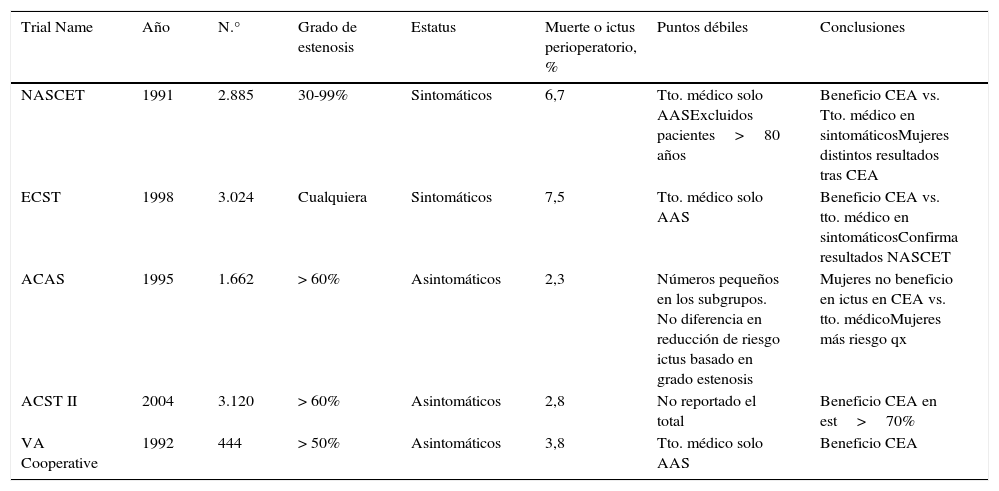
En las siguientes tabla, resumimos los ensayos más importantes publicados hasta la fecha, destacando sus puntos fuertes y débiles y algunas de sus conclusiones (tablas 1 y 2).
Resumen comparativo de principales ensayos aleatorizados publicados comparando tratamiento revascularizador con endarterectomía carotídea vs. tratamiento médico conservador (AAS a dosis 80-325mg)
| Trial Name | Año | N.° | Grado de estenosis | Estatus | Muerte o ictus perioperatorio, % | Puntos débiles | Conclusiones |
|---|---|---|---|---|---|---|---|
| NASCET | 1991 | 2.885 | 30-99% | Sintomáticos | 6,7 | Tto. médico solo AASExcluidos pacientes>80 años | Beneficio CEA vs. Tto. médico en sintomáticosMujeres distintos resultados tras CEA |
| ECST | 1998 | 3.024 | Cualquiera | Sintomáticos | 7,5 | Tto. médico solo AAS | Beneficio CEA vs. tto. médico en sintomáticosConfirma resultados NASCET |
| ACAS | 1995 | 1.662 | > 60% | Asintomáticos | 2,3 | Números pequeños en los subgrupos. No diferencia en reducción de riesgo ictus basado en grado estenosis | Mujeres no beneficio en ictus en CEA vs. tto. médicoMujeres más riesgo qx |
| ACST II | 2004 | 3.120 | > 60% | Asintomáticos | 2,8 | No reportado el total | Beneficio CEA en est>70% |
| VA Cooperative | 1992 | 444 | > 50% | Asintomáticos | 3,8 | Tto. médico solo AAS | Beneficio CEA |
Modificado de Circulation. Cutlip DE, Pinto DS Extracranial Carotid Disease Revascularization.Circulation. 2012;126:2636-2644.
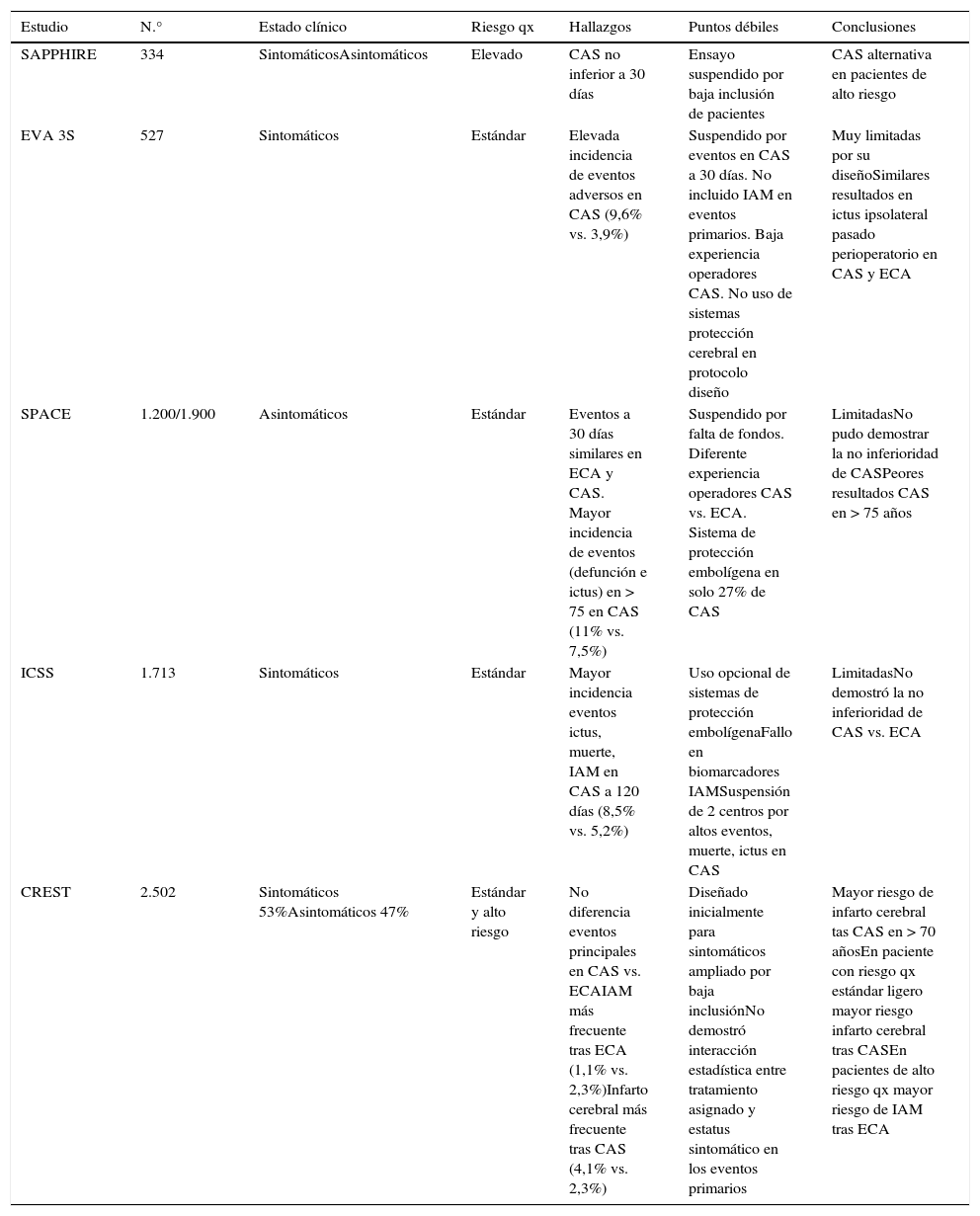
Resumen comparativo de principales ensayos aleatorizados publicados comparando endarterectomía carotídea vs. angioplastia y stent carotídeo
| Estudio | N.° | Estado clínico | Riesgo qx | Hallazgos | Puntos débiles | Conclusiones |
|---|---|---|---|---|---|---|
| SAPPHIRE | 334 | SintomáticosAsintomáticos | Elevado | CAS no inferior a 30 días | Ensayo suspendido por baja inclusión de pacientes | CAS alternativa en pacientes de alto riesgo |
| EVA 3S | 527 | Sintomáticos | Estándar | Elevada incidencia de eventos adversos en CAS (9,6% vs. 3,9%) | Suspendido por eventos en CAS a 30 días. No incluido IAM en eventos primarios. Baja experiencia operadores CAS. No uso de sistemas protección cerebral en protocolo diseño | Muy limitadas por su diseñoSimilares resultados en ictus ipsolateral pasado perioperatorio en CAS y ECA |
| SPACE | 1.200/1.900 | Asintomáticos | Estándar | Eventos a 30 días similares en ECA y CAS. Mayor incidencia de eventos (defunción e ictus) en > 75 en CAS (11% vs. 7,5%) | Suspendido por falta de fondos. Diferente experiencia operadores CAS vs. ECA. Sistema de protección embolígena en solo 27% de CAS | LimitadasNo pudo demostrar la no inferioridad de CASPeores resultados CAS en > 75 años |
| ICSS | 1.713 | Sintomáticos | Estándar | Mayor incidencia eventos ictus, muerte, IAM en CAS a 120 días (8,5% vs. 5,2%) | Uso opcional de sistemas de protección embolígenaFallo en biomarcadores IAMSuspensión de 2 centros por altos eventos, muerte, ictus en CAS | LimitadasNo demostró la no inferioridad de CAS vs. ECA |
| CREST | 2.502 | Sintomáticos 53%Asintomáticos 47% | Estándar y alto riesgo | No diferencia eventos principales en CAS vs. ECAIAM más frecuente tras ECA (1,1% vs. 2,3%)Infarto cerebral más frecuente tras CAS (4,1% vs. 2,3%) | Diseñado inicialmente para sintomáticos ampliado por baja inclusiónNo demostró interacción estadística entre tratamiento asignado y estatus sintomático en los eventos primarios | Mayor riesgo de infarto cerebral tas CAS en > 70 añosEn paciente con riesgo qx estándar ligero mayor riesgo infarto cerebral tras CASEn pacientes de alto riesgo qx mayor riesgo de IAM tras ECA |
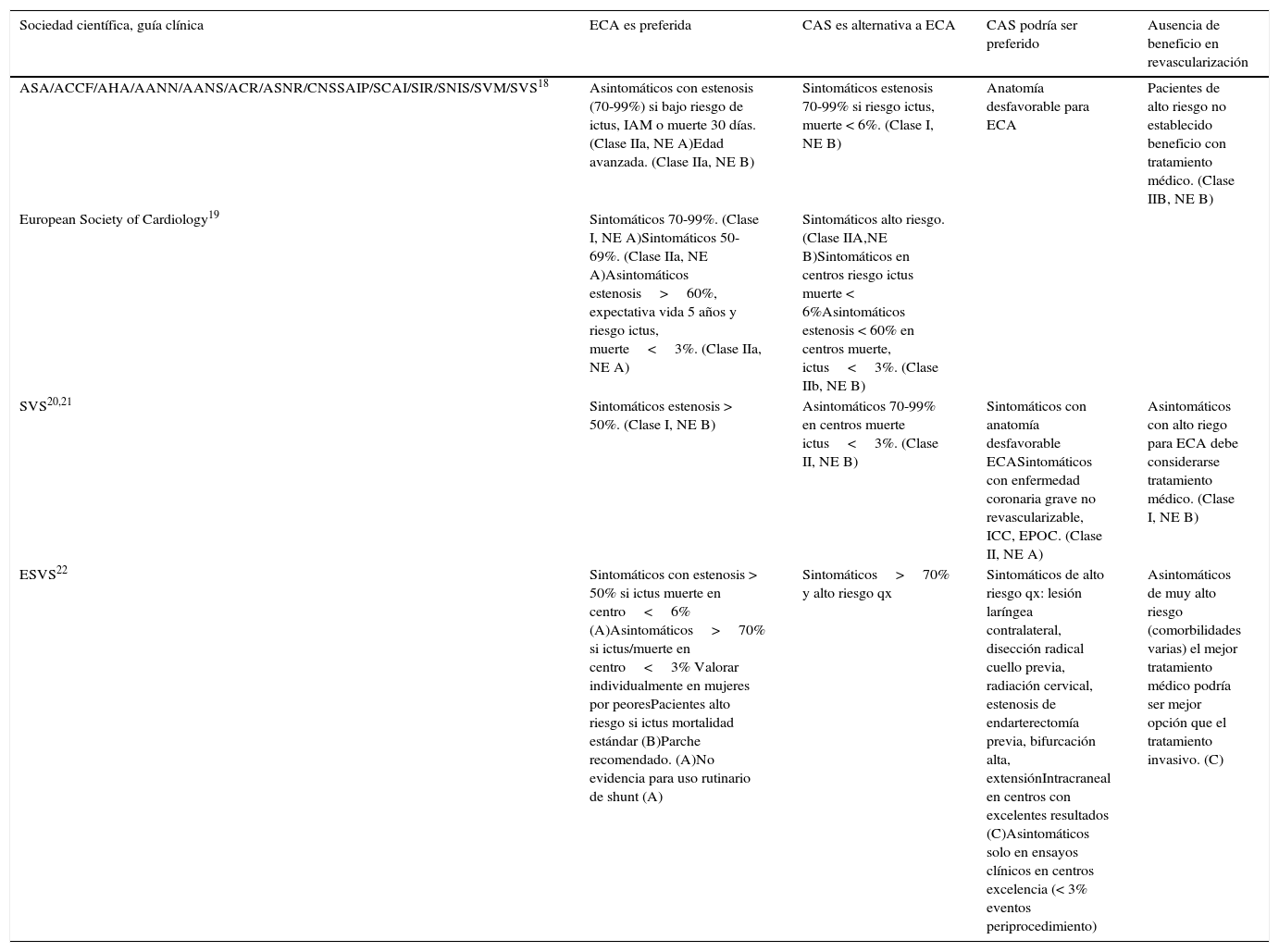
En los últimos años, el debate endarterectomía carotídea vs. tratamiento endovascular en el sector carotídeo ha ocupado un lugar importante en distintas sociedades científicas, tanto vasculares como cardiológicas y neurológicas18-22. Aunque estas sociedades coinciden en muchas de sus recomendaciones y guías clínicas, en la tabla 3 en este artículo intentamos destacar las diferencias y controversias que aparecen tras su análisis.
Comparativa de las principales recomendaciones publicadas en guías clínicas de consenso de sociedades científicas en el manejo de enfermedad carotídea
| Sociedad científica, guía clínica | ECA es preferida | CAS es alternativa a ECA | CAS podría ser preferido | Ausencia de beneficio en revascularización |
|---|---|---|---|---|
| ASA/ACCF/AHA/AANN/AANS/ACR/ASNR/CNSSAIP/SCAI/SIR/SNIS/SVM/SVS18 | Asintomáticos con estenosis (70-99%) si bajo riesgo de ictus, IAM o muerte 30 días. (Clase IIa, NE A)Edad avanzada. (Clase IIa, NE B) | Sintomáticos estenosis 70-99% si riesgo ictus, muerte < 6%. (Clase I, NE B) | Anatomía desfavorable para ECA | Pacientes de alto riesgo no establecido beneficio con tratamiento médico. (Clase IIB, NE B) |
| European Society of Cardiology19 | Sintomáticos 70-99%. (Clase I, NE A)Sintomáticos 50-69%. (Clase IIa, NE A)Asintomáticos estenosis>60%, expectativa vida 5 años y riesgo ictus, muerte<3%. (Clase IIa, NE A) | Sintomáticos alto riesgo. (Clase IIA,NE B)Sintomáticos en centros riesgo ictus muerte < 6%Asintomáticos estenosis < 60% en centros muerte, ictus<3%. (Clase IIb, NE B) | ||
| SVS20,21 | Sintomáticos estenosis > 50%. (Clase I, NE B) | Asintomáticos 70-99% en centros muerte ictus<3%. (Clase II, NE B) | Sintomáticos con anatomía desfavorable ECASintomáticos con enfermedad coronaria grave no revascularizable, ICC, EPOC. (Clase II, NE A) | Asintomáticos con alto riego para ECA debe considerarse tratamiento médico. (Clase I, NE B) |
| ESVS22 | Sintomáticos con estenosis > 50% si ictus muerte en centro<6% (A)Asintomáticos>70% si ictus/muerte en centro<3% Valorar individualmente en mujeres por peoresPacientes alto riesgo si ictus mortalidad estándar (B)Parche recomendado. (A)No evidencia para uso rutinario de shunt (A) | Sintomáticos>70% y alto riesgo qx | Sintomáticos de alto riesgo qx: lesión laríngea contralateral, disección radical cuello previa, radiación cervical, estenosis de endarterectomía previa, bifurcación alta, extensiónIntracraneal en centros con excelentes resultados (C)Asintomáticos solo en ensayos clínicos en centros excelencia (< 3% eventos periprocedimiento) | Asintomáticos de muy alto riesgo (comorbilidades varias) el mejor tratamiento médico podría ser mejor opción que el tratamiento invasivo. (C) |
Las sociedades científicas aplican distintos sistemas para graduar sus recomendaciones. La AHA, la European Society of Cardiology y las SVS guidelines usan un sistema de graduación basado en la fuerza de las recomendaciones (clase i fuerte, clase ii débil) separado de la calidad de los datos en los que se basa, nivel de evidencia (NE): A, alta; B, moderada; C, baja, y D, muy baja. Las recomendaciones no solo se basan en datos, sino en valores prevalentes y preferencias de grupos de expertos. El documento de la ESVS usa un sistema simplificado en el que solo la calidad de los datos en los que se basa aparece recogida (A: apoyado en ensayos clínicos aleatorizados; B: apoyados en ensayos clínicos de calidad pero no ensayos aleatorizados; C: apoyados tan solo en opiniones o experiencias de expertos).
Modificado de Circulation. Cutlip DE, Pinto DS. Extracranial Carotid Disease Revascularization.Circulation. 2012;126:2636-2644
La endarterectomía quirúrgica ha demostrado reducir el riesgo de presentar un accidente cerebrovascular ipsolateral en pacientes con estenosis carotídea sintomática, así como en pacientes seleccionados con estenosis carotídea severa asintomática. Aunque los objetivos básicos de la cirugía revascularizadora son siempre los mismos, las técnicas exactas utilizadas para alcanzarlos varían entre la población de cirujanos vasculares23.
A continuación, se expondrá la evidencia actual basada en la gestión técnica de los pacientes con indicación de cirugía carotídea centrándonos en la planificación previa, la optimización médica del paciente y aspectos técnicos relacionados con la intervención (el empleo de shunt carotídeo, el parche carotídeo, el tipo de endarterectomía, el tipo de anestesia y otros).
a. Planificación: en pacientes que van a ser sometidos a endarterectomía carotídea es mandatorio una correcta anamnesis e historia clínica vascular, la exploración física debe descartar la existencia de enfermedad arterioesclerótica en otras localizaciones. La evaluación cardiaca debe considerarse de manera selectiva, ya que los pacientes sometidos a ECA presentan mayor morbimortalidad relacionada con eventos coronarios respecto al tratamiento endovascular carotídeo. Esta evaluación debe realizarse mediante la prueba de esfuerzo, la ecocardiografía con dobutamina o el estudio coronario24; sin embargo, no hay evidencia de que dicha praxis reduzca el riesgo de infarto o muerte tras la endarterectomía carotídea. La radiografía de tórax preoperatoria se recomienda debido a la asociación de la arteriosclerosis carotídea con el tabaquismo y la enfermedad coronaria25. La identificación de factores de riesgo de morbimortalidad relacionados es clave, aunque no existe consenso a la hora de identificar dichos factores predictivos, la mayoría de los estudios los centran en pacientes mayores de 80 años, cardiopatía severa, enfermedad pulmonar severa, insuficiencia/fallo renal, accidente cerebrovascular previo, y aspectos de complejidad anatómica, como radiación cervical previa, cirugía de cuello previa por patología no vascular (p. ej., vaciamientos tumorales), la endarterectomía carotídea previa y la oclusión carotídea contralateral. El Programa Nacional de Mejoramiento de la Calidad Quirúrgica del Colegio Americano de Cirujanos analizó una muestra de 3.949 pacientes que recibieron la ECA como procedimiento primario en 2005 y 2006. Los pacientes con uno o más factores de «alto riesgo» (edad > 80 años, enfermedad cardiaca grave o enfermedad pulmonar obstructiva crónica) suponían el 30 por ciento de la población; los resultados mostrados indicaban que la tasa de accidente cerebrovascular a 30 días tras ECA fue similar en pacientes con y sin criterios de «alto riesgo» (1,4% vs. 1,7%). Por el contrario, la mortalidad a 30 días fue significativamente mayor en los pacientes con criterios de «alto riesgo» (1,3% vs, 0,4%), solo la enfermedad cardiaca severa se asoció de modo individual a una mayor mortalidad a 30 días; no existiendo dicha asociación cuando se analizó el factor de edad mayor de 80 años26.
– Planificación de imagen preoperatoria: los pacientes con sospecha de estenosis carotídea candidatos a ECA suelen ser evaluados con ecografía Doppler como prueba inicial para evaluar la gravedad y la extensión de la lesión carotídea. Otros métodos no invasivos útiles incluyen la angiografía por tomografía computarizada (angio-TAC) y la angiografía por resonancia magnética (ARM). Tanto en pacientes sintomáticos como asintomáticos se debe realizar un eco Doppler para estar seguro de que la arteria carótida no se ha ocluido, ya que esto contraindicaría el procedimiento. Existe cierta controversia acerca de la necesidad de cuantificar la lesión carotídea únicamente con eco Doppler o bien complementar el estudio con angio-TAC o angio-RM. Expertos en la ecografía carotídea abordaron este tema y elaboraron recomendaciones para el uso de la velocidad Doppler y los parámetros de imagen para cuantificar la estenosis de la arteria carótida interna con ecografía Doppler27. Las recomendaciones añaden que la utilidad de las pruebas ecográficas debe ser verificada en los laboratorios vasculares individuales, por lo que solo el cirujano que tenga acceso a un laboratorio vascular certificado con los programas de garantía de calidad en curso podría utilizar la ecografía Doppler como única técnica de imagen de la arteria carótida interna cervical antes de realizar la endarterectomía carotídea. En pacientes sintomáticos, la evaluación preoperatoria debe incluir la realización de TAC craneal o bien RM para estimar el infarto cerebral, así como descartar otras causas que puedan interferir con el diagnóstico del paciente (p. ej. tumor, aneurismas cerebrales).
b. Optimización tratamiento médico del paciente
b.1. Antiagregación: el tratamiento antiplaquetario con aspirina reduce el riesgo de accidente cerebrovascular de cualquier causa en pacientes sometidos a endarterectomía carotídea o angioplastia y stent carotídeo28. La aspirina a dosis baja (81 a 325mg al día) es más eficaz que la aspirina en dosis alta (650 a 1.300mg al día). Las guías de consenso de la Academia Americana de Neurología y el American College of Chest Physicians recomiendan AAS para los pacientes sintomáticos y asintomáticos sometidos a ECA29,30, iniciar previo a la intervención y continuar indefinidamente en ausencia de contraindicaciones. Para los pacientes que son alérgicos o sensibles a la aspirina, el clopidogrel se puede utilizar como un agente alternativo.
b.2. Estatinas: su uso pacientes sintomáticos sometidos a ECA parece estar asociado a mejores resultados. En un estudio observacional retrospectivo de 3.360 endarterectomías carotídeas el uso de estatinas se asoció a una reducción de la mortalidad intrahospitalaria y de la relación ictus isquémico/muerte, aunque los resultados de complicaciones cardiacas intrahospitalarias no mejoraron significativamente. En pacientes asintomáticos, el uso de estatinas no se asoció a resultados significativamente diferentes. Las publicaciones al respecto también indican que las estatinas pueden ser de beneficio en el período perioperatorio y que este beneficio podría perderse si se interrumpen las mismas31.
b.3. Antibióticos profilácticos: se recomienda su administración antes de la ECA para controlar la infección de la herida quirúrgica y debido a la frecuente utilización de material protésico (parches PTFE-dacrón)32.
c. Aspectos técnicos en relación con la endarterectomía carotídea
c.1. Tipo de anestesia: el empleo de anestesia general o anestesia local (con o sin bloqueo cervical) depende fundamentalmente de las preferencias del cirujano. Lo ideal sería que el equipo quirúrgico anestesista-cirujano dominase ambos procedimientos para poder adaptarse a las características de cada paciente. El análisis de 26.070 casos por el Colegio Americano de Cirujanos (ACS)-Programa Nacional de Mejora de la Calidad Quirúrgica identificó el uso de anestesia general en la mayoría de los casos, 84,6%, y de anestesia regional en solo un 15,4%33. No encontrando diferencias significativas para el resultado ictus/infarto de miocardio/muerte (30 días) entre ambos grupos. Los pacientes sometidos a anestesia general tenían más probabilidades de permanecer en el hospital más de un día después de la cirugía. En el ensayo clínico General Anaesthetic versus Local Anaesthetic for carotid surgery (GALA) tampoco se evidenciaron diferencias significativas entre los resultados a 30 días en términos de ictus, muerte o infarto de miocardio.
c.2. La técnica de endarterectomía carotídea: tras el abordaje cervical y la disección y control de la bifurcación carotídea las opciones quirúrgicas son 2: la endarterectomía convencional y la endarterectomía por eversión. En esta última, la arteria carótida interna se secciona horizontalmente en su origen en el bulbo carotídeo y luego la arteria es evertida, para retirar la placa que origina la estenosis. Esta opción es particularmente atractiva en arterias pequeñas y en redundantes, ya que permite eliminar bucles carotídeos; sin embargo, la revisión de la literatura y la evidencia científica no favorece aparentemente una técnica sobre la otra. El ensayo multicéntrico Eversion VERsus conventional carotid Endarterectomy Study (EVEREST) incluyó a 1.342 pacientes; comparó ambas técnicas y no se encontraron diferencias significativas para las variables principales (ictus perioperatorio o muerte, oclusión de la carótida intervenida) o variables secundarias (ictus, ictus ipsolateral, ataque isquémico transitorio, lesiones de los nervios craneales, hematomas del cuello, infarto de miocardio). Un metaanálisis posterior que incluyó al estudio EVEREST y otros 5 ensayos más pequeños identificó una tendencia hacia un menor riesgo de ictus perioperatorio (30 días) para la endarterectomía por eversión comparado con la convencional34.
c.3. Empleo de parche (patch) carotídeo: la mayoría de artículos y estudios publicados abogan por el cierre de arteria con un parche, ya sea vena safena o bien material protésico (PTFE, dacrón, pericardio bovino). El uso de parche está asociado a un menor riesgo de oclusión arterial perioperatoria y los ensayos que se han realizado indican otros 2 beneficios principales del uso de parche: una marcada reducción en la frecuencia de reestenosis a largo plazo (> 50%) y una menor tasa de ictus ipsolateral35. Estudios acerca del tipo de material para el parche carotídeo han destacado la mayor incidencia de la dilatación aneurismática con el uso del parche de vena safena (15,5%) que en el grupo de PTFE (2%)36.
d.4. Control de perfusión cerebral: aunque la mayoría de los pacientes con estenosis carotídeas, entre el 80 y el 85%, podrían tolerar el clampaje carotídeo sin consecuencias la evaluación de la capacidad de la circulación colateral a través del polígono de Willis, debe ser monitorizada para asegurar una adecuada perfusión cerebral durante el procedimiento. La monitorización puede realizarse por diferentes métodos: Doppler transcraneal, potenciales evocados somatosensoriales, electroencefalograma (EEG), EEG procesado, presión en el muñón carotídeo y otros. Bajo anestesia general, el método más usado y reportado es el Bispectral Index Monitoring. En cuanto a la medición de presión de reflujo en la carótida interna, las presiones superiores a 30 y a 50mmHg indicarían una adecuada perfusión a través del polígono de Willis, mientras que valores inferiores constituyen una indicación de colocación de shunt temporal.
d.5. Empleo de shunt carotídeo: los estudios dirigidos a definir el mejor enfoque (shunt obligatorio, shunt selectivo) no han sido concluyentes. Aburahma et al. estudiaron a 200 pacientes sometidos a ECA bajo anestesia general comparando el uso rutinario vs. uso selectivo en pacientes con presión de reflujo menor de 40mmHg, sin encontrar diferencias significativas entre ambos grupos37. Una revisión sistemática que identificó 3 ensayos clínicos incluyendo a 686 pacientes tampoco encontró diferencias significativas en las tasas de ictus totales, ictus ipsolateral o muerte a 30 días para los pacientes intervenidos con shunt de forma rutinaria frente a pacientes sin implante38. Si se usa el shunt de modo rutinario, debe asumirse que la derivación podría ser innecesaria en aproximadamente el 90% de los pacientes y que se expone a los mismos a otros riesgos específicos como la formación de un colgajo de la íntima durante la inserción del shunt que puede resultar en disección arterial distal, el desprendimiento de émbolos de la placa durante la manipulación o la embolia gaseosa debido a las burbujas en la derivación.
Resumen de indicaciones actuales de la endarterectomía carotídea vs. el stent carotídeoa. Pacientes sintomáticosTanto los primeros estudios aleatorizados en sintomáticos hace ya más de 20 (NASCET, ECST) que establecieron la endarterectomía carotídea como segura y eficaz para reducir el riesgo de accidente cerebrovascular isquémico en pacientes con aterosclerosis carotídea39,40 frente a solo tratamiento médico con aspirina, como los más recientes ensayos comparando la endarterectomía vs. esta, la angioplastia y el stent carotídeo han demostrado la superioridad de la ECA para la mayoría de pacientes sintomáticos con estenosis superiores al 50% y una esperanza de vida de al menos 5 años. Estos resultados se observan especialmente en pacientes de alto riesgo quirúrgico y con anatomías quirúrgicas complejas. Esta recomendación se debe aplicar solo cuando el riesgo perioperatorio de ictus y muerte reconocidos para el operador o el centro sea inferior al 6%. Los resultados de múltiples ensayos, ICSS, CAVATAS 2, SPACE, EVA-3S y CREST, demostraron que, a 30 días tras el procedimiento, la tasa de ictus periprocedimiento y de mortalidad no era inferior con el tratamiento endovascular que con la ECA. En 2012, un metaanálisis revisó 7 ensayos que comparaban el tratamiento endovascular vs. la endarterectomía en pacientes sintomáticos y 4 ensayos que lo comparaban en pacientes con estenosis sintomáticas y asintomáticas41. En el análisis aislado de los pacientes sintomáticos se hicieron las siguientes observaciones:
- a.
Los pacientes asignados al tratamiento endovascular tuvieron una tasa significativamente mayor de accidente cerebrovascular perioperatorio o muerte a los 30 días (8,2% vs. 5,0%; odds ratio [OR] 1,72; IC del 95%, 1,29 a 2,31).
- b.
En análisis por subgrupos, los pacientes ≥ 70 años de edad tuvieron un aumento significativo del riesgo de accidente cerebrovascular perioperatorio o muerte con el tratamiento endovascular en comparación con la endarterectomía (OR 2,20; IC del 95%, 1,47 a 3,29), pero no hubo diferencias significativas en el riesgo de accidente cerebrovascular perioperatorio o muerte para los pacientes<70 años de edad (OR 1,16; IC del 95%, 0,80 a 1,67).
- c.
En comparación con los pacientes sometidos a endarterectomía el grupo de tratamiento endovascular tuvo una tasa significativamente mayor de muerte o ictus durante el período perioperatorio o ictus ipsolateral durante el seguimiento (10,4% vs. 7,7%; OR 1,39; IC del 95%, 1,10 a 1,75).
- d.
El tratamiento con stent carotídeo en comparación con la endarterectomía se asoció a un riesgo significativamente menor de infarto de miocardio (OR 0,44), parálisis del nervio craneal (OR 0,08) y hematoma en el lugar de acceso (OR 0,37).
- e.
La tasa de ictus ipsolateral después del período perioperatorio fue similar en el grupo de tratamiento endovascular y la endarterectomía (2,2% vs. 2,4%; OR 0,93, IC del 95%, 0,60 a 1,45).
En resumen, y sobre la base de la evidencia científica publicada, solo debería indicarse el tratamiento endovascular en pacientes sintomáticos en lugar de la ECA en pacientes con estenosis carotídeas sintomáticas del 70 al 99% que presenten cualquiera de las siguientes condiciones: una lesión de la carótida con anatomía compleja para acceso quirúrgico, estenosis inducida por radiación, reestenosis tras endarterectomía previa y una elevada comorbilidad cardiopulmonar o de otra índole que incrementase significativamente el riesgo quirúrgico.
b. Pacientes asintomáticosLa endarterectomía carotídea ha demostrado beneficio en pacientes asintomáticos con estenosis de la arteria carótida interna de alto grado (60-99%), pero sin duda el beneficio no es tan significativo como lo es para los pacientes sintomáticos y especialmente en el caso de las mujeres. La eficacia de la ECA ya se evaluó hace muchos años en 3 ensayos en asintomáticos: el VA Cooperative trial, ACAS y ACST; la reducción del riesgo absoluto en el VA Cooperative fue de 1,0 durante un seguimiento medio de 4 años, en el ACAS la ARR fue de 3,0 durante 2,7 años y en el ACST la de 3,1 durante 3,4 años. Metaanálisis posteriores de estos ensayos confirmaron que la endarterectomía carotídea en pacientes asintomáticos se asocia a una pequeña reducción del riesgo absoluto para el resultado de cualquier accidente cerebrovascular.
En cuanto al tratamiento endovascular en pacientes asintomáticos, no existen estudios específicos con un número de pacientes significativo y aleatorizados comparando ambas técnicas, aunque en los estudios SAPPHIRE y en el CREST cerca de la mitad de los pacientes incluidos eran asintomáticos, lo que permitiría extraer ciertas conclusiones. Una revisión sistemática Cochrane publicada en marzo del 2007 identificó 10 ensayos controlados aleatorizados con 3.178 pacientes que compararon endarterectomía con stent carotídeo en pacientes con enfermedad carotídea sintomática o asintomática41 y se hicieron las siguientes observaciones: los resultados primarios de ictus/muerte a 30 días favorecían ligeramente a la endarterectomía respecto al stent carotídeo, pero el resultado no alcanzó significación estadística. Y es destacable que durante seguimiento a largo plazo, el análisis general no encontró diferencias significativas entre ambas técnicas en el riesgo de accidente cerebrovascular o muerte.
El tratamiento médico aislado (BMT) sin endarterectomía carotídea ni stent asociado es defendido por algunos autores en pacientes asintomáticos con estenosis carotídeas severas (60-99%) frente al BMT asociado a la ECA o el stent carotídeo. Ambas posturas han sido defendidas en la literatura por reconocidos expertos en los últimos años16 pero estos mismos expertos (incluyendo el principal investigador del CREST) también coinciden en que sería necesario aún el desarrollo de un nuevo ensayo aleatorizado más adecuado que compare los 3 brazos en pacientes asintomáticos: el mejor tratamiento médico posible, la endarterectomía y el stent carotídeo, que permitiera elaborar algoritmos adecuados para identificar a los pacientes asintomáticos que presenten estenosis carotideas con «alto riesgo de ictus»17.
c. Pacientes octogenariosAunque pueda parecer sorprendente los metaanálisis de estudios centrados en pacientes de edad avanzada han demostrado peores resultados con la técnica endovascular y mínimamente invasiva, la angioplastia y stent carotídeo, que con la endarterectomía quirúrgica42. La edad avanzada se propuso originalmente en muchos ensayos como una condición asociada a mayor riesgo quirúrgico y, por tanto, potencial una indicación para una técnica menos invasiva, pero posteriormente estudios como CREST confirmaron peores resultados en pacientes mayores de 70 años el implante de un stent que tras la ECA. Otro metaanálisis de 41 estudios combinando endarterectomía o stent en pacientes mayores de 80 años demostró que el riesgo relativo de muerte o infarto de miocardio a los 30 días fueron similares en ambas técnicas, pero la tasa de ictus cerebrovascular fue significativamente mayor para el stent carotídeo (7,0% vs. 1,9%)43. Estos resultados se han justificado y atribuido a la navegación con material específico (guías y catéteres) por arcos aórticos enfermos con abundante trombo y calcio, al no empleo de sistemas de protección embolígena distal en las etapas iniciales de desarrollo de la técnica y a la curva de aprendizaje de los operadores. Con las mejoras en los dispositivos, el empleo estandarizado de sistemas de protección distal como el filtro carotídeo, o sistemas de flujo carotídeo inverso, es probable que se disminuya el número de eventos neurológicos perioperatorios atribuibles a la técnica y los pacientes de edad avanzada puedan beneficiarse de esta técnica. A día de hoy, la endarterectomía carotídea es la técnica que ofrece mejores resultados en pacientes octogenarios sintomáticos o asintomáticos con un riesgo quirúrgico aceptable.
ConclusionesLa endarterectomía carotídea es la técnica de revascularización con más éxito demostrado para la prevención de ictus en pacientes sintomáticos o asintomáticos con enfermedad aterosclerótica carotídea. El mayor beneficio se observa en pacientes con síntomas recientes de ictus o evento isquémico transitorio ipsolateral y estenosis carotídeas severas (> 70%) con reducción de riesgo absoluto de eventos neurológicos ipsolaterales en la CEA vs. la antiagregación del 18,7 y de infarto o muerte del 21,2, demostrados en los primeros estudios NASCET y ECST.
La endarterectomía carotídea también ha demostrado en la mayoría de los ensayos clínicos aleatorizados menores tasas de eventos neurológicos postoperatorios y muerte, a corto plazo, en comparación con el stent en pacientes sintomáticos o asintomáticos. Tan solo el estudio CREST demostró mayor riesgo perioperatorio de infarto de miocardio tras la endarterectomía que tras el stent carotídeo (1,1% vs. 2,3%, p=0,01) y este mayor riesgo de evento coronario está relacionado con un incremento de la mortalidad a medio largo plazo. CREST también demostró mayor tasa de eventos neurológicos tras el stent carotídeo que tras la ECA (4,1% vs. 2,3%, p=0,01) y ha sido reportado que la valoración de la calidad de vida de los pacientes es claramente menor tras un ictus, que tras un infarto de miocardio.
Los análisis de coste de vida derivados de los ensayos realizados que comparan el stent carotídeo vs. endarterectomía también son claramente favorables para el tratamiento quirúrgico.
En asintomáticos, los beneficios de la estrategia de revascularización carotídea son mucho menores, por lo que el control de factores como la tasa de eventos neurológicos postoperatorios, el riesgo particular de IAM, la edad y posiblemente el sexo deben ser tenidos en cuenta antes de plantearse esta intervención preventiva.
La comparación de resultados de los ensayos aleatorizados publicados permite extraer conclusiones muy limitadas, tanto la endarterectomía como el stent carotídeo demostraron tener un menor riesgo de eventos neurológicos postoperatorios cuando fueron realizados por operadores con experiencia en la técnica y en centros de alto volumen. Pero en muchos de los ensayos analizados en este artículo se reconocen las limitaciones en los diseños de estos estudios, sobre todo en el brazo de stent carotídeo, lo que puede justificar y cometer un sesgo a la hora de interpretar los peores resultados del stent carotídeo respecto a la ECA. Aun así, se observó en todos los estudios un ligero mayor número de eventos neurológicos con la angioplastia y stent carotídeo en pacientes sintomáticos, con riesgo estándar y edad avanzada, que constituyen la mayoría de los casos que tratamos en nuestra actividad diaria.
Existe un subgrupo de pacientes con factores anatómicos específicos (cuellos hostiles) y clínicos (elevada comorbilidad y mayor riesgo de IAM) en los que el tratamiento endovascular con stent carotídeo puede ser la primera opción terapéutica, ya que parece asociarse a un menor riesgo de eventos coronarios perioperatorios y defunción. La indicación de stent carotídeo más allá de este grupo específico de pacientes difícilmente puede justificarse, excepto en centros de alto volumen y en manos expertas que alcancen tasas de complicaciones perioperatorias similares o inferiores a la endarterectomía.
La cuestión acerca de si el mejor tratamiento médico actual puede ser la primera opción de tratamiento para pacientes con estenosis carotídea, especialmente asintomáticos y de alto riesgo para endarterectomía o stent aún no está resuelta. En los próximos años, los ensayos ya diseñados, y en marcha, como el Transatlantic Asymptomatic Carotid Intervention Trial, el SPACE-2 y el CREST-2, que pretenden comparan los 3 brazos: el mejor tratamiento médico posible actual (BMT) vs. la endarterectomía vs. el stent carotídeo podrían ayudar a resolver esta cuestión para poder ofrecer el mayor beneficio posible a nuestros pacientes.
Debemos reconocer el interés por el desarrollo de nuevas técnicas entre cirujanos vasculares; sin embargo, la existencia y la disponibilidad de una técnica moderna, prometedora y menos invasiva que la endarterectomía carotídea no debe confundirse con el empleo no justificado de misma. A día de hoy, y salvo en algunas excepciones, el uso del stent carotídeo debería estar limitado a casos específicos o como parte de ensayos aleatorizados, aprobados por comités éticos y no influidos por la industria. Estos ensayos permitirán la comparación de una técnica mínimamente invasiva con una técnica quirúrgica estandarizada, relativamente segura y considerada el gold standard durante muchos años, pero que también evoluciona en múltiples aspectos y puede mejorar sus resultados. La innovación y el desarrollo de nuevas tecnologías para otros beneficios que no sea la mejora real de los resultados en nuestros pacientes no deberían estar nunca justificada.
Por último, los autores de este trabajo reconocen sus limitaciones, tanto en la recogida de datos y análisis de estudios y guías clínicas, que ha sido realizado de modo no sistemático, como en las conclusiones derivados del mismo. Este trabajo pretende relacionar la evidencia científica publicada en la literatura con la relación en la práctica diaria de un grupo quirúrgico, que a pesar de situarse en la vanguardia de las terapias endovasculares considera a día de hoy la ECA como la técnica de elección para el tratamiento de la estenosis carotídea en la mayoría de los pacientes.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.