Estudiar la incidencia, evolución y manejo del síndrome compartimental abdominal (SCA) en los aneurismas de aorta infrarrenal rotos (AAAr) tratados con endoprótesis en nuestro centro.
Material y metodologíaEstudio observacional retrospectivo. Analizamos todos los pacientes tratados con endoprótesis urgentes desde octubre de 2001 a diciembre de 2015. Incluimos solo pacientes con aneurismas de aorta infrarrenal rotos, excluyendo los AAA sintomáticos. Estudiamos la incidencia, evolución y tratamiento del SCA. Establecimos diagnóstico de SCA con una presión intraabdominal medida en vejiga >20mmHg, más el desarrollo de una nueva disfunción orgánica. Analizamos variables preoperatorias y postoperatorias para SCA. Utilizamos test exacto de Fisher y U de Mann-Whitney para el análisis estadístico.
ResultadosDurante el periodo analizado se implantaron 65 endoprótesis urgentes, de ellas 42 fueron por aneurismas de aorta infrarrenal rotos. La edad media fue 77±8 años; el 98% fueron hombres. De los 42 pacientes estudiados, 9 (21,4%) fallecieron en quirófano. La incidencia de SCA en los 33 pacientes restantes fue 18,2% (6/33 pacientes). La mortalidad en SCA fue 66,7 frente 18,5% para los que no desarrollaron SCA (p=0,034). Se realizó laparotomía descompresiva en 4 pacientes (4/6), siendo la mortalidad en estos pacientes del 50 frente al 100% para los que no se realizó laparotomía descompresiva (p= 0,4). Se asociaron con desarrollo de SCA la acidosis pre- y postoperatoria (57,7 vs. 7,7%, p=0,01), coagulopatía preoperatoria (41,7 vs. 4,8%, p=0,01), tensión sistólica <90mmHg preoperatoria (46,2 vs. 0%, p=0,002) y administración >3 litros de cristaloides/24 h en postoperatorio (38,5 vs. 5%, p=0,02). Los pacientes con SCA recibieron intraoperatoriamente 8±3,6 concentrados de hematíes vs. 2±2,7 (p= 0,002).
ConclusionesEstos hallazgos confirman que el SCA es una patología frecuente que asocia una elevada mortalidad en pacientes con AAAr tratados con endoprótesis. El compromiso hemodinámico importante y la administración de grandes cantidades de cristaloides intravenosos y politransfusión durante el manejo asocian mayor incidencia de este síndrome.
To study the incidence, evolution and management of abdominal compartment syndrome (ACS) in ruptured abdominal aortic aneurysms (RAAA) after endovascular aneurysm repair.
Material and methodsRetrospective observational study. We analyzed all emergency EVAR performed from October 2001 to December 2015. Only RAAA were included. Symptomatic aortic aneurysms were excluded. We studied the incidence, evolution and management of ACS. Diagnosis of ACS was established with intraabdominal pressure more than 20mmHg plus the development of a new organic dysfunction. Preoperative and postoperative variables were analyzed for ACS. Fisher exact test and Mann-Whitney U-test were used for the statistical analysis.
ResultsSixty-five emergency EVAR were performed during the analyzed period, 42 were RAAA. The mean age was 77 ± 8 years; 98% were men. Nine of 42 patients (21.4%) died in the operating room. The incidence of ACS in the 33 remaining patients was 18.2% (6/33 patients). The mortality for ACS was 66.7% vs 18.5% (p=0.034). Decompressive laparotomy was performed in 4 patients (4/6). The mortality after decompressive laparotomy was 50% vs 100% (p= 0.4). The incidence of ACS for postoperative acidosis was 57.7% vs 7.7% (p=0.01), for preoperative coagulopathy 41.7% vs 4.8% (p=0.01), for preoperative systolic blood pressure <90 mmHg 46.2% vs 0% (p=0.002). The incidence of ACS after overload of more than 3 liters of crystalloids per 24 hours in the postoperative period was 38.5% vs 5% (p=0.02). Patients with ACS received intraoperatively 8 ± 3.6 packed erythrocytes vs 2 ± 2.7 (p= 0.002).
ConclusionsThese findings confirm that ACS is a common disease that is associated with a high mortality in patients with RAAA after EVAR. Patients with a compromise hemodynamic status, multiple transfusions and those with overload of intravenous crystalloids during management were associated with higher incidence of ACS.
El síndrome de hipertensión intraabdominal (HIA) y su forma más grave, el síndrome compartimental abdominal (SCA), son complicaciones que se presentan con relativa frecuencia (25-85%) en los pacientes graves ingresados en unidades de cuidados intensivos por diferentes patologías médicas y quirúrgicas1. El SCA se define como una HIA >20mmHg asociada a una nueva disfunción orgánica2. Existen diferentes condiciones clínicas que se han asociado a este síndrome, entre ellas la disminución de la distensibilidad abdominal, el aumento del contenido intraabdominal, la presencia de edema intersticial intraabdominal, la obesidad (IMC>30) y el shock2,3. El paciente con aneurisma de aorta abdominal roto (AAAr) presenta muchas de estas condiciones, por lo cual es un paciente de alto riesgo para el desarrollo de SCA. La mortalidad asociada a este síndrome en AAAr varía del 62 al 83%4,5. Esta complicación es prevenible y tratable, por lo cual su diagnóstico oportuno es de importancia vital1,6.
Aunque los efectos de la hipertensión intraabdominal son conocidos desde el siglo XIX, el síndrome compartimental abdominal no fue descrito hasta 1984 por Kron, en pacientes sometidos a cirugía aortoiliaca7. Desde entonces se ha producido un verdadero aumento del número de publicaciones sobre las consecuencias del aumento de la presión intraabdominal (PIA)1–3,5,6,8–14. Además la World Society for Abdominal Compartment Syndrome (WSACS) ha estandarizado el método de medición de la PIA y ha establecido definiciones y recomendaciones que han permitido emplear un lenguaje común así como elaborar protocolos diagnósticos y terapéuticos para HIA y SCA2. La WSACS estableció cuatro grados de HIA basados en la PIA obtenida por medición transvesical. Se recomienda un manejo conservador en fases iniciales (grado I PIA 12-15mmHg y grado II PIA 16-20mmHg), con analgésicos, diuréticos, coloides, relajantes musculares y una vigilancia estrecha de los cambios de PIA2,15. En fases avanzadas (GIII PIA 21-25mmHg y GIV PIA >25mmHg) recomiendan laparotomía descompresiva2,8. El SCA se manifiesta como una nueva disfunción orgánica, habitualmente renal, respiratoria o circulatoria3,9. Sin tratamiento evoluciona invariablemente a fallo multiorgánico15,16.
El uso de EVAR en los AAAr se ha convertido en el método preferido en nuestro centro. En algunos estudios ha demostrado disminuir la mortalidad perioperatoria precoz en comparación con la cirugía abierta4,17,18. Sin embargo, cada vez más se van identificando nuevas complicaciones, algunas de ellas con mal pronóstico, como el SCA. Esta entidad no ha sido estudiada tan exhaustivamente en el EVAR como en la cirugía abierta5,11–13,19. Además, no hemos encontramos literatura sobre el estudio de esta patología en EVAR en nuestro medio. La incidencia estimada de SCA en AAAr es de aproximadamente 34% para la cirugía abierta y 21% para EVAR4. Sin embargo en algunas publicaciones su definición y tratamiento no están bien establecidos. Encontramos que en algunas de estas publicaciones el diagnóstico se basó en criterios clínicos, sin realizar medición de la presión intraabdominal.
A pesar de la gran cantidad de literatura disponible sobre AAAr, el SCA continúa siendo infradiagnosticado, al confundirse con otros procesos patológicos con los que comparten manifestaciones clínicas similares3. Nuestro objetivo principal fue estudiar la incidencia, evolución y manejo del SCA en AAAr tratados mediante EVAR en nuestro centro. Los objetivos secundarios fueron estudiar posibles variables asociadas a SCA.
Material y metodologíaRealizamos un estudio observacional retrospectivo. Analizamos todos los pacientes tratados mediante EVAR urgentes desde octubre de 2001 a diciembre de 2015. Incluimos solo pacientes con aneurisma de aorta infrarrenal rotos, definiéndose la rotura como la extravasación de sangre fuera de la pared aórtica confirmada en la tomografía. Se excluyeron los aneurismas de aorta sintomáticos y los pacientes tratados con EVAR por otros motivos como fístula aortoentérica o traumatismos. Los datos se han extraído de forma exhaustiva de la historia clínica, se han revisado las pruebas analíticas e imágenes de tomografía. La variable principal del estudio fue el desarrollo de SCA. Establecimos diagnóstico de SCA con una PIA medida en vejiga >20mmHg de forma mantenida, más el desarrollo de una nueva disfunción orgánica. Las variables secundarias analizadas fueron: características demográficas, tensión arterial sistólica preoperatoria <90mmHg; coagulopatía, infusión de más de 3 litros de cristaloides/día, acidosis, uso de balón de oclusión aórtica, configuración de endoprótesis, tamaño del aneurisma y transfusión de hemoderivados. Definimos acidosis y coagulopatía como: un PH arterial ≤ 7,3 y recuento plaquetario<55.000, tiempo de protrombina>15 segundos o<50%, tiempo de cefalina>2 veces por encima de valores normales o INR>1,5, respectivamente. Realizamos análisis estadístico univariante. Utilizamos el test exacto de Fisher para variables cualitativas y U de Mann-Whitney para variables continuas. Los datos numéricos fueron expresados mediante la media±desviación típica y los datos categóricos, en porcentaje. Se consideró estadísticamente significativo un valor de p<0,05.
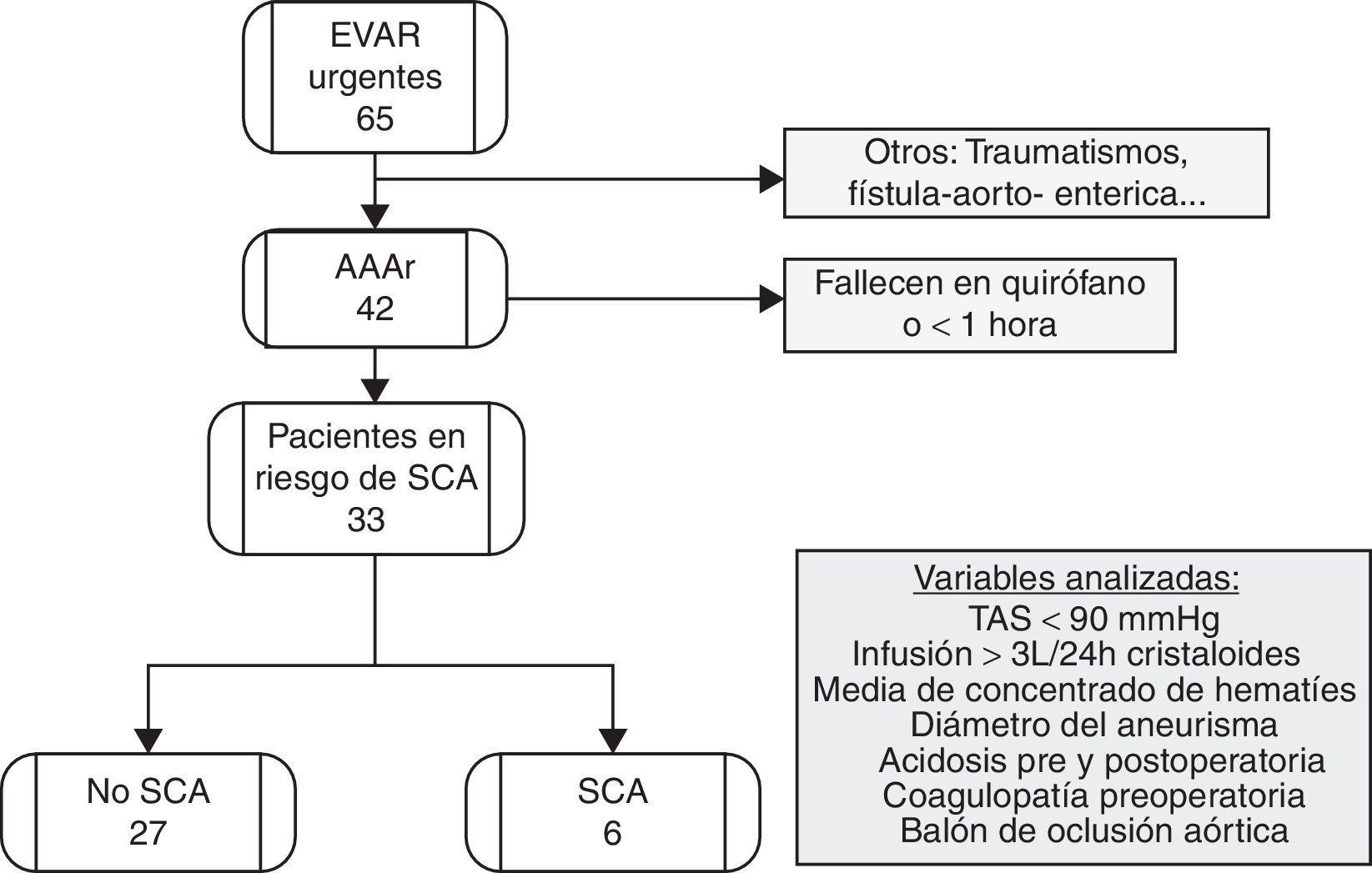
ResultadosDesde octubre de 2001 hasta diciembre de 2015 implantamos 65 endoprótesis aórticas de forma urgente, de ellas 42 fueron por AAAr. La edad media fue 77±8 años; en la muestra hubo solo una mujer. En la tabla 1 se resumen las características demográficas de la muestra. De los 42 pacientes estudiados, 9 (21,4%) fallecieron en quirófano o en la primera hora postoperatoria (fig. 1). La incidencia de SCA en los 33 pacientes restantes fue 18,2% (6/33 pacientes). El diámetro medio del aneurisma en estos pacientes fue 8,3±1,2cm frente a 8,1 ±1,8cm, p=0,9. La media de unidades de sangre transfundidas intraoperatoriamente en pacientes con SCA fue 8±3,6 frente 2±2,7 (p= 0,002). El SCA se presentó entre las 3 y 6 h postoperatorias en todos los casos.
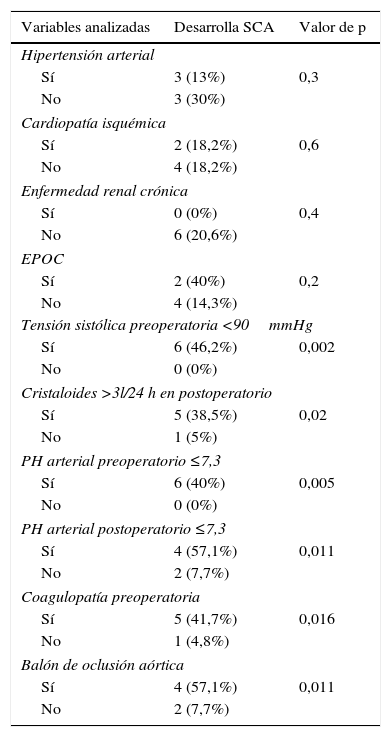
Se asociaron al desarrollo de SCA de forma estadísticamente significativa la acidosis preoperatoria (40 frente a 0%), coagulopatía preoperatoria (41,7 frente a 4,8%), tensión sistólica preoperatoria <90mmHg (46,2 frente a 0%) y el uso de balón de oclusión aórtica (57 frente a 7,7%). También se asociaron a SCA la administración de >3 litros de cristaloides/24 h en postoperatorio (38,5 vs. 5%) y la acidosis postoperatoria (57 frente a 7,7%). En la tabla 2 se resumen las variables clínicas analizadas en relación con SCA. El SCA comenzó en la totalidad de los casos con fallo renal. Cinco pacientes (83,3%) asociaron insuficiencia respiratoria, 3 sepsis y 2 complicaciones cardíacas (infarto y fibrilación ventricular). La media de días en unidad de reanimación en los pacientes con SCA fue 11,5±7,1 frente a 6,4±12, p= 0,045 y la media de días intrahospitalarios 21,2±22,4 frente a 14±19, p= 0,5.
Pacientes en riesgo de SCA (N=33)
| Variables analizadas | Desarrolla SCA | Valor de p |
|---|---|---|
| Hipertensión arterial | ||
| Sí | 3 (13%) | 0,3 |
| No | 3 (30%) | |
| Cardiopatía isquémica | ||
| Sí | 2 (18,2%) | 0,6 |
| No | 4 (18,2%) | |
| Enfermedad renal crónica | ||
| Sí | 0 (0%) | 0,4 |
| No | 6 (20,6%) | |
| EPOC | ||
| Sí | 2 (40%) | 0,2 |
| No | 4 (14,3%) | |
| Tensión sistólica preoperatoria <90mmHg | ||
| Sí | 6 (46,2%) | 0,002 |
| No | 0 (0%) | |
| Cristaloides >3l/24 h en postoperatorio | ||
| Sí | 5 (38,5%) | 0,02 |
| No | 1 (5%) | |
| PH arterial preoperatorio ≤7,3 | ||
| Sí | 6 (40%) | 0,005 |
| No | 0 (0%) | |
| PH arterial postoperatorio ≤7,3 | ||
| Sí | 4 (57,1%) | 0,011 |
| No | 2 (7,7%) | |
| Coagulopatía preoperatoria | ||
| Sí | 5 (41,7%) | 0,016 |
| No | 1 (4,8%) | |
| Balón de oclusión aórtica | ||
| Sí | 4 (57,1%) | 0,011 |
| No | 2 (7,7%) | |
La mortalidad en SCA fue 66,7 frente a 18,5% en los que no desarrollaron SCA (p=0,034). Realizamos laparotomía descompresiva en 4 pacientes. La mortalidad en este grupo de pacientes fue del 50 frente al 100% para los que no se realizó laparotomía (p= 0,4) La causa de la muerte en todos los casos con SCA fue FMO.
DiscusiónLa incidencia de SCA en nuestra serie (18,2%) fue similar a la descrita por otros autores4. Este resultado confirma que se trata de una complicación relativamente frecuente en los AAAr tratados mediante EVAR. Hemos determinado su forma de presentación y evolución. En todos los casos el SCA comenzó de forma precoz, lo que nos sugiere que las primeras 8 h postoperatorias son el momento de mayor riesgo para desarrollarlo. Al igual que en la literatura, la disfunción renal fue la forma de presentación más frecuente3, y la incidencia de complicaciones asociadas fue elevada. El incremento de la PIA>20mmHg produce disminución del flujo arterial y del drenaje venoso en todos los órganos abdominales, y el primero en verse afectado suele ser el riñón14–16,20. La isquemia-hipoxia a nivel abdominal produce alteración de las membranas celulares lo que favorece el edema intersticial y predispone a translocación bacteriana15,20. Estas alteraciones fisiopatológicas explican la afectación multiorgánica en el SCA. Como es de suponer, la presencia de esta complicación prolonga la estancia media hospitalaria y en la unidad de cuidados intensivos. Se ha descrito que sin tratamiento puede alcanzar una mortalidad del 100%15.
En nuestra serie la mortalidad por SCA fue elevada (66,7%), y similar a la descrita en la literatura4,5. Los pacientes politransfundidos, en shock, con sobrecarga de cristaloides, coagulopatía y acidosis pre- y postoperatoria asociaron mayor incidencia de SCA. Estas variables reflejan como denominador común un estado hemodinámico muy comprometido. Debido al diseño de nuestro estudio, no podemos inferir en qué grado predispone cada una de estas variables al desarrollo de SCA, sin embargo han sido descritas previamente como factores de riesgo por otros autores6,12. Algunos estudios sugieren que tal riesgo podría disminuir utilizando coloides, concentrados plaquetarios y plasma en lugar de cristaloides1,6. La WSACS también recomienda limitar el uso de cristaloides2.
Respecto a las características demográficas de la muestra, no encontramos asociación entre la edad, las comorbilidades y el SCA. En otros estudios la edad y estas comorbilidades han sido establecidas como factores de riesgo1,2,6. Suponemos que esta diferencia con respecto a los otros estudios podría deberse al pequeño tamaño de la muestra.
De los pacientes que desarrollaron SCA, los dos a los que no se les realizó laparotomía descompresiva fallecen, mientras que la mitad de los que sí se le realiza (2/4) sobreviven. Esto confirma que esta entidad sin tratamiento adecuado tiene una evolución fatal, y que es imperioso establecer pautas de diagnóstico y manejo adecuado que nos ayuden a identificar y tratar adecuadamente a estos pacientes.
En la literatura se describe como factor de riesgo la presencia de colecciones y masas intraabdominales1,2,6. Sin embargo, no encontramos asociación entre el desarrollo de SCA y el tamaño del aneurisma. Además, no hemos estudiado la presencia y dimensiones del hematoma retroperitoneal y su asociación con el SCA. Por lo que no podemos hacer inferencias sobre este punto.
El diseño retrospectivo y el tamaño de la muestra son las principales limitaciones del estudio. Por lo que no hemos podido realizar un análisis multivariante debido al tamaño muestral. Sin embargo, hasta ahora no hemos encontrado ningún estudio sobre el síndrome compartimental abdominal asociado a EVAR en AAAr en nuestro medio. Este primer estudio confirma que se trata de una complicación frecuente y de mal pronóstico, por lo que su conocimiento es imperativo. Nuestros hallazgos servirán como base para conocer mejor esta entidad y los factores asociados a ella y proponer protocolos en la atención de este subgrupo de pacientes. También servirá como base para el estudio en prospectivo de esta patología, que sin duda nos aportará más conocimiento para el manejo de la misma.
ConclusiónEn nuestro medio, el SCA es una patología frecuente que asocia una elevada morbimortalidad en pacientes con AAAr tratados mediante EVAR. El compromiso hemodinámico importante y la administración de grandes cantidades de cristaloides intravenosos y politransfusión durante el manejo asocian mayor incidencia de este síndrome.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Los autores queremos agradecer a los directores y tutores de la tercera edición del curso «Cómo escribir un artículo científico» de la SEACV su orientación para finalizar este artículo. Especialmente al Dr. Fidel Fernández Quesada y a la Dra. Melina Vega de Ceniga.