Objetivos. Determinar si el tratamiento endovascular (TEV) es una opción coste-efectiva en la terapia del aneurisma de aorta abdominal (AAA) respecto a la cirugía abierta, y evaluar el impacto presupuestario de una mayor utilización de estos dispositivos en el Sistema Nacional de Salud. Pacientes y métodos. Realizamos un análisis costeefectividad y coste-utilidad del TEV frente a cirugía abierta utilizando un modelo de Markov de ciclos mensuales basado en datos clínicos de la literatura (esencialmente el estudio EVAR-1) y la opinión de expertos. Tuvimos en consideración una población española hipotética de pacientes con AAA igual o superior a 5 cm y tributarios de cirugía abierta. El análisis lo realizamos desde la perspectiva del Sistema Nacional de Salud, y se descontaron costes y efectos futuros al 3,5%. Adicionalmente realizamos el impacto presupuestario y un análisis de sensibilidad probabilístico con la simulación de Monte-Carlo. Resultados. Los resultados mostraron que el TEV se asocia a una mayor efectividad que la cirugía abierta, con ganancias de entre 0,03 y 0,18 años de vida por paciente a uno y cuatro años, respectivamente (resultados similares si se utilizan años de vida ajustados por calidad). El coste medio por paciente fue mayor en TEV, entre 2.879 y 3.492 euros según distintos escenarios, el coste por años de vida ganado con TEV fue de 111.064 a 19.852 euros y el coste por años de vida ajustados por calidad ganado fue de 137.206 a 27.077 euros (análisis a uno y cuatro años, respectivamente). El impacto presupuestario de aumentar la introducción de la endoprótesis evaluada en España durante los próximos cuatro años representa el 0,5-2,2% del coste total de las AAA. Conclusiones. El TEV es una alternativa coste-efectiva con respecto a la intervención quirúrgica convencional, ya que a los cuatro años de seguimiento presenta valores por debajo del umbral de eficiencia usualmente aceptado en España. [ANGIOLOGÍA 2009; 61: 51-61]
Aims. To determine whether endovascular treatment (EVT) is a cost-effective option for the treatment of abdominal aortic aneurysm (AAA) with respect to open surgery, and to evalúate the budget impact of a more widespread utilisation of these devices in the Spanish National Health Service. Patients and methods. We performed a costeffectiveness and cost-utility analysis of EVT versus open surgery using a Markov model of monthly cycles based on clinical data from the literature (essentially the EVAR-1 study) and the opinion of experts. The sample taken into account was a hypothetical Spanish population of patients with AAA equal to or larger than 5 cm and who were candidates for open surgery. The analysis was performed from the perspective of the National Health Service, and future costs and effects were discounted at 3.5%. Additionally we also examined the budget impact and performed a probabilistic sensitivity analysis with Monte-Carlo simulation. Results. The results showed that EVT is associated to a higher degree of effectiveness than open surgery, with gains of between 0.03 and 0.18 years of life per patient at one and four years, respectively (similar results to those obtained if quality adjusted life years are used). The mean cost per patient was greater in EVT, between 2879 and 3492 euros, depending on the different scenarios, the cost-life years gained with EVT was from 111 064 to 19 852 euros and the cost-quality adjusted life years gained was from 137 206 to 27 077 euros (analysis at one and four years, respectively). The budget impact of increasing the introduction of stents evaluated in Spain over the next four years represents 0.5-2.2% of the total cost of AAA. Conclusions. EVT is a cost-effective alternative with respect to conventional surgical interventions, because at four years of follow-up it offers values that are below the efficiency threshold that is usually accepted in Spain. [ANGIOLOGIA 2009; 61: 51-61]
La incidencia y prevalencia de los aneurismas de aorta abdominal (AAA) están condicionadas por el mayor acceso a medios diagnósticos, así como por los cambios de criterio cuantitativo para definir el aneurisma de aorta, la edad, el sexo y la raza [1-4]. En España, para aneurismas ≥ 3 cm en varones de 65-75 años de edad hubo una prevalencia del 4,2% [5]. Por otra parte, la mortalidad fue de 2.614 personas mayores de 40 años (2.343 hombres y 271 mujeres) en el período 2002-2004 [6]. El registro EUROSTAR, con más de 5.000 pacientes con AAA, muestra supervivencias de cinco años del 76% [7].
Si bien históricamente el tratamiento de los AAA se efectuaba mediante cirugía abierta (CA), Parodi et al [8] introdujeron la técnica de reparación endovascular (TEV), que se asocia a una recuperación más rápida en el postoperatorio inmediato, con reducidos períodos en la Unidad de Cuidados Intensivos (UCI) y menor estancia hospitalaria [9].
El TEV ha demostrado su eficacia y seguridad en diversos ensayos clínicos controlados, estudios observacionales y series de casos [10-13].
El objetivo del estudio fue determinar si el TEV es una opción coste-efectiva en el tratamiento de los AAA en comparación con la CA y evaluar el impacto presupuestario de una utilización mayor de estos dispositivos en el Sistema Nacional de Salud (SNS).
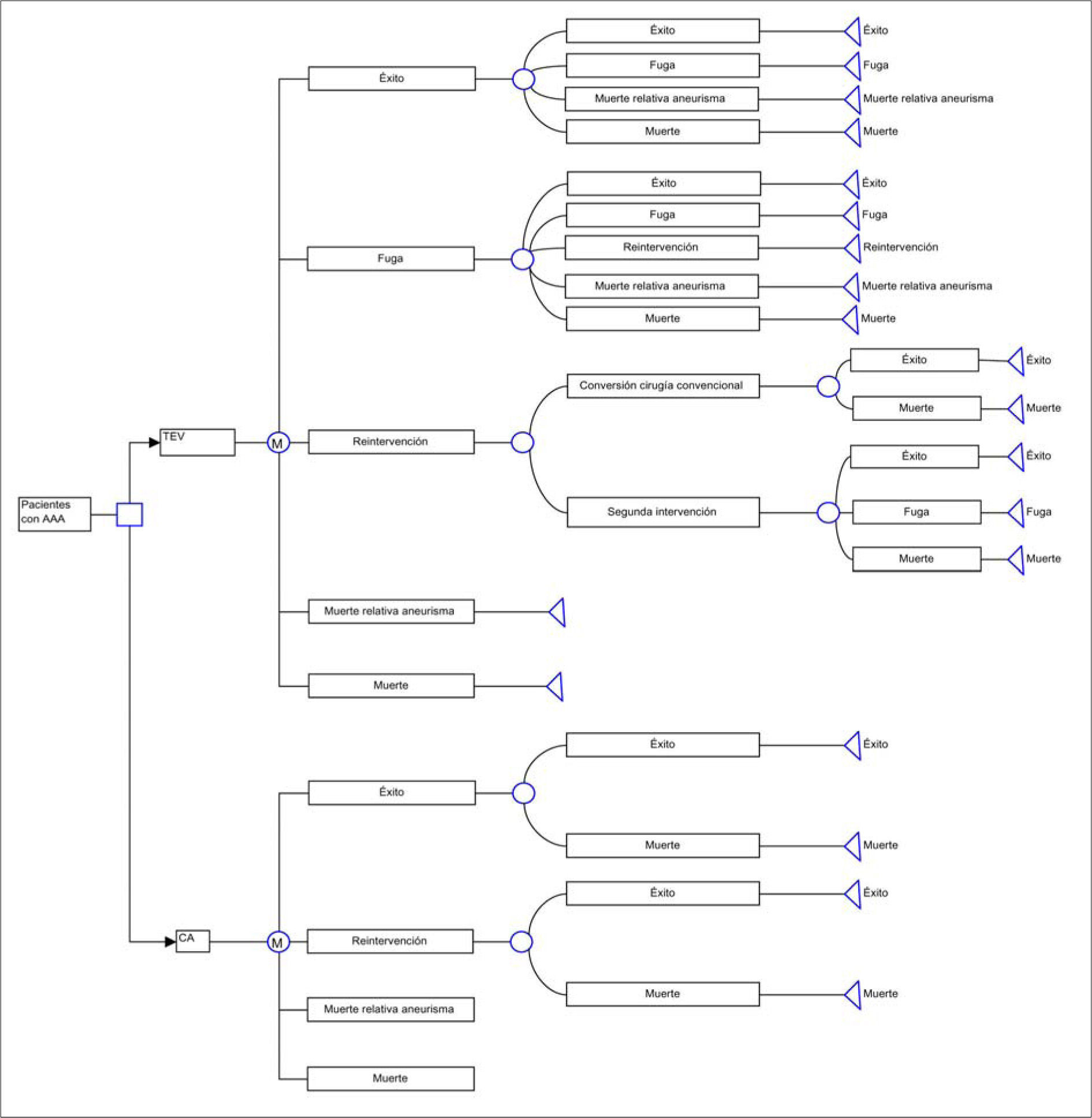
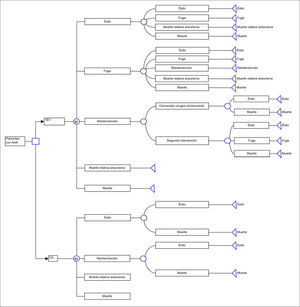
Pacientes y métodosModeloRealizamos un análisis coste-efectividad del TEV frente a CA con el empleo de un modelo de simulación de Markov (ciclos mensuales) para la estimación de los resultados a corto y largo plazo (Fig. 1).
El modelo permitió calcular los costes por paciente asociados a cada opción y estimar el costeefectividad incremental de TEV frente a la CA en España mediante la fórmula: (CostesTEV– CostesCA) / (EfectividadTEV– EfectividadCA).
Tuvimos en consideración una población española hipotética de pacientes con AAA ≥ 5 cm y tributarios de CA. Para el estudio excluimos los pacientes que requerían reparación urgente del AAA. Calculamos los años de vida (AV), los años de vida ajustados por calidad (AVAC) y el coste medio por paciente a uno, dos, tres y cuatro años para cada opción, y se estimó como indicador de coste-efectividad el coste/AV ganado, y como coste-utilidad, el coste/AVAC ganado. El análisis lo realizamos desde la perspectiva del SNS, con un horizonte temporal máximo de cuatro años, y descontando costes y efectos futuros al 3,5% anual. Todos los costes están expresados en euros del año 2008.
Parámetros del modeloLos parámetros clínicos y económicos del modelo fueron extraídos de los datos publicados en la literatura [10,12,14-21], y fueron validados por clínicos expertos. Los datos clínicos (Tabla I) los tomamos de comparaciones directas entre las opciones analizadas, en la mayoría de los casos el ensayo clínico aleatorizado EVAR-1. Los datos de mortalidad a largo plazo del TEV han sido extraídos de los estudios de Torsello et al [12], que no sólo son a largo plazo sino que se ajustan a la realidad de su utilización, y de Luengo y Polo [18], que reflejan las complicaciones encontradas en el registro español.
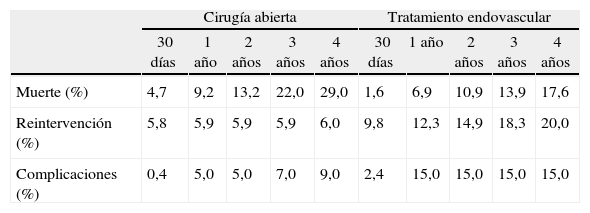
Principales parámetros del modelo [10,12,15,16,18-20]
| Cirugía abierta | Tratamiento endovascular | |||||||||
| 30 días | 1 año | 2 años | 3 años | 4 años | 30 días | 1 año | 2 años | 3 años | 4 años | |
| Muerte (%) | 4,7 | 9,2 | 13,2 | 22,0 | 29,0 | 1,6 | 6,9 | 10,9 | 13,9 | 17,6 |
| Reintervención (%) | 5,8 | 5,9 | 5,9 | 5,9 | 6,0 | 9,8 | 12,3 | 14,9 | 18,3 | 20,0 |
| Complicaciones (%) | 0,4 | 5,0 | 5,0 | 7,0 | 9,0 | 2,4 | 15,0 | 15,0 | 15,0 | 15,0 |
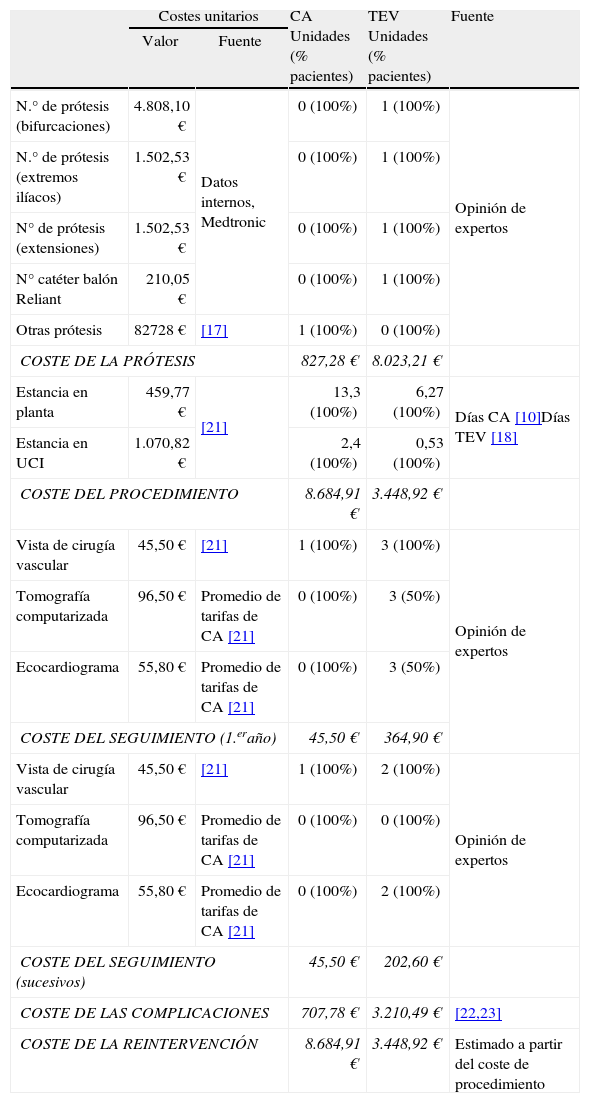
A partir del uso de recursos asociado al seguimiento y reintervenciones descrito por un grupo de expertos y los costes unitarios españoles, estimamos el coste al realizar CA o TEV (Tabla II). Para obtener específicamente el coste hospitalario de la intervención multiplicamos las estancias en la UCI (2,4 días CA frente a 0,53 días TEV) y en planta (13,3 días CA frente a 6,27 TEV) [10,18] por los costes medios por día de estancia según el tipo de sala (1.070,82 € y 459,77 €, respectivamente) [21].
Uso de recusos, costes unitarios y costes totales del modelo.
| Costes unitarios | CA Unidades (% pacientes) | TEV Unidades (% pacientes) | Fuente | ||
| Valor | Fuente | ||||
| N.° de prótesis (bifurcaciones) | 4.808,10 € | Datos internos, Medtronic | 0 (100%) | 1 (100%) | Opinión de expertos |
| N.° de prótesis (extremos ilíacos) | 1.502,53 € | 0 (100%) | 1 (100%) | ||
| N° de prótesis (extensiones) | 1.502,53 € | 0 (100%) | 1 (100%) | ||
| N° catéter balón Reliant | 210,05 € | 0 (100%) | 1 (100%) | ||
| Otras prótesis | 82728 € | [17] | 1 (100%) | 0 (100%) | |
| COSTE DE LA PRÓTESIS | 827,28 € | 8.023,21 € | |||
| Estancia en planta | 459,77 € | [21] | 13,3 (100%) | 6,27 (100%) | Días CA [10]Días TEV [18] |
| Estancia en UCI | 1.070,82 € | 2,4 (100%) | 0,53 (100%) | ||
| COSTE DEL PROCEDIMIENTO | 8.684,91 € | 3.448,92 € | |||
| Vista de cirugía vascular | 45,50 € | [21] | 1 (100%) | 3 (100%) | Opinión de expertos |
| Tomografía computarizada | 96,50 € | Promedio de tarifas de CA [21] | 0 (100%) | 3 (50%) | |
| Ecocardiograma | 55,80 € | Promedio de tarifas de CA [21] | 0 (100%) | 3 (50%) | |
| COSTE DEL SEGUIMIENTO (1.eraño) | 45,50 € | 364,90 € | |||
| Vista de cirugía vascular | 45,50 € | [21] | 1 (100%) | 2 (100%) | Opinión de expertos |
| Tomografía computarizada | 96,50 € | Promedio de tarifas de CA [21] | 0 (100%) | 0 (100%) | |
| Ecocardiograma | 55,80 € | Promedio de tarifas de CA [21] | 0 (100%) | 2 (100%) | |
| COSTE DEL SEGUIMIENTO (sucesivos) | 45,50 € | 202,60 € | |||
| COSTE DE LAS COMPLICACIONES | 707,78 € | 3.210,49 € | [22,23] | ||
| COSTE DE LA REINTERVENCIÓN | 8.684,91 € | 3.448,92 € | Estimado a partir del coste de procedimiento | ||
CA: cirugía abierta; TEV: tratamiento endovascular; UCI: Unidad de Cuidados Intensivos.
Los costes de seguimiento de TEV provienen de un registro del Hospital Clínic de Barcelona donde se recogieron, además de los parámetros clínicos, una serie de parámetros económicos [17]. Para ajustar los costes de seguimiento de CA, se tuvo en cuenta que los pacientes con CA no requieren de un seguimiento especial, en cambio los pacientes que han recibido TEV pueden requerir tomografía computarizada o ecografías para valorar la presencia de fugas [21]. Para el grupo de TEV incluimos tres visitas el primer año y dos visitas de seguimiento los siguientes.
Asimismo, el coste de las complicaciones se tomaron directamente de la explotación de los grupos de diagnósticos relacionados del Ministerio de Sanidad y Consumo [22] para la TEV y se aplicó un ajuste de éstos para estimar los costes unitarios de las complicaciones para CA [23].
Los costes de los dispositivos se basaron en precios actuales de mercado para el TEV y de una estimación según datos bibliográficos para la CA [17].
Los valores de utilidad para cada estado de salud, según la media del indicador EQ-5D, provienen directamente del estudio EVAR-1. Los valores del EQ-5D son un indicador numérico que representa el valor que la sociedad concede al estado de salud actual, que toma valores de 1 cuando representa la mejor salud posible y 0 representa la muerte. En este estudio mostraron que los primeros tres meses después de la cirugía, los pacientes con CA tienen una calidad de vida más baja (con una utilidad de 0,67), mientras que los pacientes con TEV tienen una calidad de vida significativamente más elevada (con una utilidad de 0,73). A partir del primer año observaron que la calidad de vida era similar tanto para el TEV como para la CA (EVAR-1).
El grupo de expertos confirmó la elección del ensayo EVAR-1 como el más próximo a nuestra realidad asistencial, tal y como se puede comprobar en los datos del uso tutelado del ISCIII y de la evaluación de Luengo y Polo [18]. Además, excluimos la incorporación de datos provenientes del ensayo multicéntrico aleatorio controlado EVAR-2 debido a que sólo contemplaba pacientes > 60 años con un tamaño de aneurisma > 5,5 cm en los cuales no era electiva la CA. Igualmente, los resultados encontrados en el estudio EVAR-2 se deben tomar con precaución, ya que un número sustancial de pacientes aleatorizados al grupo sin cirugía precisó finalmente intervención. Por otro lado, la utilización del EVAR-2 nos hubiese obligado a llevar a cabo comparaciones indirectas entre TEV y CA que derivarían en resultados con un grado de incertidumbre muy elevado.
Análisis del impacto presupuestarioAdicionalmente analizamos el impacto presupuestario basado en los costes estimados en el modelo de coste-efectividad, y lo combinamos con estimaciones del uso de los TEV evaluados en España. Para desarrollar el análisis hemos comparado cómo afectaría económicamente una mayor introducción de la endoprótesis evaluada (Talent ®) respecto a la evolución natural del mercado de endoprótesis durante los próximos cuatro años. Asumimos que el crecimiento de la implantación en el mercado de las endoprótesis se basa en la decisión de los clínicos, y la tendencia es incrementar la presencia de esta técnica en el SNS, independientemente de que Talent ® incremente su presencia en el ámbito español.
Análisis de sensibilidadPara valorar la influencia de la incertidumbre de los parámetros en los resultados del estudio y confirmar la solidez de los resultados obtenidos, realizamos un análisis de sensibilidad probabilístico mediante una simulación de Monte-Carlo de segundo orden, de tal forma que simulamos 1.000 veces el coste-efectividad de cada comparación [24]. Para llevar a cabo el análisis de sensibilidad seleccionamos unas distribuciones fijas, y estimamos los parámetros de cada distribución en función de los datos primarios recopilados [25]. Este tipo de tratamiento de la incertidumbre es aconsejable cuando cabe la posibilidad de que los resultados puedan sufrir importantes cambios. Es evidente que no todos los pacientes se comportan como el paciente 'típico', así que el modelo refleja de forma explícita la variabilidad que pueda existir entre los distintos sujetos analizados. En el presente estudio, por ejemplo, los días de estancia en planta o la probabilidad de los pacientes de recibir un tratamiento específico no son parámetros constantes. La incorporación de esta incertidumbre es el objeto del análisis de sensibilidad probabilístico. Al simular los resultados, conseguimos observar con qué probabilidad las conclusiones de los resultados básicos se mantienen estables, ya que todos los parámetros estudiados son objeto de variación de forma simultánea. Con ello logramos la validación interna de los resultados e imputamos una distribución log-normal para los costes, una distribución normal para el uso de recursos y una distribución beta para las probabilidades del modelo según la variabilidad descrita en los estudios.
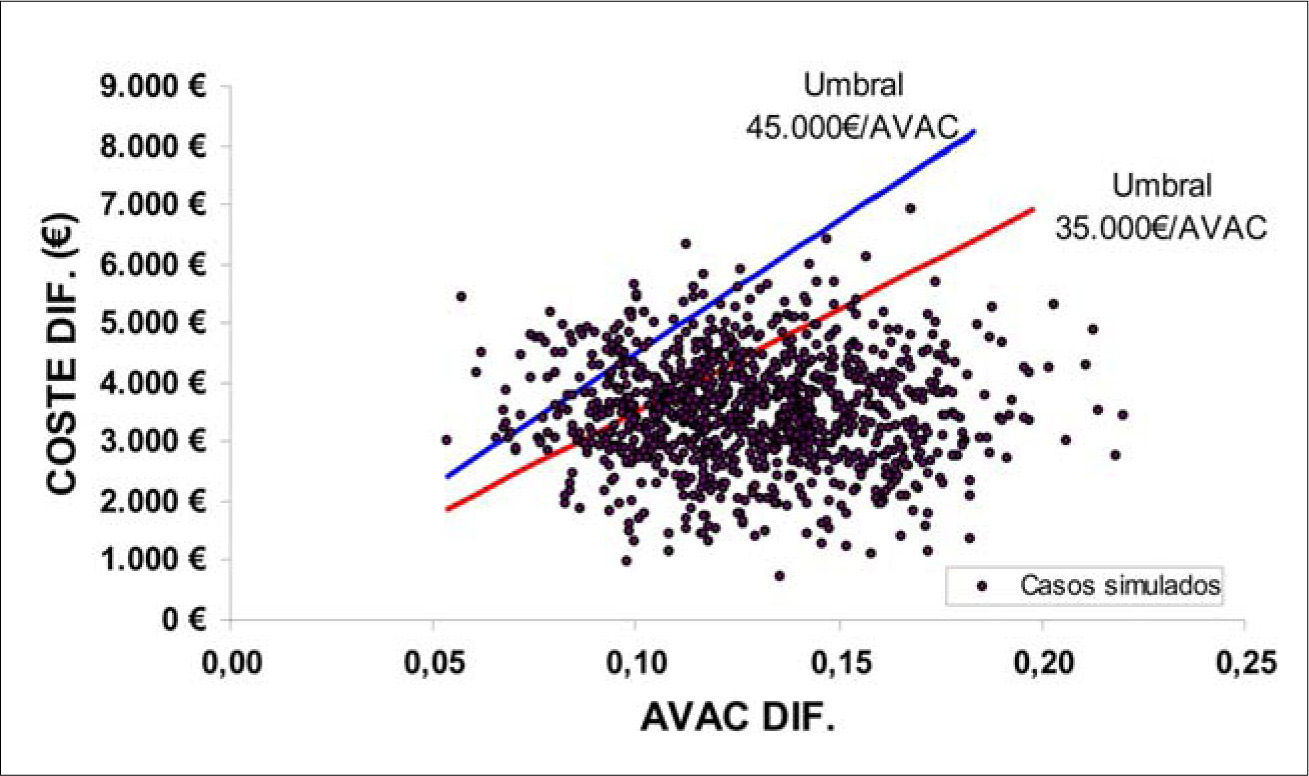
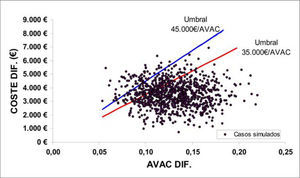
Los resultados del análisis de sensibilidad del modelo los expresamos mediante el plano coste-efectividad en el que representamos en el eje de abscisas los AVAC incrementales, y en el eje de ordenadas, los costes incrementales de TEV frente a CA. Cada punto mostrado en la gráfica simboliza la diferencia en los costes y los efectos de TEV respecto a CA del escenario simulado según las distribuciones y los parámetros estipulados. En el mismo plano mostramos el umbral de eficiencia que indica la razón coste-efectividad incremental asumible por las administraciones de la sanidad española según la bibliografía (aproximadamente 35.000 €/AVAC para ser coste-efectivo y 45.000 €/AVAC para ser costeefectivo de forma moderada) [26,27].
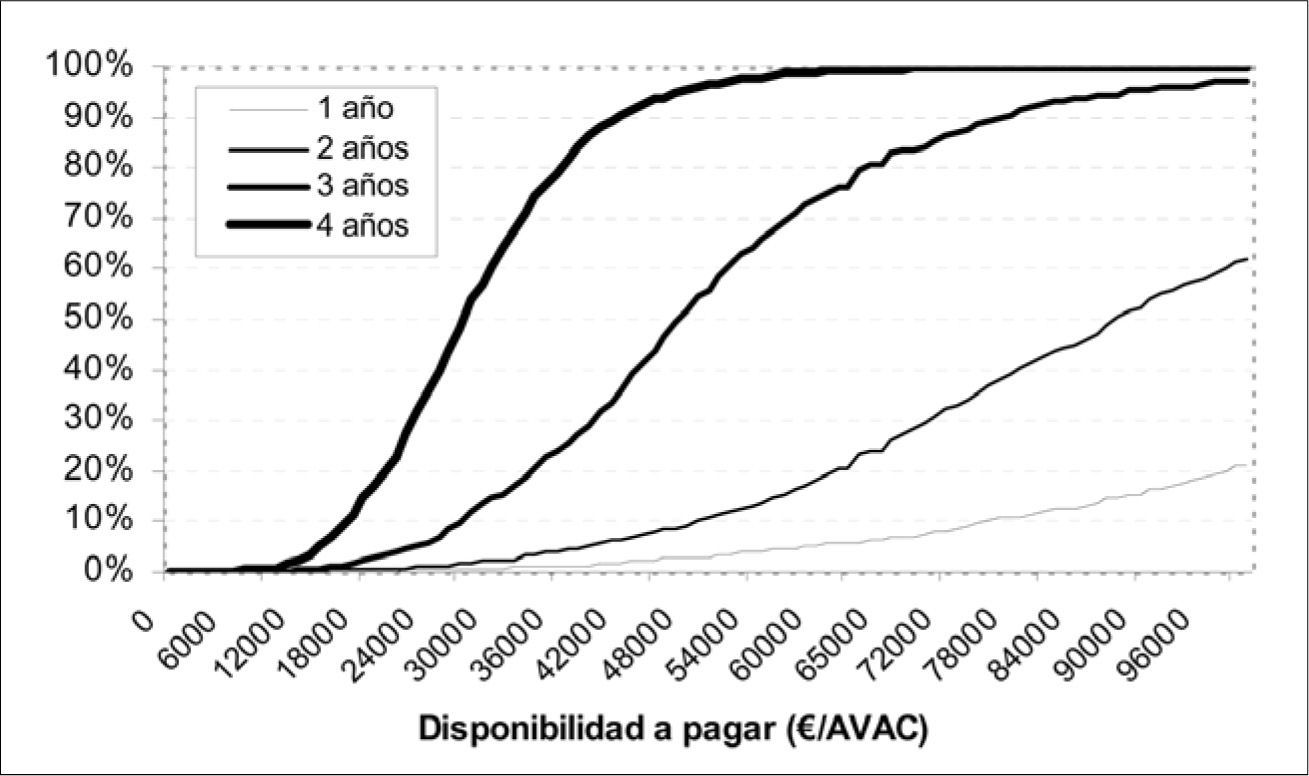
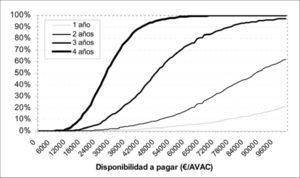
Por otro lado, representamos la curva de aceptabilidad, donde estimamos mediante el modelo de simulación con qué probabilidad un decisor debe escoger un tratamiento según su disponibilidad a pagar.
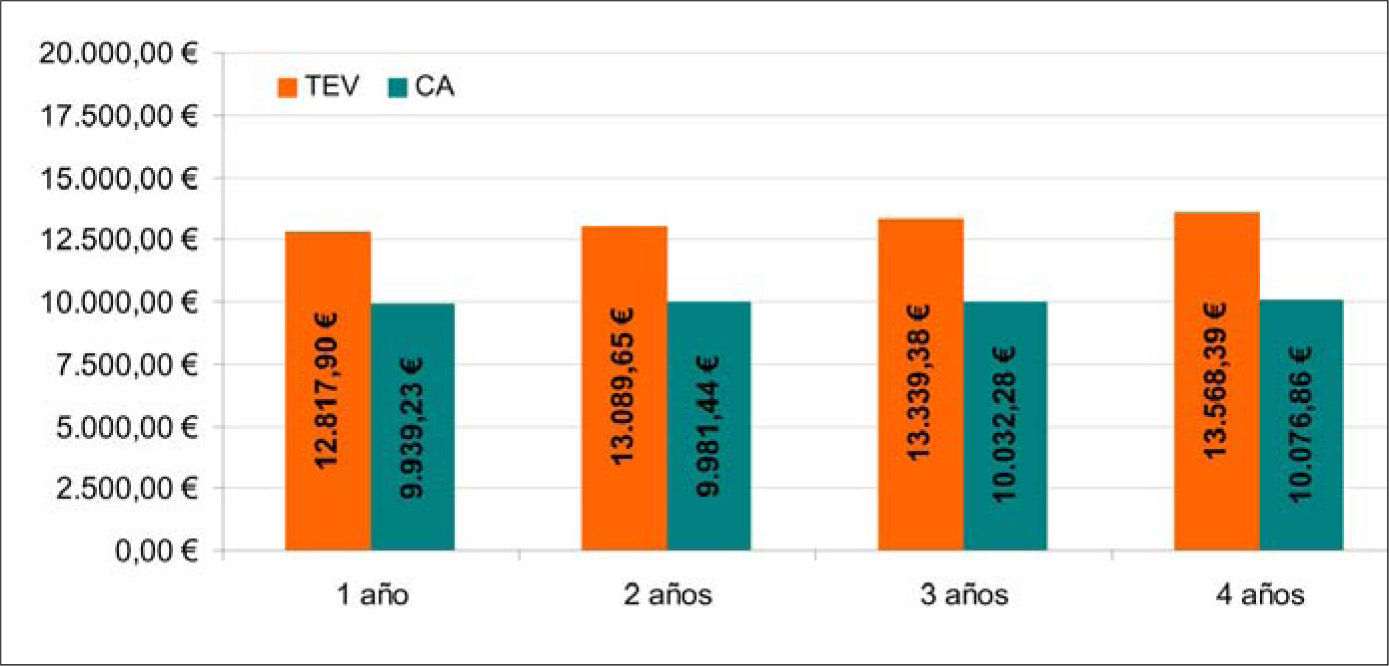
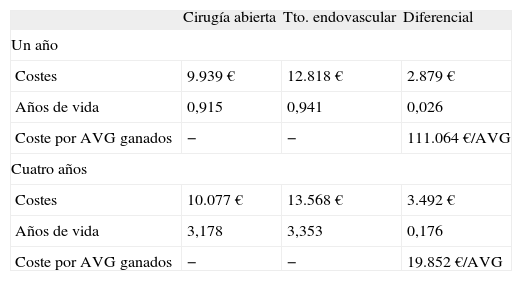
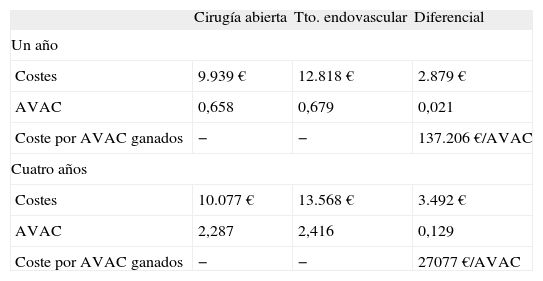
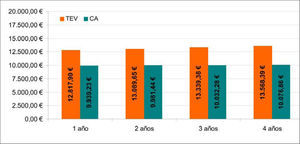
ResultadosAnálisis coste-efectividadEl coste medio por paciente del TEV a los cuatro años fue de 13.568 € y de 10.076 € para la CA (Fig. 2). De tal forma que el coste medio anual por paciente fue mayor en el TEV, intervalo entre 2.879 € y 3.492 € adicionales. El coste de la prótesis para el TEV queda parcialmente compensado a los 30 días debido a que el coste hospitalario del procedimiento era aproximadamente un 60% inferior al de la CA.
Los resultados respecto a la salud (años de vida) mostraron que el TEV se asocia a una mayor efectividad en relación con la CA, con ganancias de dos meses de vida adicionales por paciente a los cuatro años (Tabla III). De forma similar a los resultados de AV ganados, el TEV produce un aumento de 0,02 AVAC y 0,13 AVAC respecto a la CA al año y a los cuatro años, respectivamente (Tabla IV).
Resultados del análisis coste-efectividad del tratamiento endovascular frente a cirugía abierta.
| Cirugía abierta | Tto. endovascular | Diferencial | |
| Un año | |||
| Costes | 9.939 € | 12.818 € | 2.879 € |
| Años de vida | 0,915 | 0,941 | 0,026 |
| Coste por AVG ganados | − | − | 111.064 €/AVG |
| Cuatro años | |||
| Costes | 10.077 € | 13.568 € | 3.492 € |
| Años de vida | 3,178 | 3,353 | 0,176 |
| Coste por AVG ganados | − | − | 19.852 €/AVG |
AVG: años de vida ganados.
Resultados del análisis coste-utilidad del tratamiento endovascular frente a cirugía abierta.
| Cirugía abierta | Tto. endovascular | Diferencial | |
| Un año | |||
| Costes | 9.939 € | 12.818 € | 2.879 € |
| AVAC | 0,658 | 0,679 | 0,021 |
| Coste por AVAC ganados | − | − | 137.206 €/AVAC |
| Cuatro años | |||
| Costes | 10.077 € | 13.568 € | 3.492 € |
| AVAC | 2,287 | 2,416 | 0,129 |
| Coste por AVAC ganados | − | − | 27077 €/AVAC |
AVAC: años de vida ajustados por calidad.
De tal modo que observamos que el coste/AV ganado con TEV fue de 111.064 € a 19.852 € y el coste/AVAC ganado fue de 137.206 € a 27.077 € (análisis de uno y cuatro años, respectivamente) (Tablas III y IV). Asimismo, si se tiene en cuenta que el umbral de eficiencia en España es aproximadamente de 35.000 €/AVAC para ser coste-efectivo y de 45.000 €/AVAC para ser coste-efectivo de forma moderada (equivalente para €/AVG), se observa que el TEV es una opción moderadamente coste-efectiva a partir del tercer año y es coste-efectiva al cuarto año [26,27].
El análisis de sensibilidad probabilístico mostró que el coste-utilidad mediano a los cuatro años es de 27.384 €/AVAC (rango intercuartílico: 12.836 €/ AVAC). La mayor parte de los 1.000 casos simulados presentó razones de coste por AVAC ganado por debajo del umbral de eficiencia comúnmente utilizado en España [26] (Fig. 2). La representación de la curva de aceptabilidad durante los cuatro años del análisis (TEV frente a CA) permite cuantificar mejor estos resultados, que muestran que el TEV es una opción coste-efectiva en un 60, 77 y 94% de los casos simulados (Figs. 3 y 4). Para estos resultados se utilizó como umbral de coste-efectividad un valor de 30.000, 35.000 y 45.000 € por AVAC ganado, respectivamente [26,27].
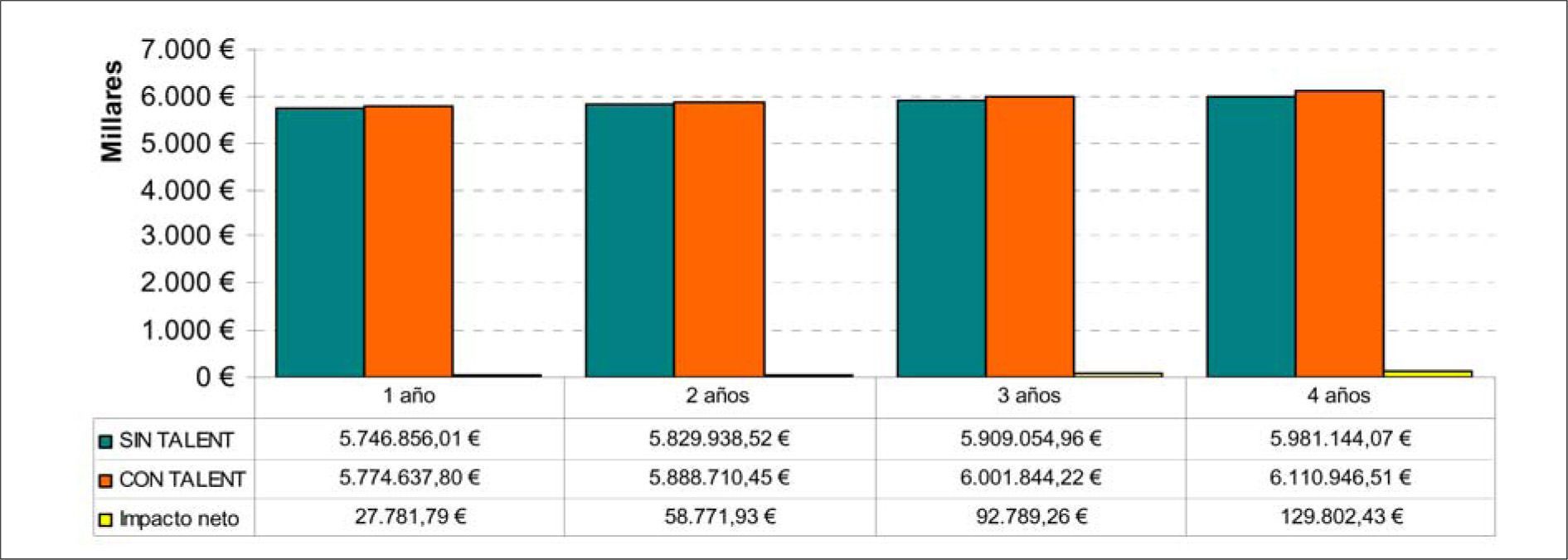
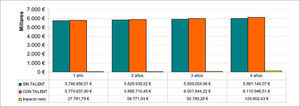
Impacto presupuestarioCon el análisis del impacto presupuestario estimamos de forma cuantitativa la alteración prevista en el gasto sanitario asociado a la atención de una patología tras la introducción de una intervención sanitaria nueva [28]. En términos de impacto presupuestario para una población hipotética de 500 pacientes, asumimos un incremento de uso del TEV del 3,6% anual, y que la endoprótesis evaluada supondrá entre el 35 y 40% del total de prótesis endovasculares implantadas en España durante los próximos cuatro años. Específicamente, el coste total adicional variaría entre 27.782 y 129.802 € (aproximadamente un 0,5 y un 2,2% del coste total de los AAA) durante los próximos cuatro años (Fig. 5). Como resultado, el coste neto total de la introducción progresiva de este dispositivo tendrá unas consecuencias mínimas.
DiscusiónEl tratamiento con el TEV se ha mostrado como una alternativa efectiva y segura que ofrece mejores resultados perioperatorios que la CA en el manejo de los AAA. Esta alternativa está recomendada para pacientes que prefieran el procedimiento menos invasivo y aquellos para los que el abordaje mediante la CA resulta demasiado arriesgado [13,15]. Además, los pacientes con menos patología asociada (coronariopatías o neumopatías, etc.) suelen cumplir con mayor facilidad los criterios anatómicos para el TEV [13]. Estas circunstancias dificultan una evaluación no sesgada de las dos técnicas.
La comparación de TEV con CA mostró que el primero compensa los costes adicionales debido a una menor incidencia de la mortalidad a corto plazo. Ésta se traduce en una ganancia en AVAC progresiva en el tiempo, y muestra que el análisis de coste-efectividad tiene una relación estrecha con el horizonte temporal. Por otro lado, un estudio en el Reino Unido demostró que el TEV aumenta 0,10 AVAC respecto a la CA, aunque obtuvieron una razón coste-efectividad incremental de 110.000 £ por AVAC ganado, que es considerablemente más elevada que la presentada en nuestro estudio [29]. Los AVAC constituyen una medida de los resultados que incorpora en una única medida las dos dimensiones relevantes del beneficio de un tratamiento: la mejora en la supervivencia y las ganancias en calidad de vida. Los valores que se utilizan para ponderar o ajustar los AV ganados en función de la calidad reflejan las preferencias de los individuos en relación con los diferentes estados de salud. Sin embargo, en función del análisis de sensibilidad y los escenarios consiguieron una razón coste-efectividad incremental por debajo del umbral de eficiencia de 30.000 £. Bosch et al [30] probaron que la implementación del TEV presenta una razón de coste-efectividad incremental de 9.905 $ por AVAC respecto a la CA, y que los resultados son sensibles a las complicaciones, las roturas y los fallos a largo plazo. Previamente, Patel et al [31] ya demostraron que el TEV era coste-efectivo respecto a la CA con una razón coste-efectividad de 22.829 $, y los resultados no variaron significativamente al aumentar los costes asociados al procedimiento del TEV. Estos autores observaron que a pesar del coste adicional de la prótesis y la necesidad del seguimiento postoperatorio, el TEV es una alternativa coste-efectiva para el tratamiento de los AAA. Las diferencias en los resultados de los estudios coste-efectividad recientemente publicados son, en parte, secundarios a la disparidad en el diseño de los estudios, la estructura de costes en los diferentes países y a los supuestos asumidos, entre los que destacan el descuento aplicado a los costes o las características de los pacientes incluidos [32].
La principal limitación del presente estudio radica en que los parámetros clínicos del modelo provienen del único ensayo clínico controlado (EVAR-1), donde se comparan las dos opciones evaluadas, es decir, el TEV y la CA. Sin embargo, este estudio, aunque se suponga la mejor evidencia científica disponible, actualmente podría haber quedado obsoleto, ya que desde su realización, la práctica clínica en el manejo de los AAA ha cambiado significativamente. Hoy en día, los resultados del TEV han mejorado en forma de menores tasas de reintervenciones y disminución de la estancia hospitalaria [12]. Por ello podemos suponer que nuestro análisis probablemente ha sobreestimado el coste del TEV y ha subestimando su efectividad.
Actualmente no disponemos de información sobre los costes unitarios para este tipo de pacientes y su tratamiento con el fin de poder separar correctamente la imputación de los costes. Por ello se está llevando a cabo un estudio prospectivo de la endoprótesis utilizada (Talent ®) que permitirá conocer estos costes en la práctica clínica en España.
Por último, cabe constatar que no existen resultados a largo plazo que permitan asegurar la situación del TEV frente a la CA [33]. Las innovaciones y mejoras constantes en los dispositivos, así como el aumento de la experiencia de los cirujanos han permitido ampliar el espectro de los pacientes susceptibles de ser tratados mediante la técnica endovascular.
En conclusión, el presente estudio sugiere que el TEV es una alternativa coste-efectiva con respecto a la intervención quirúrgica convencional, ya que presenta valores por debajo del umbral de eficiencia definido en España.
Conflicto de intereses. J.M.R. trabaja para Medtronic Ibérica, que es la empresa promotora del estudio; C.C. trabaja para una consultora independiente y ha participado en la investigación como experto en evaluación económica; los demás autores han participado como expertos clínicos en el estudio.
Agradecimientos. E. Ros (H. Clínico San Cecilio, Granada), J.A. Lechón (H. Miguel Servet), R. Rodríguez (H. Virgen de La Salud), M. Matas (H. Vall d'Hebron, Barcelona) y Max Brosa (Oblikue Consulting).