Puntos clave
La púrpura trombopénica idiopática (PTI) es el trastorno autoinmunitario más común en niños, con una incidencia estimada de 5 casos/100.000 niños al año1, con un pico máximo de edad de 2 a 5 años. Se trata de un proceso generalmente benigno, adquirido y de origen desconocido. La presentación típica es un niño sano, que de forma brusca presenta un cuadro de púrpura mucocutánea o sangrado menor, secundario a trombopenia sin otras alteraciones clínicas ni analíticas. En el 60% de los casos está precedida de una infección viral o bacteriana aguda. También se ha descrito después de la vacuna triple vírica. Se debe a la presencia de autoanticuerpos dirigidos frente a antígenos de la membrana de las plaquetas. Estas plaquetas recubiertas son destruidas por los macrófagos del bazo y otros tejidos reticuloendoteliales. En algunos casos el mecanismo de acción parece mediado por linfocitos T citotóxicos. Puede cursar de forma aguda, cuando se resuelve en menos de 6 meses o de forma crónica.
En este artículo se revisará el tratamiento de la PTI aguda y crónica.
TratamientoEl manejo de la PTI sigue debatiéndose desde hace décadas. La mayoría de los niños diagnosticados de PTI se recupera espontáneamente en 6 meses, incluso en 6 semanas, con o sin tratamiento e independientemente del tratamiento elegido2. La mayoría no presenta clínica de sangrado importante, incluso con < 10.000 plaquetas/μl3,4 y el riesgo de hemorragia intracraneal, complicación más seria de la PTI, que ocurre en el 0,1 y el 0,5%5. El tratamiento acelera la recuperación de la cifra de plaquetas, pero no reduce el riesgo de desarrollar PTI crónica ni se ha demostrado que disminuya el riesgo de complicaciones vitales, dada su baja prevalencia2,4,5.
Tanto la British Society for Hematology (2006)6, que basa sus decisiones en la clínica y no en la cifra de plaquetas, como la American Society of Hematology (1996)7, que también limita el tratamiento, pero que establece el mínimo para indicar tratamiento médico en < 10.000 plaquetas/μl, han propuesto unas guías de manejo basadas en la opinión de expertos y estudios observacionales sobre las que han trabajado otros grupos8 (tabla 1).
Recomendaciones generales de la American Society of Hematology (ASH) y la British Society for Hematology (BSH)
| ASH-1996 | BSH-2003 |
|---|---|
| No deben hospitalizarse con > 30.000 plaquetas | Manejo basado en la clínica de sangrado |
| Tratamiento de elección: corticoides o IGIV | Niños con sangrado leve se vigilarán con controles frecuentes en función de los síntomas. No precisan ingreso |
| Indicación de tratamiento si < 20.000 plaquetas con sangrado importante y < 10.000 plaquetas con o sin sangrado | Tratamiento de elección: corticoides orales (máximo 2 semanas independientemente de la respuesta) |
| La IGIV y IG anti-D deben reservarse para sangrado más serio | |
| Esplenectomía: si > 12 meses de evolución con clínica de sangrado y < 10.000 plaquetas | Esplenectomía: si sangrado vital o PTI refractaria con clinica de sangrado y limitación de la calidad de vida |
PTI: púrpura trombocitopénica idiopática; IGIV: gammaglobulina hiperinmune intravenosa.
Cada vez está más aceptado que el diagnóstico de PTI aguda se establece por el cuadro clínico y una analítica compatibles, y en este momento no son necesarios estudios adicionales.
Tratamiento de soporteIndependientemente del tratamiento que se siga, debe recomendarse reposo relativo restringiendo el deporte, sobre todo los deportes de contacto. Debe evitarse medicación con actividad antiplaquetaria (como el ácido acetilsalicílico y sus derivados) y los anticoagulantes.
Tratamiento médicoCuando se decide iniciar tratamiento farmacológico, las opciones terapéuticas de primera línea son los corticoides, la inmunoglobulina intravenosa (IGIV) y la gammaglobulina anti-Rho (IG anti-D)8. Varios estudios han demostrado que cualquiera de estos tratamientos acorta el tiempo de trombopenia sintomática frente a no tratamiento, pero no está claro que se prevenga sangrado mayor en pacientes con mínimo o sin sangrado5 ni tampoco la evolución a PTI crónica.
Corticoides. Los corticoides se usan desde hace años en el tratamiento de la PTI en todos los grupos de edad y está demostrado que aumentan el número de plaquetas más rápido que sin tratamiento.
Hay una gran variedad de regímenes, y ninguno ha demostrado una clara superioridad sobre los otros. Las pautas más comunes son:
- –
Prednisona: 2mg/kg (máximo 60mg dosis) al día dividido en 3 dosis durante 2 semanas, bajando la dosis en la semana posterior.
- –
Prednisona: 4mg/kg al día dividido en 3 dosis durante 4 días.
- –
Metilprednisolona: 30mg/kg al día intravenoso (i.v.), durante 3 días.
Se puede repetir la pauta en caso de persistencia, recurrencia o PTI crónica.
La mayoría de los pacientes responden inicialmente a los corticoides, pero algunos recurren al suspender el tratamiento.
Los efectos secundarios incluyen cambios en el comportamiento, alteración del sueño, aumento del apetito, ganancia de peso y los derivados del hipercortisolismo. Es deseable evitar un tratamiento crónico de corticoides por sus efectos a largo plazo, como en el crecimiento. Por esto deben plantearse tratamientos alternativos en los niños que necesitan tratamientos prolongados o repetidos.
Inmunoglobulina intravenosa. El mecanismo de acción no es del todo conocido. La IGIV aumenta más rápidamente el número de plaquetas que los corticoides9, la IG anti-D o sin tratamiento.
Las pautas varían desde 400mg/kg/día por 5 días a dosis únicas de 800–1.000mg/kg. Es preferible la administración de una sola dosis. La dosis única de 800mg/kg parece igual de efectiva que dosis superiores. La respuesta al tratamiento generalmente se observa desde las primeras 24h.
Los efectos secundarios incluyen síntomas gripales, como náuseas, vómitos, cefalea y fiebre. También puede aparecer neutropenia hasta en un 30% de los casos.
Inmunoglobulina anti-Rho (D). En los últimos años se ha incluido dentro del tratamiento de primera línea para la PTI. Hay varios estudios que muestran una seguridad y eficacia comparable a la IGIV para la forma aguda y crónica10–12.
Se administra una dosis única de 50 o 75μg/kg i.v.
Los efectos secundarios son menores que con la IGIV, pero se puede producir hemólisis con un descenso de 0,5-2g/dl de hemoglobina y, aunque raro, se ha descrito fallo renal y coagulación intravascular diseminada12,13.
Transfusión de plaquetas. Indicada ante situaciones de sangrado vital, como la hemorragia intracraneal y, en ocasiones, ante sangrado profuso digestivo, genitourinario, nariz o boca14. Deben transfundirse las plaquetas (hasta 5–10 unidades por cada 10kg) junto con altas dosis de corticoides (p. ej., 30mg/kg de metilprednisolona) e IGIV (800–1.000mg/kg). Sólo en casos excepcionales debe considerarse la esplenectomía.
Púrpura trombocitopénica crónicaEn un 20-30% de los niños persistirá la trombopenia a los 6 meses del diagnóstico. En un tercio de éstos todavía se han observado remisiones espontáneas en los meses siguientes, incluso años después, sobre todo en los menores de 10 años15. Los pacientes con PTI crónica deben ser evaluados para excluir otras causas subyacentes de trombopenia, incluyendo anticuerpos antivirales (virus de la inmunodeficiencia humana, hepatitis C, Ebstein-Barr, citomegalovirus, parvovirus, herpesvirus-6 y 8), aspirado y biospia de médula ósea (mielodisplasia o fallo medular), estudio de enfermedades autoinmunitarios y del colágeno (anticuerpos antinucleares, anti- ADN, C3, C4, etc.), inmunoglobulinas (inmunodeficiencia variable común) y cribado para Helicobacter pylori15.
De los pacientes con PTI crónica muchos mantienen cifras > 20.000/μl y no van a precisar tratamiento. El tratamiento médico debe usarse en pacientes con sangrado o que van a requerir cirugía o extracción dental. Niñas con sangrado excesivo durante la menstruación pueden requerir además tratamiento hormonal y tienden a comportarse como la PTI del adulto.
La PTI crónica refractaria severa ocurre en un 2-10% de los niños con PTI aguda15. El tratamiento debe ser individualizado y enfocado a minimizar el riesgo de sangrado valorando los efectos secundarios y la calidad de vida.
Tratamiento médico. Las opciones son similares a las de la PTI aguda, con corticoides, IGIV e IG anti-D. Debe evitarse el tratamiento prolongado con corticoides por sus efectos a largo plazo. Su efecto suele ser transitorio, mejorando la clínica y la cifra de plaquetas, pero no resuelven la PTI crónica.
Esplenectomía. La esplenectomía es curativa en el 70-80% de los niños, a pesar de lo cual el momento para para su realización, indicación y manejo en niños no está estandarizada16,17. Las dudas se deben al riesgo a largo plazo de sepsis por gérmenes encapsulados, sobre todo en los más pequeños, las remisiones espontáneas que todavía ocurrren años después y tratamientos alternativos recientes. Hay consenso acerca de su indicación para niños con trombopenia severa persistente después de 12–24 meses, sangrado vital o sangrado crónico que limita la calidad de vida16,17. La tendencia es a la esplenectomía por laparoscopia sobre la cirugía abierta. Debe realizarse profilaxis previa a la cirugía para reducir el riesgo de sangrado intra y postoperatorio. Se administrará IGIV o IG anti-D +/– corticoides parenterales si la cifra de plaquetas es < 50.000/μl y se transfundirán plaquetas sólo si la cifra es < 10.000/μl7. Deben vacunarse un mínimo de 2 semanas antes frente al neumococo, haemophilus tipo b y meningococo. Debe realizarse profilaxis infecciosa poscirugía con penicilina o equivalente durante un mínimo de 1 año o hasta los 5 años de vida, y algunos expertos la recomiendan hasta de por vida. En caso de no ser efectiva la esplenectomía debe buscarse la presencia de bazo accesorio y resecarlo.
Rituximab (anti-CD20). Anticuerpo monoclonal. Se ha convertido en tratamiento de primera línea para niños que no responden a la esplenectomía y se usa cada vez más para evitarla. La administración de 375mg/m2/dosis/semana durante 4 semanas ha demostrado en niños una respuesta total o parcial del 30-50% a largo plazo18–20. Pacientes que han respondido, pero luego recaen, pueden responder de forma similar en cursos siguientes. Se puede administrar de forma ambulante.
Con la perfusión se han descrito reacciones generalmente leves como fiebre, escalofríos y picor de garganta. La incidencia de enfermedad del suero es del 5-10%. A pesar de la deplección prolongada de linfocitos B, un descenso de inmunoglobulinas es raro (excepto quizás en los más pequeños) y las infecciones graves son raras. Puede reactivarse la infección por hepatitis B en protadores crónicos, por lo que debe estudiarse previamente21.
Otros tratamientos para la púrpura trombocitopénica crónica refractaria (tabla 2)Se ha ensayado el uso de vincristina, azatioprina, mercaptopurina, micofenolato, ciclosporina, danazol, interferon y ciclofosfamida, basado en estudios observacionales en adultos.
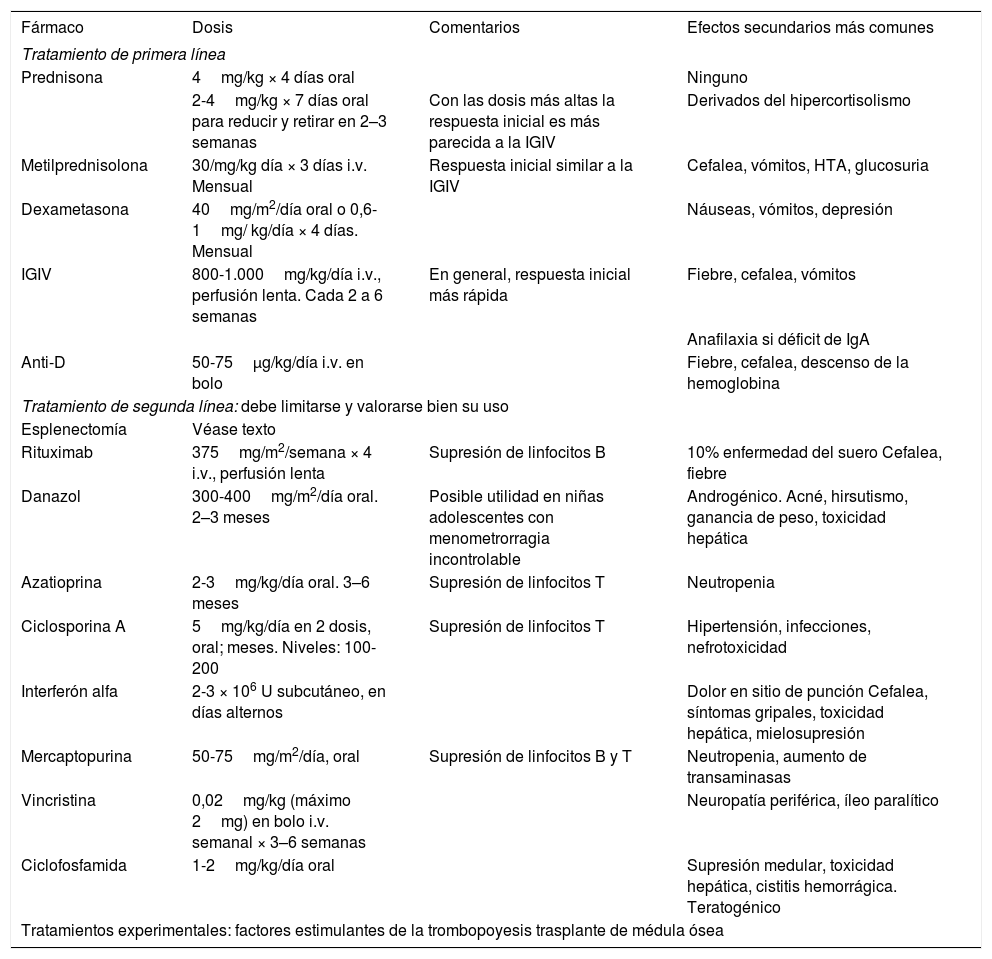
Pautas más habituales de tratamiento
| Fármaco | Dosis | Comentarios | Efectos secundarios más comunes |
|---|---|---|---|
| Tratamiento de primera línea | |||
| Prednisona | 4mg/kg × 4 días oral | Ninguno | |
| 2-4mg/kg × 7 días oral para reducir y retirar en 2–3 semanas | Con las dosis más altas la respuesta inicial es más parecida a la IGIV | Derivados del hipercortisolismo | |
| Metilprednisolona | 30/mg/kg día × 3 días i.v. Mensual | Respuesta inicial similar a la IGIV | Cefalea, vómitos, HTA, glucosuria |
| Dexametasona | 40mg/m2/día oral o 0,6-1mg/ kg/día × 4 días. Mensual | Náuseas, vómitos, depresión | |
| IGIV | 800-1.000mg/kg/día i.v., perfusión lenta. Cada 2 a 6 semanas | En general, respuesta inicial más rápida | Fiebre, cefalea, vómitos |
| Anafilaxia si déficit de IgA | |||
| Anti-D | 50-75μg/kg/día i.v. en bolo | Fiebre, cefalea, descenso de la hemoglobina | |
| Tratamiento de segunda línea: debe limitarse y valorarse bien su uso | |||
| Esplenectomía | Véase texto | ||
| Rituximab | 375mg/m2/semana × 4 i.v., perfusión lenta | Supresión de linfocitos B | 10% enfermedad del suero Cefalea, fiebre |
| Danazol | 300-400mg/m2/día oral. 2–3 meses | Posible utilidad en niñas adolescentes con menometrorragia incontrolable | Androgénico. Acné, hirsutismo, ganancia de peso, toxicidad hepática |
| Azatioprina | 2-3mg/kg/día oral. 3–6 meses | Supresión de linfocitos T | Neutropenia |
| Ciclosporina A | 5mg/kg/día en 2 dosis, oral; meses. Niveles: 100-200 | Supresión de linfocitos T | Hipertensión, infecciones, nefrotoxicidad |
| Interferón alfa | 2-3 × 106 U subcutáneo, en días alternos | Dolor en sitio de punción Cefalea, síntomas gripales, toxicidad hepática, mielosupresión | |
| Mercaptopurina | 50-75mg/m2/día, oral | Supresión de linfocitos B y T | Neutropenia, aumento de transaminasas |
| Vincristina | 0,02mg/kg (máximo 2mg) en bolo i.v. semanal × 3–6 semanas | Neuropatía periférica, íleo paralítico | |
| Ciclofosfamida | 1-2mg/kg/día oral | Supresión medular, toxicidad hepática, cistitis hemorrágica. Teratogénico | |
| Tratamientos experimentales: factores estimulantes de la trombopoyesis trasplante de médula ósea | |||
HTA: hipertensión arterial; IGIV: gammaglobulina hiperinmune intravenosa; i.v.: intravenoso.
Tratamiento de Helicobacter pylori. En varios estudios se ha implicado la infección por H. pylori en la PTI de los adultos, pero en la actualidad no hay ninguna evidencia que indique un beneficio para realizar el cribado en niños con PTI crónica15.
Trasplante hematopoyético. Debe reservarse para los casos más refractarios que requieren transfusiones frecuentes y han fallado tras la esplenectomía y otros agentes15. Con la ciclofosfamida a altas dosis se pretende eliminar los linfocitos reactivos implicados en esta enfermedad.
Tratamientos experimentales. Hay evidencia de que en algunos pacientes con PTI crónica hay un defecto de producción de plaquetas. Puede ser por anticuerpos antiplaquetarios que actúan sobre la maduración de los megacariocitos y/o un déficit relativo de trombopoyetina endógena22,23.
Se han mostrado eficaces 2 factores estimulantes de la trombopoyesis ensayados en adultos: