Puntos clave
- •
La hipoglucemia es frecuente en el neonato pero es controvertida su trascendencia fisiopatológica en el niño asintomático.
- •
En el periodo de transición a la vida extrauterina, las cifras bajas de glucosa desencadenan mecanismos contrarreguladores.
- •
No se han definido valores de glucosa críticos o duración de los mismos que conlleven efectos adversos en el recién nacido asintomático. Posiblemente, la provisión de sustratos alternativos para el cerebro sea determinante.
- •
La causa más frecuente de hipoglucemia neonatal es una alteración en el proceso fisiológico de transición metabólica.
- •
Se debe controlar la glucemia en los recién nacidos de grupos de riesgo (prematuros tardíos, pequeños para la edad gestacional e hijos de madre diabética), en los sintomáticos (la clínica es inespecífica) y en los que presentan otra condición que aumente el riesgo.
- •
Las recomendaciones sugieren intervención en el niño asintomático si la glucemia plasmática es < 36mg/dl, aumentando el aporte enteral. En niños sintomáticos, con cifras < 20–25mg/dl o hipoglucemia recurrente se indicará tratamiento iv.
La hipoglucemia es una de las alteraciones metabólicas más frecuentes en el neonato1 y resulta de un desequilibrio entre el aporte de glucosa y su utilización. A pesar de la gran cantidad de literatura sobre este tema, persisten muchas controversias respecto a la definición, el método y el lugar de obtención de la muestra, la sintomatología, el significado de la hipoglucemia asintomática, las indicaciones del tratamiento y su posible efecto en el neurodesarrollo2.
En esta actualización describiremos principalmente las novedades con respecto a las recomendaciones de monitorización y tratamiento del recién nacido con riesgo de hipoglucemia durante el período transicional. De forma más escueta, nos referiremos a otras afecciones menos prevalentes, cuándo sospecharlas y qué terapias específicas pueden requerir.
Homeostasis de la glucosaDefiniciones3–5La homeostasis de la glucosa es un proceso complejo, regulado por sistemas hormonales y enzimáticos. Para poder entender los cambios metabólicos que tienen lugar en el recién nacido, conviene recordar algunas definiciones sobre metabolismo energético:
- –
Gluconeogénesis: es la ruta metabólica por la que se sintetiza glucosa a partir de precursores que no son carbohidratos, principalmente el lactato (formado en músculo), el glicerol (que proviene de la degradación de triglicéridos) y casi todos los aminoácidos (de la dieta o la degradación de proteínas en músculo), a excepción de leucina y lisina. Es una ruta muy importante para mantener la glucemia en los periodos de ayuno.
- –
Glucogenólisis: es la ruta metabólica por la que se obtiene glucosa a partir del glucógeno que se almacena a nivel hepático. La segunda fuente importante de almacenamiento de glucosa es el glucógeno del músculo esquelético, pero este no está disponible para otros tejidos, debido a que el músculo carece de la enzima glucosa-6-fosfatasa.
- –
Glucogenogénesis: es la vía metabólica que se encarga de la síntesis de glucógeno a partir de la glucosa y que se realiza mediante la acción de la enzima glucógeno-sintasa.
- –
Glucólisis: es la ruta de degradación de la glucosa mediante la oxidación. Mediante esta vía, la glucosa se convierte principalmente en piruvato (glucólisis aerobia), que podrá entrar en el ciclo de Krebs que tiene lugar en la mitocondria. Así pues, es una vía de obtención de energía, que consigue hasta 38 moléculas de trifosfato de adenosina (ATP) de cada molécula de glucosa.
En la regulación de la glucosa y de las diferentes vías metabólicas implicadas, existen diversas hormonas que tienen un papel determinante, especialmente la insulina. Su síntesis tiene lugar en las células β de los islotes de Langerhans pancreáticos y su secreción depende, sobre todo, de la glucosa, siendo sus principales efectos anabólicos (tabla 1).
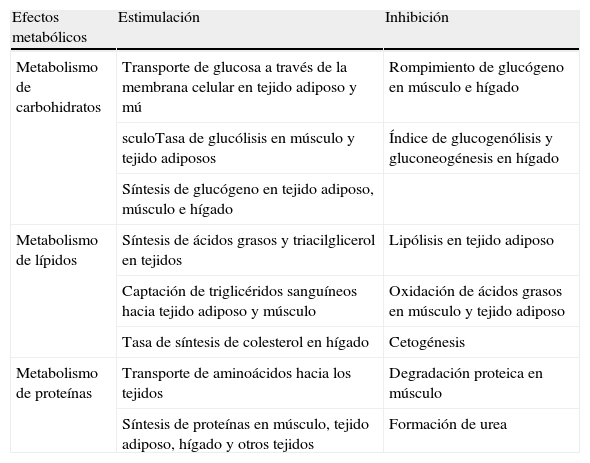
Efectos metabólicos de la insulina.
| Efectos metabólicos | Estimulación | Inhibición |
| Metabolismo de carbohidratos | Transporte de glucosa a través de la membrana celular en tejido adiposo y mú | Rompimiento de glucógeno en músculo e hígado |
| sculoTasa de glucólisis en músculo y tejido adiposos | Índice de glucogenólisis y gluconeogénesis en hígado | |
| Síntesis de glucógeno en tejido adiposo, músculo e hígado | ||
| Metabolismo de lípidos | Síntesis de ácidos grasos y triacilglicerol en tejidos | Lipólisis en tejido adiposo |
| Captación de triglicéridos sanguíneos hacia tejido adiposo y músculo | Oxidación de ácidos grasos en músculo y tejido adiposo | |
| Tasa de síntesis de colesterol en hígado | Cetogénesis | |
| Metabolismo de proteínas | Transporte de aminoácidos hacia los tejidos | Degradación proteica en músculo |
| Síntesis de proteínas en músculo, tejido adiposo, hígado y otros tejidos | Formación de urea |
La principal hormona contrarreguladora es el glucagón, secretado por las células α de los islotes de Langerhans pancreáticos. La liberación de glucagón viene determinada fundamentalmente por los niveles de glucemia (la hiperglucemia la inhibe y la hipoglucemia la estimula) pero otros factores pueden favorecer su secreción (aminoácidos, adrenalina, estimulación simpática)7. El principal efecto fisiológico del glucagón es aumentar la concentración de glucosa plasmática mediante la activación de la neoglucogénesis y la glucogenólisis, inhibiendo a su vez la glucólisis; todos estos efectos tienen lugar a nivel hepático. En el adipocito, el glucagón favorece la lipólisis mediante la fosforilación de la lipasa sensible a hormona, la enzima encargada de fraccionar los triglicéridos almacenados en diacilglicerol y los ácidos grasos libres. Los ácidos grasos libres se usan como energía en la mayoría de tejidos y para la cetogénesis en el hígado, donde el glicerol liberado se puede utilizar también para la neoglucogénesis8.
Otras hormonas que también desempeñan un papel en la regulación de la glucemia son la hormona de crecimiento (GH), el cortisol, las catecolaminas y la hormona tiroestimulante. Sus funciones se resumen en la tabla 2.
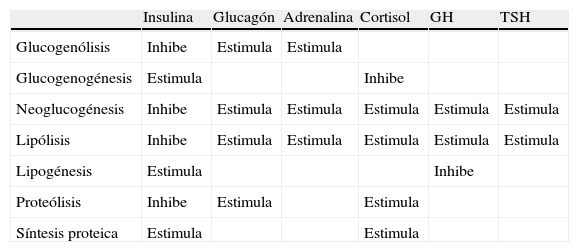
Funciones de la insulina y las hormonas contrarreguladoras.
| Insulina | Glucagón | Adrenalina | Cortisol | GH | TSH | |
| Glucogenólisis | Inhibe | Estimula | Estimula | |||
| Glucogenogénesis | Estimula | Inhibe | ||||
| Neoglucogénesis | Inhibe | Estimula | Estimula | Estimula | Estimula | Estimula |
| Lipólisis | Inhibe | Estimula | Estimula | Estimula | Estimula | Estimula |
| Lipogénesis | Estimula | Inhibe | ||||
| Proteólisis | Inhibe | Estimula | Estimula | |||
| Síntesis proteica | Estimula | Estimula |
El período posnatal inmediato conlleva una serie de cambios dramáticos en muchos órganos y sistemas. El mantenimiento de la homeostasis de la glucosa depende de múltiples ajustes en los citados sistemas endocrinos y metabólicos, que permitirán pasar de una fase de aporte continuo de glucosa a otra con períodos de ayuno e ingesta en los que el recién nacido debe mantener la glucemia utilizando sus propias reservas y mecanismos de regulación.
En la vida intrauterina, la provisión de glucosa hacia el feto es estable y mantenida por el aporte placentario, por lo que el feto no necesita realizar gluconeogénesis activa. La glucosa que no se utiliza es almacenada en el hígado fetal en forma de glucógeno. El nivel de glucosa en sangre de cordón será el punto de partida para el inicio de la transición metabólica9,10. Esta cifra depende de distintos factores, como la última ingesta materna, la duración del trabajo de parto y la vía del mismo11 o el tipo de fluidoterapia administrada a la madre12. Los valores habituales se sitúan entre los 45 y los 55mg/dl9,10.
Lectura rápida
Con la sección del cordón umbilical, el aporte continuo de glucosa a través de la placenta se interrumpe y la glucemia del recién nacido disminuye hasta un nadir en torno a la primera y segunda hora de vida. Como consecuencia, existe un incremento de catecolaminas y glucagón, y se inicia la glucogenólisis y la gluconeogénesis para intentar recuperar la normoglucemia.
La recuperación de las cifras de glucosa depende de los mecanismos contrarreguladores, que se ponen en marcha tanto por el proceso del parto como por la caída de las cifras de glucemia. Las catecolaminas aumentan de manera dramática (la adrenalina es la más implicada en los cambios metabólicos), estimulando la liberación de GH y de glucagón. El incremento de catecolaminas y glucagón ponen en marcha la glucogenólisis hepática, mientras que los picos de GH y cortisol promueven la gluconeogénesis5. Los niveles de insulina descienden inicialmente y permanecen en rangos bajos durante varios días, sin demostrar una respuesta vigorosa a estímulos fisiológicos15, permitiendo la estimulación de la gluconeogénesis y la movilización del glucógeno por la activación de la glucógeno-fosforilasa (en donde los niveles elevados de cortisol también parecen tener un papel importante16). Se debe tener en cuenta que los depósitos hepáticos de glucógeno son limitados y que disminuyen 10 veces durante las primeras 12h de vida, por lo que el mantenimiento de la normoglucemia dependerá del aporte exógeno de nutrientes y/o de la gluconeogénesis endógena, que se inicia a las 2–3h del nacimiento y aumenta de manera progresiva hasta alcanzar su máximo a las 12h de vida17. Estas hormonas, junto con el cortisol y la TSH, también favorecen la lipólisis y la proteólisis.
Para garantizar el acceso a sustratos alternativos para el funcionamiento del cerebro durante este período en el que las cifras de glucosa permanecen bajas, existe un aumento de cuerpos cetónicos durante el período posnatal precoz. Esta respuesta está presente también en otros mamíferos y parece un mecanismo fisiológico para garantizar la provisión de nutrientes a partir de la movilización de depósitos de grasa mientras se establece la lactancia de manera efectiva. En niños pequeños para la edad gestacional (PEG), las cifras más bajas de glucosa se asocian a niveles más altos de cuerpos cetónicos18. En un estudio, la alimentación con fórmula artificial en este grupo no incrementó de manera significativa los niveles de glucosa, pero sí que tuvo un efecto negativo sobre la cetogénesis, quizá por el bloqueo de mecanismos contrarreguladores ante una ingesta precoz con alto contenido energético.
Causas de hipoglucemiaLa causa más habitual es la alteración en la transición metabólica en niños con factores de riesgo o de forma secundaria a otra afección. En casos más infrecuentes, están involucradas alteraciones metabólicas y endocrinas primarias1,19,20 (tabla 3).
Causas de hipoglucemia neonatal según su mecanismo.
| Aumento en la utilización de la glucosa |
| Hiperinsulinismo: diabetes mellitus materna, eritroblastosis, PEEG, PEG o afección de las células de islote pancreátrico u otra endocrinopatía |
| Aumento del gasto calórico para mantener la termorregulación (RNMBP y PEG) o por aumento de actividad muscular (distrés respiratorio, irritabilidad del SNC, retirada de determinados fármacos) |
| Cambio de metabolismo aerobio a anaerobio (hipoxemia, hipotensión, hipoventilación, shock séptico…) |
| Exceso relativo de tejidos glucosa-dependientes (alta ratio cabeza/hígado en PEG) |
| Errores congénitos del metabolismo con sustratos alternativos inadecuados (ácidos grasos libres, cuerpos cetónicos, glicerol, aminoácidos, lactato). |
| Daño cerebral agudo que aumenta la utilización de glucosa (convulsiones, intoxicación, meningitis, encefalitis o hipermetabolismo posterior a un evento agudo como hipoxia-isquemia, traumatismo o hemorragia) |
| Producción o distribución de sustrato inadecuada |
| Retrasos o inadecuación de las tomas o de las calorías administradas por la nutrición parenteral |
| Regulación hormonal aberrante del metabolismo glucídico o lipídico (trastornos hipotalámicos, pituitarios o endocrinos periféricos) |
| Inmadurez transitoria de vías metabólicas críticas para la producción de glucosa y /u otros sustratos |
| Reservas insuficientes de precursores o sustratos alternativos |
| Déficit de transportadores de glucosa cerebrales (genético o post hipoxia-isquemia) |
| Supresión de la neoglucogénesis, glucogenólisis y de la liberación hepática de glucosa (hiperinsulinismo) |
PEEG: peso elevado para edad gestacional; PEG: pequeño para edad gestacional; RNMBP: recién nacido de muy bajo peso; SNC: sistema nervioso central. Modificado de Cornblath e Ichord20.
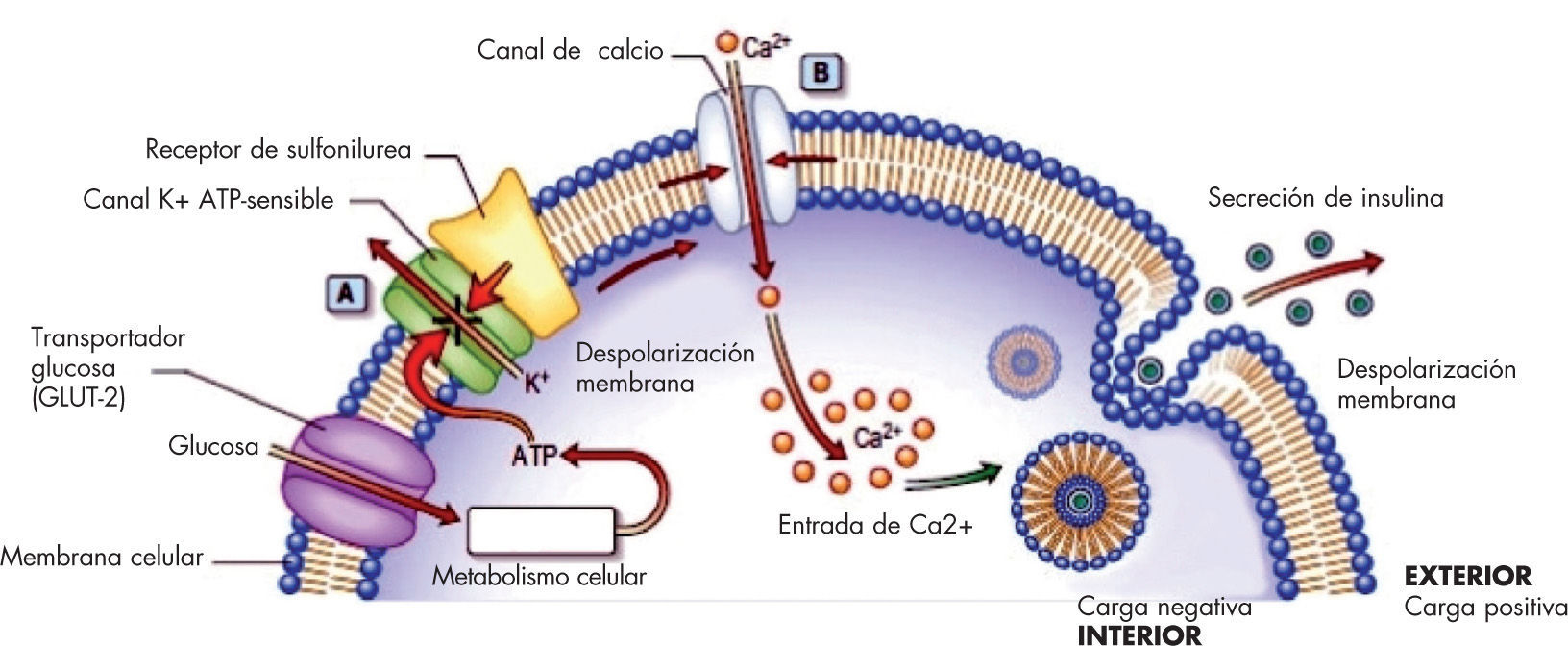
El hiperinsulinismo congénito (HIC) es la causa más frecuente de hipoglucemia grave, recurrente y persistente en el periodo neonatal21. Es una enfermedad con diferentes presentaciones clínicas, histología (formas focales o difusas), biología molecular y genética (se han descrito mutaciones en 8 genes distintos, aunque solo en el 50% se hallan los defectos genéticos)22. La principal causa de HIC (40–45% de casos) se debe a mutaciones de proteínas que forman parte del canal de K+ (genes ABCC8 que codifica la proteína SUR1 y KCNJ11 que codifica la proteína KIR6.2)23. Esto altera la sensibilidad de las células β a los cambios plasmáticos de glucosa que son el estímulo que necesitan para liberar insulina (fig. 1). La mayoría de las mutaciones son recesivas y dan lugar a una lesión difusa24.
Regulación de la secreción de insulina en una célula β pancreática. La glucosa entra en la célula vía transportador GLUT2. Dentro, la glucocinasa fosforila la molécula de glucosa en la fase inicial de la glucólisis, generando acetil-CoA y trifosfato de adenosina (ATP) mediante el ciclo de Krebs. Esto provoca el cierre de los canales de K+ ATP sensibles (A), con un incremento secundario del K+ intracelular que despolariza la membrana y provoca la apertura de los canales de Ca2+ voltaje dependientes (B). La entrada de Ca2+ a la célula activa la fosfolípido proteincinasa dependiente de Ca2+, favoreciendo la exocitosis de los gránulos. Imagen tomada de:http://medicinexplained.blogspot. com.es/2011/08/insulin-secretion-local-regulation.html
Los recién nacidos suelen ser macrosomas y presentan típicamente episodios persistentes y recurrentes de hipoglucemia que precisan aportes altos de glucosa por vía intravenosa para mantener la normoglucemia. Cuando la hipoglucemia es precoz, severa (con clínica de convulsiones o coma), prolongada o responde mal al tratamiento, los pacientes presentan peor pronóstico neurológico23. Desde el punto de vista bioquímico, el HIC se caracteriza por una secreción inadecuada y disregulada de insulina por parte de las células β-pancreáticas que se traduce en la presencia de concentraciones de insulina y péptido C inapropiadamente altas para las cifras de glucosa en sangre23, lo que da lugar a una mayor captación de glucosa por parte de los tejidos insulina-sensibles (hígado, tejido adiposo y músculo esquelético) y de manera simultánea inhibe la producción de glucosa22. Además, la insulina inhibe la lipólisis y eso desprotege al cerebro en circunstancias de hipoglucemia23. Por lo tanto, el diagnóstico bioquímico será el de una hipoglucemia con hiperinsulinemia y concentración disminuida de ácidos grasos y cuerpos cetónicos22.
El tratamiento inmediato consiste en administrar suficiente glucosa, ya sea por vía intravenosa y/o enteral, para mantener la glucemia por encima de 55–65mg/dl, ya que estos pacientes tienen menos sustratos alternativos21,25. Una vez se ha conseguido estabilizar la glucosa se deben valorar otras terapias (tabla 4). Los pacientes que no responden al tratamiento médico deben ser sometidos a pancreatectomía total o parcial según el subtipo histológico.
Lectura rápida
La causa más frecuente de hipoglucemia es la alteración de la transición metabólica habitual en niños con factores de riesgo o de forma secundaria a otra afección (hijos de madres con diabetes mellitus, bajo peso o peso elevado para la edad gestacional, prematuridad, hipotermia, policitemia, enfermedad hipóxico-isquémica o errores congénitos del metabolismo). En niños con macrosomía e hipoglucemias graves recurrentes y que requieren altos aportes de glucosa se sospechará hiperinsulismo congénito.
Farmacoterapia en el tratamiento de la hipoglucemia neonatal.
| Fármaco | Acción | Indicaciones | Administración | Efectos secundarios |
| Glucagón | Activación hepática de glucogenólisis y gluconeogénesis | Imposibilidad de mantener cifras de glucemia normales con aportes altos de glucosa en sospecha de HI | BIC iv, im o sc 0,5 a 2mg/día | |
| Corta duración de la acción | La respuesta a glucagón (incremento de glucemia en 36 a 54mg/dl tras 0,5mg sc) apoya la sospecha de HI. La falta de respuesta sugiere glucogenosis | Tratamientos cortos | ||
| Diazóxido | Estimula | Sospecha de HI | ||
| Los HI persistentes causados por mutaciones con defectos del canal de potasio son resistentes al diazóxido. La respuesta indica que son probablemente transitorios o causados por otras mutaciones | ||||
| Octreótido | Análogo de la somatostatina | Resistencia al diazóxido | 10–50μg/kg/ día en BIC o c/6–8h | Vómitos, diarrea, distensión abdominal que se suelen limitar en 7–10 días |
| Disminuye la secreción de glucagón, insulina, GH y TSH | HI | También se puede administrar im | Litiasis biliar | |
| Hipoglucemia si dosis muy alta (suprime el glucagón y la GH) | ||||
| Esteroides | Inhibe la glucogenogénesis y estimula la neoglucogénesis | Hoy día se utilizan raramente salvo deficiencia hormonal demostrada | Hidrocortisona 5mg/kg/día | Hipertensión |
| Prednisona 2mg/kg/día | Inmunosupresión | |||
| Afectación del neurodesarrollo en prematuros |
GH: hormona de crecimiento; HI: hiperinsulinismo; TSH: hormona tiroestimulante. Modificado de Arnoux et al5151.
La diabetes materna poco controlada da lugar a una hiperglucemia crónica intraútero que puede provocar hiperplasia de las células β, condicionando hiperinsulinismo con macrosomía y episodios de hipoglucemia en el recién nacido que se resuelven en los primeros días de vida24. La incidencia máxima de hipoglucemia suele ocurrir entre las 4 y 6h de vida pero puede prolongarse hasta las 48h. En aquellos neonatos en los que además existe macrosomía o son prematuros, el riesgo de presentar hipoglucemias es mayor25,26.
Lectura rápida
La clínica de la hipoglucemia es inespecífica y puede ser secundaria a diversos procesos por lo que se debe descartar causa subyacente.
La monitorización está indicada en aquellos neonatos asintomáticos que presenten un riesgo aumentado (pequeños para edad gestacional [PEG], hijos de madre diabética, prematuros tardíos…), en aquellos neonatos sintomáticos y en aquellos pacientes con afecciones de base que aumenten el riesgo de hipoglucemia.
Las causas de macrosomía fetal se pueden dividir en no modificables (carga genética, sexo, paridad, edad y altura materna) y modificables (antropometría materna pregestacional, ingesta nutricional materna, ganancia ponderal materna durante la gestación, nivel de actividad física, hábito tabáquico y parámetros metabólicos, sobre todo aquellos relacionados con el metabolismo de la glucosa)27. El riesgo de hipoglucemia en neonatos con peso elevado para la edad gestacional (peso al nacimiento superior al percentil 90) es superior al de los pacientes con peso adecuado, incluso si no existe el antecedente materno de diabetes28,29, posiblemente por hiperinsulinismo transitorio30.
Neonatos con retraso del crecimiento intrauterinoLos neonatos con retraso del crecimiento intrauterino presentan un mayor riesgo de desarrollar hipoglucemia durante los primeros días, presentando una incidencia de 12–24% (7 veces superior al que presentan los neonatos con crecimiento prenatal correcto)31. Los factores que contribuyen a este hecho son el retraso de la gluconeogénesis y los escasos depósitos de glucógeno y otros sustratos energéticos, como las ácidos grasos libres por falta de tejido adiposo31,32. Además, se ha demostrado una hiperinsulinemia relativa y/o un aumento de sensibilidad a la insulina y una respuesta contrarreguladora incompleta en respuesta a la hipoglucemia31,33. Por último, estos pacientes presentan un incremento de la demanda energética por un tamaño cerebral relativo superior17.
Neonatos pretérminosEn los neonatos nacidos prematuramente existen limitaciones en enzimas clave de los procesos generadores de glucosa34,35, tienen menor concentración de sustratos alternativos y de depósitos de glucógeno36 y grasa, con lo que su respuesta cetogénica es menor37, y su sistema contrarregulador presenta una respuesta incompleta38, por lo que presentan mayor riesgo de hipoglucemia prolongada1. Además, tienen también una alta ratio cerebro-cuerpo. La incidencia de hipoglucemia está relacionada con la disminución en el peso al nacimiento y en la edad gestacional ya que el tercer trimestre del embarazo es el período para completar el crecimiento fetal y los depósitos de sustratos energéticos (glucógeno y grasa) que serán usados en el período neonatal39,40.
Errores congénitos del metabolismoLas mutaciones que dan lugar a alteraciones enzimáticas, tanto de la síntesis como de la degradación del glucógeno, de la gluconeogénesis, del metabolismo de los aminoácidos o del metabolismo de los ácidos grasos pueden comenzar como hipoglucemia en el periodo neonatal inmediato30,32.
Enfermedad hipóxico-isquémicaAlgunos autores han determinado la existencia de variaciones en los perfiles glucémicos de los neonatos que han presentado una asfixia, con una alta incidencia tanto de hipoglucemia como de hiperglucemia41. El grado de hipoglucemia parece estar correlacionado con la severidad de la enfermedad hipóxico-isquémica en neonatos a término41,42. Se debe tener en cuenta que la hipoglucemia en sí misma disminuye la respuesta cerebrovascular a la hipoxia e incrementa la producción cerebral de radicales superóxido y los niveles de aspartato en el espacio cerebral extracelular, lo que resulta en necrosis neuronal41, por lo que la relación entre glucemia y pronóstico neurológico en estos neonatos tiene una especial relevancia. Estas hipoglucemias pueden ser secundarias a una depleción perinatal de glucógeno41 por liberación de catecolaminas por la hipoxia y la hipersecreción de insulina43, y también por un mayor consumo de glucosa en el cerebro, secundario a la glucólisis anaerobia que tiene lugar en esta situación: la glucólisis anaerobia consigue solo 2 moléculas de ATP por cada molécula de glucosa frente a las 38 moléculas de ATP que se generan en la glucólisis aerobia42.
Otras causas35- –
Eritroblastosis grave: se ha considerado el hiperinsulinismo como causa de hipoglucemia, aunque se desconoce si esta es realmente la causa y cuál sería su etiología si existiese. Posiblemente un aumento de la glutatión reductasa, resultado de una importante hemólisis, actúe como estímulo para la liberación de insulina. Además, presentan anemia y hepatomegalia con eritropoyesis extramedular, lo que puede interferir en los depósitos de glucógeno en la vida fetal.
- –
Hipotermia: el frío da lugar a estrés que a su vez produce liberación de noradrenalina que puede causar hipoglucemia secundaria.
- –
Policitemia: la hipoglucemia asociada a policitemia puede ser el resultado de una mayor utilización de glucosa por parte de un mayor número de hematíes.
- –
Sepsis: aunque el mecanismo no se conoce, las sepsis se pueden asociar con hipoglucemia. Se han postulado mecanismos como un aumento en la utilización de la glucosa, depleción de depósitos de glucógeno o gluconeogénesis alterada.
- –
Déficits de transportadores de glucosa44: el síndrome de Fanconi Bickel es una afección autosómica recesiva en la que el transportador GLUT2 es disfuncional. Se caracteriza por la acumulación hepatorrenal de glucógeno, hipoglucemia durante el ayuno, hiperglucemia posprandial e hipergalactosemia, y disfunción tubular proximal renal. En el déficit de GLUT1 (transportador que se encuentra predominantemente en la barrera hematoencefálica), la concentración baja de glucosa solo se encuentra en el líquido cefalorraquídeo y da lugar a convulsiones, retraso severo del desarrollo y microcefalia adquirida.
Es importante identificar de forma precoz tras el nacimiento la presencia de factores maternos o neonatales asociados con riesgo de hipoglucemia (véase el apartado anterior) y que determinarán si está indicado monitorizar los niveles de glucosa, así como establecer un control clínico más estrecho.
Los síntomas asociados a la hipoglucemia neonatal son similares a los que se presentan en múltiples afecciones en este período, por lo que ha de descartarse siempre otra causa diferente o asociada, como la infección, hipoxia-isquemia periparto, alteraciones iónicas…. Pueden aparecer temblor, llanto débil o anormalmente agudo, hipotonía o letargia, apnea, taquipnea o cianosis y dificultades para la alimentación en un niño con buena ingesta previa.
En la exploración física del niño con hipoglucemia sintomática se buscarán signos sugestivos de afección de base (como defectos de la línea media facial o hepatomegalia)19. En el recién nacido PEG los episodios de hipoglucemia parecen más prevalentes en aquellos que presentan fenotipo desnutrido18.
Debido a lo inespecífico de la clínica, uno de los datos que apoyarán que la hipoglucemia sea el factor causal será la desaparición de los mismos con la normalización de los niveles de glucosa20. Las complicaciones neurológicas severas como convulsiones o coma, que suelen aparecer con hipoglucemias severas (cifras de glucosa plasmática < 10mg/dl), prolongadas o repetidas, pueden tardar en mejorar tras el inicio del aporte exógeno de glucosa19.
Diagnóstico: a quién y cómo monitorizar¿A quién?Está indicado realizar determinación de glucosa sanguínea en los siguientes grupos de recién nacidos:
- 1.
Pacientes asintomáticos de poblaciones de riesgo. Aunque la incidencia dependerá del umbral definido como hipoglucemia, se calcula que alrededor de la mitad de los niños pertenecientes a grupos de riesgo presentarán hipoglucemia45:
- –
PEG.
- –
Hijos de madre diabética.
- –
Prematuros tardíos
Es controvertido si se ha de monitorizar a los niños de peso elevado con una gestación sin complicaciones, entre otros motivos porque resulta difícil descartar con seguridad la presencia de diabetes gestacional o de hiperglucemia materna durante el embarazo.
En los niños pertenecientes a estos grupos se debería iniciar la alimentación de forma precoz (primera hora de vida) y después cada 2–3h.
- 2.
Pacientes sintomáticos. Por las características inespecíficas de la clínica, la hipoglucemia habrá de entrar dentro del diagnóstico diferencial del recién nacido con cualquier sintomatología.
- 3.
Pacientes con otra afección que aumente el riesgo de hipoglucemia (véase el apartado «Causas de hipoglucemia»).
Se desconoce si se debe determinar la glucosa en el niño asintomático con riesgo de hipoglucemia durante el nadir fisiológico. En este sentido, ningún estudio ha demostrado daño causado por unas horas de hipoglucemia asintomática durante el período de adaptación posnatal hasta el establecimiento de la homeostasis fisiológica de la glucosa19,46, por lo que las cifras han de interpretarse de forma relativa y sobre todo en relación a la tendencia. Algunos autores recomiendan iniciar la monitorización después de la segunda toma25. Las recomendaciones contemplan diferencias en la frecuencia, la periodicidad y la duración de la monitorización dependiendo de la condición de riesgo en niños asintomáticos47, pero un reciente estudio epidemiológico sugiere que se puede estandarizar la monitorización al no hallar diferencias entre grupos45. En general, se iniciarán determinaciones de glucemia previas a las tomas a partir de las 2–3h de vida y se repetirán de forma periódica durante al menos las primeras 24h. Después de las 24h, se habrá de continuar el cribado si las cifras de glucosa plasmática permanecen por debajo de los 45mg/dl o la valoración clínica del recién nacido no es satisfactoria47. Los recién nacidos PEG pueden presentar hipoglucemias durante un período más prolongado31.
Lectura rápida
Los valores de glucemia dependen de diversos factores relacionados con la extracción y la metodología de medición, pero antes de iniciar el tratamiento y sin retrasar el mismo, se debería obtener una muestra para comprobar mediante laboratorio.El inicio del tratamiento no sólo depende del valor de glucemia, sino que también en la evolución en el tiempo, la respuesta a la ingesta, la clínica y la causa de la hipoglucemia si está es secundaria a alguna afección. El primer objetivo del tratamiento será garantizar un aporte suficiente de glucosa, ya sea por vía enteral o parenteral según las características del paciente.
Los valores de glucosa varían dependiendo del tipo de muestra (habitualmente capilar o venosa), de si la determinación se realiza en sangre total o en plasma y de la tecnología usada para la medición.
En general, se admite la utilización de muestras capilares y glucómetros como técnica de cribado, a pesar de que numerosos estudios demuestran su falta de precisión en la población neonatal, especialmente en cifras bajas de glucosa48. Por consenso internacional, las recomendaciones se refieren a niveles de glucosa plasmática. Las cifras medidas en sangre total son aproximadamente un 10% más bajas debido a la diferencia en contenido de agua entre el plasma y el eritrocito, y pueden verse artefactadas por la presencia de hematocritos altos —en las que se infraestimaría el valor de glucosa plasmática. Ha de tenerse en cuenta que, aunque los glucómetros funcionan con sangre total, muchos separan la muestra antes de la medición, de forma que la lectura refleja la glucosa en plasma49. Antes de iniciar el tratamiento y sin retrasar este, debería obtenerse una muestra para realizar confirmación mediante un método de laboratorio.
Indicaciones para el tratamientoLa indicación para el tratamiento y la estrategia de este han de basarse no solo en la concentración de glucosa sanguínea, sino también en la evolución a lo largo del tiempo, la respuesta a la ingesta y la clínica.
En la mayoría de niños asintomáticos con hipoglucemia leve o moderada será suficiente con optimizar las tomas (frecuentes y adecuadas), mantener un control clínico estrecho y medir repetidamente la glucemia19. En este sentido, es importante garantizar en todo lo posible el refuerzo de la lactancia materna. Aunque en algunos casos será necesario recurrir a la administración de fórmula, es importante recordar que estos suplementos pueden, por un lado, disminuir la producción de sustratos alternativos y, por otro, estimular la secreción de insulina tras la toma.
Dado que no se conocen los niveles de glucosa sanguínea a partir de los cuales se produce daño neurológico, las recomendaciones actuales de tratamiento se basan en la opinión de un panel de expertos1. En el niño asintomático se recomienda intervención solo si la glucemia plasmática es persistentemente inferior a 36mg/dl, si no aumenta progresivamente tras la ingesta o si aparecen síntomas. Los niños sintomáticos o con cifras < 20–25mg/dl habrán de recibir tratamiento por vía intravenosa con un minibolus de 200mg/kg de glucosa (2ml/kg de glucosa al 10%), seguido por una perfusión a 4–8mg/kg/min y continuar controles frecuentes durante el seguimiento19. En el paciente con alguna afección concomitante se iniciará también tratamiento de la misma.
Una vez empezado el tratamiento se intentará mantener la glucemia plasmática por encima de 45mg/dl de forma estable, evitando el aumento excesivo que puede incrementar la secreción de insulina y suprimir la respuesta contrarreguladora. La recuperación de la glucosa será importante sobre todo si las cifras han sido muy bajas o persistentes o si han aparecido síntomas neurológicos graves. Si se sospecha hiperinsulinismo puede ser recomendable mantener cifras más elevadas, por el bloqueo de la producción de sustratos alternativos.
La recomendación de 45mg/dl se basa en las cifras concordantes halladas en sangre de cordón de fetos sanos en la segunda mitad de la gestación9, en los niños sanos a término después de las primeras horas de adaptación metabólica13 y en los recién nacidos prematuros que presentaron desarrollo neurológico más favorable (aunque de forma transitoria) que los niños con cifras inferiores50.
Si las cifras no remontan, se aumentará el aporte de glucosa, subiendo el ritmo de perfusión o la concentración de glucosa (para infundir concentraciones superiores a 12,5% se habrá de considerar la canalización de una vía central). En este momento, o si la hipoglucemia persiste más allá de la primera semana de vida44, se habrán de considerar otras causas y otros tratamientos (tabla 4). Necesidades de glucosa superiores a 10–12mg/kg/min (aproximadamente 15g/kg/día), por ejemplo, son indicativas de hiperinsulinismo.
En cualquier neonato en el que se haya demostrado una alteración del período de transición metabólica y que haya requerido control o tratamiento por este motivo, se ha de garantizar que es capaz de mantener, con una ingesta apropiada e independiente, cifras de glucosa normales durante un período razonable (al menos 2 o 3 ciclos de ayuno-ingesta)19,47.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.