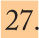Se trata de estandarizar un procedimiento complejo no exento de riesgo, que consiste en extraer uno o dos volúmenes de sangre del recién nacido (RN) e intercambiarla por concentrado de hematíes fresco y plasma de un donante compatible1. La introducción de esta técnica disminuyó la mortalidad y morbilidad de la enfermedad hemolítica del RN, cambiando la historia del kernícterus o ictericia nuclear2–4.
El objetivo al realizar una exanguinotransfusión (ET) es el descenso de la bilirrubina y la corrección de la anemia. En la ET parcial, la sangre extraída al RN es sólo la necesaria para corregir la poliglobulia, o la anemia en caso de hidropesía.
La mejora y protocolización del diagnóstico, tratamiento prenatal y posnatal de la incompatibilidad Rh y ABO5–8, y de todos los RN con riesgo de hiperbilirrubinemia de cualquier etiología, junto al seguimiento generalizado de las normas dictadas por las guías de la Academia Americana de Pediatría (AAP)9,10, han conducido a disminuir el número de ET que se realizan. Esto trae como consecuencia un aumento de las complicaciones inherentes a la realización de la técnica, contribuyendo a esto la inexperiencia en la realización del procedimiento11.
Puntos clave
La isoinmunización anti-D fue la más frecuente; en la actualidad, otras causas de enfermedad hemolítica, como de incompatibilidad de grupos ABO, Kell, Duffy, Kidd o de Rh (Rh E, Rh C), son indicación de ET (tabla 1).
Indicaciones de exanguinotransfusión
|
El tratamiento pre y posnatal6–8 que más ha contribuido reducir las necesidades de ET por isoinmunización Rh (D) es la administración de inmunoglobulina anti-Rh D a las gestantes negativas en la semana 28. También debe administrarse inmunoglobulina anti-Rh D en abortos espontáneos o inducidos, embarazo ectópico o sangrado vaginal y siempre que se realice una técnica que suponga un riesgo de hemorragia fetomaterna (biopsia corial, amniocentesis, cordocentesis, versión fetal en presentaciones anómalas). Tras el parto, la administración se hará nuevamente cuando el hijo sea Rh positivo. La dosis es de 300μg, que se reduce a 50μg sólo cuando el riesgo es en el primer trimestre.
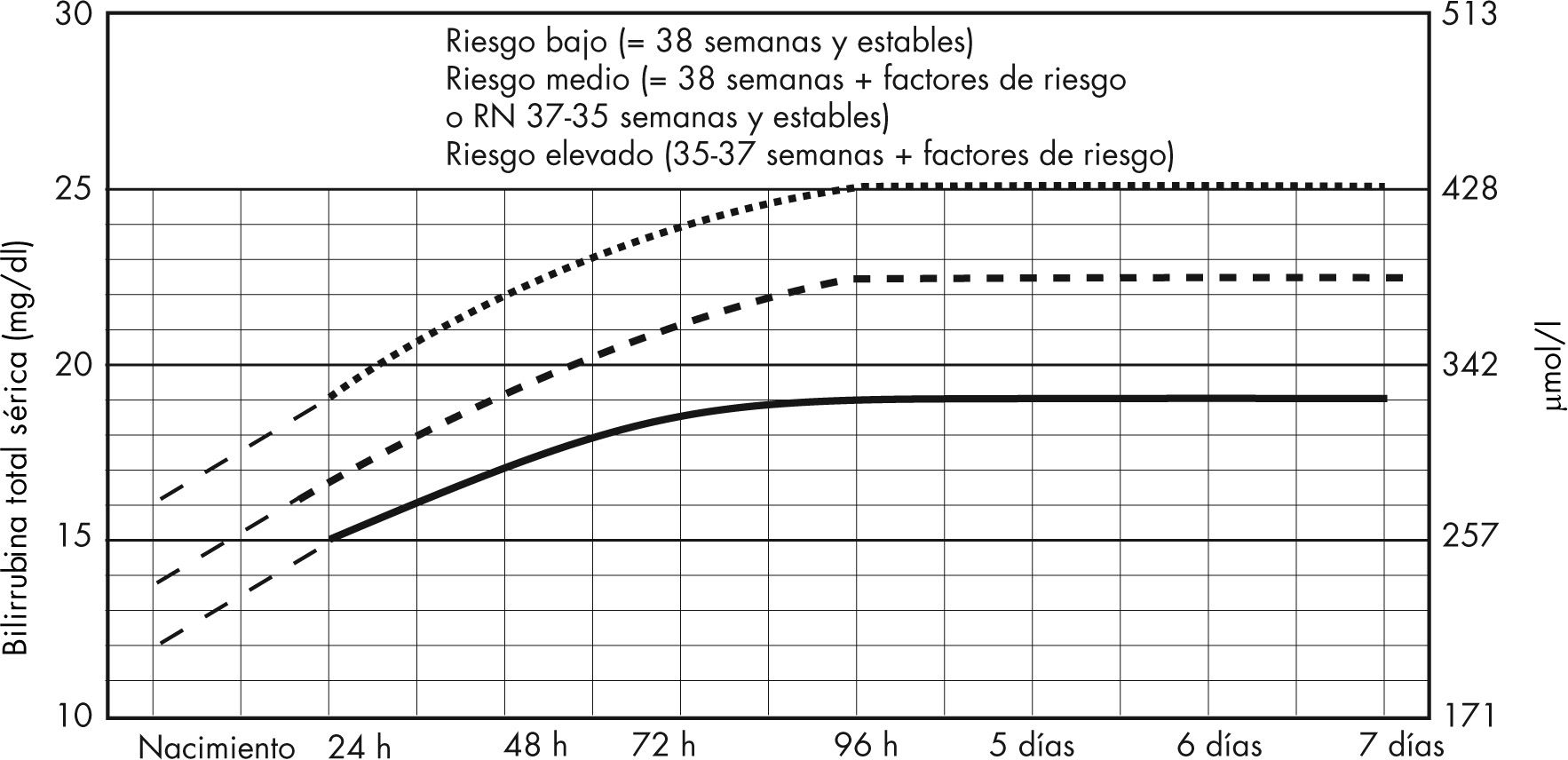
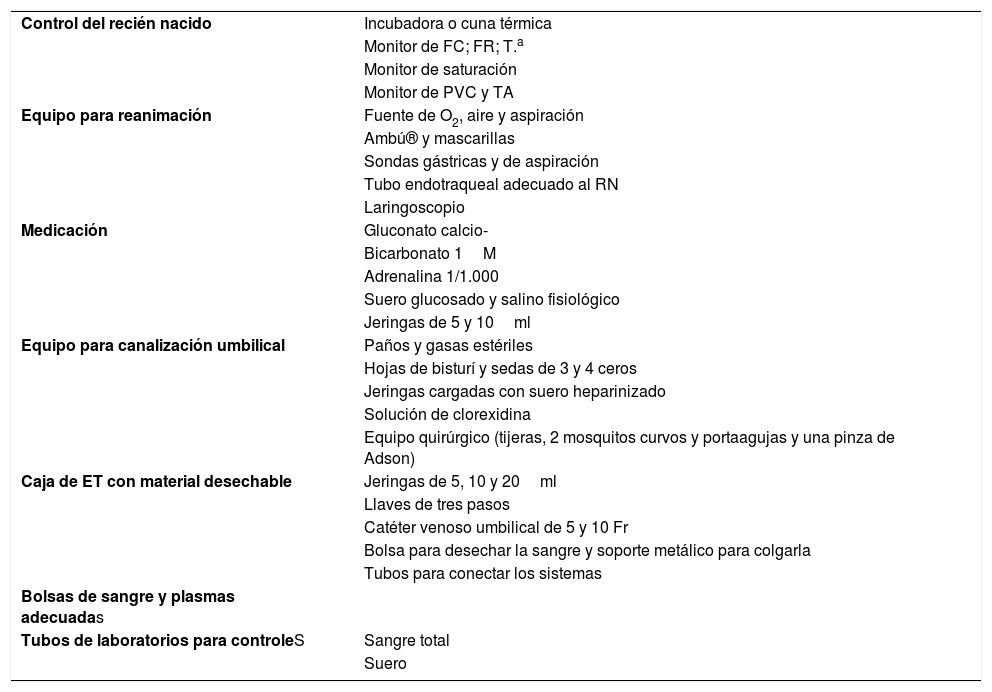
A pesar de todos los avances en el diagnóstico y tratamiento posnatal11–15, inicio temprano de fototerapia, administración de inmunoglobulina16, la pregunta de cuál es el umbral crítico de bilirrubina para la realización de una ET en el RN, en términos de lesividad a largo plazo para el sistema nervioso central (SNC), sigue sin ser contestada al estar implicadas muchas variables9,12–14,16–19, como edad gestacional y posnatal en horas del RN, presencia de hemólisis, anemia, acidosis metabólica, patología acompañante, etc., que tendremos que valorar al plantearnos realizar una ET y no sólo una determinación aislada de bilirrubina, aunque ésta sea de 20mg/dl18 (fig. 1).
OBJETIVOS AL REALIZAR UNA EXANGUINOTRANSFUSIÓNEn los RN con hiperbilirrubinemia hemolítica, secundaria a isoinmunización Rh (D, C, E) o incompatibilidad de grupos (ABO, Kell, Duffy, Kidd) serán:
- 1.
Corregir la anemia y mejorar los signos de insuficiencia cardíaca en los RN con hidropesía, aportando hematíes no vulnerables a los anticuerpos maternos circulantes.
- 2.
Disminuir la concentración de bilirrubina indirecta libre en el plasma, consiguiendo la prevención de la neurotoxicidad causada por aquélla.
- 3.
Interrumpir el proceso de hemólisis, extrayendo los anticuerpos circulantes presentes en el plasma y los hematíes parcialmente hemolizados o recubiertos de anticuerpos, remplazándolos por los hematíes y el plasma del donante libre de antígenos sensibilizantes.
El objetivo en los RN con ictericia hemolítica no isoinmune (esferocitosis, déficit de glucosa-6 fosfato deshidrogenasa) es la corrección de la anemia y el descenso de la bilirrubina.
Cuando realizamos una ET parcial por policitemia sintomática, el objetivo será el descenso del hematocrito (Hto) hasta niveles del 55-60%19 y la desaparición de la sintomatología dependiente.
SELECCIÓN Y PREPARACIÓN DE LA SANGRE PARA LA EXANGUINOTRANSFUSIÓNUtilizaremos sangre total reconstituida, preparada a partir de concentrados de hematíes y plasma fresco congelado, consiguiendo un Hto y una hemoglobina (Hb) adecuados para el RN1,20–22.
- 1.
Selección del concentrado de hematíes según indicación de la ET:
- a)
En RN con isoinmunización anti-D el concentrado de hematíes será isogrupo con el RN y el factor Rh negativo.
- b)
En casos de incompatibilidad de grupo (ABO) el concentrado de hematíes será grupo O, con factor Rh igual al del RN.
- c)
En otras enfermedades hemolíticas isoinmunitarias la sangre no contendrá el antígeno sensibilizante, siendo preciso determinar la compatibilidad cruzada con la madre.
- d)
En la hiperbilirrubinemia no inmunitaria, la sangre se cruza con los hematíes y el plasma del RN.
- a)
- 2.
Características del concentrado de hematíes:
- a)
Antigüedad menor de 7 días, para evitar la hiperpotasemia y el desplazamiento de la curva de disociación de la hemoglobina por descenso del 2–3 difosfoglicerato.
- b)
Desleucotizado, para evitar las infecciones por (citomegalovirus, retrovirus HTLV-1 y 2 y Chagas). Se realiza por filtración prealmacenamiento, con filtros específicos, para garantizar un contenido inferior a 1 × 106 leucocitos por unidad de concentrado de hematíes.
- c)
Irradiado, para prevenir la reacción injerto contra huésped, indicado cuando la ET se realiza en RN pretérminos o en RN inmunodeficientes.
- d)
Actualmente, el anticoagulante más usado es el CPD (citrato-fosfato-destrosa).
- a)
- 3.
Características del plasma fresco congelado para usar en la ET:
- a)
En isoinmunización Rh e incompatibilidad ABO, el grupo del plasma será el mismo que el del RN.
- b)
El plasma fresco debe ser segurizado (Real Decreto 1088/2005), preferiblemente por cuarentena (es decir, el plasma del donante debe estar inmovilizado, hasta la próxima donación, un mínimo de 4 meses).
- c)
La sangre reconstituida no tiene plaquetas, por lo que deberá transfundirse una vez finalizada la ET.
- a)
La mezcla se realizará en condiciones de asepsia, preferiblemente en cámara de flujo laminar en el banco de sangre.
La sangre pasará por un sistema que la mantenga a una temperatura de 36 oC, evitando tanto la hipotermia como la hipertermia del RN, así como alteraciones en la integridad de los hematíes.
En los RN no anémicos, la ET se realiza con una mezcla de concentrado de hematíes y plasma fresco para obtener una unidad de sangre con un Hto 45-50%.
El Hto del concentrado de hematíes del banco es aproximadamente del 70%; aplicando la fórmula obtendremos una unidad reconstituida con un Hto del 50%.
En RN con anemia se realiza la mezcla con menor cantidad de plasma, para conseguir un mayor Hto.
La realización de una ET para conseguir el descenso de bilirrubina y la retirada de anticuerpos requiere un intercambio de dos veces la volemia del RN. Con ello se recambia el 87-90% de la sangre del RN. La volemia del RN se calcula multiplicando 80ml por el peso (kg).
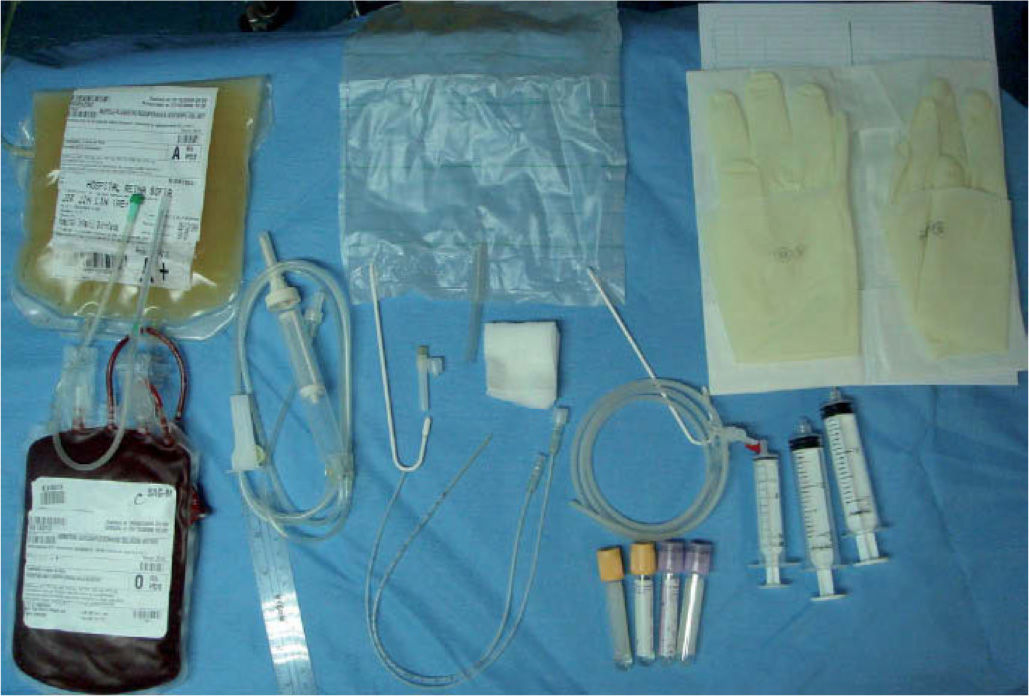
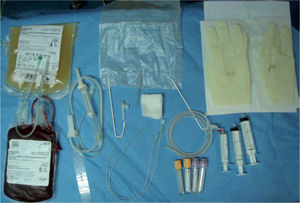
TÉCNICA PARA LA REALIZACIÓN DE LA EXANGUINOTRANSFUSIÓNDeben llevarla a cabo dos personas (neonatólogo y enfermera), ambos cualificados y entrenados para su realización, equipados con bata, guantes, mascarilla y gorro. El RN ocupará un puesto de cuidado intensivo neonatal (CIN). El material necesario para todo el procedimiento se muestra en la tabla 2.
Equipamiento necesario para realizar la exanguinotransfusión
| Control del recién nacido | Incubadora o cuna térmica |
| Monitor de FC; FR; T.a | |
| Monitor de saturación | |
| Monitor de PVC y TA | |
| Equipo para reanimación | Fuente de O2, aire y aspiración |
| Ambú® y mascarillas | |
| Sondas gástricas y de aspiración | |
| Tubo endotraqueal adecuado al RN | |
| Laringoscopio | |
| Medicación | Gluconato calcio- |
| Bicarbonato 1M | |
| Adrenalina 1/1.000 | |
| Suero glucosado y salino fisiológico | |
| Jeringas de 5 y 10ml | |
| Equipo para canalización umbilical | Paños y gasas estériles |
| Hojas de bisturí y sedas de 3 y 4 ceros | |
| Jeringas cargadas con suero heparinizado | |
| Solución de clorexidina | |
| Equipo quirúrgico (tijeras, 2 mosquitos curvos y portaagujas y una pinza de Adson) | |
| Caja de ET con material desechable | Jeringas de 5, 10 y 20ml |
| Llaves de tres pasos | |
| Catéter venoso umbilical de 5 y 10 Fr | |
| Bolsa para desechar la sangre y soporte metálico para colgarla | |
| Tubos para conectar los sistemas | |
| Bolsas de sangre y plasmas adecuadas | |
| Tubos de laboratorios para controleS | Sangre total |
| Suero |
ET: exanguinotransfusión; FC: frecuencia cardíaca; FR: frecuencia respiratoria; Fr: french; PVC: presión venosa central; PA: presión arterial; RN: recién nacido.
Suero heparinizado —preparar por cada 100ml de suero fisiológico 25 unidades de heparina (0,025ml de heparina al 1%).
Iniciar esta técnica en las condiciones más estables del RN, corregir previamente a la realización de la ET las alteraciones que pueda presentar (acidosis, hipotermia, hipoglucemia, hipotensión)20,22.
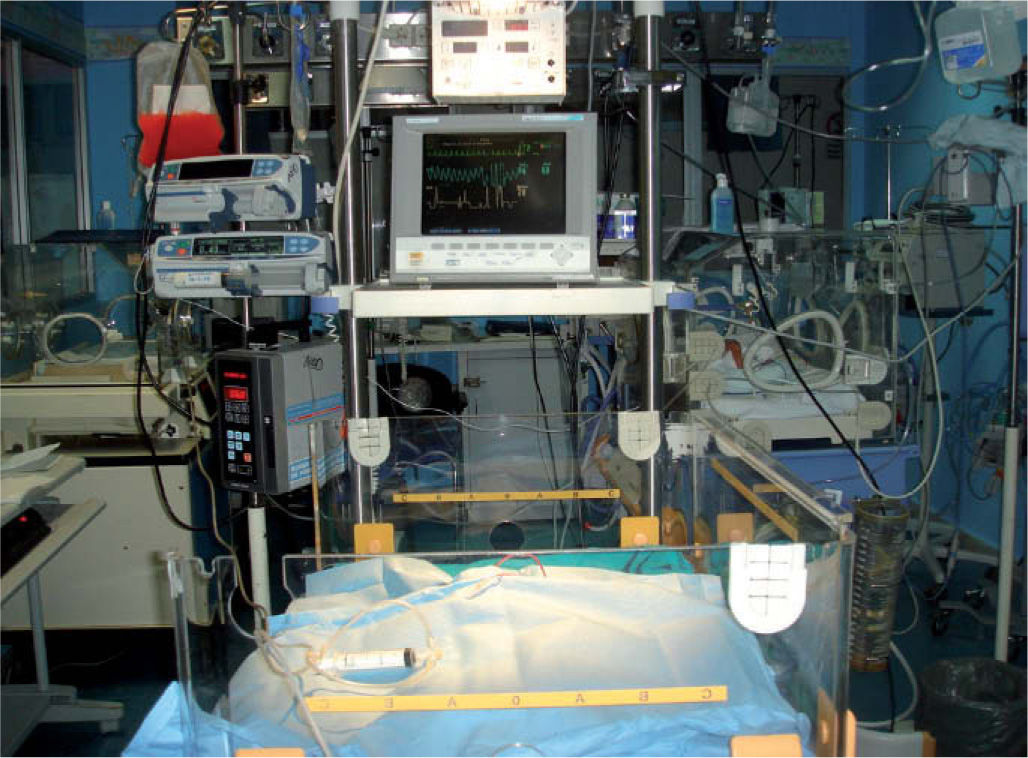
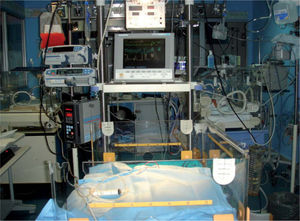
El RN a término debe estar preferiblemente en cuna térmica, el pretérmino en incubadora; ambas con características de CIN (fig. 2), y la temperatura durante el procedimiento, controlada por servocontrol. Hay que monitorizar constantes vitales, frecuencia cardíaca, respiratoria, tensión arterial y presión venosa central.
Se debe controlar la diuresis, colocar bolsa de orina y/o sonda vesical. Mantener sonda nasogástrica abierta a bolsa y retirar el contenido gástrico si previamente ha iniciado nutrición enteral.
Preparar el equipo necesario para reanimación23, fuente de oxígeno, aspirador, Ambú®, tubos endotraqueales, fármacos vasoactivos.
Vías para la realización de la ETCanalizaremos la vena umbilical, de elección para la realización de la ET, y la vena periférica, preferiblemente percutáneo-cava, para la administración de fluido, terapia base y medicación24. El catéter se introducirá preferiblemente hasta vena cava inferior o la distancia necesaria para que la sangre refluya. Se deberá localizar la posición del catéter por radiografía.
En casos de onfalitis o imposibilidad de canalizar la vena umbilical, podemos realizarla por catéter venoso en femoral24. También se obtienen resultados similares utilizando accesos vasculares periféricos25. La canalización de arteria umbilical es necesaria para la exanguinotransfusión isovolumétrica.
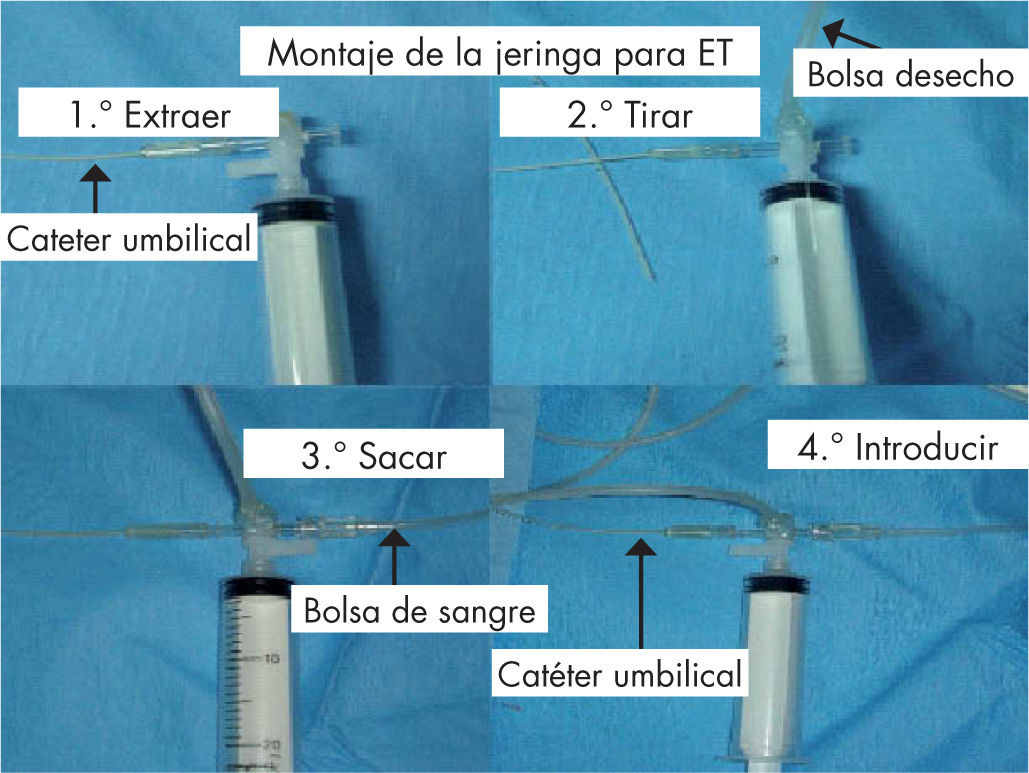
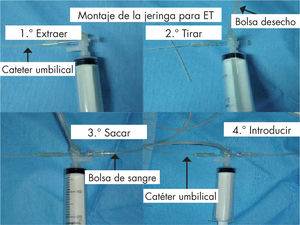
Modos de realizarla (figs. 3 y 4, y vídeo)El material fungible y desechable para la realización de la ET se presenta en una caja específica (tabla 2). La técnica más comúnmente usada es la extracción-inyección a través de la vena umbilical:
- 1.
erpaso: el catéter se conecta a una llave de tres pasos acoplada a una jeringa de 20ml; se procede a extraer alícuotas de sangre del RN que no produzcan cambios hemodinámicos ni fluctuaciones en el flujo sanguíneo cerebral. Variarán según el peso: 5ml para RN menores de 1.500g, 10ml para RN de 1.500-2.500g y 15ml para los de peso superior a 2.500g.
- 2.
opaso: la sangre extraída se tirará a la bolsa de desecho.
- 3.
erpaso: sin desconectar la jeringa, y siguiendo la rotación de las manecillas del reloj, extraeremos la misma cantidad de sangre de la bolsa de sangre preparada y pasaremos a introducirla por el catéter umbilical de nuevo al RN.
Un ayudante deberá ir anotando cuántas veces hacemos los pases y la cantidad de cada uno de ellos, para conocer la cantidad total en ml que llevamos en todo momento.
Cada 100ml cambiados, o cada 15–20 minutos, realizaremos los siguientes pasos- 1.
Agitar la bolsa de sangre para evitar la sedimentación de los hematíes y mantener el Hto constante.
- 2.
Vigilar y anotar las constantes vitales: frecuencia cardíaca (FC), respiratoria (FR), temperatura, presión venosa central (PVC) y presión arterial (PA), que deberán estar monitorizadas.
- 3.
Administrar 1ml de gluconato cálcico a la vez que inyectamos la sangre al RN.
Si el estado general y hemodinámico del RN lo permite, realizaremos la ET de dos volúmenes (80ml/kg) × 2; con ello la cifra sérica de bilirrubina disminuye al 45% de las previas al inicio del procedimiento.
Los rebotes con aumentos de hasta el 60% en la bilirrubina previa a la ET se relacionan con la lisis de hematíes de los fondos comunes extravasculares (bazo y médula ósea), o por lisis de hematíes recién formados, por anticuerpos aún presentes.
La ET de un volumen (80ml/kg) o menos está indicada en los RN muy inestables, con signos de hidropesía, para corregir la anemia y mejorar los signos de insuficiencia cardíaca (IC). Antes de iniciar la ET, si la presión venosa central está elevada, tendremos que realizar recambios negativos con las primeras emboladas y hasta que la PVC baje y mejoren los signos de IC es aconsejable iniciar tratamiento con inotrópicos.
La velocidad de recambio tiene poca influencia sobre la cantidad de bilirrubina retirada, pero influye en las condiciones hemodinámicas del RN.
Los cambios en la PA y, quizá, los transmitidos retrógradamente por las venas mesentéricas26,27 explican las frecuentes alteraciones intestinales isquémicas que se producen tras la realización de ET.
Las emboladas muy rápidas y con alícuotas grandes conducen a hipotensión, hipoxemia y, con frecuencia, a alteraciones en glucemia, calcemia, niveles de electrolitos que son mal tolerados por el RN.
La duración mínima para la realización de una ET de dos volúmenes es de una hora, si bien en pacientes inestables el tiempo necesario puede ser de 90–120 minutos.
Exanguinotransfusión isovolumétrica simultáneaConsiste en la realización simultánea de extracción e introducción del mismo volumen de sangre a través de dos catéteres (uno arterial y otro venoso)20,22, usando bombas de perfusión o con dos personas extrayendo y perfundiendo simultáneamente a una velocidad de 2–3ml/kg/min. Con ello se reducen las oscilaciones de PA media, gasto cardíaco y PVC, que se relacionan con los cambios en el volumen de flujo sanguíneo cerebral demostrados cuando la ET se realiza con la técnica convencional de introducción/extracción. Por eso este modo de proceder estará indicado en los RN muy inestables hemodinámicamente, en los inmaduros o en los RN con patología asociada (cardiopatía congénita, sepsis, etc.).
Actuaciones y controles postexanguinotransfusiónEl RN se colocará de nuevo en fototerapia, monitorizado y controlando bilirrubina, Hto, Hb y coagulación cada 4, 6 y 8h.
Habrá que prevenir y/o tratar la hipocalcemia e hipomagnesemia secundaria a la unión del citrato de la sangre transfundida con calcio iónico y magnesio; también se debe prevenir la hipoglucemia secundaria a un hiperinsulinismo debido a la elevada cantidad de glucosa en la sangre transfundida.
El catéter debe fijarse y localizarse por radiografía.
Se dejará a dieta una o dos tomas, dependiendo del estado del RN.
COMPLICACIONES DE LA EXANGUINOTRANSFUSIÓN Y LA PREVENCION (tabla 3)Los síntomas que indican un catéter mal colocado, doblado u obstruido son: llanto al inyectar, dificultad en la extracción, PVC elevada y distrés brusco.
Complicaciones de la exanguinotransfusión
| Relacionadas con el catéter | Vasoespasmo |
| Trombosis | |
| Embolismo pulmonar | |
| Arritmias | |
| Alteraciones metabólicas | Hiperhipoglucemia |
| Hipocalcemia | |
| Hipercaliemia | |
| Hipomagnasemia | |
| Acidosis metabólica | |
| Cardiorrespiratorias | Apneas-paro respiratorio |
| Bradicardia-paro cardiaco | |
| Sobrecarga volumétrica/insuficiencia cardíaca | |
| Hipotensión-hipertensión | |
| Infarto de miocardio | |
| Gastrointestinales | Enterocolitis necrotizante, perforación intestinal |
| Mala tolerancia digestiva | |
| Infecciosas | Onfalitis, sepsis |
| Alteraciones en la temperatura | Hipotermia, hipertermia |
| Relacionadas con los hemoderivados | Reacciones transfusionales |
| Enfermedad injerto contra huésped | |
| Infecciones víricas (hepatitis B y C, VIH, TORCH) | |
| Otras Infecciones (Chagas, paludismo) |
La hemólisis causante de hemoglobinemia, hemoglobinuria e hiperpotasemia se evita controlando la temperatura de la sangre transfundida.
La aparición de arritmia se relaciona con catéter localizado en la aurícula derecha y/o con los intercambios realizados con excesiva rapidez o gran volumen.
La enfermedad injerto contra huésped, más frecuente en fetos que han recibido transfusiones de concentrado de hematíes intraútero, puede minimizarse con el uso de sangre radiada con un mínimo de 1.500 rads, pudiendo llegar a 3.200 rads1.
Las reacciones transfusionales no hemolíticas son causadas por una respuesta alérgica inespecífica frente a antígenos proteicos o fragmentos leucocitarios y se previenen con hemoderivados desleucotizados.
El uso de sangre negativa para citomegalovirus (CMV) y concentrados de hematíes desleucotizados previene la infección por CMV. Las pruebas serológicas y enzimáticas realizadas a los donantes y el cumplimento de las normativas vigentes han disminuido la incidencia de hepatitis (A, B y C) e infección por VIH, que en la actualidad es de 1,9 por millón de unidades transfundidas.