La molécula A relacionada con la cadena de clase i del CMH (MICA) es un ligando del grupo 2 de células asesinas naturales, y miembro D (NKG2D) de la activación de inmunorreceptores. La unión de la superficie de la célula tumoral MICA con NKG2D estimula las células asesinas (NK) y la inmunidad de las células T antitumorales. La eliminación de MICA por las células tumorales facilita la evasión inmune del tumor, lo cual podría contribuir en parte a la progresión tumoral.
Materiales y métodosSe aplicó inmunohistoquímica tanto en tejidos renales normales como neoplásicos. Se transfectaron las líneas de células tumorales de riñón humano 786-O y ACHIN, y se establecieron secuencias objetivo para silenciar la MMP2 humana a través de la expresión ARNhc. Se midió el grado de eliminación de MICA y se llevó a cabo una PCR cuantitativa en tiempo real, así como el análisis de Western blot.
ResultadosLa membrana de tipo metaloproteinasa de matriz-2 (MMP2) media en la eliminación de MICA, que se bloquea por la supresión de la expresión de MMP2. Simultáneamente, la sobreexpresión de MMP2 aumenta la eliminación de MICA, lo cual indica que MMP2 interviene en la liberación proteolítica de MICA soluble (sMICA) asociada al carcinoma de células renales, que facilita el escape tumoral inmune.
ConclusionesDichos resultados sugieren que MMP2 podría ser un nuevo objetivo potencial para la terapia inmune de tumores. Un esclarecimiento de los mecanismos por los que los tumores eliminan MICA podría ser de gran importancia para el tratamiento del cáncer, para así reforzar las NK y la inmunidad antitumoral de las células T.
The MHC class i chain-related molecule A (MICA) is a ligand for the natural killer group 2, member D (NKG2D) immunoreceptor activation. The engagement of tumor cell surface MICA to NKG2D stimulates the NK and T cell antitumor immunity. Shedding of MICA by tumor cells facilitates tumor immune evasion, which might partially contribute to tumor progression.
Material and methodsInmunohistochemistry was performed on both normal and neoplastic renal tissue. Human renal carcinoma cell lines 786-0 and ACHIN were transfected and target sequences to silence human MMP2 by shRNA expression were established. The degree of MICA shedding was measured and quantitative real-time PCR and Western-blot analysis were performed.
ResultsThe membrane type matrix metalloproteinase 2 (MMP2) mediated the MICA shedding, which was blocked by suppression of MMP2 expression. Concomitantly, MMP2 over-expression enhanced the MICA shedding, indicating that MMP2 was involved in the renal cell carcinoma-associated proteolytic release of soluble MICA (sMICA), which facilitated the tumor immune escape.
ConclusionsThese findings suggested that MMP2 might be a new potential target for tumor immune therapy. Elucidation of the mechanisms by which tumors shed MICA could be of a great importance for cancer treatment in order to reinforce the NK and T cell antitumor immunity.
El carcinoma de células renales (CCR) es el séptimo tipo de cáncer más común en China y se pronosticó que en 2011 causaría aproximadamente 13.000 muertesc. La cirugía es la primera línea de tratamiento para este cáncer; una resección realizada con éxito suele resultar en un estado de ausencia de enfermedad a largo plazo. Aunque la tasa de supervivencia global para este tipo de cáncer es de más del 60% a los 5 años, aproximadamente el 30% de los pacientes diagnosticados de CCR localizado desarrollan recidiva metastásica2. Por consiguiente, el desarrollo de nuevos enfoques para tratar dichos cánceres tan agresivos supone un gran reto para los doctores e investigadores médicos.
El grupo 2 de células asesinas naturales, miembro D (NKG2D) es un inmunorreceptor activador de lectinas de tipo C. MICA (molécula A relacionada con la cadena de clase i del CMH), situado en el locus HLA, es el ligando de NKG2D. NKG2D tiene 3 dominios extracelulares, que incluyen: α1, α2 y α33. Cuando NKG2D se une a MICA constituyen un sistema de vigilancia inmunológica para proteger al receptor de células malignas y virus4. MICA se expresa en la mayoría de los tumores epiteliales humanos, pero generalmente está ausente en tejidos normales5. Se cree que la separación de MICA asociado al tumor de la superficie celular es relevante para el escape tumoral inmune6. Diversos estudios han mostrado que el nivel de MICA soluble (sMICA) es más elevado en el suero de los pacientes con cáncer en comparación con el de los controles sanos. Por tanto, se ha propuesto que la acumulación de sMICA en el suero podría llevar a una regulación decreciente de NKG2D a través de una absorción de NKG2D más fácil y una degradación lisosomal7. Dichos resultados indican que sMICA podría ser un indicador de pronóstico de cáncer.
Por otro lado, la familia de metaloproteinasas de matriz (MMP) representa un grupo de 26 endopeptidasas dependientes de cinc en los seres humanos, que degradan componentes de la matriz extracelular, como colágenos y gelatina. Se debe tener en cuenta a dichas MMP dada su implicación en un gran número de procesos fisiológicos y patológicos, incluida la oncogénesis. Las MMP se clasifican en función de la especificidad del sustrato y sus características biológicas8. Se ha comprobado que los inhibidores del amplio espectro de metaloproteinasas, incluidas las MMP, interfieren en la eliminación de MICA9.
Un estudio previo demostró que la MMP2 (gelatinasa A) es el miembro de las gelatinasas presente en grandes cantidades en tejidos cancerígenos10. Las proteínas de MMP2 escindidas solubilizan componentes de la matriz pericelular y eliminan ectodominios celulares11. Sin embargo, pocos estudios han demostrado que MICA está expresado en el carcinoma renal y que se detectan sMICA en el suero de pacientes con carcinoma renal12,13. Por lo tanto, nos preguntamos si la actividad de MMP2 media en la división de MICA en el carcinoma renal.
Nuestros estudios muestran que la eliminación de MICA no solo tiene lugar en tumores mal diferenciados, sino también en tumores bien diferenciados, así como en tumores en estadios tempranos. La liberación de sMICA se suprime significativamente con un MMP2 ARNhc y aumenta con una sobreexpresión de MMP2, lo que sugiere que MMP2 podría estar profundamente involucrada en la eliminación proteolítica de MICA.
Materiales y métodosMuestras de tejido humanoSe prepararon muestras parafinadas, incluyendo muestras cancerígenas y normales, tras una escisión quirúrgica en el Departamento de Cirugía Urológica del Shanghai Tenth People's Hospital, Universidad de Tongji, desde 2010 hasta 2012. El Comité de Ética de la Universidad de Tongji aprobó la recogida de muestras. Todas las muestras de tejido se fijaron en formalina neutra al 10% durante 24h. Se cortaron las secciones de 4-μ de espesor para llevar a cabo procedimientos inmunohistoquímicos.
Línea y cultivo celularSe adquirieron líneas celulares de cáncer renal humano, 786-O y ACHN, de la Colección de cultivos tipo del Banco de células de la Academia China de Ciencias (CBTCCCAS, Shangai, China). Las células 786-O y ACHN se multiplicaron en RPMI-1460 Medium (HyClone) y en Dulbecco's Modified Eagle Medium (Gibco), respectivamente. El medio fue suplementado con suero bovino fetal (FBS) al 10% (Gibco), 100U/ml de penicilina, y 100U/ml de estreptomicina. Las células se cultivaron a 37°C con un 5% de CO2.
InmunohistoquímicaSe analizó la expresión de MICA en un procedimiento en 2 fases utilizando el kit de detección Envision TM (DAKO). En resumen, las secciones de tejido desparafinadas fueron incubadas con un 1% de H2O2 en metanol durante 30min a temperatura ambiente para bloquear la actividad peroxidasa endógena, a lo que siguió una incubación en suero normal de cabra al 1,5% a 37°C durante 30min para evitar las uniones no específicas. La incubación con anticuerpos anti-MICA (dilución de 1:40; Abcam) se realizó a 4°C durante la noche empleando una dilución óptima predeterminada. Como controles negativos las secciones se incubaron en suero normal de cabra al 1,5%. Dichas secciones fueron entonces incubadas con inmunoglobulina anti-conejo durante 60min y se visualizaron los productos de la reacción según el procedimiento del kit de detección Envision TM. Además, las secciones se contratiñeron con la solución de Mayer (WAKO Pure Chemical Industries). Junto con un microscopio Nikon (Eclipse Ti-U) se utilizó un método semicuantitativo para calcular el grado de inmunotinción, que incluyó – (sin expresión),+(débil), ++ (moderada), y +++ (alta) en una base célula por célula en 5 campos microscópicos (aumento ×100), tal y como se ha descrito previamente14.
RNAi con infección de ARNhcSe clonó el ARNhc contra MMP2 en el vector retroviral pMKO.1 y MMP2 ADNc se clonó en el vector retroviral pBabe-puro para obtener la sobreexpresión. Los plásmidos se transfectaron en células HEK 293T con CaCl2. Cuarenta y ocho horas después de la transfección se recogieron, filtraron y se emplearon los sobrenadantes para infectar las células 786-O y ACHN en placas de 6 pocillos a una confluencia del 70% con 4μg/ml de polibreno (Sigma). Setenta y dos horas después de dicha infección se recogieron las células para su posterior análisis. Las secuencias objetivo para silenciar la MMP2 humana a través de la expresión de ARNhc se establecieron mediante técnicas previamente descritas15.
Ensayo de eliminación de MICALas células 786-O y ACHN se sembraron en una placa de 6 pocillos a una densidad de 4-105 por pocillo. Cada pocillo contenía un total de 2ml de medio completo. Tras 24h las células fueron infectadas con el vector retroviral y se cultivaron durante otras 72h. El sobrenadante se recogió y filtró con un filtro de 0,45-μm. Se midió la cantidad de MICA soluble en el sobrenadante con el kit Duo Set sandwich ELISA para MICA humano (R&D Systems). La medición del grado de eliminación de MICA en las células se realizó según lo descrito previamente16. Todas las muestras fueron analizadas por triplicado.
Reacción en cadena de la polimerasa cuantitativa en tiempo realEl ARN total de cada grupo de células fue extraído mediante Trizol Reagent (Invitrogen). La primera cadena de ADNc se sintetizó utilizando la transcriptasa inversa RNasa H SuperScript II (Invitrogen) y un cebador (Promega) de Oligo (DT) a partir de 2μg del ARN total, según las indicaciones del fabricante. Las primeras secuencias de MMP2 y GAPDH fueron las siguientes: cebadores sentido y antisentido de MMP2 (5′-TTATTTGGCGGACAGTGACA-3′ y 5′-ACACGGCATCAATCTTTTCC-3′) y cebadores sentido y antisentido de GAPDH (5′-GGCATTGCTCTCAATGACAA-3′ y 5′-ATGTAGGCCATGAGGTCCAC-3′). La amplificación mediante PCR se llevó a cabo en 40 ciclos a 94°C durante 30s, a 60°C durante 30s, y a 72°C durante 30s, en un Applied Biosystems 7900HT (Applied Biosystems) con 1,0μl de ADNc y empleando el SYBR Green Realtime PCR Master Mix (Takara). Al término del ciclo se realizó el análisis de la curva de Melting para establecer la especificidad de los productos de la PCR. Se recopilaron los datos y se analizaron con el software SDS2.3 (Applied Biosystems). El nivel de expresión de cada gen candidato se normalizó internamente contra el nivel de expresión de GAPDH. El valor cuantitativo relativo se expresó con el método 2-ΔΔCt, representando la cantidad de expresión del gen candidato con los mismos calibradores. Se realizó cada experimento por triplicado y se repitieron 3 veces.
Análisis de Western blotLas células se lisaron en un buffer (50mM Tris/HCl pH 7,4, 150mM NaCl, 1% NP-40, 0,1% SDS) ensayo de radioinmunoprecipitación (RIPA) que contenía un cóctel de inhibidores de proteasas (Roche) con hielo durante 30min. Seguidamente fueron homogeneizados y centrifugados a 15.000RPM durante 20min a 4°C. Se determinó la concentración de proteínas celulares mediante el kit para el análisis cuantitativo de proteínas (K3000-BCA Shenergy Biocolor). Las muestras se separaron en gel SDS al 10%, se transfirieron a membranas de PVDF (GE Healthcare Life Sciences), y se bloquearon con TBS (salina tamponada con Tris), que contenía leche en polvo sin grasa al 5%. Tras la incubación con los anticuerpos MICA (dilución de 1:200; Abcam), MMP2 (dilución de 1:400; Cell Signaling) y β-actina (dilución de 1:2000; Abcam) durante 12h a 4°C, las membranas fueron posteriormente incubadas durante 30min a temperatura ambiente con los anticuerpos secundarios apropiados. Las señales fueron entonces visualizadas mediante quimioluminiscencia mejorada (ECL).
Análisis estadísticoLas diferencias estadísticas entre los grupos de tratamiento se determinaron con un análisis de varianza (ANOVA) unidireccional. Cuando solo se compararon 2 condiciones se empleó la prueba «t» de Student para analizar los resultados en cuanto a la significación estadística. Se consideró estadísticamente significativo un valor de p<0,05.
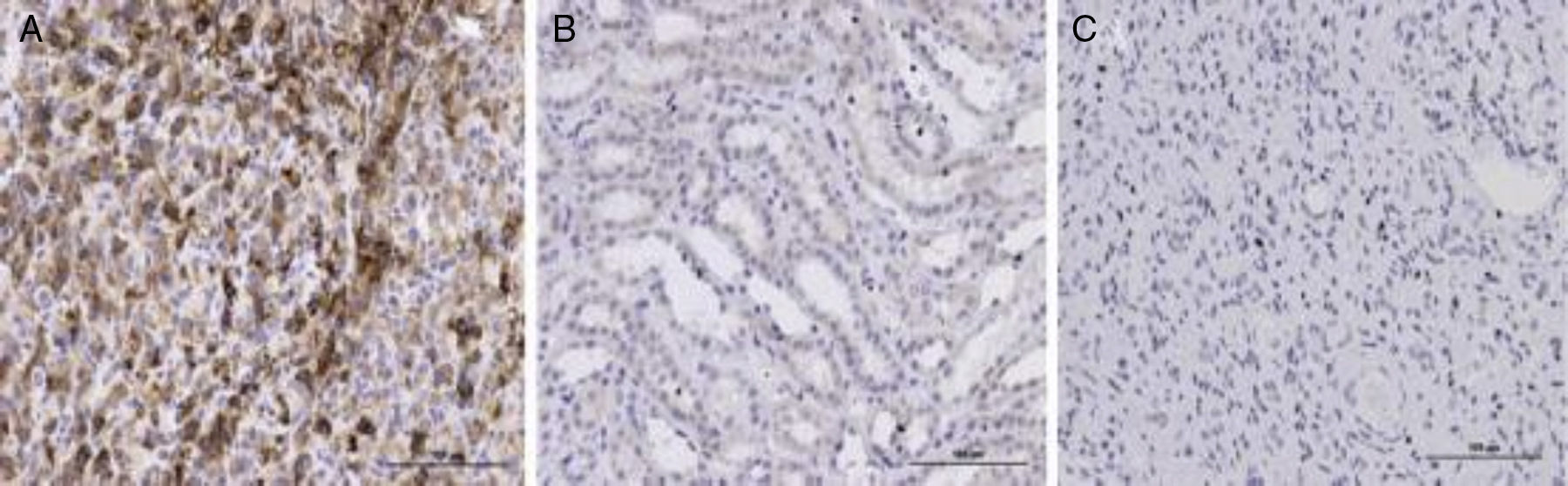
ResultadosExpresión de MICA en el carcinoma de células renales y en tejido renal normalSe examinó la expresión inmunohistoquímica de MICA en muestras de carcinoma de células renales y en muestras de tejidos renales normales. Las células tumorales del carcinoma de células renales mostraron una expresión sobrerregulada de MICA (fig. 1A). De los 30 carcinomas de células renales 25 (83,3%) fueron positivos en cuanto a MICA. Los niveles de expresión fueron catalogados como –, +, ++ y +++ con valores de 5/30 (16,7%), 10/30 (33,3%), 8/30 (26,7%), y 7/30 (23,3%), respectivamente. De los 28 tejidos renales normales 18/28 (64,3%), 6/28 (21,4%), 3/28 (10,7%) y 1/28 (3,6%) casos fueron catalogados como –, +, ++ y +++, respectivamente (tabla 1). Se halló una diferencia significativa en la expresión de MICA entre los tejidos con carcinoma de células renales y los tejidos renales normales.
Expresión inmunohistoquímica de MICA en el carcinoma de células renales y en los tejidos renales normales. A. Representante de carcinoma de células renales, que expresaba con fuerza MICA en el citoplasma y citomembrana. B. Tejido renal normal que mostró una expresión limitada en citomembrana. C. Un control negativo (barra de escala: 100μm).
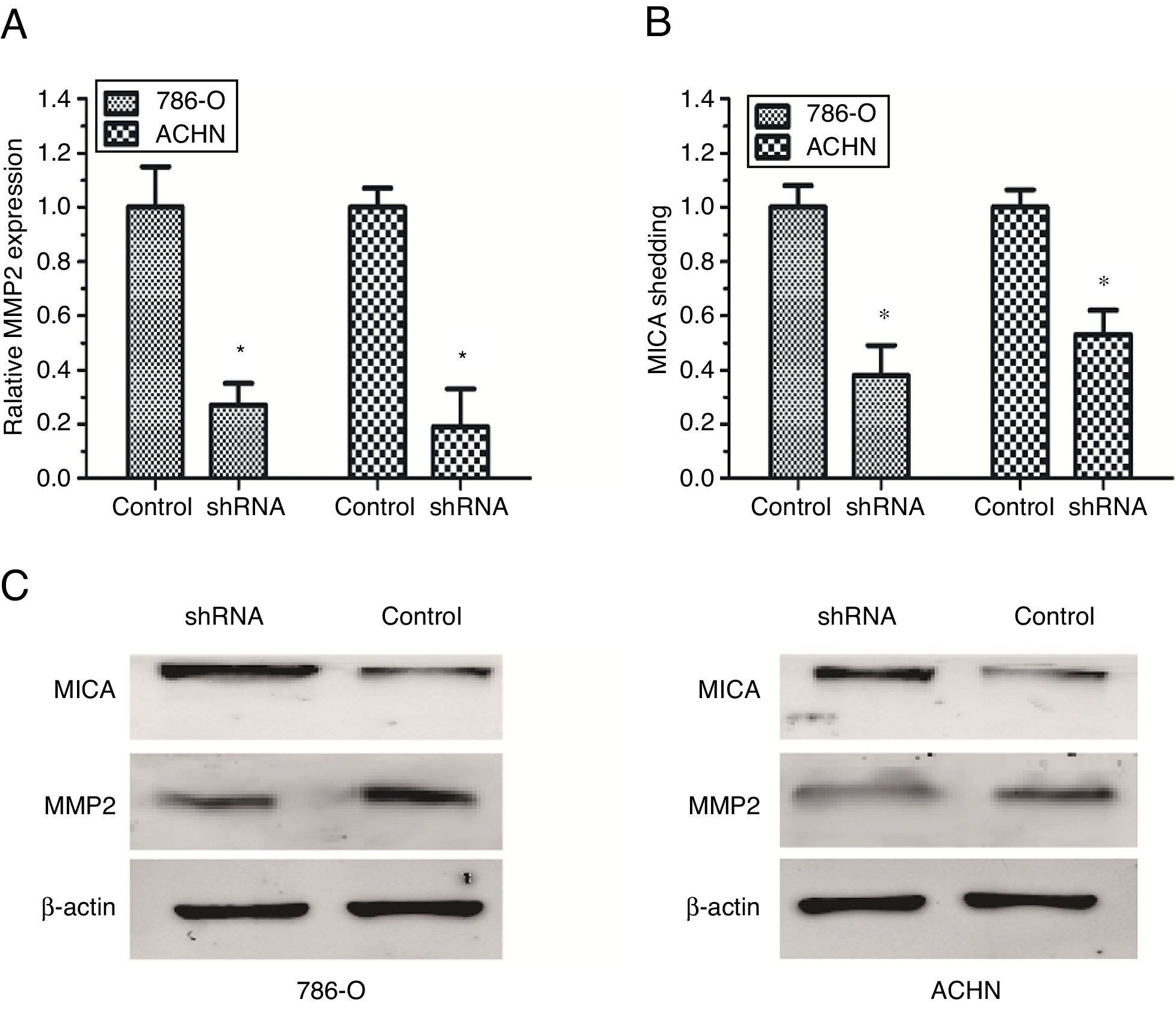
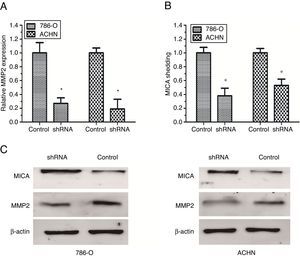
Para identificar las MMP específicas implicadas en la eliminación de MICA creamos ARN de horquilla corta (ARNhc) para una MMP2 específica en un vector de expresión lentiviral. La expresión de MMP2 se suprimió en las células objetivo en más del 70-90% con ARNhc específico conforme a la evaluación de la PCR cuantitativa en tiempo real y al análisis de Western blot (fig. 2A, y 2C). El ELISA para la eliminación de MICA mostró que el silenciamiento de MMP2 tuvo un efecto significativo en la eliminación de MICA en las células 786-O y ACHN (fig. 2 B). Además, el análisis de Western blot reveló que la supresión de MMP2 podría aumentar la expresión de superficie de MICA en las células 786-O y ACHN (fig. 2 C). Dichos resultados sugieren que MMP2 está implicada en la eliminación de MICA en las células renales cancerosas.
Inhibición de la expresión de MMP2 o eliminación de MICA bloqueada por actividad. A. La PCR cuantitativa en tiempo real mostró supresión shRNA de la expresión de MMP2 en células 786-O y ACHN. B. ELISA mostró el grado de eliminación MICA por las células 786-O y ACHN con la supresión de la expresión de MMP2. C. El análisis de Western blot confirmó la inhibición de la expresión de MMP2 y la expresión y superficie celular de la expresión de MICA por shRNA en células 786-O y ACHN a nivel de proteínas. Los datos representan los resultados de 3 experimentos independientes.
*P<0,05 en comparación con el control).
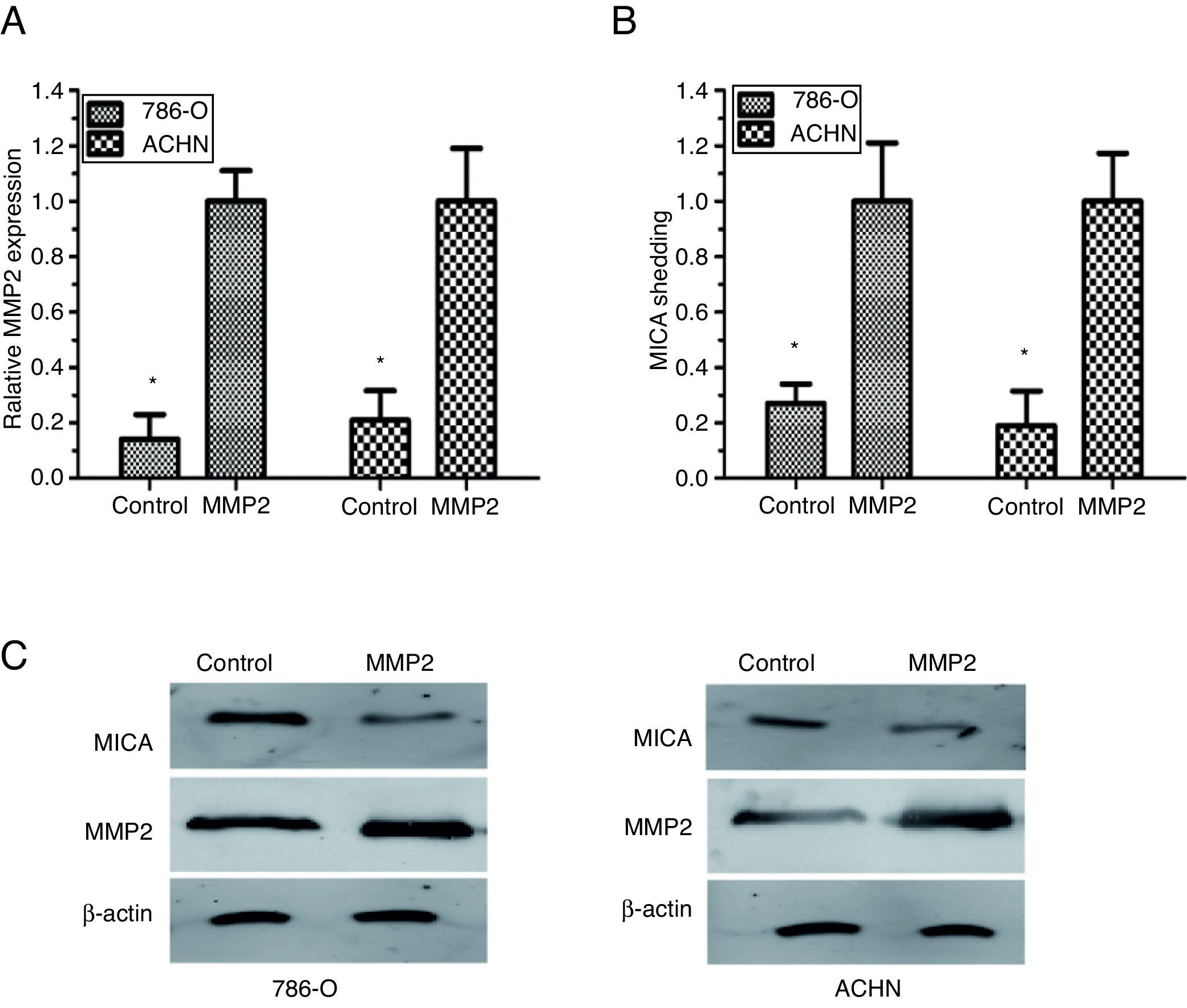
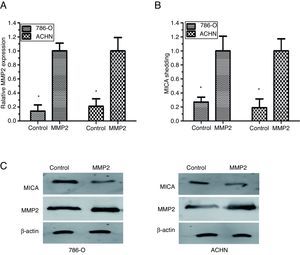
Con el objetivo de proporcionar más pruebas que refutaran que MMP2 está directamente implicada en la eliminación de MICA, se sobreexpresó la forma activa de la MMP2 humana en las células 786-O y ACHN. La expresión de MMP2 se incrementó en las células objetivo tal y como quedó demostrado en la PCR cuantitativa en tiempo real y en el análisis de Western blot (fig. 3A). Los resultados mostraron que la sobreexpresión de MMP2 aumenta significativamente la eliminación de MICA (fig. 3 B). Además, el análisis de Western blot reveló que la sobreexpresión de MMP2 reduce significativamente la expresión de superficie de MICA en las células 786-O y ACHN (fig. 3 C).
La sobreexpresión de MMP-2 aumentó la eliminación de MICA constitutiva. A. La PCR cuantitativa en tiempo real mostró la expresión de MMP-2 en las células 786-O y ACHN. B. ELISA mostró que la sobreexpresión de MMP2 aumentó significativamente la eliminación de MICA constitutiva en células 786-O y ACHN. C. Western blot mostró que una sobreexpresión de MMP2 redujo la expresión de MICA de superficie celular en las células 786-O y ACHN. Estos datos representaron los resultados de 3 experimentos independientes.
*P<0,05 en comparación con el control.
MICA es un ligando importante para la activación del receptor NKG2D. Generalmente se expresa en la superficie de las células infectadas, así como en muchas de las células humanas transformadas3. Las células tumorales que expresan altos niveles de MICA son el objetivo de las células NK, las células CD8+ T y de las células γδ T para su eliminación17. En el presente estudio evaluamos la expresión de la proteína MICA en 30 casos de carcinoma de células renales y en 28 casos de tejidos renales normales. Hallamos un nivel significativamente más elevado de la expresión de MICA en el carcinoma de células renales en comparación con la expresión de los tejidos renales normales. Sin embargo, no hallamos ninguna diferencia significativa en la expresión de MICA entre las muestras de carcinoma de células renales independientemente de sus diferentes fases. Dichos resultados sugieren que la proteína MICA está implicada en la inmunidad anticarcinoma de células renales. No obstante, las células inmunes innatas no podían matar eficazmente las células tumorales renales, lo que sugiere la posibilidad de una disfunción en la vigilancia inmunológica mediada por NKG2D-MICA.
Se ha observado que sMICA está asociado con la regulación negativa sistémica de la expresión de superficie de NKG2D en las células NK, CD8+ T, y γδ T. Tras la unión de sMICA a NKG2D en la superficie de las células NK el complejo es interiorizado y se reduce la función citotóxica18. Por consiguiente, una reducción de la expresión de MICA en la superficie celular podría debilitar la fuerza de la respuesta inmunológica. Muchos estudios clínicos han mostrado que un nivel sérico elevado de sMICA está estrechamente relacionado con malos resultados clínicos en pacientes con distintos tipos de cáncer19. Los estudios también han mostrado que la prevención de la eliminación de MICA inhibe la iniciación tumoral en modelos animales20. Por lo tanto, la restauración de la vigilancia inmunológica mediada por NKG2D-MICA podría suponer una estrategia auxiliar para el tratamiento del cáncer. Sin embargo, el mecanismo exacto por el que MICA es eliminado en las células tumorales sigue siendo incierto. Lu et al. observaron un nivel sérico más elevado de sMICA en pacientes con osteosarcoma en comparación con los niveles de individuos sanos21. En este estudio hallamos que la mayoría de las muestras de carcinoma de células renales en un estadio inicial y bien diferenciado expresaron MICA en su estoma. Nuestra hipótesis se basó en que la eliminación de MICA podría haber ocurrido en las primeras etapas del carcinoma de células renales, cuando las células inmunes innatas no pudieron eliminar las células malignas a tiempo.
Las MMP son endoproteinasas dependientes de Ca2+– y Zn2+– que se clasifican en colagenasas intersticiales, estromelisinas, y gelatinasas según la especificidad del sustrato22. La metaloproteinasa de matriz-2 (MMP2) es una gelatinasa, también denominada colagenasa de tipo iv. La MMP2 es un colágeno de tipo iv asociado a la superficie celular con la capacidad de degradar las moléculas ECM, incluyendo: gelatinas, fibronectina y colágeno i, que está altamente expresado y es secretado por células renales cancerígenas humanas e invasivas. Esto podría sugerir que la MMP2 es un factor clave para el crecimiento tumoral, la angiogénesis, metástasis y la invasión celular. Diversos informes han indicado que la inhibición de la expresión y actividad de MMP2 disminuye la migración e invasión celular en células de cáncer de mama humano23.
Por consiguiente, se considera que la MMP2 es un objetivo para el desarrollo de medicamentos contra el cáncer. Nuestros estudios mostraron que MMP2 ARNhc, un RNAi específico para MMP2, aumenta la expresión de MICA anclado a la membrana y reduce la liberación de sMICA. Estos resultados sugieren un papel potencial de MMP2 en la eliminación de MICA. Se asumió que MMP2 podría haber hidrolizado MICA en la superficie celular del carcinoma de células renales, liberado MICA soluble, y finalmente haber debilitado la vigilancia inmunológica mediada por NKG2D-MICA. Esto sugiere que MMP2 podría desempeñar un papel en la eliminación de MICA en las células cancerígenas renales, aparte de su importante función en los procesos de invasión, metástasis y angiogénesis, permitiendo que estas células eludan el ataque inmunológico.
En resumen, nuestro estudio proporcionó evidencias de que MICA representa un producto de escisión de MMP2 que se forma en la primera etapa del carcinoma de células renales. Por lo tanto, el bloqueo de la actividad de MMP2 podría representar un tratamiento potencial contra el cáncer al tener como objetivo la invasión y escape tumoral en el carcinoma de células renales.
FinanciaciónEste trabajo ha sido parcialmente apoyado por becas de la Fundación de Ciencias Naturales de China (N.° 81270831 y 81000311).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses potencial con respecto a la autoría y/o publicación de este artículo.