La alteración en las propiedades viscoelásticas de la sangre ha sido anteriormente propuesta como etiopatogenia de complicaciones severas por COVID-19 y algunos casos de sordera súbita (SS). Pretendemos verificar si la aparición de casos de SS en pacientes ingresados por infección por SARS-CoV-2 puede correlacionarse de este modo.
Pacientes y métodosEstudio longitudinal prospectivo de pacientes ingresados en nuestro Centro por COVID-19, efectuando monitorización de la viscosidad sanguínea (VS) a alta velocidad de cizallamiento (300 seg-1) y un requerimiento periódico personal sobre hipoacusia. Esta determinación se extendió a casos atendidos por SS sin infección en 2019 y 2020 y un grupo control de sujetos sanos normoacúsicos.
ResultadosEl rango de normalidad se situó en 4,16±0,62 cps. Entre el 24 de febrero de 2020 y el 24 de marzo de 2021 se evaluaron 330 casos ingresados por COVID-19, 85 asistidos en la Unidad de Cuidados Intensivos (UCI). Fueron identificadas tras anamnesis y Audiometría Tonal Liminar (ATL) todo lo inmediata que el status clínico lo permitió hasta nueve casos con SS, todos pertenecientes al grupo de UCI. La VS media fue 4,38±0,43 cps en el grupo de sala, 4,53±0,39 cps en los pacientes en UCI sin SS, y 4,85±0,52 cps en los casos con SS, con diferencias estadísticamente significativas. Las mayores elevaciones de la VS en los casos con SS se detectaron entre los días seis y 10 del ingreso hospitalario. En 2019 consultaron cuatro casos y otros 2 en 2020 sin diagnóstico de COVID-19, con valores normales de VS.
ConclusionesDurante la infección por SARS-CoV-2 los pacientes pueden presentar elevación en la VS y SS, si bien se hacen necesarios un grupo control hospitalario y un volumen muestral mayor para confirmar la predisposición a la hiperviscosidad. La incidencia del daño auditivo resulta considerable si se tiene en cuenta su posible aparición en pacientes críticos con COVID-19.
Changes in blood viscoelastic properties have been proposed previosuly as etiopathogenesis for severe complications in COVID-19 and some cases of Sudden Deafness (SD). This is an attempt to verify if SD cases in patients admitted for SARS-CoV-2 infection can be correlated.
Patients and methodsA prospective follow-up was carried out with COVID-19 patients, monitoring their blood viscosity (BV) at high shear rate (300 sec-1) and inquiring them periodically for eventual hearing loss. This measurement was extended to cases bearing of SD in 2019 and 2020 without infection and a control group of healthy normoacoustic subjects.
ResultsThe normality range was 4,16±0,62 cps. 330 cases admitted for COVID-19 were evaluated from February 24th, 2020 to March 24th, 2021, 85 of them attended in ICU. After anamnesis and Audiometric Tone Thresholds developed as soon as possible, 9 SD were detected, all belonging to ICU group. The mean BV was 4,38±0,43 cps in the ward group, 4,53±0,39 cps in the ICU patients without SD, and 4,85±0,52 cps in the cases with SD, with statistically significant differences. Highest BV elevations in the SD cases were detected between days 6 and 10 of hospital admission. In 2019 four cases consulted with SD, and another two did it in 2020 without a diagnosis of COVID-19, with normal BV values.
ConclusionsDuring SARS-CoV-2 infection, patients may show high BV and SS, although an inpatients control group and a larger sample volume are necessary to confirm the predisposition to hyperviscosity. The incidence of hearing damage is considerable if its possible appearance is taken into account, within the limitations of critical patients with COVID-19.
El SARS-CoV-2 es un nuevo tipo de coronavirus transmisible entre humanos y detectado por primera vez en diciembre de 2019 en la ciudad de Wuhan, provincia de Hubei, en China. La enfermedad que causa se denomina COVID-19 y su propagación pandémica resultó en más de 78 millones de casos y 1,47 de muertes en todo el mundo y más de 1,85 millones de casos y 49.698 muertes oficialmente reconocidas en España a finales de diciembre de 2020, justo antes de iniciarse el programa mundial de vacunación. A finales de marzo de 2021 se declararon 3,26 millones de casos en España con un 5,29% de la población adecuadamente vacunada.
En un 80% de los casos transcurre subclínico y en el 80% de los sintomáticos solo produce leves manifestaciones respiratorias, pero en su diagnóstico y tratamiento se evidencia una creciente morbimortalidad con relación a complicaciones cardiovasculares y neurológicas mayormente isquémicas1. De estas últimas, las otológicas han ido acaparando interés progresivamente, y entre ellas la sordera súbita (SS).
La SS puede ser considerada síndrome por las numerosas circunstancias clínicas que a ella pueden desembocar, así como por sus variadas opciones terapéuticas. Pese a su diversidad etiopatogénica la detección de casos en el entorno del COVID-19 sugiere una relación de la misma con la reacción inflamatoria, desencadenando significativas variaciones en el flujo sanguíneo2. La viscosidad sanguínea (VS) es la resistencia de la sangre a fluir por los vasos y su incremento puede provocar un cuadro conocido como síndrome de hiperviscosidad (SHV), dependiente tanto del componente celular como del plasmático de la sangre. Se considera una urgencia diagnóstica y terapéutica porque es potencialmente letal.
En la SS ya ha sido documentada previamente la alteración en la VS, la cual se correlacionaría bien con la profundidad y el pronóstico de la hipoacusia3. Esta peculiaridad aúna teorías causales como la vírica, vascular, inflamatoria o autoinmune, ya que el resultado de todas ellas a menudo concluye en leucocitosis, trombocitosis, hiperproteinemia y elevación de reactantes de fase aguda1,4. Estos hallazgos de laboratorio están presentes a menudo en la SS y el COVID-19, especialmente en cuadros severos.
Los signos y síntomas del SHV se vinculan con alteraciones circulatorias provocadas por una mayor resistencia al flujo sanguíneo y se imbrican con las manifestaciones propias de la enfermedad de base que lo provocan. Clásicamente caracterizado por una tríada de alteraciones oftalmológicas, neurológicas y coagulopatía, el SHV puede ser además multisistémico con un rango de expresión clínica que evoluciona desde un mero cuadro gripal al fracaso multiorgánico1,4.
El interés del presente trabajo reside en la naturaleza prospectiva de la revisión efectuada en casos ingresados en nuestro Centro en los que fue monitorizada la VS, independientemente de la gravedad del cuadro clínico, manteniendo la alerta en la detección de SS en su estancia hospitalaria.
El presente estudio se ha propuesto el objetivo de valorar eventuales anomalías en las propiedades viscoelásticas de la sangre detectables que debutan con SS durante su infección por SARS-CoV-2. Ello permitiría por un lado relacionar etiológicamente este desorden auditivo con los SHV, por otro identificar pacientes COVID-19 con mayor riesgo de padecer SS y finalmente verificar si su incidencia es mayor que la habitualmente descrita, entre cinco y 27 casos/100.000 habitantes-año5,6.
Pacientes y métodosEste trabajo forma parte de una actuación multidisciplinar de seguimiento del mayor volumen posible de pacientes diagnosticados de COVID-19 e ingresados en nuestro Centro –con cobertura asistencial para 66.000 habitantes- desde el inicio de la pandemia. De este grupo se ha obtenido y sigue recopilándose información epidemiológica y hallazgos clínicos y de laboratorio convencional y de investigación. Así se creó una base de datos específica con asignación de un código numérico a cada caso según la normativa de confidencialidad de datos, una vez obtenida la aprobación del Comité Ético de Investigación Clínica del Centro.
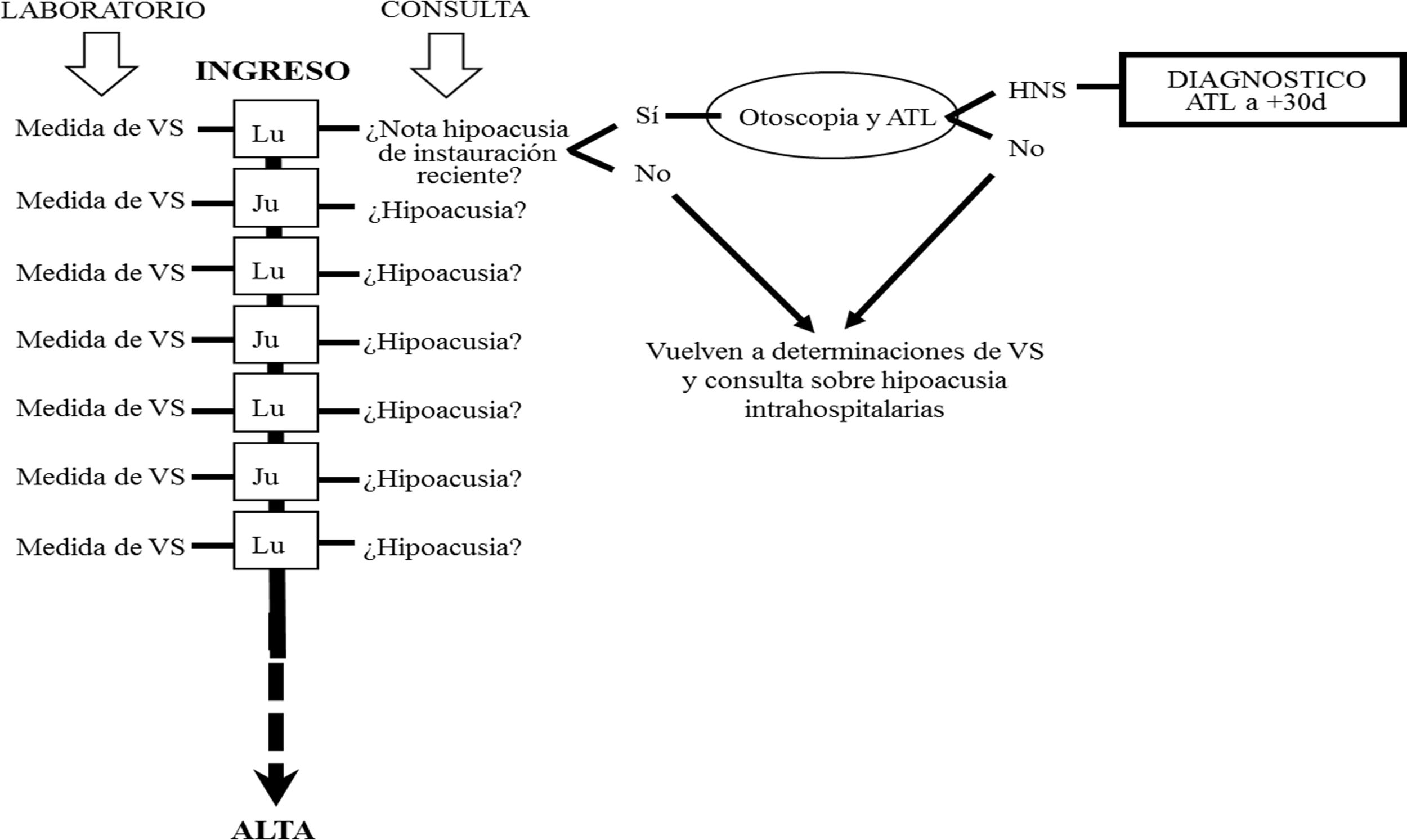
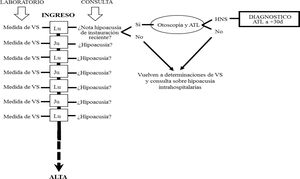
SujetosEn un seguimiento longitudinal y prospectivo fueron incluidos todos aquellos pacientes que desde la aparición de la infección por SARS-CoV-2 dieron consentimiento informado y firmado (ellos mismos o sus tutores, familiares o representantes legales) para una monitorización del perfil de VS durante su estancia hospitalaria. Así, entre el 24 de febrero de 2020 y el 24 de marzo de 2021 fueron incluídos a estudio 330 de los 412 ingresos contabilizados. A todos se les consultó dos veces por semana si advertían hipoacusia o dificultad para entender siempre que fueran receptivos a una conversación, conforme al diagrama de flujo ilustrado en la figura 1. En aquellos que contestaron afirmativamente se efectuó una valoración mediante Audiometría Tonal Liminar (ATL) en el momento que su situación clínica lo permitió y otra 30 días después. Se consideró SS aquel deterioro auditivo perceptivo con pérdidas de 30 dB HL o superiores en tres o más frecuencias consecutivas del espectro auditivo en menos de 72 horas. La recuperación auditiva se basó en los criterios de Grupo de Trabajo de la Comisión de Audiología de la Sociedad Española de Otorrinolaringología (SEORL)7 mostrados en la tabla 1.
Diagrama de flujo de actuación en ingresos COVID-19. Cada lunes y jueves de estancia hospitalaria se efectuó determinación de viscosidad sanguínea (VS) e interrogatorio sobre percepción de hipoacusia. Cuando existió impresión de deterioro auditivo se efectuó otoscopia y Audiometría Tonal Liminar (ATL) en búsqueda de valorar existencia de hipoacusia neurosensorial (HNS) de instauración súbita.
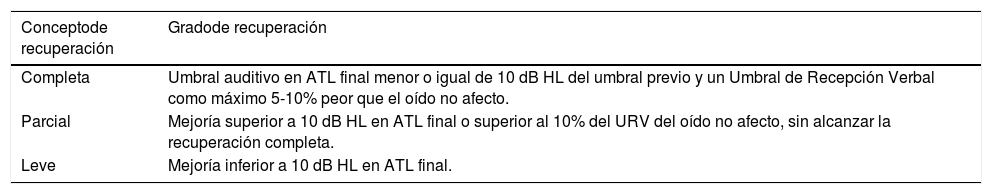
Criterios de la SEORL de 2019 sobre mejoría auditiva en SS, considerando el grado de recuperación por el promedio del umbral auditivo desde 250 a 8000 Hz en la segunda ATL a 30 días de la primera
| Conceptode recuperación | Gradode recuperación |
|---|---|
| Completa | Umbral auditivo en ATL final menor o igual de 10 dB HL del umbral previo y un Umbral de Recepción Verbal como máximo 5-10% peor que el oído no afecto. |
| Parcial | Mejoría superior a 10 dB HL en ATL final o superior al 10% del URV del oído no afecto, sin alcanzar la recuperación completa. |
| Leve | Mejoría inferior a 10 dB HL en ATL final. |
ATL: audiometría tonal liminar; SEORL: Sociedad Española de Otorrinolaringología; SS: sordera súbita; URV: umbral de recepción verbal.
Las características clínico-epidemiológicas de los sujetos valorados incluyeron el diagnóstico de infección aguda por COVID-19, la patología de base asociada, el número de tratamientos de mantenimiento, la estancia y su ubicación hospitalaria, independientemente del motivo de ingreso. Ello generó dos grupos de individuos estudiados:
- •
Ingresados con diagnóstico de infección por SARS-CoV-2 en Unidad de Cuidados Intensivos (UCI).
- •
Ingresados con diagnóstico de infección por SARS-CoV-2 en sala.
Los datos sobre pacientes infectados se tramitaron para su declaración individualizada de casos COVID-19 a la Red Nacional de Vigilancia Epidemiológica a través de la aplicación informática SiViEs, contabilizándose los casos notificados según la estrategia de alerta vigente en cada momento, y que hasta el 10 de mayo de 2020 incluía casos confirmados y probables, detectados mediante cualquiera de las técnicas de laboratorio disponibles (reacción en cadena de la polimerasa [PCR], test serológico ELISA, test rápido de anticuerpos o test de antígeno). A partir del 11 de mayo, el Ministerio de Sanidad obligó a contabilizar los casos confirmados diagnosticados por PCR y en algunos casos específicos los diagnosticados por IgM por ELISA, con base en fichas individualizadas comunicadas por la Comunidad Autónoma a través de SiViEs, de acuerdo con la Estrategia de Diagnóstico, Vigilancia y Control en la Fase de Transición de la Pandemia de COVID-19.
Asimismo, se controlaron los pacientes que en 2019 y en el período de estudio consultaron por SS sin otro motivo de asistencia y que también fueron sometidos a pruebas diagnósticas para el SARS-CoV-2.
Se efectuó finalmente una determinación de la VS sobre un grupo control de 99 individuos sanos en el período de tiempo entre el 1 de junio de 2019 y 1 de marzo de 2020, cuyos resultados permitieron establecer un rango de normalidad.
En pacientes con SS en su ingreso no se procedió con terapias específicas al haber sido tratados en el Centro con corticoides intravenosos a dosis no inferiores a 1 mg/kg/día de metilprednisolona y heparina de bajo peso molecular. En caso de ausencia de respuesta se propuso corticoterapia intratimpánica (CIT) a posteriori en protocolo de una dosis semanal de 0,9 cc de un vial de 40 mg de metilprednisolona, tres semanas consecutivas.
Los criterios de inclusión exigidos al estudio, además del consentimiento informado y firmado conforme a las especificaciones del Comité de Etica de nuestro Centro, fueron la documentación del estado de infección aguda o pasada por SARS-CoV-2, su perfil de VS y la realización de las exploraciones mediante ATL.
ViscosimetríaPara la determinación de la VS se emplearon viscosímetros rotacionales cono-plato de Wells-Brookfield con sistema de control de temperatura de 0 a 100°C modelo DV3TLVCP y husillos de cono angulados 4° modelo CPA-40Z para medidas basales de velocidad de cizallamiento (VC) de 7,5 seg-1. El giro del recipiente cónico a una velocidad predeterminada genera un movimiento de rotación en 5 cc de la muestra sanguínea a estudio anticoagulada con ácido etilendiaminotetraacético (EDTA).El viscosímetro basa su medida en la fuerza necesaria para hacer rotar el husillo en el interior de la muestra a una velocidad de giro predeterminada y constante de 300 seg-1, lo cual se consigue amplificando el giro del cono a 40 rpm. Los conos son extraíbles para su limpieza y esterilización. La unidad de medida para la VS fue el centipoise (cps), que equivale a 1 miliPascal por segundo (mPa.seg).
De esta forma fue calculado un rango de normalidad de VS a 300 seg-1 con el grupo control. Entre casos se efectuaron medidas de la VS de forma sistemática los lunes y jueves de su ingreso, configurando así un perfil cronológico de evolución de la variable a lo largo de la estancia hospitalaria en sala y/o UCI. En los sujetos asistidos por SS y que no presentaron infección por el virus se determinó igualmente la VS en el momento del diagnóstico y a los 30 días del mismo.
Análisis estadísticoPara la comparación de grupos y cohortes se empleó la técnica de análisis factorial de la varianza (ANOVA-test) en el estudio del efecto de uno o más factores. Ello se procesó en la formulación que ofrece Excel de Micrososoft Office 2013 y el paquete estadístico SPSS 26.0. La variable principal a comparar fue la VS monitorizada en el tiempo.
Cuando la comparación de datos independientes se efectuó entre diferentes individuos pertenecientes a dos grupos poblacionales se trabajó con la prueba t de Student, con comparación de medias y desviaciones estándard. La variable cuantitativa debió distribuirse de forma normal en cada una de las cohortes, verificada mediante el test de Kolmogorov-Smirnov con grupos que tienen más de 50 eventos y con las varianzas dentro de los grupos aproximadamente iguales en todos ellos.
Con valores de p superior a 0,001 no se asumieron evidencias suficientes para considerar que al menos dos medias son distintas, implicando que en el estudio se habría observado un tamaño de efecto pequeño y las técnicas de inferencia no encontraban significancia estadística para rechazar. Se consideró así pues significación estadística cuando p<0,001.
ResultadosEn los 13 meses de estudio se efectuó seguimiento a 330 pacientes ingresados con diagnóstico de infección por SARS-CoV-2. De ellos 245 solo precisaron atención hospitalaria en sala, otros 69 la iniciaron así pero su evolución precisó traslado a UCI y hasta 16 casos ingresaron directamente en ella. En un intento de simplificación, estos dos últimos grupos fueron considerados grupo de UCI (n = 85). La prevalencia anual de la infección en nuestro Departamento de Salud fue del 5,59%.
En este tiempo, 33 pacientes respondieron afirmativamente sobre la impresión de pérdida auditiva uni o bilateral. En nueve de ellos se evidenció otitis seromucosa con ATL que confirmó hipoacusia de transmisión, en cinco la ATL no detectó déficit auditivo y en otros 10 no resultó posible efectuar la exploración audiométrica. En los nnueve pacientes restantes que fueron consultados la ATL confirmó una pérdida auditiva neurosensorial unilateral o asimétrica congruente con SS, considerando el oído contralateral como umbral de referencia sobre el que comparar. Todos ellos habían sido asistidos en UCI (el 2,2% de todos los pacientes ingresados con COVID-19 y el 10,5% de los atendidos en UCI). Se trató de seis hombres y tres mujeres, con edades comprendidas entre los 42 y 77 años. De ellos tres casos asociaron acufeno en el oído afecto y uno presentó crisis de inestabilidad referida como sensación de giro. Otros dos individuos varones de 49 y 59 años consultaron por SS sin COVID-19 mientras se han estado recogiendo estos resultados en 1.266 visitas hospitalarias sobre 1.006 pacientes. En 2019 habían sido diagnosticados cuatro casos con SS en 3.966 visitas efectuadas sobre 3.691 pacientes.
El grupo de controles sanos (n = 99), con edades entre 25 y 66 años y una relación hombre/mujer de 1,25, normoacúsicos, mostró una VS media de 4,16±0,62 cps a una VC de 300 seg-1, para una distribución normal del parámetro con un intervalo de confianza de 0,95.
La tabla 2 muestra las circunstancias hospitalarias en las cohortes consideradas. El grupo con los nueve casos de SS mostró una VS media (4,85±0,52 cps) significativamente mayor respecto a los pacientes con COVID-19 en UCI, pero sin SS (n = 76; 4,53±0,39 cps, p<0,001) y al de pacientes con COVID-19 atendidos en sala (n = 245; 4,38±0,43 cps, p<0,001). Además, los casos con SS presentaron mayor estancia hospitalaria media que ingresados en sala. Aunque el volumen medio de patologías asociadas fue similar en los tres grupos, los pacientes ingresados en sala tomaban una media de medicaciones significativamente menor que los sujetos en UCI, padecieran o no SS. En la tabla 3 se indican los umbrales detectados en los pacientes que evidenciaron SS, así como el valor promedio de su VS durante su estancia hospitalaria, no solo durante el estudio sino también en el año anterior. Esta hipoacusia fue siempre unilateral, con una incidencia total de la enfermedad en 2019 de 6/100.000 habitantes-año (1 caso por cada 1.000 pacientes atendidos en nuestro Servicio) y en el período de estudio de 16,6/100.000 habitantes-año (10 por cada 1.000 pacientes atendidos).
Características de los pacientes ingresados por COVID-19 y agrupados en las 3 cohortes consideradas (*p < 0,001)
| Cohorte | n | Estancia hospitalaria | N° medidas/paciente | VST grupal media | Patologías de base | Medicaciones |
|---|---|---|---|---|---|---|
| COVID + en UCI con SS | 9 | 20,4±8,7 días (13-29)* | 6,7 medidas (5-11)* | 4,85±0,52 cps* | 3,1±2,3 | 3,1±2,2 |
| COVID + en UCI | 76 | 17,3±7,4 días (7-25)* | 7 medidas (4-11) | 4,53±0,39 cps | 3,0±2,1 | 3,2±1,2 |
| COVID + en sala | 245 | 7,2±5,9 días (4-20) | 5,9 medidas (4-8) | 4,38±0,43 cps | 2,6±1,2 | 1,5±1,7* |
UCI: Unidad de Cuidados Intensivos.
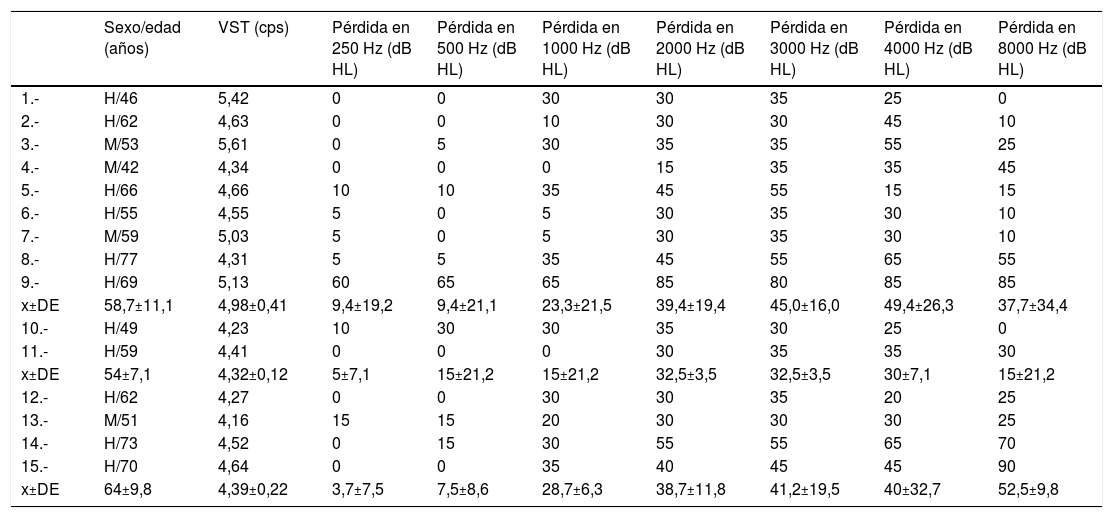
Descenso de umbrales en la primera ATL desglosado por frecuencias y valor medio de la VST a VC a 300 seg-1 de cada caso con SS. Los casos 1 a 9 son ingresos con COVID-19. Los casos 10 y 11 son ambulatorios no infectados en 2020. Los casos 12 a 15 son casos detectados en 2019
| Sexo/edad (años) | VST (cps) | Pérdida en 250 Hz (dB HL) | Pérdida en 500 Hz (dB HL) | Pérdida en 1000 Hz (dB HL) | Pérdida en 2000 Hz (dB HL) | Pérdida en 3000 Hz (dB HL) | Pérdida en 4000 Hz (dB HL) | Pérdida en 8000 Hz (dB HL) | |
|---|---|---|---|---|---|---|---|---|---|
| 1.- | H/46 | 5,42 | 0 | 0 | 30 | 30 | 35 | 25 | 0 |
| 2.- | H/62 | 4,63 | 0 | 0 | 10 | 30 | 30 | 45 | 10 |
| 3.- | M/53 | 5,61 | 0 | 5 | 30 | 35 | 35 | 55 | 25 |
| 4.- | M/42 | 4,34 | 0 | 0 | 0 | 15 | 35 | 35 | 45 |
| 5.- | H/66 | 4,66 | 10 | 10 | 35 | 45 | 55 | 15 | 15 |
| 6.- | H/55 | 4,55 | 5 | 0 | 5 | 30 | 35 | 30 | 10 |
| 7.- | M/59 | 5,03 | 5 | 0 | 5 | 30 | 35 | 30 | 10 |
| 8.- | H/77 | 4,31 | 5 | 5 | 35 | 45 | 55 | 65 | 55 |
| 9.- | H/69 | 5,13 | 60 | 65 | 65 | 85 | 80 | 85 | 85 |
| x±DE | 58,7±11,1 | 4,98±0,41 | 9,4±19,2 | 9,4±21,1 | 23,3±21,5 | 39,4±19,4 | 45,0±16,0 | 49,4±26,3 | 37,7±34,4 |
| 10.- | H/49 | 4,23 | 10 | 30 | 30 | 35 | 30 | 25 | 0 |
| 11.- | H/59 | 4,41 | 0 | 0 | 0 | 30 | 35 | 35 | 30 |
| x±DE | 54±7,1 | 4,32±0,12 | 5±7,1 | 15±21,2 | 15±21,2 | 32,5±3,5 | 32,5±3,5 | 30±7,1 | 15±21,2 |
| 12.- | H/62 | 4,27 | 0 | 0 | 30 | 30 | 35 | 20 | 25 |
| 13.- | M/51 | 4,16 | 15 | 15 | 20 | 30 | 30 | 30 | 25 |
| 14.- | H/73 | 4,52 | 0 | 15 | 30 | 55 | 55 | 65 | 70 |
| 15.- | H/70 | 4,64 | 0 | 0 | 35 | 40 | 45 | 45 | 90 |
| x±DE | 64±9,8 | 4,39±0,22 | 3,7±7,5 | 7,5±8,6 | 28,7±6,3 | 38,7±11,8 | 41,2±19,5 | 40±32,7 | 52,5±9,8 |
ATL: audiometría tonal liminar; H: hombre; M: mujer; SS: sordera súbita; VC: velocidad de cizallamiento; VST: viscosidad en sangre total.
Conforme a los criterios de recuperación auditiva7, de los nueve casos con COVID-19, en tres se evidenció una mejoría de grado completo, en tres la mejoría fue parcial y en otros tres resultó nula –pese a la administración en tres de ellos de tandas de CIT-, pudiendo concluirse que en dos tercios de los casos no ha habido reversión de la enfermedad. En ninguno de los tres casos con acufeno este ha remitido. El desorden del equilibrio que presentó uno de los pacientes desapareció en 30 días.
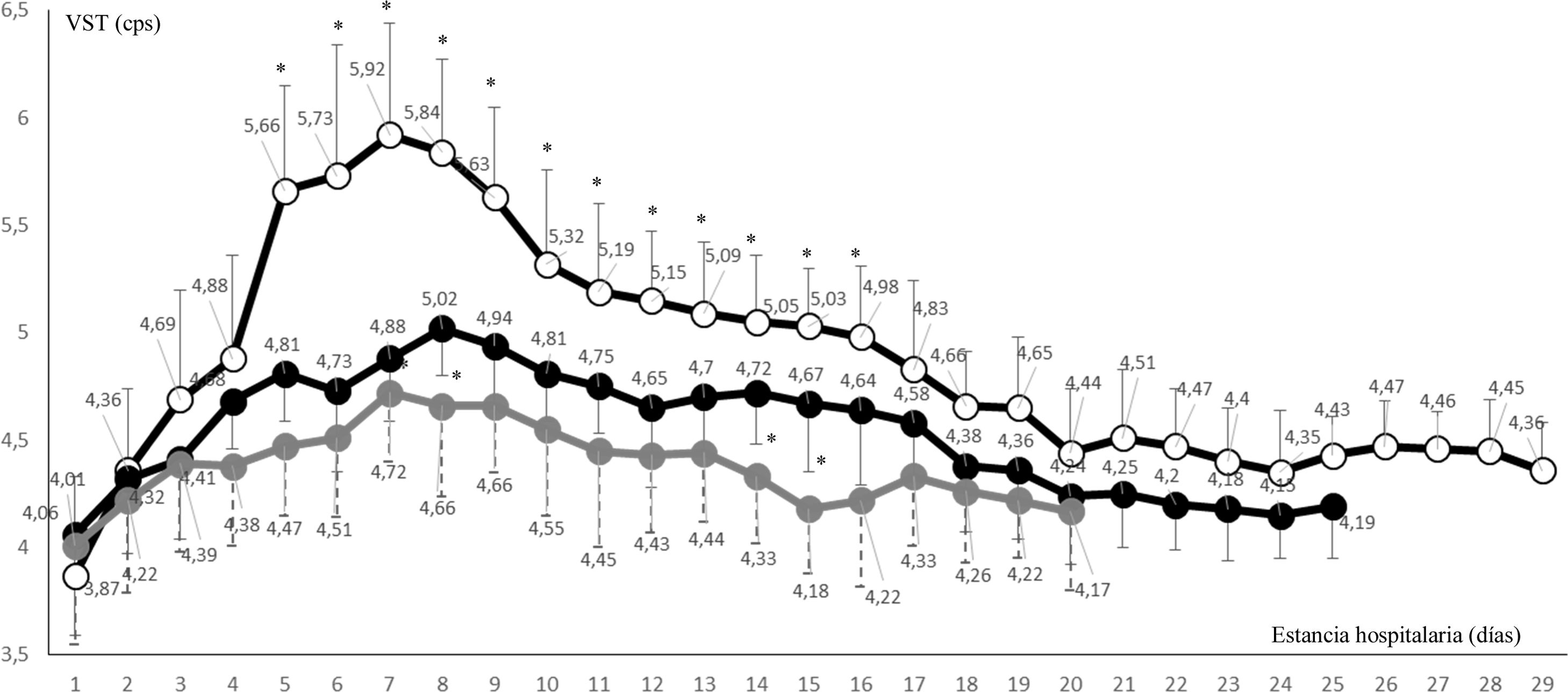
La figura 2 representa la variabilidad temporal en la media de la VS de todos los casos con infección por SARS-CoV-2, considerados por cohortes según su estancia hospitalaria fuera en sala o en UCI. Puede apreciarse su elevación entre los casos en los que se detectó SS, concretamente del día cinco al 16, con diferencias estadísticamente significativas frente al grupo de pacientes con COVID-19 ingresados en UCI, pero sin deterioro auditivo, así como frente a los pacientes en sala. En casos con SS la determinación de su VS siempre resultó mayor que el valor superior del rango de normalidad, con un pico máximo en el día siete del ingreso (n = 9; 5,92±0,52 cps).
Variación diaria en la media de la viscosidad sanguínea de todos los ingresos con infección por SARS-CoV-2, considerados por cohortes (sala, UCI sin sordera súbita, UCI con sordera súbita). Los tres grupos mostraron valores de viscosidad sanguínea más altos que el rango de normalidad obtenido. El grupo COVID en UCI con sordera súbita mostró una viscosidad sanguínea media significativamente mayor que los pacientes en UCI sin sordera súbita durante los días 5 a 16 de su estancia (*p < 0,001).
En el grupo de pacientes ingresados en UCI sin daño auditivo se apreció una elevación menos pronunciada, con un pico máximo en el día ocho (n = 76; 5,02±0,22 cps), único día en que la diferencia de este valor fue estadísticamente significativa, aunque entre los días cuatro y 16 las cifras de VS también superaron el rango de normalidad. Entre pacientes con COVID-19 ingresados en sala (n = 245) la VS estuvo también por encima de los valores de normalidad, pero por debajo de los dos subgrupos de UCI.
DiscusiónLas etiologías más comúnmente aceptadas en la SS son la vírica, autoinmune y vascular. En la patogenia de todas ellas tendrían cabida procesos de incremento en la VS documentados en desórdenes tumorales, inflamatorios y circulatorios, y que a menudo evolucionan al fracaso de uno o varios órganos. La hiperviscosidad endovascular local es susceptible de generar disfunción en el endotelio y las tres líneas celulares sanguíneas y ello activar secundariamente los mecanismos de la coagulación que promueven el fenómeno de la microtrombosis8. Allí donde un órgano dependa exclusivamente de una circulación monocariante –como el laberinto- su anulación puede concluir en el deterioro rápido y potencialmente irreversible de su función9.
La sangre es un fluido no newtoniano y varía su viscosidad en función de su composición y velocidad de flujo. Esta es el resultante de la razón entre la fuerza que actúa paralelamente a la superficie del vaso en cada unidad de flujo o fuerza de cizallamiento (FC) y la diferencia de velocidades entre dos capas adyacentes de este flujo o VC. A su vez, la VC se relaciona con la velocidad de flujo y el radio interno de los vasos conforme a la fórmula VC = 4.v/r, y tiene un valor entre 101,1 y 102,2 seg-1 en arteriolas y 102,2 y 102,5 seg-1 en capilares10. Así, con VC pequeña las fuerzas que actúan sobre los hematíes también son reducidas y aquellos agregan en rouleaux, muy potenciado por el fibrinógeno circulante, con lo que la VS se eleva2. Si la VC se eleva se desagregan los rouleaux y los eritrocitos se deforman dejando de ser discoideos para hacerse ovales con eje mayor en el sentido longitudinal de la corriente sanguínea, lo cual opone una mínima resistencia al flujo. En condiciones fisiológicas la VC de la sangre es de varios centenares de seg-1 en casi todo el árbol vascular, por lo que la FC es lo suficientemente alta como para desagregar a los hematíes y llevarlos a un estado de deformación máxima que minimiza la viscosidad y optimiza el trabajo cardíaco. La VS se eleva en flujos lentos, propiciando la agregabilidad eritrocitaria, y disminuye en flujos rápidos por su gradiente de deformabilidad11.
La circulación laberíntica es terminal y depende de una arteriola cuya regulación no está en función de la perfusión cerebral, pero su flujo puede verse influido por variaciones en la VS si se alteran algunos de los factores que inciden en ella, como el hematocrito, la deformabilidad y agregabilidad eritrocitarias, agregabilidad plaquetar, leucostasis, la hiperfibrinogenemia e hiperlipemias11,12. La VS a altas VC intenta emular las condiciones de perfusión del oído interno y está documentada su elevación en individuos que han padecido SS al reducirse la filtrabilidad sanguínea y la oxigenación tisular. Los valores obtenidos para el grupo control en nuestro trabajo son similares a los detectados en 1997 trabajando con viscosímetros menos sofisticados, mostrando valores aproximados de 4,2 cps para altas VC4. Se acepta que la viscosidad plasmática, no estudiada en este trabajo, no supera los 2 cps y no se ve influenciada a variaciones de la VC.
La hiperviscosidad sanguínea ya ha sido apreciada anteriormente en cuadros de presbiacusia, hipoacusias neurosensoriales rápidamente progresivas y SS. En estas últimas además se pudieron establecer correlaciones entre los índices de deformabilidad eritrocitaria y de filtrabilidad sanguínea reducidos y niveles de fibrinógeno elevados con mayores pérdidas auditivas y menor capacidad de recuperación9,11,13, proponiéndose actuaciones específicas como parte del tratamiento de la SS, entre ellas agentes hemorreoactivos, la hemodilución normovolémica y la aféresis de lípidos y fibrinógeno4,14-16.
Entre las diversas vías en las que se ha advertido daño tisular de SARS-CoV-2 figura la capacidad de desoxigenación de los hematíes al desestructurar las cadenas β de la hemoglobina incrementando la rigidez de la bicapa lipídica de su membrana17. Además, la presencia de enzima convertidora de la angiotensina-2 (ECA-2) en músculo liso arteriolar le hace perder elasticidad en caso de infección promoviendo uniones entre hematíes y fibrinógeno y este con el endotelio íntegro, incluso antes de que las plaquetas actúen localmente y potencien el estasis microvascular1,18. Todo ello facilita la agregabilidad eritrocitaria y eleva la VS en los vasos de pequeño calibre, como la arteria auditiva interna, concluyendo en la activación de la hemostasia mucho antes que la de la coagulación. Otros mecanismos como el neurotropismo del virus y su acceso por líquido cefalorraquídeo (LCR) al VIII par y la ototoxicidad de terapias convencionales en la infección también han sido propuestas19. La afectación de oído medio detectada en nuestro estudio también ha sido documentada por Fidan20, pero carece de la trascendencia clínica del cuadro que nos ocupa.
Además del daño pulmonar, el COVID-19 se ha caracterizado por una especial afectación neurológica de naturaleza tromboembólica en pacientes con evolución desfavorable existiendo buena correlación con los niveles de fibrinógeno y D-dímeros1,16, lo cual alcanza al 36% de los ingresados por la infección21. Nuestro estudio detecta un significativo incremento en la VS de los pacientes ingresados en UCI y por tanto clínicamente más comprometidos, característicamente a partir del sexto día del ingreso. Se trata del período de máxima liberación de citocinas IL-1, IL-2, IL-4, IL-7, IL-10, IL-12, IL-13, IL-17, proteína-1α inflamatoria de macrófagos, interferón-γ, factor de necrosis tumoral-α, de crecimiento hepatocítico y estimuladores de colonias de granulocitos y macrófagos en ausencia de un adecuado control inmunitario ante la entrada del SARS-CoV-222. El interceptor IL-6 y el receptor de IL-2 promueven el reclutamiento de líneas celulares sanguíneas y la elevación de reactantes de fase aguda. Ello predispone al daño endotelial y sobre todo al incremento en la FC y por tanto en la VS23. El resultado es la pérdida del glicocálix en la pared endotelial, la inhibición del sistema del plasminógeno desde la vía renina-angiotensina y finalmente la aparición del SHV. Este desorden, descrito por Ahmed et al. con turbulencias en el flujo sanguíneo resulta ser el fundamento de la trombogénesis en la infección por el virus24.
Hipertensos, diabéticos y dislipémicos muestran mayor predisposición al SHV. Son por otra parte grupos de riesgo y factor de mal pronóstico en casos graves de COVID-19, donde los hallazgos de laboratorio más significativos incluyen la elevación de fibrinógeno, citocinas, inmunocomplejos circulantes y plaquetas6,25. Con anterioridad se han detectado estas modificaciones en sangre e involucrado en la etiopatogenia de la SS. Sería razonable admitir que los mismos hallazgos entre infectados con el coronavirus puedan desarrollar el trastorno auditivo.
La documentación de casos de SS en el contexto del COVID-19 no es excepcional. Son publicaciones con casos aislados o series muy limitadas que valoraron pacientes con el trastorno auditivo con y sin infección, casi todas ellas resumidas en el trabajo de Saniasiaya17. El primer caso descrito parece documentarse por Sriwijitalai et al. en Tailandia en marzo, sin especificaciones clínicas ni terapéuticas25. Curiosamente, en el primer documento con un significativo volumen poblacional, Chari et al. compararon los registros de SS en 75 días consecutivos entre marzo y mayo de 2019 y 2020, notificando incidencias del cuadro de 1,77 vs. 1,91%, en un área de cobertura de sanitaria con 592.853 individuos en Massachusetts y una prevalencia de la infección por SARS-CoV-2 del 16,4%, sugiriendo una ausencia de implicación del mismo en este desorden, aunque también sopesaban el sesgo dependiente del paciente asociado al temor a contraer la enfermedad al consultar26.
Harenberg et al. sin embargo se posicionan en sentido contrario al encontrar mayor riesgo de SS entre pacientes con COVID-19, lo que atribuyen al neurotropismo por la presencia neuronal de receptores del virus ECA2, a la endotelitis concomitante y a la agregabilidad plaquetar27. Maier et al. describen 15 pacientes asistidos en UCI por neumonía grave y tratados con anticoagulantes por presentar valores medios de fibrinógeno de 708 mg/dL y de viscosidad plasmática siempre superiores a su rango de normalidad entre 1,4 y 1,8 cps, verificando además cuatro eventos trombóticos con este parámetro en 3,5 cps8. De forma similar, Venter et al. detectan elevaciones en el fibrinógeno y viscosidad plasmáticos de hasta 1000 mg/dL y 2,8 cps, respectivamente, en su serie de 29 casos con complicaciones vasculares graves4. Puede establecerse con ello un vínculo entre inflamación, hiperviscosidad y coagulopatía en pacientes críticos con COVID-19 y recomendarse la identificación de los componentes celulares o plasmáticos como medida de severidad de la enfermedad.
Nuestro estudio detecta de forma prospectiva modificaciones significativas en la VS como potencial causa del trastorno auditivo, siendo el primero en relacionar viscoelasticidad con SS en el entorno del COVID-19. Desde este punto de vista coincidimos con Hildesheimer et al. en que la normalización de este factor puede convertirse en meta obligatoria del tratamiento encaminado a la recuperación auditiva12. Al menos parece lógico pensar que el conocimiento de estos parámetros es de utilidad en la elección del tratamiento, la clarificación de la etiología y el establecimiento de un pronóstico. Insistimos en la necesidad de preguntar al paciente ingresado tan pronto como sea posible sobre alteraciones en su audición.
En la actualidad, esta oferta terapéutica ya incluye la corticoterapia sistémica conforme a las especificaciones del grupo Rapid Evidence Appraisal for COVID-19 Therapies (REACT) de la Organización Mundial de la Salud (OMS), lo cual permite quizás prevenir el desorden auditivo y reducirlo a una incidencia todavía desconocida para nosotros en este contexto de una enfermedad nueva28. La inherente capacidad infectocontagiosa del SARS-CoV-2 no está permitiendo efectuar un diagnóstico precoz y un tratamiento más específico si cabe, excepto la posibilidad de CIT cuando el sujeto se encuentra en condiciones. El seguimiento prospectivo de casos diagnosticados recientemente y su requerimiento sistemático sobre aparición de hipoacusia debería ser la norma. Bajo estas premisas se hará necesario un volumen mayor de casos con criterios definidos de circunstancias clínicas, hallazgos de laboratorio y, por supuesto, terapias efectuadas.
ConclusionesLas variaciones en las propiedades viscoelásticas de la sangre han sido detectadas en pacientes con SS y COVID-19, pudiendo presentar VS elevada. En ambos contextos resulta destacable la elevación del fibrinógeno. Ello hace recomendable investigar la presencia de hipoacusias de estas características en el COVID-19 asumiendo que la desconexión del paciente con el entorno puede ser alta, su colaboración limitada y las actuaciones diagnósticas y terapéuticas diferidas. Muestras poblacionales más extensas permitirán establecer asociaciones fisiopatológicas óptimas.
Nuestro más significado agradecimiento a todos los pacientes que nos han permitido trabajar e investigar en un momento clínico y social tan delicado y al personal sanitario que ha participado en la detección y tratamiento de la enfermedad, así como en la obtención, recolección y procesamiento de las muestras para la realización de este estudio. Especial reconocimiento al trabajo de laboratorio desarrollado por las Srtas. Dª Ana Ortiz y Dª Julia González.FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.