El uso de los implantes de titanio se inició con el descubrimiento de la integración de este material al hueso, cuando Branemark (Suecia), en los años sesenta, describió que los osteocitos crecían en aposición de la superficie del titanio y desarrollaban una fuerte unión, iniciando su uso en las cirugías oral y reconstructivas craneofaciales1. Con la introducción de Tjellstrom y Granstrom en 1977 de una ayuda auditiva adaptada a un implante de titanio en el hueso temporal, bone-anchored hearing aid (BAHA), se inicio el uso de un dispositivo para amplificación y restauración de la audición en ciertas condiciones donde la amplificación convencional no era la adecuada2. El BAHA está indicado en pacientes con pérdidas conductivas, mixtas o neurosensoriales unilaterales, que no puedan ser corregidas quirúrgicamente o no toleren la adaptación de audífonos tradicionales, en casos tales como: atresias aurales, otosclerosis, cavidades húmedas o grandes, otitis externas crónicas, canales estrechos y oídos únicos.
Los procesadores Compact y Divino están indicados en pérdidas auditivas con promedio tonal puro para la vía ósea µ 45 dB HL, para el modelo Cordelle II, las pérdidas pueden ser hasta de 70 dB HL con una discriminación bisilábica > 60 % en el mejor oído3.
MATERIAL Y MÉTODOSeguimiento retrospectivo de 12 pacientes desde enero de 2004 a enero de 2006. Se les realizó implante de BAHA con diversas indicaciones (tabla I).
Las cirugías se realizaron con anestesia general por el mismo grupo quirúrgico en dos instituciones. Pasos quirúrgicos:
– Demarcación del área del implante. Rasurado e infiltración del área.
– Realización de colgajo de piel con dermatomo, pediculado inferior.
– Resección de tejido celular subcutáneo.
– Incisión de 5 mm en cruz del periostio mastoideo.
– Fresado e inserción del implante de titanio según la técnica estándar de Branemark. En los niños de menos de 14 años se implanta un segundo tornillo4.
– Colocación de puntos de material absorbible desde bordes subcutáneos hasta periostio.
– Puntos de material no absorbible del colgajo a la piel circundante.
– Exteriorización en adultos. En los niños se exterioriza en un segundo tiempo.
– El dispositivo de amplificación es activado a los 3 meses en los adultos y a los 4-6 meses en los niños.
Se recolectaron los datos audiométricos preoperatorios: umbrales de tonos puros (PTA) óseos y aéreos en las frecuencias de 500, 1.000, 2.000 y 4.000 Hz, de igual forma el umbral de recepción del habla (SRT) para palabras bisilábicas en cada oído. El PTA y el SRT en campo libre con el dispositivo BAHA fueron realizados en las mismas frecuencias.
Asimismo se registró tanto las complicaciones mayores y menores como su tratamiento y el tiempo de uso en horas al día.
El análisis de los resultados se realizó usando el software SPSS versión 11.5 (SPSS Inc., Chicago, Illinois, Estados Unidos). El umbral de significación estadística fue p < 0,05.
RESULTADOSEl seguimiento de los pacientes fue una media de 10,9 ± 4,5 meses. Dos pacientes implantados con BAHA no tuvieron el seguimiento audiológico adecuado, por lo que se los excluyó de los resultados. La media de edad fue 31,6 ± 18,9 años. En las 8 mujeres y los 2 varones, el oído implantado y la etiología tuvieron una frecuencia similar (tabla I).
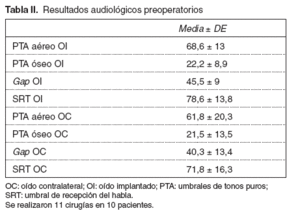
El PTA aéreo y óseo del oído implantado y el contralateral se muestran en la tabla II. Todos los pacientes presentaron algún tipo de déficit auditivo, y se observó que los PTA estaban en rangos similares y el gap osciló entre 45,5 y 40,3 dB en el oído implantado y en el contralateral, respectivamente (p = 0,392).
Con respecto al seguimiento audiológico del oído implantado, encontramos una mejoría significativa con el uso del audífono BAHA; la mejoría en el PTA fue de 34,5 dB, el SRT mejoró en promedio 37,7 dB y el gap cerró a 11,9 dB (tabla III).
Tabla I. Línea de base
Tabla II. Resultados audiológicos preoperatorios
Tabla III. Resultados audiológicos en el oído implantado
En los adultos se realizo la cirugía en un solo tiempo quirúrgico y se activó el implante a los 3,8 meses. En niños se activó el implante a los 8 meses. La paciente n.º 3 presentó extrusión del implante activo a los 2 meses, por lo que se tuvo que utilizar el implante de rescate y se esperó a activarlo a los 12 meses. Los pacientes refieren utilizar el audífono 12,1 h/día.
Se presentaron tres complicaciones. La referida en el caso 3 se debió a una pérdida espontánea del implante sin causa desencadenante, con una adecuada respuesta posterior a la activación del tornillo de rescate. El caso 6 presentó infección tardía en el colgajo de piel alrededor del pedestal, que se trató con antibiótico oral y tópico, con una resolución completa de su cuadro infeccioso, retornando al uso de su ayuda auditiva. En el caso 9 se presentó un colgajo libre de piel durante la realización con el dermatomo, se manejó con reposición, asegurando la aposición de éste con el periostio con vendaje compresivo, con buena integración en el seguimiento a los 3 meses.
DISCUSIÓNLos pacientes con hipoacusia conductiva o mixta que no son candidatos quirúrgicos o no toleran la adaptación de ayudas auditivas convencionales para su rehabilitación auditiva pueden beneficiarse de los implantes tipo BAHA4. Convencionalmente se ha utilizado los amplificadores por vibración percutánea, pero se han reportado resultados divergentes e insatisfacción de los usuarios, dados la variabilidad de posición, el pobre ajuste, la incomodidad y la pérdida de energía sonora a través de la piel, lo que conlleva pérdidas de la fidelidad sonora hasta de 10-20 dB4-7. La adaptación del procesador de sonido directamente al implante óseo corrige muchas de las desventajas descritas5 y se ha demostrado otras ventajas como la estimulación bilateral de las cócleas y que no hay retroalimentación8.
Otra alternativa es la cirugía reconstructiva en el caso de malformaciones congénitas o funcionales. Con pobres resultados audiológicos en las malformaciones severas con puntajes < 7 en la escala de Jahrsdoerfer9.
Las razones más comunes para la implementación del sistema BAHA en nuestro estudio fueron la cavidades mastoideas drenantes y las malformaciones congénitas no quirúrgicas. Todos nuestro pacientes tuvieron alguna clase de mejoría auditiva, encontrando cierre del gap aéreo-óseo < 10 dB en el 27 %, < 15 dB en el 72 % y < 20 dB en 10/11 (90,9 %) pacientes.
El promedio de cierre del gap en nuestro grupo fue de 12 dB, con un promedio de mejoría en la audición de 34,5 dB. Estudios similares, como el estudio de Lustig et al, reportan un cierre de gap de 18 dB y mejoría auditiva de 28 dB. Por otra parte, la discriminación medida en el SRT mejoró en 37,7 dB; Liepert y DiToppa, en su experiencia de 15 pacientes, reportan una ganancia de 30 dB.
Los reportes de estudios con BAHA demuestran una baja tasa de complicaciones y las más frecuentes son pérdida parcial o completa del colgajo, crecimiento de piel sobre el pedestal, irritación o infección del colgajo y extrusión del implante10. Otras causas menos frecuentes y reportes aislados refieren pérdidas del implante por traumatismo, enfermedad mental o absceso intracerebral11,12. Entre las complicaciones, se presentó un injerto libre en un paciente intraoperatoriamente, que se integró satisfactoriamente al periostio subyacente, a pesar de reportes de pérdidas de hasta el 46,7 % del injerto alrededor del implante13.
Cabe mencionar que seguimos las recomendaciones mundiales de dejar un tornillo de rescate en niños, por la alta tasa de extrusión. Como sucedió en la paciente 3, de 6 años14.
Los audífonos de implantación ósea ofrecen a la otorrinolaringología una buena alternativa para la rehabilitación de los pacientes con déficit auditivo que no son candidatos al uso de ayudas auditivas tradicionales.
Correspondencia: Dr. J.F. Monroy Barreneche. Calle 68 # 1-54 este. Apartamento 502. Ed. Nueva Granada. Bogotá. Colombia. Correo electrónico: monroyjuanf@gmail.com
Recibido el 27-11-2006. Aceptado para su publicación el 5-9-2007.