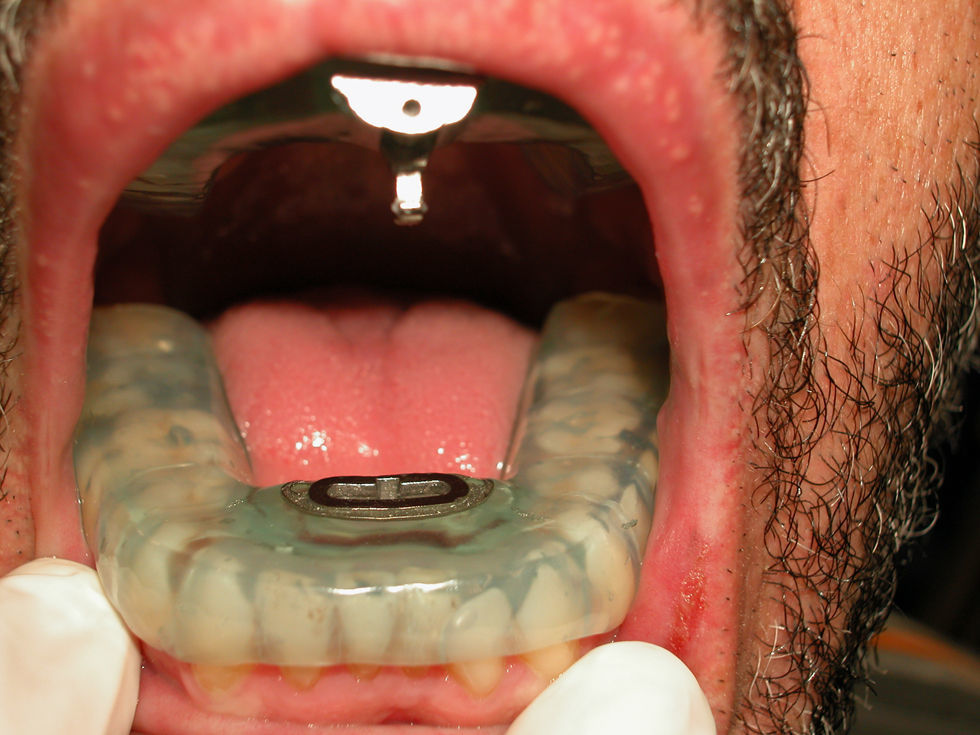
Los dispositivos de avance mandibular se muestran cada vez más útiles en el tratamiento de los trastornos respiratorios del sueño en adultos. En 2008 se inició un estudio prospectivo para adaptar 40 dispositivos sin coste, con el objetivo de evaluar su eficacia en nuestros pacientes.
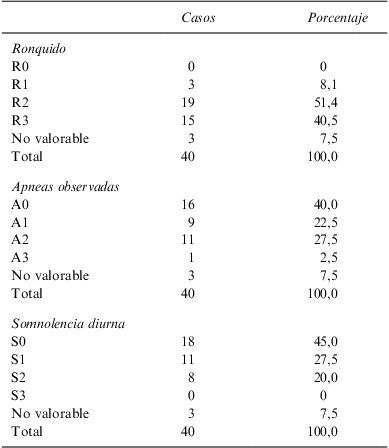
Material y métodoSe analiza su aplicación en 40 pacientes adultos con un índice de apnea hipoapnea inferior a 40. La totalidad de los casos referían ronquido, el 52,5% apneas observadas y el 47,5% somnolencia diurna.
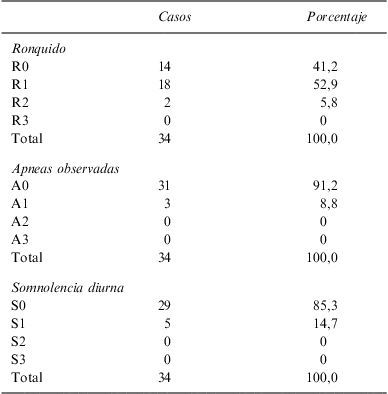
ResultadosCon un seguimiento mínimo de 6 meses, los casos con ronquido descienden a 59%, la mayoría de intensidad significativamente inferior, los casos con apneas observadas al 8,8% y la somnolencia diurna al 14,7%. La mejoria clínica global se consideró en 31 pacientes (91,2%). El índice de apnea hipoapnea medio pasó a 8,4±9,6 y la mejoría polisomnográfica se objetivó en 25 casos (75%). Un resultado positivo global, que requiere la mejoría tanto subjetiva como objetiva, se obtuvo en 23 pacientes (69,7%). Abadonaron su utilización 2 pacientes en los primeros días y otro caso a los 6 meses. Las compliaciones fueron relativamente frecuentes (58,8% de casos), pero leves. Los niveles de cumplimiento fueron satisfactorios: una media de 6,5±1,1 noches a la semana y 7,4±1,09h por noche.
ConclusiónLos dispositivos de avance mandibular son una alternativa terapéutica eficaz para tratar los trastornos respiratorios del sueño. Los niveles de cumplimiento pueden ser satisfactorios si se cuenta con la colaboración de un equipo odontológico experto.
Mandibular advancement devices are being shown to be increasingly useful in the treatment of adult respiratory sleep disorders. A prospective study was started in April 2008 to apply 40 devices free of charge, with the aim of assessing their usefulness in our patients.
Material and methodsThe device was applied to 40 patients with an apnoea-hypopnoea index of less than 40. All the cases snored, with 52.5% observed apnoeas and 47.5% diurnal sleepiness.
ResultsWith a minimum follow-up of six months, the cases that snored decreased to 59%, most with a significantly lower intensity; 8.8% of cases had observed apnoeas and 14.7% mentioned diurnal sleepiness. There was an overall clinical improvement in 31 (91.2%) patients. The mean apnoea-hypopnoea index fell to 8.4±9.6 and polysomnographic improvement could be seen in 25 (75%) cases. An overall positive result, showing subjective as well as objective improvement, was obtained in 23 (69.7%) patients. Two patients stopped using the device in the first few days and another patient after six months. Complications were relatively common, but always slight. Compliance levels were satisfactory: a mean of 6.5±1.1 nights per week and 7.4±1.09 days per week.
ConclusionMandibular advancement devices are an effective therapeutic option for the treatment of respiratory sleep disorders. Compliance levels can be satisfactory if working with an expert odontology team.