La lesión renal aguda ha sido descrita como una complicación frecuente de las cirugías cardíacas en pacientes pediátricos; se asocia con una mayor comorbilidad en la unidad de cuidados intensivos pediátricos, síndrome de disfunción orgánica múltiple y mayor riesgo de mortalidad. El objetivo de este estudio fue determinar los factores demográficos y clínicos que favorecen la presencia de lesión renal aguda en pacientes pediátricos sometidos a bypass cardiopulmonar.
Población y métodosEstudio observacional analítico de cohorte retrospectivo en pacientes pediátricos sometidos a bypass cardiopulmonar admitidos en la unidad de cuidados intensivos pediátricos en la Clínica Cardio VID entre enero de 2015 a junio del 2019. Se definió lesión renal aguda según los criterios de Kidney Disease: Improving Global Outcomes. Se cuantificó la incidencia de lesión renal aguda en el postoperatorio y se analizaron factores asociados mediante una regresión logística binaria.
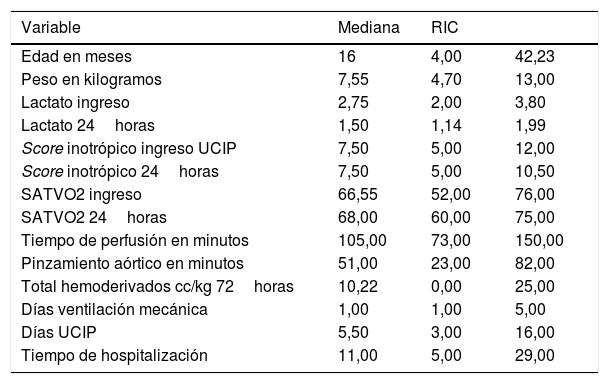
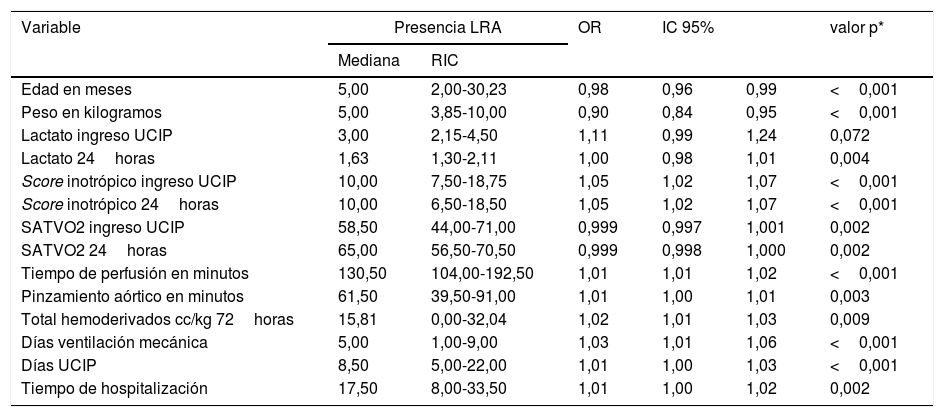
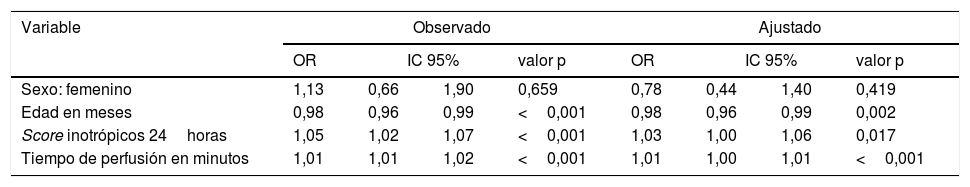
ResultadosSe analizaron 326 pacientes, de los cuales el 22% desarrollaron lesión renal aguda. Se identificaron como principales factores asociados la edad (OR: 0,98; IC 95%: 0,96-0,99; valor de p: 0,002), el score de inotrópicos 24 horas (OR: 1,03; IC 95%: 1,00-1,06; valor de p: 0,017) y el tiempo de perfusión (OR: 1,01 IC 95%: 1,00-1,01; valor de p<0,001).
ConclusiónLa edad, el tiempo de perfusión y el score de inotrópicos a las 24 horas podrían explicar hasta el 20% de los casos de lesión renal aguda en esta cohorte de pacientes.
Acute kidney injury has been described as a frequent complication of cardiac surgeries in paediatric patients. It is associated with higher comorbidity in the paediatric intensive care unit, multiple organ dysfunction syndrome, and increased risk of mortality. The objective of this study was to determine the demographic and clinical factors that promote the presence of acute kidney injury in paediatric patients undergoing cardiopulmonary bypass.
Population and methodsRetrospective, observational, analytical cohort study in paediatric patients undergoing cardiopulmonary bypass admitted to the paediatric intensive care unit at Clínica CardioVID between January 2015 and June 2019. Acute kidney injury was defined according to the guideline Kidney Disease: Improving Global Outcomes (KDIGO). The incidence of acute kidney injury in the postoperative period was quantified and associated factors were analysed using binary logistic regression.
ResultsThree hundred and twenty-six patients were analysed, of whom 22% developed an acute kidney injury. Age (OR .98: 95% CI .96-.99 p value .002), 24-hour inotropic score (OR: 1.03; 95% CI: 1.00-1.06; P value: .017) and pump time (OR: 1.01; CI 95%: 1.00-1.01; P value<.001) were identified as the main associated factors.
ConclusionAge, pump time and inotropic score at 24hours could explain up to 20% of the cases of acute kidney injury in this cohort of patients.
Artículo
Socios de la Asociación de Medicina Crítica y Cuidado Intensivo
Para acceder a la revista
Es necesario que lo haga desde la zona privada de la web de la AMCI, clique aquí
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora