La eficacia de la rehabilitación respiratoria (RR) se ha constatado no únicamente en la enfermedad pulmonar obstructiva crónica sino también en otras enfermedades respiratorias que no son enfermedad pulmonar obstructiva crónica. La RR es una intervención con un gran impacto en mejorar la disnea, la capacidad de esfuerzo y la calidad de vida relacionada con la salud, con un alto nivel de evidencia y recomendación. En los últimos años se ha demostrado que la RR es tan eficaz si se realiza en un centro hospitalario como en el domicilio de los pacientes, e incluso con los sistemas de telemedicina. También hemos cambiado el concepto del momento de inicio de un programa tras una agudización, demostrándose que es más eficaz cuanto antes se inicie sin provocar efectos secundarios. Sin embargo, para alcanzar el máximo rendimiento sin riesgos es imprescindible una evaluación por el equipo de RR y una prescripción del programa totalmente personalizada según las necesidades y posibilidades de cada paciente. En los últimos años se están proponiendo nuevas estrategias más sencillas y que faciliten el acceso a todos los posibles candidatos a fin de conseguir una mayor adherencia a los programas y un mantenimiento de los beneficios a largo plazo, fundamentalmente incidiendo en los hábitos de vida y favoreciendo la actividad física.
Pulmonary rehabilitation (PR) has been seen to be useful not only in chronic obstructive pulmonary disease, but also in other non-chronic obstructive pulmonary disease respiratory diseases. It is highly effective in improving dyspnea, exercise tolerance, and health-related quality of life, and is supported by a high level of evidence and grade of recommendation. In recent years, PR has been shown to be equally effective in both the hospital and home setting, and can even be used in telemedicine. The recommended timing of PR after an exacerbation has also changed following evidence that early intervention is more beneficial and has no negative impact on side effects. However, to achieve maximum effect while avoiding risk, each patient must be evaluated by the PR team, and rehabilitation must be tailored to their needs and capabilities. In recent years, new, simpler strategies have been put forward to give all potential candidates access to PR. This approach should help achieve greater adherence to rehabilitation programs and maintain long-term benefits, primarily by influencing patient lifestyles and encouraging physical activity.
En los años 70 la rehabilitación respiratoria (RR) se consideraba como «un arte» y, se centraba fundamentalmente en técnicas de fisioterapia respiratoria. En los últimos 40 años su importancia ha crecido de forma exponencial. Actualmente comporta una evidencia científica contundente, no solo en los beneficios alcanzados sino también en la eficacia de todos sus componentes.
La eficacia de la RR se ha constatado no únicamente en la enfermedad pulmonar obstructiva crónica (EPOC) sino también en otras enfermedades, como el asma bronquial, las bronquiectasias, la enfermedad intersticial, la hipertensión pulmonar, etc. La evidencia científica ha demostrado que la RR es más eficaz cuanto antes se inicie sin provocar efectos secundarios y, hemos comprendido que lo importante es buscar estrategias diseñadas de forma personalizada, que consigan mantener sus efectos a largo plazo, fundamentalmente incidiendo en los hábitos de vida y favoreciendo la actividad física.
La RR es una intervención que centra su eficacia en mejorar la disnea, la capacidad de esfuerzo y la calidad de vida relacionada con la salud (CVRS), con un alto nivel de evidencia en pacientes con enfermedad respiratoria crónica1–5 (1 A).
A pesar de la evidencia disponible, la RR está poco extendida, su implantación dista mucho de lo que debería ser, existiendo una gran variabilidad geográfica y, sobre todo, un importante grado de infrautilización6. La falta de conocimiento por parte de los profesionales de la salud, y la falta de expectativas o simplemente de motivación de los pacientes hace que únicamente entre un 12-15% de pacientes candidatos reciban RR7.
DefiniciónLa American Thoracic Society (ATS) y la European Respiratory Society (ERS) han definido la RR como: «una intervención integral basada en una minuciosa evaluación del paciente seguida de terapias diseñadas a medida, que incluyen, pero no se limitan, al entrenamiento muscular, la educación y los cambios en los hábitos de vida, con el fin de mejorar la condición física y psicológica de las personas con enfermedad respiratoria crónica y promover la adherencia a conductas para mejorar la salud a largo plazo»3. Recientemente un comité de expertos de la ATS se ha reafirmado en esta definición, sin embargo enfatiza en la necesidad de complementarla con una guía específica de los componentes, así como en establecer medidas específicas para valorar la calidad de los programas7.
De hecho, esta definición incluye conceptos nuevos contemplando no solo los pacientes con EPOC sino también a una amplia gama de enfermedades con manifestaciones respiratorias; además de resaltar la multidimensionalidad y de ampliar las estrategias. Sin embargo, en mi opinión, no tiene en cuenta las situaciones agudas que también precisan de soporte de RR, así como los pacientes propuestos para cirugía torácica.
Candidatos a rehabilitación respiratoriaLa RR debería ser asequible a todo paciente con enfermedad respiratoria crónica (EPOC y no EPOC) independientemente de la edad o el grado de enfermedad, siendo fundamental adaptar el programa a cada paciente de forma individualizada3,5,8.
En general, el síntoma que determina una indicación de RR es la disnea que no mejora a pesar de un tratamiento adecuado0,3,4,8. Se consideran, pues, candidatos todos los pacientes con disnea limitante de grado igual o superior a 2 según la escala modificada del Medical Research Council y, en concreto en los pacientes con EPOC si tienen un índice BODE ≥3 (1 A)2,5. La Guía de Práctica clínica para la EPOC de la American College of Physicians, American College of Chest Physicians1, y de la ATS/ERS3 recomiendan que se debiera indicar RR para aquellos pacientes sintomáticos con un flujo espiratorio forzado en el primer segundo (FEV1)<50% y considerarla para aquellos con FEV1 >50% pero sintomáticos o con limitación al esfuerzo. El deterioro del estado de salud, la disminución de la tolerancia al ejercicio, de la actividad física, de la fuerza muscular, de las actividades de la vida diaria e incremento en el consumo de fármacos, deben ser evaluados en pacientes con enfermedades respiratorias crónicas2,3.
La RR también está indicada en otras enfermedades crónicas distintas a la EPOC como pacientes con hipersecreción bronquial secundaria a fibrosis quística (FQ) o bronquiectasias (1B), pacientes con enfermedad neuromuscular y tos ineficaz (1C), con enfermedad pulmonar intersticial difusa (EPID) o con hipertensión pulmonar (HP)(1B)2,5,9.
La RR también se contemplará en enfermedades respiratorias agudas como el derrame pleural, la neumonía, la agudización de una enfermedad respiratoria crónica (EPOC o no EPOC) o en pacientes con enfermedades neuromusculares o de caja torácica que presenten síntomas respiratorios2,9. También está en indicada en pacientes en tratamiento de cirugía torácica (1C) tengan o no enfermedad respiratoria previa1–5,9.
Existen algunas situaciones especiales de acuerdo con las nuevas normativas3–5, tales como: pacientes con cáncer de pulmón no quirúrgico que han recibido tratamientos con quimioterapia y/o radioterapia, y en pacientes con síndrome de apnea-hipoapnea del sueño.
La edad no es una contraindicación. Los criterios de exclusión se centran en: trastornos psiquiátricos o de conducta que impidan la colaboración, patología cardiovascular en fase aguda inestable o que limite la realización de ejercicio; enfermedades del aparato locomotor incompatibles con el entrenamiento muscular o que ponga al paciente en situación de riesgo durante la RR y, en cualquier condición que interfiera con el proceso de rehabilitación. En estos pacientes, sin embargo, no debe despreciarse la posibilidad de realizar un tratamiento con fisioterapia respiratoria3,5. La coexistencia de otras enfermedades no es un criterio de exclusión para RR, siempre que estas estén debidamente tratadas y se adapte el programa a las posibilidades del paciente.
Características de los programas de rehabilitación respiratoriaLos programas de RR deben incluir fundamentalmente el entrenamiento muscular asociando el entrenamiento de extremidades superiores e inferiores, combinando el entrenamiento de fuerza con el de resistencia (1 A), la educación (centrada en el conocimiento de la enfermedad y su tratamiento) (1 B) y la fisioterapia respiratoria (1 B), siendo aconsejable también contemplar la terapia ocupacional (2 D), el soporte psicosocial (2C) y la intervención nutricional (2C). El entrenamiento específico de los músculos respiratorios debería añadirse a un entrenamiento general únicamente cuando los pacientes presentan debilidad muscular respiratoria1–5 (tabla 1).
Componentes de los programas de RR y sus técnicas
| Educación |
| Incluye 3-4 sesiones en grupo, contemplando el conocimiento (evidencia D):• Del sistema respiratorio• De la enfermedad• Del tratamiento (incluyendo tratamiento broncodilatador, oxigenoterapia, CPAP y ventilación mecánica, si están indicados)• De los síntomas de alarma.• De las técnicas de ahorro de energía en pacientes con enfermedades con disnea limitante |
| Fisioterapia respiratoria |
| (Evidencia A, B, dependiendo de las enfermedades):• Técnicas de reeducación respiratoria• Técnicas de drenaje de secreciones• Técnicas de relajación |
| Soporte psicosocial |
| (Evidencia B):• Consejo y apoyo por el equipo de RR• Evaluación por si fuera necesario el tratamiento por psicólogo/psiquiatra |
| Entrenamiento muscular general |
| (Evidencia A)1. Entrenamiento de piernas con cicloergómetro2. Entrenamiento de brazos con pesas |
| Entrenamiento de músculos respiratorios |
| (Evidencia B)En pacientes con disminución de las presiones respiratorias máximas (PImáx/PEmáx).Es necesario enseñar la técnica antes de prescribirlo para el domicilio |
A: nivel de evidencia alto; B: nivel de evidencia moderado; C: nivel de evidencia bajo; CPAP: presión continua positiva en vías respiratorias; D: nivel de evidencia basado en opinión de expertos; PEmáx: presión espiratoria máxima; PImáx: presión inspiratoria máxima; RR: rehabilitación respiratoria.
Los programas de RR deben ser supervisados (1 A), por simples y autónomos que sean. Generalmente se llevan a cabo en el medio hospitalario, ya sea en el paciente hospitalizado o en régimen ambulatorio, aunque se pueden alcanzar beneficios similares cuando se realizan en el domicilio3–5. Ambas alternativas han demostrado una mejoría en los síntomas, CVRS y capacidad de esfuerzo (1A)3,4,8,10. Se deben considerar diversos factores cuando se elige la ubicación de la RR, tales como las características del sistema sanitario de cada país, la disponibilidad de programas hospitalarios o domiciliarios, la gravedad de la enfermedad, las barreras, etc. Las nuevas tecnologías tienen un importante papel en mejorar los servicios con la telemonitorización al proporcionar RR remota en regiones inaccesibles. Esta tecnología va desde el uso de podómetros a tecnología de teléfonos móviles o de programas de ordenador para una supervisión a distancia. Pero aún existe evidencia limitada de su uso en RR11.
La duración óptima de los programas de RR no está clara, existiendo una gran diferencia entre los países3,4,6. El consenso de la ATS/ERS3 llama la atención sobre la falta de evidencia en cuánto debe durar un programa de RR y sugiere que el mantenimiento de los beneficios a lo largo del tiempo tiene una relación directa con la duración del programa. Este consenso recomienda un mínimo de 20 sesiones de entrenamiento, o bien de 8 a 12 semanas de programa2,3 tal como demostraron Solanes et at.12.
El número de sesiones semanales de los programas también varía, generalmente es de 2 a 5 días a la semana. La duración de cada sesión suele ser de 1-4 h1–5.
En la revisión de Holland et al.7, se especifica de forma muy gráfica cuáles son los componentes deseables de un programa de RR a partir de una buena evaluación del paciente, así como la forma de administración del tratamiento y la valoración de la calidad tanto del programa como de los conocimientos de los profesionales.
La terapia suplementaria con oxígeno durante el entrenamiento al ejercicio debe ser considerada en 2 situaciones: los pacientes que presentan hipoxemia en reposo, portadores de oxigenoterapia y los que presentan una saturación de la oxihemoglobina (SpO2)<90% al esfuerzo.
El uso de la ventilación mecánica no invasiva (VMNI) en la RR es controvertido. En una revisión sistemática13 que evalúa los efectos de la VMNI en pacientes con EPOC se concluye que administrada como adyuvante (nocturna o durante la RR) aumenta los beneficios del ejercicio, probablemente porque permite incrementar el nivel de trabajo realizado en los pacientes con EPOC grave3,4. Sin embargo, la recomendación, hasta el momento, es que no debe prescribirse la VMNI solo para realizar la RR (Grado D).
¿En qué momento se debe iniciar la rehabilitación respiratoria?Tradicionalmente la mayoría de los programas de RR en pacientes con una enfermedad respiratoria crónica se inician cuando ya existen síntomas limitantes. Clásicamente se planteaba el inicio de la RR al menos un mes tras una agudización. Actualmente existe evidencia del papel de la RR durante e inmediatamente tras la hospitalización. Una revisión de la Cochrane14, que incluye programas realizados durante el ingreso o en el margen de hasta 4 semanas postalta, pone de manifiesto que la RR iniciada de forma precoz es factible, segura y efectiva conllevando mejoras en la tolerancia al esfuerzo, síntomas y CVRS, además de reducir el uso de recursos sanitarios, reingresos y mortalidad, sin provocar efectos secundarios. Un estudio reciente15 que compara el inicio de la RR durante el ingreso vs. al mes del alta en pacientes con EPOC grave demuestra una mayor mejoría cuando se inicia al mes, una vez alcanzada la estabilidad, lo que coincide con la recomendación de la guía de la ERS/ATS16.
Una situación especial es la de los pacientes ingresados en unidades de cuidados intensivos (UCI) dada la asociación a una peor supervivencia secundaria al decondicionamiento general, a un empeoramiento funcional y a una CVRS reducida. Esto indica la necesidad de la RR precoz durante el ingreso, centrada fundamentalmente en una movilización temprana, realizada por el equipo de fisioterapeutas de la UCI. Algunas modalidades de tratamiento como el «cycling» pasivo, movilización de articulaciones, estiramiento muscular y estimulación eléctrica neuromuscular no interfieren ni en la sedación ni en otros tratamientos y han demostrado reducir la estancia en UCI y la hospitalaria, además de mejorar el tiempo libre de ventilación mecánica, la fuerza y masa muscular y estado funcional al alta3. En una proporción de pacientes que tienen un destete de la ventilación mecánica dificultoso, existe evidencia que está asociada con el fracaso de los músculos respiratorios, por lo que, el entrenamiento de los músculos inspiratorios y la fisioterapia respiratoria pueden ser beneficiosos en esta situación3.
En los últimos años hay evidencia de que pacientes con enfermedad más leve o en fases iniciales que presentan una ligera o moderada alteración ventilatoria (obstructiva o restrictiva) pueden tener también una baja actividad física, problemas en la realización de las actividades de la vida diaria, hiperinsuflación dinámica con el ejercicio, limitación de extremidades inferiores, osteoporosis, ansiedad y depresión3,4,8. La RR en estas fases de la enfermedad tiene el potencial de alterar de forma significativa el curso de la enfermedad y, sobre todo la CVRS3, al promover un cambio de conductas y de hábitos de vida y estimular la actividad física.
Resultados de la rehabilitación respiratoria en distintas enfermedadesLos síntomas respiratorios tales como la disnea o la alteración en la capacidad de esfuerzo y en la CVRS se presentan en casi todas las enfermedades respiratorias crónicas, no solo en la EPOC. La función de la musculatura esquelética se deteriora en la EPID, en la FQ, el asma bronquial, el síndrome de apnea-hipopnea del sueño, el cáncer de pulmón o la HP entre otras (tabla 2).
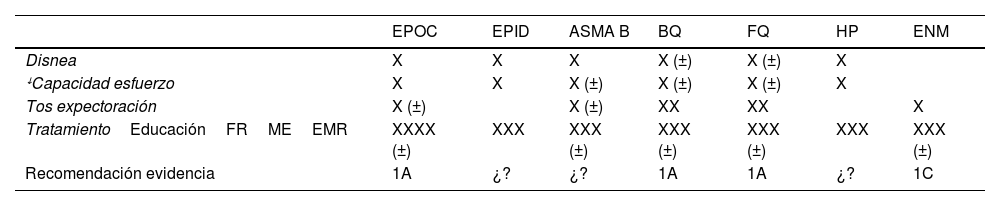
Tratamiento según síntomas y niveles de evidencia según cada enfermedad
| EPOC | EPID | ASMA B | BQ | FQ | HP | ENM | |
|---|---|---|---|---|---|---|---|
| Disnea | X | X | X | X (±) | X (±) | X | |
| ꜜCapacidad esfuerzo | X | X | X (±) | X (±) | X (±) | X | |
| Tos expectoración | X (±) | X (±) | XX | XX | X | ||
| TratamientoEducaciónFRMEEMR | XXXX (±) | XXX | XXX (±) | XXX (±) | XXX (±) | XXX | XXX (±) |
| Recomendación evidencia | 1A | ¿? | ¿? | 1A | 1A | ¿? | 1C |
A: nivel de evidencia alto; BQ: bronquiectasias; BR: bronquial; C: nivel de evidencia bajo; EM: entrenamiento muscular; EMN: enfermedad neuromuscular; EMR: entrenamiento de músculos respiratorios; EPID enfermedad pulmonar intersticial difusa; EPOC: enfermedad pulmonar obstructiva crónica; FQ: fibrosis quística; FR: fisioterapia respiratoria; HP: hipertensión arterial pulmonar; X (±): no en todos los pacientes; 1: nivel de recomendación fuerte; 2: nivel de recomendación débil.
Todas ellas se pueden beneficiar de la RR3. No existen programas específicos para cada enfermedad, por lo que se aconseja adecuar en cada grupo de patología los programas establecidos para los pacientes con EPOC, según los síntomas a tratar. Sin embargo, los resultados evidenciados en enfermedades distintas de la EPOC son muy escasos y poco concluyentes1,3,4,9.
La RR ha demostrado que consigue disminuir la disnea, mejorar la CVRS e incrementar la capacidad de esfuerzo en los pacientes con EPOC (1A)1,3–5. Los componentes más eficaces de la RR son el entrenamiento muscular de extremidades inferiores y superiores (1A), mientras que la educación, la fisioterapia respiratoria y el entrenamiento específico y aislado de los músculos respiratorios tiene un nivel de recomendación alto aunque con una evidencia moderada (1B)1,3. En concreto el entrenamiento de los músculos respiratorios estaría claramente indicado en aquellos pacientes con disminución de la presión inspiratoria máxima (PImáx) y/o de la presión espiratoria máxima (PEmáx). La ayuda psicosocial tiene un papel discutido en los programas de RR. Los resultados son controvertidos, algunos sugieren que la RR en sí misma reduce estos síntomas17–24, mientras otros no encuentran beneficios23. El soporte nutricional hasta el momento actual ha demostrado escasa eficacia dentro de los programas de RR3–5(2C). No hay estudios que directamente evalúen el impacto de la RR sobre la supervivencia, sin embargo, uno reciente de Camillo et al.25, demuestra que los pacientes que incrementan la distancia recorrida en la prueba de 6 min de marcha tras un programa de RR en menos de 30 metros tienen una menor supervivencia. La RR ha demostrado que reduce el número de días de hospitalización y el uso de los servicios sanitarios en los pacientes con EPOC (2B), y, por lo tanto, es una intervención potencialmente coste-efectiva (2C)1,3–5.
La actividad física regular se ha demostrado que reduce el riesgo de presentar una exacerbación asmática3. Estudios recientes sugieren que el entrenamiento también tiene beneficios psicológicos y de los síntomas26,27.
La fisioterapia respiratoria es el componente más importante tanto en la FQ como en las bronquiectasias, específicamente las técnicas de drenaje de secreciones ya sean manuales o instrumentales (1 A). Niveles elevados de actividad física se han asociado a una mejor supervivencia en la FQ. Una revisión de la Cochrane28 muestra mejoría de la capacidad de ejercicio, fuerza muscular y CVRS después de un programa de RR.
En los últimos años se ha demostrado que la RR y, en concreto las técnicas de entrenamiento muscular, con un adecuado soporte de oxigenoterapia, se obtiene mejoría en los síntomas, la tolerancia al esfuerzo y en la CVRS en los pacientes con EPID9,29.
Existen algunos estudios recientes que sugieren que la RR puede mejorar la capacidad de ejercicio y CVRS en pacientes con HP grave sin efectos adversos tras realizar entrenamiento tipo aeróbico30,31.
El control de las secreciones respiratorias, junto con la prevención de las aspiraciones alimentarias y el mantenimiento de una adecuada ventilación alveolar, es fundamental para el manejo de los problemas respiratorios de las enfermedades neuromusculares (1C) y constituye el núcleo fundamental de la RR en estas entidades5.
En los pacientes con alteración de la caja torácica es importante realizar programas de fisioterapia respiratoria que incluyan fundamentalmente reeducación respiratoria. El entrenamiento muscular ha sido poco explorado en estas enfermedades, aunque parecería lógico pensar que es útil considerando que la limitación al esfuerzo en estos pacientes tiene un origen similar a la de los pacientes con EPOC5.
Aunque es controvertida la prescripción de RR en pacientes con síndrome de apnea-hipopnea del sueño, existen estudios controlados y aleatorizados con pequeño número de participantes que muestran con un entrenamiento aeróbico de intensidad moderada, una reducción del índice de apnea-hipopnea del sueño y mejoran objetivamente y subjetivamente la calidad del sueño, los síntomas depresivos y la somnolencia, entre otros beneficios (2C)5.
El problema más importante es cómo mantener los resultados de la RR a largo plazo. Hay diversos factores que favorecen la pérdida progresiva de los beneficios, tales como la evolución de la enfermedad, la existencia de comorbilidades, la intensidad, duración y ubicación de los programas y sobre todo la aplicación o no de técnicas de mantenimiento32–34. Se han ensayado diversas técnicas para mantener los beneficios tras un programa de RR: autogestión35 (2C); programas basados en la asistencia extrahospitalaria, bien comunitaria o domiciliaria supervisados3,36,37, y repetición de los programas periódicamente38. Sin embargo, ninguna de las estrategias han demostrado ser eficaces a largo plazo, dado el número importante de abandonos y siendo de difícil aplicación en la práctica clínica. Es posible que el fomentar la actividad física supervisada39–42 o la aplicación de técnicas de telemedicina43,44, consigan una mayor adherencia a los programas, aunque hasta el momento los resultados son escasos.
¿Hacia dónde se encamina la rehabilitación respiratoria?A pesar de que la RR ha demostrado eficacia y seguridad en muchas enfermedades respiratorias, siempre que se adapten sus programas a cada paciente, parece evidente que las estrategias convencionales tienen que cambiar en los próximos años. Un reciente documento de la ATS7 pone de manifiesto los posibles modelos de programas y métodos de implementación a fin de optimizar la motivación, acceso y, sobre todo, la continuidad del tratamiento.
Algunas de estas estrategias ya han evidenciado su eficacia tales como la actividad física estructurada o la marcha nórdica39–42, pero otras como el aquagym, taichi, baile, yoga, juegos, videos, e-health…no existe, de momento, suficiente evidencia científica45.
También hay que buscar ubicaciones que faciliten el desplazamiento de los pacientes, tales como programas comunitarios o domiciliarios que ya han demostrado eficacia, sin embargo, técnicas tan prometedoras como la telerrehabilitación, el uso de móviles y otras de momento carecen de suficiente robustez en sus resultados43,44.
La pandemia del COVID 19 nos ha obligado a pensar en nuevas estrategias fundamentalmente para el tratamiento de las secuelas. Las más remarcables serían: la necesidad de un equipo multidisciplinar y la posibilidad de buscar nuevas estrategias de tratamiento global (respiratorio, osteomuscular, cardiaco, neurológico…) así como un inicio precoz, una evaluación de necesidades como oxígeno, ortesis, ayudas para la marcha, etc., y posiblemente una ubicación más sencilla, segura y asequible para los pacientes y familiares46,47.
Un punto clave es que cualquier programa de RR precisa de una evaluación muy cuidadosa y de una prescripción personalizada realizada por el equipo de rehabilitación (médico neumólogo/rehabilitador y fisioterapeuta).
AddendumLos grados de recomendación y la fortaleza de la evidencia se basan en el sistema GRADE propuesto por Guyatt et al.48. La recomendación está definida en dos niveles: fuerte (grado 1) o débil (grado 2). La fortaleza de la evidencia se clasifica en tres niveles: alta (grado A); moderada (grado B) y baja (grado C). En algunos puntos, señalados como nivel de evidencia D, esta se basa a casos clínicos u opinión de expertos, según la guía de la BTS4.
Conflicto de interesesLa autora declara no tener ningún conflicto de intereses.