El análisis modal de fallos y efectos (AMFE) se ha utilizado como una herramienta en la gestión de los riesgos y la planificación de la calidad. El objetivo de este estudio es identificar de forma sistemática todas las debilidades en los procesos de la Unidad de Ensayos Clínicos de un Servicio de Farmacia Hospitalaria (SFH) con gran actividad investigadora, con el fin de mejorar su seguridad de los procedimientos habituales.
MétodosSe creó un equipo de trabajo multidisciplinar para analizar cada uno de los puntos críticos, identificados como posibles oportunidades de fallo, del desarrollo de los ensayos clínicos en el SFH. Para cada modo de fallo se identificó la posible causa y efecto, se calculó la criticidad mediante el número de prioridad de riesgo y se discutieron las posibles acciones correctoras.
ResultadosSe definieron 6subprocesos en la actividad de los ensayos clínicos en el SFH. El AMFE determinó 67 posibles fallos, siendo el subproceso de dispensación y prescripción/validación los más susceptible de generar errores. Todas las acciones de mejora establecidas en el AMFE fueron implementadas en la Unidad de Ensayos Clínicos.
DiscusiónEl AMFE se trata de una herramienta útil en la gestión proactiva de los riesgos ya que nos permite identificar dónde estamos cometiendo errores y analizar las causas que los originan, para priorizar y adoptar soluciones definitivas a la reducción de riesgos. Todo ello trae consigo la mejora en la seguridad de los procesos y en la calidad del SFH.
The failure mode and effects analysis (FMEA) has been used as a tool in risk management and quality improvement. The objective of this study is to identify the weaknesses in processes in the clinical trials area, of a Pharmacy Department (PD) with great research activity, in order to improve the safety of the usual procedures.
MethodsA multidisciplinary team was created to analyse each of the critical points, identified as possible failure modes, in the development of clinical trial in the PD. For each failure mode, the possible cause and effect were identified, criticality was calculated using the risk priority number and the possible corrective actions were discussed.
ResultsSix sub-processes were defined in the development of the clinical trials in PD. The FMEA identified 67 failure modes, being the dispensing and prescription/validation sub-processes the most likely to generate errors. All the improvement actions established in the AMFE were implemented in the Clinical Trials area.
DiscussionThe FMEA is a useful tool in proactive risk management because it allows us to identify where we are making mistakes and analyze the causes that originate them, to prioritize and to adopt solutions to risk reduction. The FMEA improves process safety and quality in PD.
El análisis modal de fallos y efectos (AMFE) es un método sistemático de investigación de las debilidades potenciales de procesos, así como una técnica para cuantificar y evaluar el riesgo de fallo en los ya existentes1. Aunque la técnica se aplica fundamentalmente para analizar un producto o proceso en una fase de diseño, es un método válido para cualquier proceso, entendiendo que estos se encuentran en todos los ámbitos de la empresa2,3. Un análisis AMFE refleja cómo estamos trabajando en un momento dado y en una Unidad en concreto. El principal interés del AMFE es el de resaltar los puntos críticos con el fin de eliminarlos o establecer medidas correctoras para evitar su aparición o minimizar sus consecuencias, con lo que se puede convertir en un riguroso procedimiento de detección de defectos potenciales, si se aplica de manera sistemática4-6. Además, el análisis AMFE tiene la ventaja de que permite cuantificar el riesgo de fallo de los procesos, aunque la incidencia de estos sea tan baja como para no ser detectada en un estudio de observación7.
El método AMFE es la herramienta más utilizada para la gestión de los riesgos y la planificación de la calidad. En el ámbito hospitalario, este método debe aplicarse en las situaciones previas a la implantación de un nuevo proceso y en el rediseño de procesos, en que las condiciones de funcionamiento de un área van a sufrir un cambio. Tanto la Norma ISO 9001:2015, como la Joint Commission on Accreditation of Healthcare Organizations consideran la metodología AMFE como método de elección para identificar los fallos dentro de un proceso y lo recomiendan para obtener la seguridad de los procesos sanitarios8,9.
La preocupación creciente en los sistemas de salud, por la gran incidencia de errores de medicación, ha promovido la aparición de una cultura de seguridad basada en una dinámica de mejora continuada de la calidad en los procesos asistenciales10. Las organizaciones con mayor grado de eficacia son aquellas que se centran en la prevención de errores y en la búsqueda de enfoques innovadores que mejoren la calidad11.
Un ensayo clínico con medicamento es toda investigación efectuada en seres humanos con el fin de determinar la eficacia y la seguridad de uno o varios medicamentos en investigación12. Cualquier centro de investigación u hospital que desarrolle ensayos clínicos con medicamentos necesita contar con la colaboración del Servicio de Farmacia Hospitalaria (SFH) para el control de la medicación del ensayo13,14. Los SFH deben disponer de Unidades de Investigación, ya que desempeñan un papel importante en el desarrollo del ensayo clínico y en los procedimientos de recepción, custodia, preparación y dispensación de las muestras para investigación (MPI) de los ensayos clínicos, cumpliendo con la normativa legal vigente y las normas de buena práctica15.
El aumento del número de ensayos clínicos con medicamentos en los SFH, los estrictos protocolos de trabajo que conllevan, el complejo circuito de las MPI desde su recepción hasta su dispensación, las especificaciones de preparación de la medicación para cada ensayo clínico, la coordinación de todos los profesionales sanitarios, hacen que el SFH, por tratarse de un área especialmente vulnerable a los errores de medicación, instaure medidas de calidad necesarias en los procedimientos que garanticen la ejecución adecuada de los ensayos clínicos con medicamentos16.
El objetivo del estudio fue analizar de forma sistemática todas las debilidades de los procedimientos habituales de una Unidad de Ensayos Clínicos de un SFH con el fin de identificar acciones de mejora que permitan mejorar la seguridad en todos los procesos.
Material y métodosSe realizó un estudio descriptivo de cada uno de los puntos críticos de los procesos implicados en la gestión de los ensayos clínicos, identificados como posibles oportunidades de fallo, en el SFH de un hospital de tercer nivel con gran actividad investigadora (436 ensayos clínicos activos en el año 2016).
En primer lugar, se creó un equipo de trabajo multidisciplinar en el que se incluyó a profesionales con experiencia en la investigación clínica y el conocimiento de los procedimientos de trabajo de la Unidad de Ensayos Clínicos. Se compuso de 4farmacéuticos especialistas en farmacia hospitalaria, un investigador clínico asociado, un coordinador del Servicio de Oncología, una enfermera del SFH con experiencia en la preparación de MPI citostáticas y una auxiliar del SFH con experiencia en la dispensación de MPI.
A continuación, se diseñó un diagrama de flujo de todos los procesos y se describieron todos los componentes de la Unidad de Ensayos Clínicos del SFH. El equipo de trabajo llevó a cabo una tormenta de ideas para identificar los posibles modos de fallo de cada proceso17.
Una vez seleccionados los potenciales modos de fallos, se identificaron las posibles causas que los originaban y los efectos derivados de cada modo de fallo. A su vez, se analizó la criticidad de cada modo de fallo mediante el índice de criticidad, también conocido como número de prioridad de riesgo (NPR)18. Para el cálculo del NPR, se consideraron 3variables: la ocurrencia (O), la detectabilidad (D) y la gravedad (G)3. El NPR se obtuvo multiplicando los valores asignados a cada una de estas 3variables para cada punto crítico identificado, según la ecuación: NPR = O×D×S. La tabla 1 muestra los valores correspondientes a la frecuencia asignada para cada una de las variables.
Índices para el cálculo de la criticidad. Valoración en función del criterio
| Probabilidad de ocurrencia (O) del modo de fallo | ||
| Frecuencia | Criterio | Valor |
| Muy baja | Ningún fallo se asocia a procesos casi idénticos, ni se ha dado nunca en el pasado, pero es concebible | 1 |
| Baja | Fallos aislados en procesos similares o casi idénticos. Es poco probable que suceda | 2-3 |
| Moderada | Defecto aparecido ocasionalmente en procesos similares o previos al actual. Probablemente aparecerá algunas veces | 4-5 |
| Alta | El fallo se ha presentado con cierta frecuencia en el pasado en procesos similares o previos | 6-8 |
| Muy alta | Fallo casi inevitable. Es seguro que el fallo se producirá frecuentemente | 9-10 |
| Probabilidad de la facilidad de detección (D) del modo de fallo | ||
| Detectabilidad | Criterio | Valor |
| Muy alta | El defecto es obvio. Resulta muy improbable que no sea detectado por los controles existentes | 1 |
| Alta | El defecto, aunque es obvio y fácilmente detectable, podría en alguna ocasión escapar a un primer control, aunque sería detectado con toda seguridad a posteriori | 2-3 |
| Mediana | El defecto es detectable y posiblemente no llegue al cliente | 4-5 |
| Pequeña | El defecto es de tal naturaleza que resulta difícil detectarlo con los procedimientos establecidos hasta el momento | 6-8 |
| Improbable | El defecto no puede detectarse. Casi seguro que lo percibirá el cliente final | 9-10 |
| Probabilidad de la gravedad (G) del modo de fallo | ||
| Gravedad | Criterio | Valor |
| Muy baja | Repercusiones imperceptibles. Probablemente, el cliente ni se daría cuenta del fallo | 1 |
| Baja | Repercusiones irrelevantes apenas perceptibles. Probablemente, el tipo de fallo originaria un ligero inconveniente al cliente | 2-3 |
| Moderada | El fallo produce cierto disgusto e insatisfacción en el cliente | 4-5 |
| Alta | El fallo puede ser crítico y producir un grado de insatisfacción elevado | 6-8 |
| Muy alta | El fallo muy crítico afecta al funcionamiento de seguridad del proceso o involucra seriamente el incumplimiento de normas reglamentarias | 9-10 |
Para cada modo de fallo, el equipo de trabajo discutió las posibles acciones correctoras con base en la criticidad del modo de fallo, la viabilidad y el tiempo estimado para establecer la mejora y el coste.
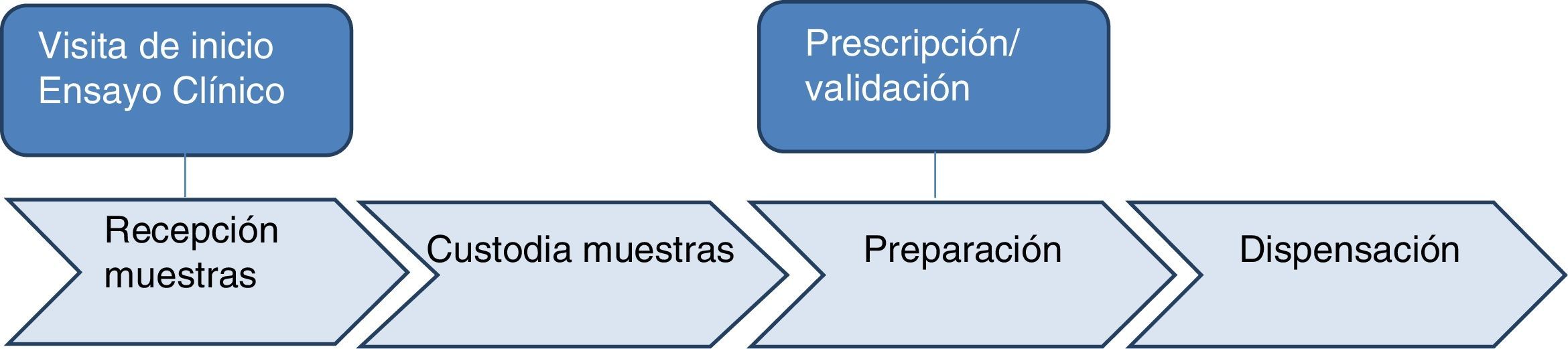
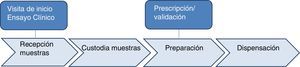
ResultadosEl equipo de trabajo definió 6 subprocesos en la actividad de la Unidad de Investigación del SFH según se detalla en la figura 1: visita de inicio del ensayo clínico, recepción de las muestras, custodia de las muestras, prescripción/validación, preparación y dispensación.
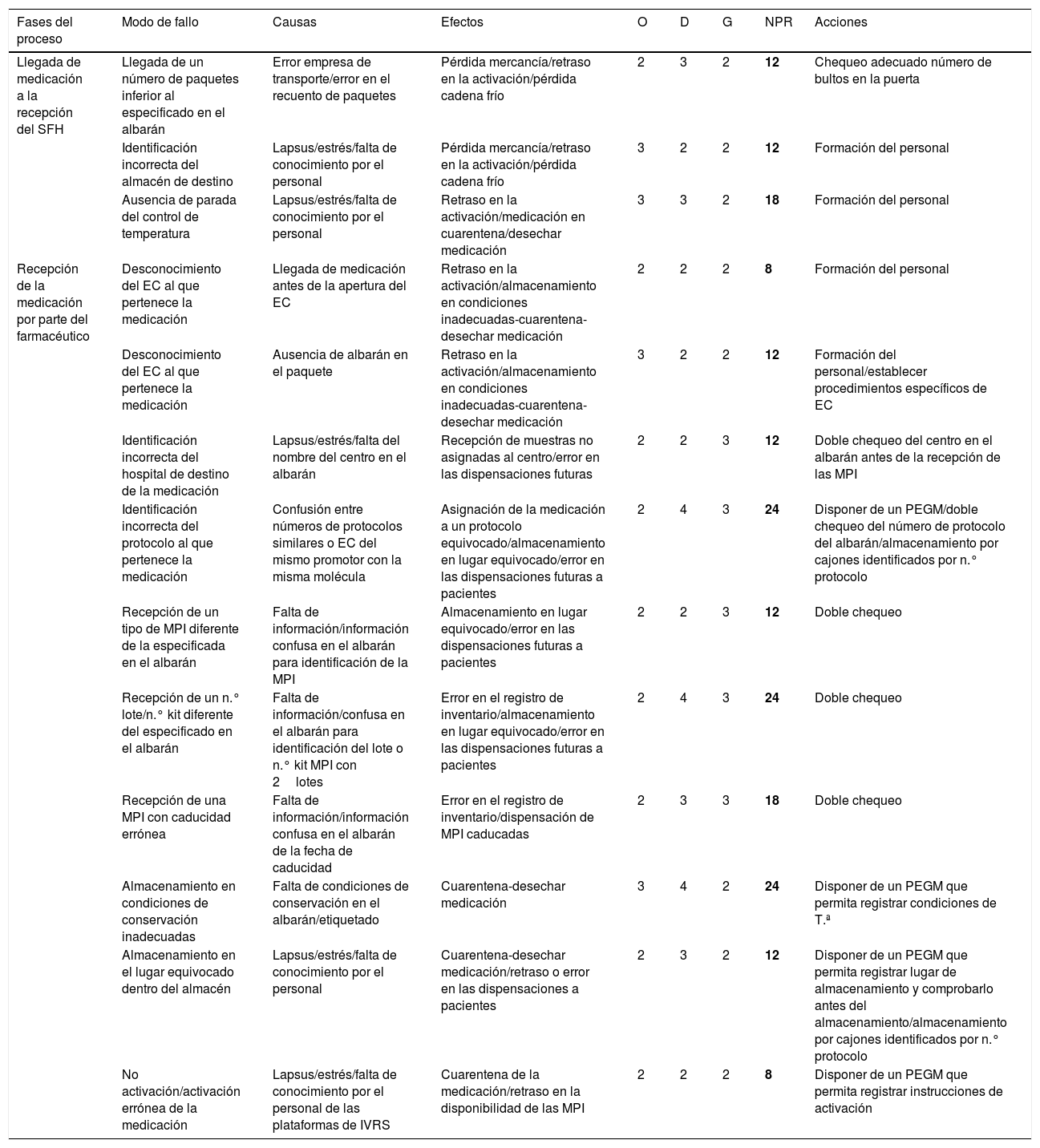
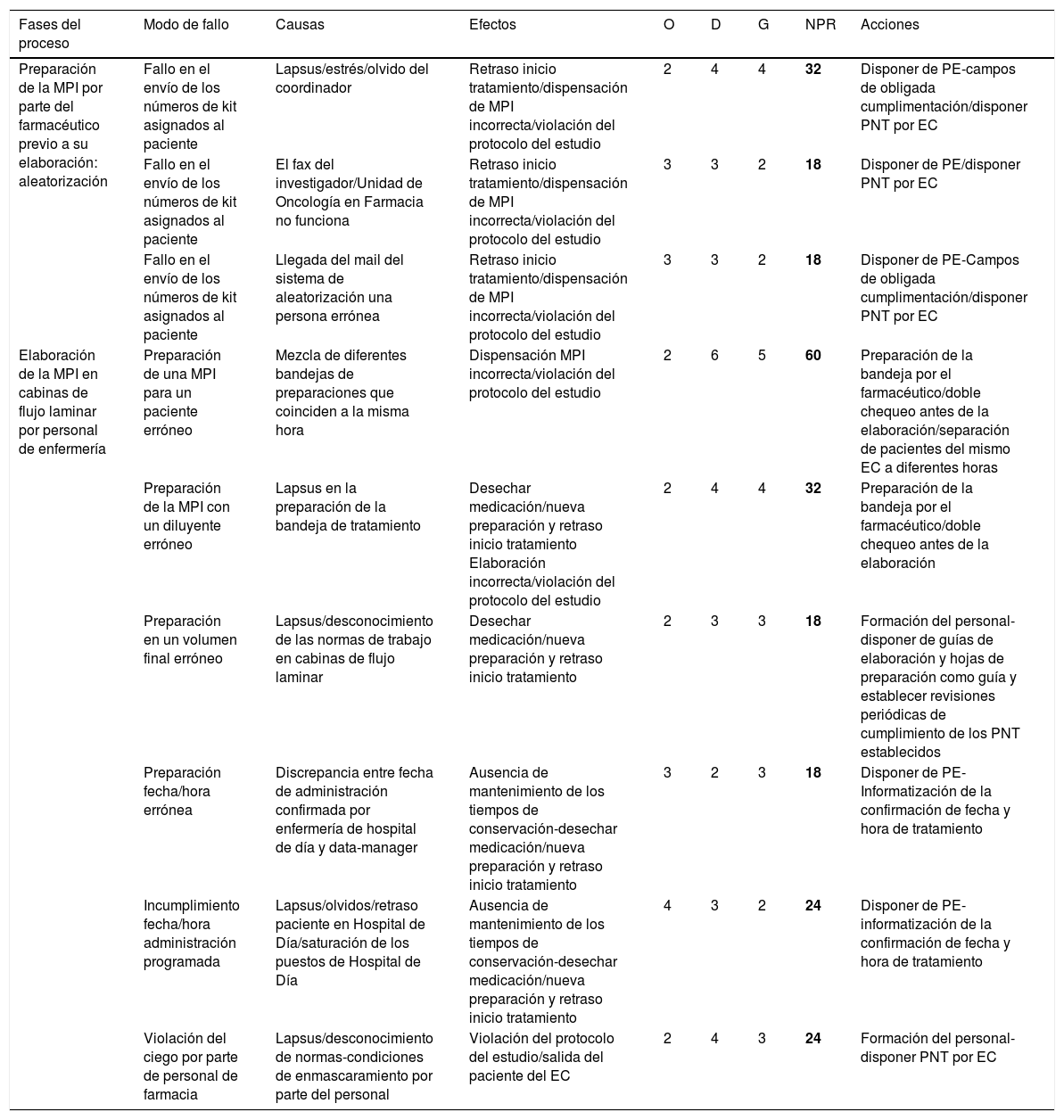
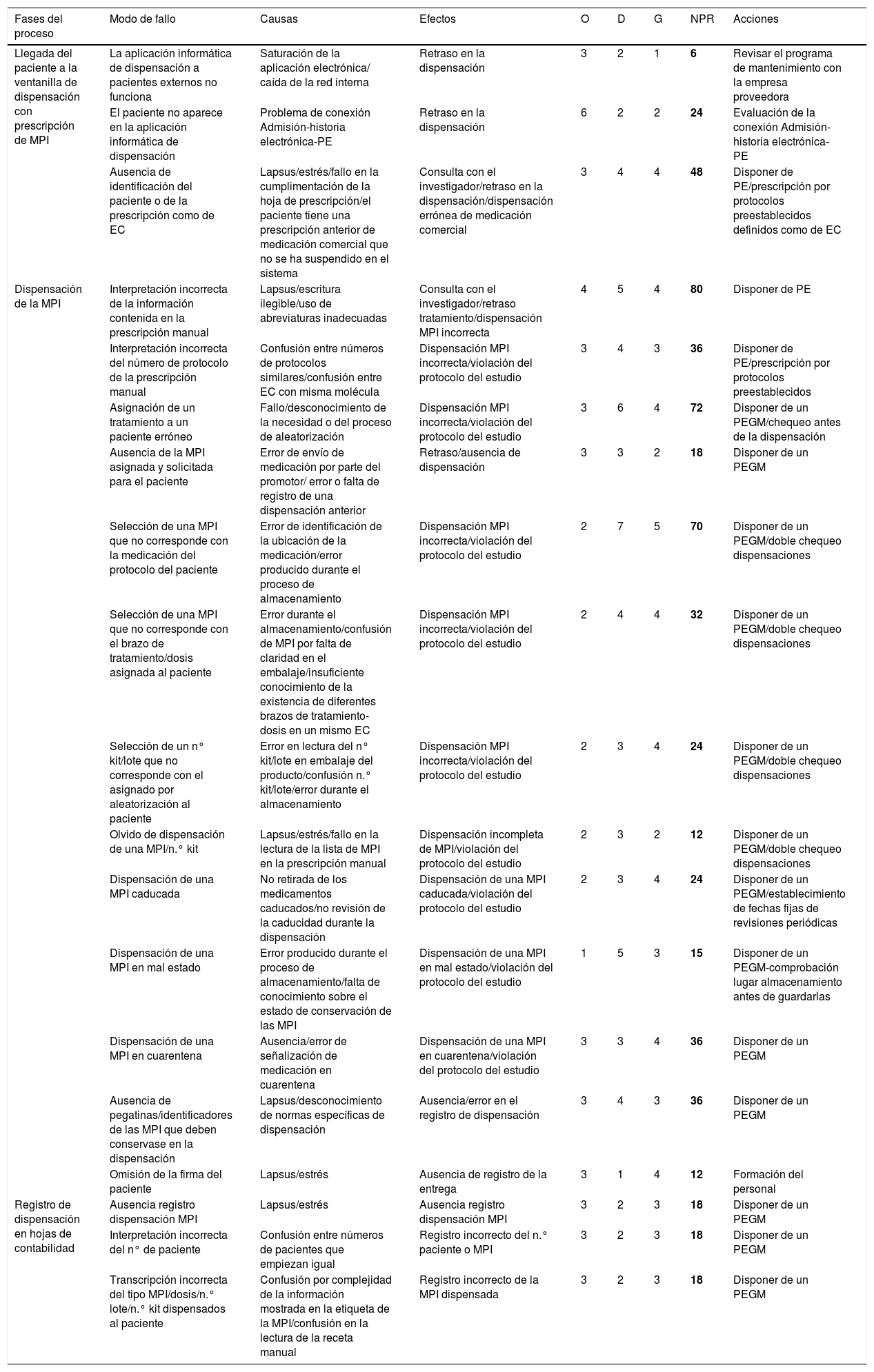
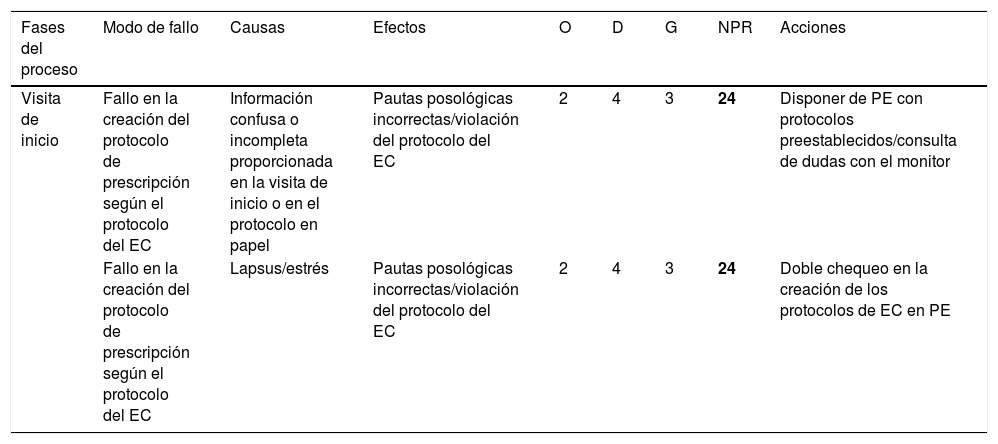
En las tablas 2-7 se identifican los posibles modos de fallo detectados para cada subproceso, las causas que los originaban, los efectos derivados de los mismos y la puntuación asignada por el equipo de trabajo en las variables de O, D y G, así como el NPR calculado. Asimismo, se especifican las acciones de mejora identificadas como resultado de este análisis.
Análisis modal de fallos y efectos en la Unidad de Ensayos Clínicos. Proceso de recepción de muestras
| Fases del proceso | Modo de fallo | Causas | Efectos | O | D | G | NPR | Acciones |
|---|---|---|---|---|---|---|---|---|
| Llegada de medicación a la recepción del SFH | Llegada de un número de paquetes inferior al especificado en el albarán | Error empresa de transporte/error en el recuento de paquetes | Pérdida mercancía/retraso en la activación/pérdida cadena frío | 2 | 3 | 2 | 12 | Chequeo adecuado número de bultos en la puerta |
| Identificación incorrecta del almacén de destino | Lapsus/estrés/falta de conocimiento por el personal | Pérdida mercancía/retraso en la activación/pérdida cadena frío | 3 | 2 | 2 | 12 | Formación del personal | |
| Ausencia de parada del control de temperatura | Lapsus/estrés/falta de conocimiento por el personal | Retraso en la activación/medicación en cuarentena/desechar medicación | 3 | 3 | 2 | 18 | Formación del personal | |
| Recepción de la medicación por parte del farmacéutico | Desconocimiento del EC al que pertenece la medicación | Llegada de medicación antes de la apertura del EC | Retraso en la activación/almacenamiento en condiciones inadecuadas-cuarentena-desechar medicación | 2 | 2 | 2 | 8 | Formación del personal |
| Desconocimiento del EC al que pertenece la medicación | Ausencia de albarán en el paquete | Retraso en la activación/almacenamiento en condiciones inadecuadas-cuarentena-desechar medicación | 3 | 2 | 2 | 12 | Formación del personal/establecer procedimientos específicos de EC | |
| Identificación incorrecta del hospital de destino de la medicación | Lapsus/estrés/falta del nombre del centro en el albarán | Recepción de muestras no asignadas al centro/error en las dispensaciones futuras | 2 | 2 | 3 | 12 | Doble chequeo del centro en el albarán antes de la recepción de las MPI | |
| Identificación incorrecta del protocolo al que pertenece la medicación | Confusión entre números de protocolos similares o EC del mismo promotor con la misma molécula | Asignación de la medicación a un protocolo equivocado/almacenamiento en lugar equivocado/error en las dispensaciones futuras a pacientes | 2 | 4 | 3 | 24 | Disponer de un PEGM/doble chequeo del número de protocolo del albarán/almacenamiento por cajones identificados por n.° protocolo | |
| Recepción de un tipo de MPI diferente de la especificada en el albarán | Falta de información/información confusa en el albarán para identificación de la MPI | Almacenamiento en lugar equivocado/error en las dispensaciones futuras a pacientes | 2 | 2 | 3 | 12 | Doble chequeo | |
| Recepción de un n.° lote/n.° kit diferente del especificado en el albarán | Falta de información/confusa en el albarán para identificación del lote o n.° kit MPI con 2lotes | Error en el registro de inventario/almacenamiento en lugar equivocado/error en las dispensaciones futuras a pacientes | 2 | 4 | 3 | 24 | Doble chequeo | |
| Recepción de una MPI con caducidad errónea | Falta de información/información confusa en el albarán de la fecha de caducidad | Error en el registro de inventario/dispensación de MPI caducadas | 2 | 3 | 3 | 18 | Doble chequeo | |
| Almacenamiento en condiciones de conservación inadecuadas | Falta de condiciones de conservación en el albarán/etiquetado | Cuarentena-desechar medicación | 3 | 4 | 2 | 24 | Disponer de un PEGM que permita registrar condiciones de T.ª | |
| Almacenamiento en el lugar equivocado dentro del almacén | Lapsus/estrés/falta de conocimiento por el personal | Cuarentena-desechar medicación/retraso o error en las dispensaciones a pacientes | 2 | 3 | 2 | 12 | Disponer de un PEGM que permita registrar lugar de almacenamiento y comprobarlo antes del almacenamiento/almacenamiento por cajones identificados por n.° protocolo | |
| No activación/activación errónea de la medicación | Lapsus/estrés/falta de conocimiento por el personal de las plataformas de IVRS | Cuarentena de la medicación/retraso en la disponibilidad de las MPI | 2 | 2 | 2 | 8 | Disponer de un PEGM que permita registrar instrucciones de activación |
D: detectabilidad; EC: ensayo clínico; G: gravedad; MPI: muestra para investigación clínica, n.∘: número; NPR: número de prioridad de riesgo; O: ocurrencia; PE: prescripción electrónica; PEGM: programa electrónico de gestión muestra; PNT: procedimientos normalizados de trabajo; SFH: Servicio de Farmacia Hospitalaria; T.a: temperatura.
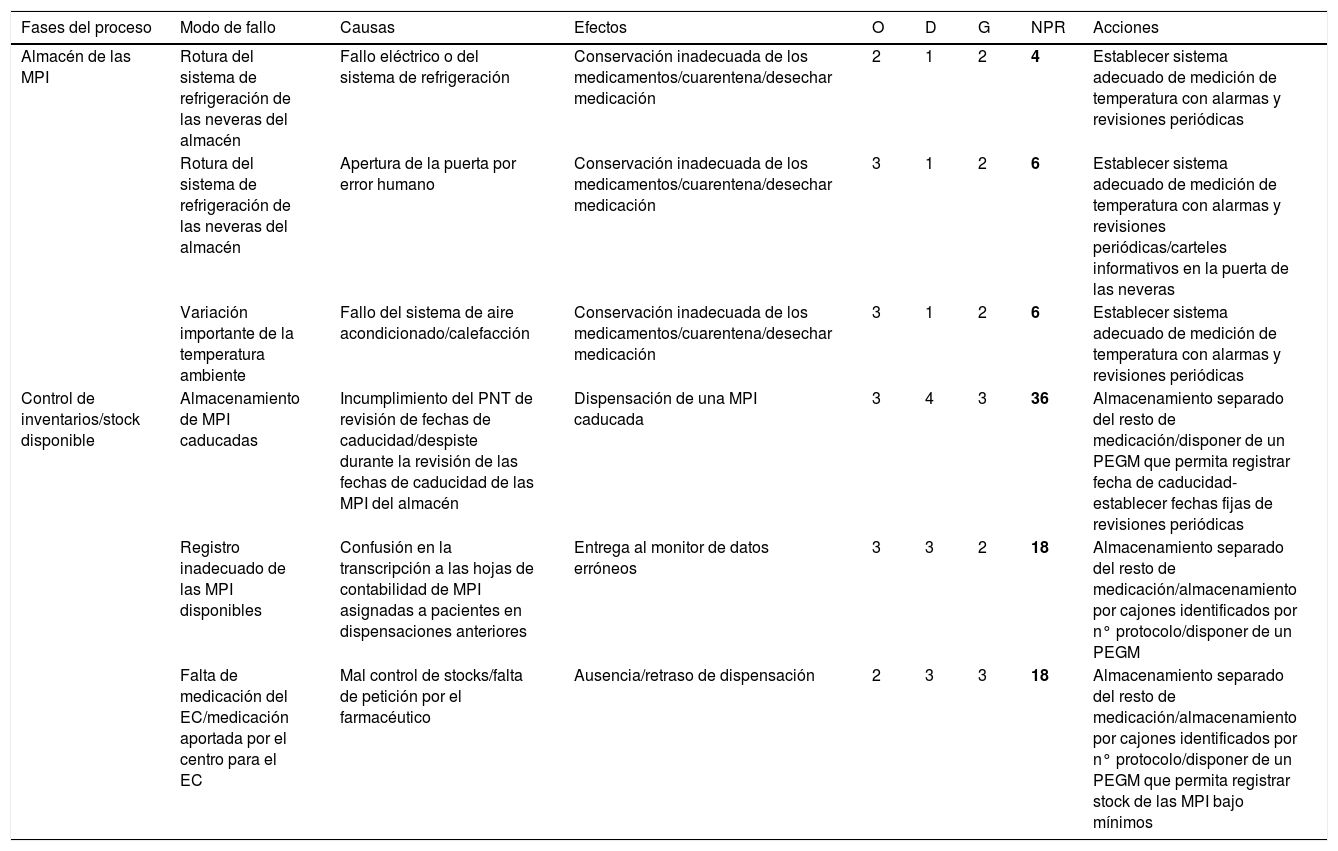
Análisis modal de fallos y efectos en la Unidad de Ensayos Clínicos. Proceso de custodia de muestras
| Fases del proceso | Modo de fallo | Causas | Efectos | O | D | G | NPR | Acciones |
|---|---|---|---|---|---|---|---|---|
| Almacén de las MPI | Rotura del sistema de refrigeración de las neveras del almacén | Fallo eléctrico o del sistema de refrigeración | Conservación inadecuada de los medicamentos/cuarentena/desechar medicación | 2 | 1 | 2 | 4 | Establecer sistema adecuado de medición de temperatura con alarmas y revisiones periódicas |
| Rotura del sistema de refrigeración de las neveras del almacén | Apertura de la puerta por error humano | Conservación inadecuada de los medicamentos/cuarentena/desechar medicación | 3 | 1 | 2 | 6 | Establecer sistema adecuado de medición de temperatura con alarmas y revisiones periódicas/carteles informativos en la puerta de las neveras | |
| Variación importante de la temperatura ambiente | Fallo del sistema de aire acondicionado/calefacción | Conservación inadecuada de los medicamentos/cuarentena/desechar medicación | 3 | 1 | 2 | 6 | Establecer sistema adecuado de medición de temperatura con alarmas y revisiones periódicas | |
| Control de inventarios/stock disponible | Almacenamiento de MPI caducadas | Incumplimiento del PNT de revisión de fechas de caducidad/despiste durante la revisión de las fechas de caducidad de las MPI del almacén | Dispensación de una MPI caducada | 3 | 4 | 3 | 36 | Almacenamiento separado del resto de medicación/disponer de un PEGM que permita registrar fecha de caducidad-establecer fechas fijas de revisiones periódicas |
| Registro inadecuado de las MPI disponibles | Confusión en la transcripción a las hojas de contabilidad de MPI asignadas a pacientes en dispensaciones anteriores | Entrega al monitor de datos erróneos | 3 | 3 | 2 | 18 | Almacenamiento separado del resto de medicación/almacenamiento por cajones identificados por n° protocolo/disponer de un PEGM | |
| Falta de medicación del EC/medicación aportada por el centro para el EC | Mal control de stocks/falta de petición por el farmacéutico | Ausencia/retraso de dispensación | 2 | 3 | 3 | 18 | Almacenamiento separado del resto de medicación/almacenamiento por cajones identificados por n° protocolo/disponer de un PEGM que permita registrar stock de las MPI bajo mínimos |
D: detectabilidad; EC: ensayo clínico; G: gravedad; MPI: muestra para investigación clínica; N.∘: número; NPR: número de prioridad de riesgo; O: ocurrencia; PE: prescripción electrónica; PEGM: programa electrónico de gestión muestra; PNT: procedimientos normalizados de trabajo; SFH: Servicio de Farmacia Hospitalaria; T.a: temperatura.
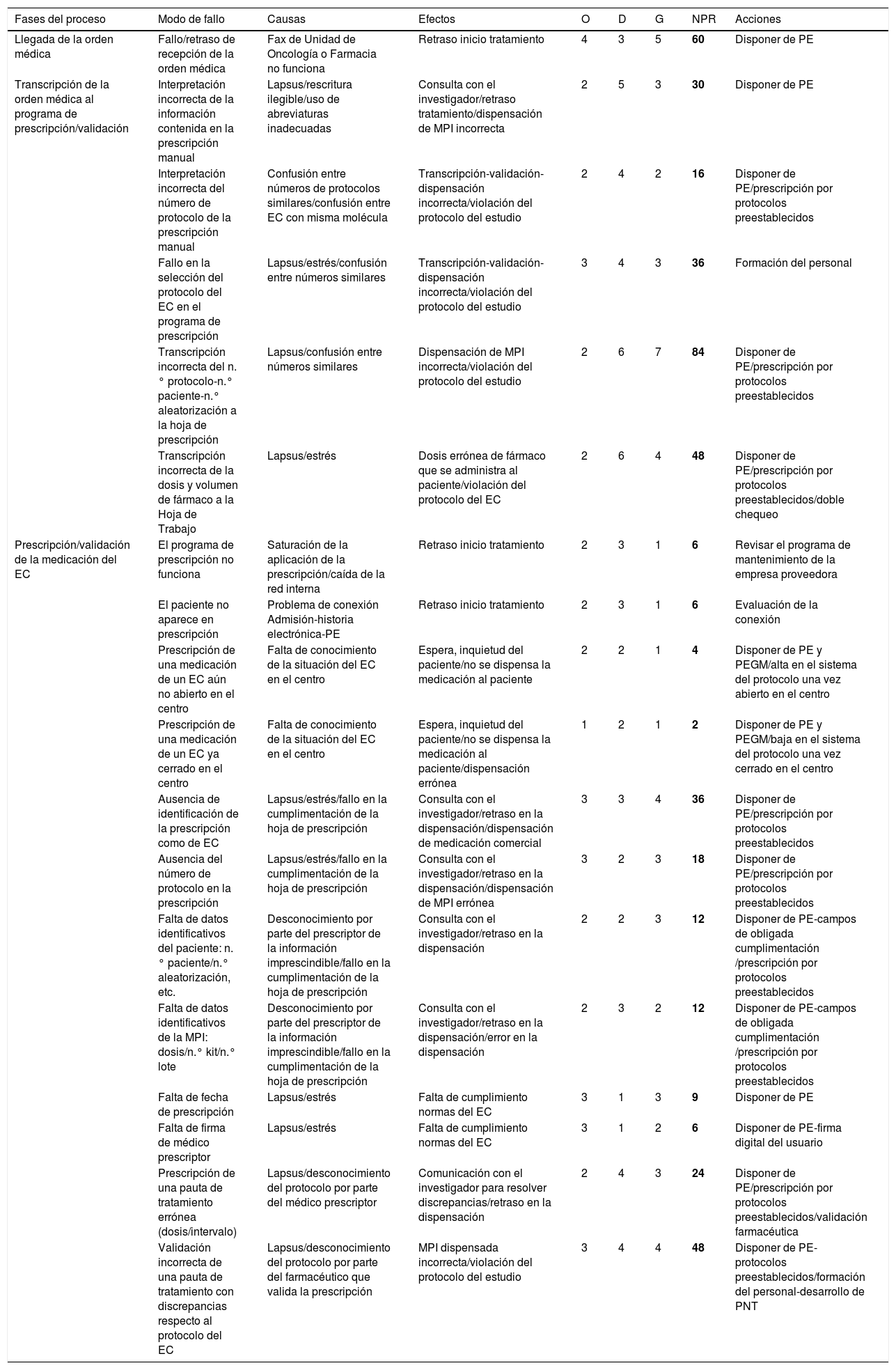
Análisis modal de fallos y efectos en la Unidad de Ensayos Clínicos. Proceso de Prescripción/validación de muestras
| Fases del proceso | Modo de fallo | Causas | Efectos | O | D | G | NPR | Acciones |
|---|---|---|---|---|---|---|---|---|
| Llegada de la orden médica | Fallo/retraso de recepción de la orden médica | Fax de Unidad de Oncología o Farmacia no funciona | Retraso inicio tratamiento | 4 | 3 | 5 | 60 | Disponer de PE |
| Transcripción de la orden médica al programa de prescripción/validación | Interpretación incorrecta de la información contenida en la prescripción manual | Lapsus/rescritura ilegible/uso de abreviaturas inadecuadas | Consulta con el investigador/retraso tratamiento/dispensación de MPI incorrecta | 2 | 5 | 3 | 30 | Disponer de PE |
| Interpretación incorrecta del número de protocolo de la prescripción manual | Confusión entre números de protocolos similares/confusión entre EC con misma molécula | Transcripción-validación-dispensación incorrecta/violación del protocolo del estudio | 2 | 4 | 2 | 16 | Disponer de PE/prescripción por protocolos preestablecidos | |
| Fallo en la selección del protocolo del EC en el programa de prescripción | Lapsus/estrés/confusión entre números similares | Transcripción-validación-dispensación incorrecta/violación del protocolo del estudio | 3 | 4 | 3 | 36 | Formación del personal | |
| Transcripción incorrecta del n.° protocolo-n.° paciente-n.° aleatorización a la hoja de prescripción | Lapsus/confusión entre números similares | Dispensación de MPI incorrecta/violación del protocolo del estudio | 2 | 6 | 7 | 84 | Disponer de PE/prescripción por protocolos preestablecidos | |
| Transcripción incorrecta de la dosis y volumen de fármaco a la Hoja de Trabajo | Lapsus/estrés | Dosis errónea de fármaco que se administra al paciente/violación del protocolo del EC | 2 | 6 | 4 | 48 | Disponer de PE/prescripción por protocolos preestablecidos/doble chequeo | |
| Prescripción/validación de la medicación del EC | El programa de prescripción no funciona | Saturación de la aplicación de la prescripción/caída de la red interna | Retraso inicio tratamiento | 2 | 3 | 1 | 6 | Revisar el programa de mantenimiento de la empresa proveedora |
| El paciente no aparece en prescripción | Problema de conexión Admisión-historia electrónica-PE | Retraso inicio tratamiento | 2 | 3 | 1 | 6 | Evaluación de la conexión | |
| Prescripción de una medicación de un EC aún no abierto en el centro | Falta de conocimiento de la situación del EC en el centro | Espera, inquietud del paciente/no se dispensa la medicación al paciente | 2 | 2 | 1 | 4 | Disponer de PE y PEGM/alta en el sistema del protocolo una vez abierto en el centro | |
| Prescripción de una medicación de un EC ya cerrado en el centro | Falta de conocimiento de la situación del EC en el centro | Espera, inquietud del paciente/no se dispensa la medicación al paciente/dispensación errónea | 1 | 2 | 1 | 2 | Disponer de PE y PEGM/baja en el sistema del protocolo una vez cerrado en el centro | |
| Ausencia de identificación de la prescripción como de EC | Lapsus/estrés/fallo en la cumplimentación de la hoja de prescripción | Consulta con el investigador/retraso en la dispensación/dispensación de medicación comercial | 3 | 3 | 4 | 36 | Disponer de PE/prescripción por protocolos preestablecidos | |
| Ausencia del número de protocolo en la prescripción | Lapsus/estrés/fallo en la cumplimentación de la hoja de prescripción | Consulta con el investigador/retraso en la dispensación/dispensación de MPI errónea | 3 | 2 | 3 | 18 | Disponer de PE/prescripción por protocolos preestablecidos | |
| Falta de datos identificativos del paciente: n.° paciente/n.° aleatorización, etc. | Desconocimiento por parte del prescriptor de la información imprescindible/fallo en la cumplimentación de la hoja de prescripción | Consulta con el investigador/retraso en la dispensación | 2 | 2 | 3 | 12 | Disponer de PE-campos de obligada cumplimentación /prescripción por protocolos preestablecidos | |
| Falta de datos identificativos de la MPI: dosis/n.° kit/n.° lote | Desconocimiento por parte del prescriptor de la información imprescindible/fallo en la cumplimentación de la hoja de prescripción | Consulta con el investigador/retraso en la dispensación/error en la dispensación | 2 | 3 | 2 | 12 | Disponer de PE-campos de obligada cumplimentación /prescripción por protocolos preestablecidos | |
| Falta de fecha de prescripción | Lapsus/estrés | Falta de cumplimiento normas del EC | 3 | 1 | 3 | 9 | Disponer de PE | |
| Falta de firma de médico prescriptor | Lapsus/estrés | Falta de cumplimiento normas del EC | 3 | 1 | 2 | 6 | Disponer de PE-firma digital del usuario | |
| Prescripción de una pauta de tratamiento errónea (dosis/intervalo) | Lapsus/desconocimiento del protocolo por parte del médico prescriptor | Comunicación con el investigador para resolver discrepancias/retraso en la dispensación | 2 | 4 | 3 | 24 | Disponer de PE/prescripción por protocolos preestablecidos/validación farmacéutica | |
| Validación incorrecta de una pauta de tratamiento con discrepancias respecto al protocolo del EC | Lapsus/desconocimiento del protocolo por parte del farmacéutico que valida la prescripción | MPI dispensada incorrecta/violación del protocolo del estudio | 3 | 4 | 4 | 48 | Disponer de PE-protocolos preestablecidos/formación del personal-desarrollo de PNT |
D: detectabilidad; EC: ensayo clínico; G: gravedad; MPI: muestra para investigación clínica; N.∘: número; NPR: número de prioridad de riesgo; O: ocurrencia; PE: prescripción electrónica; PEGM: programa electrónico de gestión muestra; PNT: procedimientos normalizados de trabajo; SFH: Servicio de Farmacia Hospitalaria; T.a: temperatura.
Análisis modal de fallos y efectos en la Unidad de Ensayos Clínicos. Proceso de preparación/aleatorización de muestras
| Fases del proceso | Modo de fallo | Causas | Efectos | O | D | G | NPR | Acciones |
|---|---|---|---|---|---|---|---|---|
| Preparación de la MPI por parte del farmacéutico previo a su elaboración: aleatorización | Fallo en el envío de los números de kit asignados al paciente | Lapsus/estrés/olvido del coordinador | Retraso inicio tratamiento/dispensación de MPI incorrecta/violación del protocolo del estudio | 2 | 4 | 4 | 32 | Disponer de PE-campos de obligada cumplimentación/disponer PNT por EC |
| Fallo en el envío de los números de kit asignados al paciente | El fax del investigador/Unidad de Oncología en Farmacia no funciona | Retraso inicio tratamiento/dispensación de MPI incorrecta/violación del protocolo del estudio | 3 | 3 | 2 | 18 | Disponer de PE/disponer PNT por EC | |
| Fallo en el envío de los números de kit asignados al paciente | Llegada del mail del sistema de aleatorización una persona errónea | Retraso inicio tratamiento/dispensación de MPI incorrecta/violación del protocolo del estudio | 3 | 3 | 2 | 18 | Disponer de PE-Campos de obligada cumplimentación/disponer PNT por EC | |
| Elaboración de la MPI en cabinas de flujo laminar por personal de enfermería | Preparación de una MPI para un paciente erróneo | Mezcla de diferentes bandejas de preparaciones que coinciden a la misma hora | Dispensación MPI incorrecta/violación del protocolo del estudio | 2 | 6 | 5 | 60 | Preparación de la bandeja por el farmacéutico/doble chequeo antes de la elaboración/separación de pacientes del mismo EC a diferentes horas |
| Preparación de la MPI con un diluyente erróneo | Lapsus en la preparación de la bandeja de tratamiento | Desechar medicación/nueva preparación y retraso inicio tratamiento Elaboración incorrecta/violación del protocolo del estudio | 2 | 4 | 4 | 32 | Preparación de la bandeja por el farmacéutico/doble chequeo antes de la elaboración | |
| Preparación en un volumen final erróneo | Lapsus/desconocimiento de las normas de trabajo en cabinas de flujo laminar | Desechar medicación/nueva preparación y retraso inicio tratamiento | 2 | 3 | 3 | 18 | Formación del personal-disponer de guías de elaboración y hojas de preparación como guía y establecer revisiones periódicas de cumplimiento de los PNT establecidos | |
| Preparación fecha/hora errónea | Discrepancia entre fecha de administración confirmada por enfermería de hospital de día y data-manager | Ausencia de mantenimiento de los tiempos de conservación-desechar medicación/nueva preparación y retraso inicio tratamiento | 3 | 2 | 3 | 18 | Disponer de PE-Informatización de la confirmación de fecha y hora de tratamiento | |
| Incumplimiento fecha/hora administración programada | Lapsus/olvidos/retraso paciente en Hospital de Día/saturación de los puestos de Hospital de Día | Ausencia de mantenimiento de los tiempos de conservación-desechar medicación/nueva preparación y retraso inicio tratamiento | 4 | 3 | 2 | 24 | Disponer de PE-informatización de la confirmación de fecha y hora de tratamiento | |
| Violación del ciego por parte de personal de farmacia | Lapsus/desconocimiento de normas-condiciones de enmascaramiento por parte del personal | Violación del protocolo del estudio/salida del paciente del EC | 2 | 4 | 3 | 24 | Formación del personal-disponer PNT por EC |
D: detectabilidad; EC: ensayo clínico; G: gravedad; MPI: muestra para investigación clínica; N.∘: número; NPR: número de prioridad de riesgo; O: ocurrencia; PE: prescripción electrónica; PEGM: programa electrónico de gestión muestra; PNT: procedimientos normalizados de trabajo; SFH: Servicio de Farmacia Hospitalaria; T.a: temperatura.
Análisis modal de fallos y efectos en la Unidad de Ensayos Clínicos. Proceso de dispensación de muestras
| Fases del proceso | Modo de fallo | Causas | Efectos | O | D | G | NPR | Acciones |
|---|---|---|---|---|---|---|---|---|
| Llegada del paciente a la ventanilla de dispensación con prescripción de MPI | La aplicación informática de dispensación a pacientes externos no funciona | Saturación de la aplicación electrónica/ caída de la red interna | Retraso en la dispensación | 3 | 2 | 1 | 6 | Revisar el programa de mantenimiento con la empresa proveedora |
| El paciente no aparece en la aplicación informática de dispensación | Problema de conexión Admisión-historia electrónica-PE | Retraso en la dispensación | 6 | 2 | 2 | 24 | Evaluación de la conexión Admisión-historia electrónica-PE | |
| Ausencia de identificación del paciente o de la prescripción como de EC | Lapsus/estrés/fallo en la cumplimentación de la hoja de prescripción/el paciente tiene una prescripción anterior de medicación comercial que no se ha suspendido en el sistema | Consulta con el investigador/retraso en la dispensación/dispensación errónea de medicación comercial | 3 | 4 | 4 | 48 | Disponer de PE/prescripción por protocolos preestablecidos definidos como de EC | |
| Dispensación de la MPI | Interpretación incorrecta de la información contenida en la prescripción manual | Lapsus/escritura ilegible/uso de abreviaturas inadecuadas | Consulta con el investigador/retraso tratamiento/dispensación MPI incorrecta | 4 | 5 | 4 | 80 | Disponer de PE |
| Interpretación incorrecta del número de protocolo de la prescripción manual | Confusión entre números de protocolos similares/confusión entre EC con misma molécula | Dispensación MPI incorrecta/violación del protocolo del estudio | 3 | 4 | 3 | 36 | Disponer de PE/prescripción por protocolos preestablecidos | |
| Asignación de un tratamiento a un paciente erróneo | Fallo/desconocimiento de la necesidad o del proceso de aleatorización | Dispensación MPI incorrecta/violación del protocolo del estudio | 3 | 6 | 4 | 72 | Disponer de un PEGM/chequeo antes de la dispensación | |
| Ausencia de la MPI asignada y solicitada para el paciente | Error de envío de medicación por parte del promotor/ error o falta de registro de una dispensación anterior | Retraso/ausencia de dispensación | 3 | 3 | 2 | 18 | Disponer de un PEGM | |
| Selección de una MPI que no corresponde con la medicación del protocolo del paciente | Error de identificación de la ubicación de la medicación/error producido durante el proceso de almacenamiento | Dispensación MPI incorrecta/violación del protocolo del estudio | 2 | 7 | 5 | 70 | Disponer de un PEGM/doble chequeo dispensaciones | |
| Selección de una MPI que no corresponde con el brazo de tratamiento/dosis asignada al paciente | Error durante el almacenamiento/confusión de MPI por falta de claridad en el embalaje/insuficiente conocimiento de la existencia de diferentes brazos de tratamiento-dosis en un mismo EC | Dispensación MPI incorrecta/violación del protocolo del estudio | 2 | 4 | 4 | 32 | Disponer de un PEGM/doble chequeo dispensaciones | |
| Selección de un n° kit/lote que no corresponde con el asignado por aleatorización al paciente | Error en lectura del n° kit/lote en embalaje del producto/confusión n.° kit/lote/error durante el almacenamiento | Dispensación MPI incorrecta/violación del protocolo del estudio | 2 | 3 | 4 | 24 | Disponer de un PEGM/doble chequeo dispensaciones | |
| Olvido de dispensación de una MPI/n.° kit | Lapsus/estrés/fallo en la lectura de la lista de MPI en la prescripción manual | Dispensación incompleta de MPI/violación del protocolo del estudio | 2 | 3 | 2 | 12 | Disponer de un PEGM/doble chequeo dispensaciones | |
| Dispensación de una MPI caducada | No retirada de los medicamentos caducados/no revisión de la caducidad durante la dispensación | Dispensación de una MPI caducada/violación del protocolo del estudio | 2 | 3 | 4 | 24 | Disponer de un PEGM/establecimiento de fechas fijas de revisiones periódicas | |
| Dispensación de una MPI en mal estado | Error producido durante el proceso de almacenamiento/falta de conocimiento sobre el estado de conservación de las MPI | Dispensación de una MPI en mal estado/violación del protocolo del estudio | 1 | 5 | 3 | 15 | Disponer de un PEGM-comprobación lugar almacenamiento antes de guardarlas | |
| Dispensación de una MPI en cuarentena | Ausencia/error de señalización de medicación en cuarentena | Dispensación de una MPI en cuarentena/violación del protocolo del estudio | 3 | 3 | 4 | 36 | Disponer de un PEGM | |
| Ausencia de pegatinas/identificadores de las MPI que deben conservase en la dispensación | Lapsus/desconocimiento de normas específicas de dispensación | Ausencia/error en el registro de dispensación | 3 | 4 | 3 | 36 | Disponer de un PEGM | |
| Omisión de la firma del paciente | Lapsus/estrés | Ausencia de registro de la entrega | 3 | 1 | 4 | 12 | Formación del personal | |
| Registro de dispensación en hojas de contabilidad | Ausencia registro dispensación MPI | Lapsus/estrés | Ausencia registro dispensación MPI | 3 | 2 | 3 | 18 | Disponer de un PEGM |
| Interpretación incorrecta del n° de paciente | Confusión entre números de pacientes que empiezan igual | Registro incorrecto del n.° paciente o MPI | 3 | 2 | 3 | 18 | Disponer de un PEGM | |
| Transcripción incorrecta del tipo MPI/dosis/n.° lote/n.° kit dispensados al paciente | Confusión por complejidad de la información mostrada en la etiqueta de la MPI/confusión en la lectura de la receta manual | Registro incorrecto de la MPI dispensada | 3 | 2 | 3 | 18 | Disponer de un PEGM |
D: detectabilidad; EC: ensayo clínico; G: gravedad; MPI: muestra para investigación clínica; n.∘: número; NPR: número de prioridad de riesgo; O: ocurrencia; PE: prescripción electrónica; PEGM: programa electrónico de gestión muestra; PNT: procedimientos normalizados de trabajo; SFH: Servicio de Farmacia Hospitalaria; T.a: temperatura.
Análisis modal de fallos y efectos en la Unidad de Ensayos Clínicos. Proceso de visita de inicio de ensayo clínico
| Fases del proceso | Modo de fallo | Causas | Efectos | O | D | G | NPR | Acciones |
|---|---|---|---|---|---|---|---|---|
| Visita de inicio | Fallo en la creación del protocolo de prescripción según el protocolo del EC | Información confusa o incompleta proporcionada en la visita de inicio o en el protocolo en papel | Pautas posológicas incorrectas/violación del protocolo del EC | 2 | 4 | 3 | 24 | Disponer de PE con protocolos preestablecidos/consulta de dudas con el monitor |
| Fallo en la creación del protocolo de prescripción según el protocolo del EC | Lapsus/estrés | Pautas posológicas incorrectas/violación del protocolo del EC | 2 | 4 | 3 | 24 | Doble chequeo en la creación de los protocolos de EC en PE |
D: detectabilidad; EC: ensayo clínico; G: gravedad; NPR: número de prioridad de riesgo; O: ocurrencia; PE: prescripción electrónica.
Se determinaron 67 posibles fallos. De todos los subprocesos, el de dispensación resulto el más susceptible de generar errores, con 19 modos de fallo, seguido de la prescripción/validación, con 18 modos de fallo. Los fallos más críticos se obtuvieron en la dispensación (NPR = 599), donde destacaron: la dispensación incorrecta de la MPI por interpretación incorrecta de la información en la prescripción manual (NPR = 84); la asignación de un tratamiento a un paciente erróneo (NPR = 72), y la selección de una MPI que no corresponde con la medicación del protocolo en el que está incluido el paciente (NPR = 70). A su vez, se registraron en la prescripción/validación (NPR = 457), donde destacaron: transcripción incorrecta de la orden médica a la hoja de prescripción (NPR = 84) y fallo/retraso de recepción de la orden médica en Farmacia (NPR = 60). El subproceso de preparación también obtuvo fallos críticos (NPR = 244), destacando preparación de una MPI para un paciente erróneo (NPR = 60).
Todas las acciones de mejora establecidas en el AMFE fueron implementadas en la Unidad de Ensayos Clínicos del SFH. Entre ellas, destacaron:
- -
La reorganización del personal farmacéutico por áreas de conocimiento y la asignación de un responsable de la Unidad de investigación del SFH.
- -
Una reestructuración logística, con diferenciación de los ensayos clínicos que requerían o no prepararse en el SFH.
- -
Una adaptación de las instalaciones físicas con almacenamiento de específico de las MPI y automatización del control de temperatura.
- -
Una mejora de la gestión logística mediante la implantación de un programa electrónico de gestión de MPI.
- -
Una mejora en la seguridad de los procesos con la implantación de la prescripción electrónica en los ensayos clínicos y la elaboración de los procedimientos de la Unidad.
En nuestro análisis, de todos los subprocesos, el de dispensación resultó el más susceptible de generar errores, con 19 modos de fallo, seguido de la prescripción/validación, con 18 modos de fallo. A sí mismo, los fallos más críticos ocurrieron principalmente en la dispensación, con una puntuación total de 599 NPR, y en la prescripción/validación, con una puntuación total de 457 NPR. La ausencia de un programa electrónico de gestión de MPI y de la prescripción electrónica fueron los principales responsables.
En el subproceso de dispensación, la mayoría de los modos de fallo se podían evitar con la implantación de un programa electrónico de gestión de muestras, que permitiese registrar las características de cada ensayo clínico, sus muestras, sus condiciones de conservación, los pacientes incluidos, las hojas de contabilidad, así como los informes de dispensación por paciente y alertas de caducidad, cuarentena, etc.
La mayoría de los medicamentos que requerían preparación en el SFH eran de carácter citostático y administración intravenosa, un posible fallo podía originar un efecto de alta gravedad. La implantación de la prescripción electrónica y de los procedimientos podía evitar los posibles modos de fallo; sin embargo, se realizó la observación de que a pesar de los cambios propuestos podría no evitarse el modo de fallo de algunos procesos del AMFE. Por ello, se consideró la necesidad de disponer de personal exclusivo de la Unidad de Ensayos Clínicos y fomentar su formación mediante los procedimientos de la Unidad (que incluían la preparación de las bandejas individualizadas por paciente, por el personal farmacéutico, así como actividades de doble chequeo de las preparaciones) y los procedimientos normalizados de trabajo con información práctica sobre cada uno de los ensayos clínicos. Se diseñaron además hojas de preparación específicas para servir de guía en la preparación de los ensayos clínicos.
En el subproceso de custodia y recepción de las MPI, la adaptación de las instalaciones físicas con un almacenamiento separado del resto de la medicación del Servicio, la identificación de las MPI por número de protocolo de ensayos clínicos, la automatización de la temperatura en la sala y la implantación del programa electrónico de gestión de MPI fueron las medidas que destacaron para reducir los posibles modos de fallo.
En último lugar, la revisión de los protocolos creados en la prescripción electrónica se posicionó como medida necesaria para evitar el modo de fallo del subproceso de visitas de inicio de los ensayos clínicos.
Cabe destacar que la participación y la difusión de este tipo de trabajo sirvieron para fomentar el compromiso y la responsabilidad de todos los profesionales participantes en el desarrollo de los ensayos clínicos19.
Los trabajos publicados en los que se utiliza esta metodología enfocada al ámbito sanitario coinciden en la utilidad de esta herramienta para la detección de los puntos débiles del sistema y para la priorización de recursos con el fin de mejorar la seguridad de todos los procesos20-22. En un estudio en el que se realizó un análisis AMFE en una unidad de ensayos clínicos, los subprocesos que se definieron fueron similares a los encontrados en nuestro estudio23. El mayor número de potenciales modos de fallo se concentró en los subprocesos de preparación y dispensación de las MPI, a diferencia de nuestro estudio, donde fueron los subprocesos de dispensación y de prescripción/validación de las MPI los que presentaron un mayor número de puntos débiles. Las medidas correctoras fueron implementadas en su unidad disminuyendo considerablemente el riesgo.
Basándonos en este estudio y otros que aplican la metodología AMFE en un contexto sanitario, podemos detectar como principal limitación de nuestro estudio que no se determinó el impacto de las medidas adoptadas. Es necesario, que en el momento en el que todas las acciones correctoras se encuentren implantadas en su totalidad, que se valore su impacto en la Unidad de investigación del SFH. A su vez, encontramos como limitación la extrapolación de los resultados a otras instituciones. Esto es debido a la gran variabilidad de los procesos, las diferentes metodologías empleadas y la escasez de validez externa del AMFE24-26. A pesar de ello, cabe mencionar que es una herramienta muy utilizada en la gestión de los riesgos en los procesos relacionados con la farmacia hospitalaria y preparación de medicamentos27,28.
En conclusión, el AMFE ha demostrado ser una herramienta útil en la gestión proactiva de los riesgos. Los subprocesos de dispensación y prescripción/validación de las MPI fueron los más susceptibles a generar errores. Entre las medidas correctoras implantadas destacaron el programa electrónico de gestión de MPI y la prescripción electrónica. Estas medidas garantizan la reducción de los riesgos, permitiendo incrementar la seguridad de forma considerable en todos los procesos del desarrollo de los ensayos clínicos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.