La población que se inyecta droga presenta una alta prevalencia de VHC y elevado riesgo de transmisión. Es prioritario establecer un plan ágil de diagnóstico y tratamiento.
Objetivos1) Valorar la efectividad de un nuevo plan asistencial coordinado de derivación desde el Centro de Atención Integral al Drogodependiente (CAID) a atención especializada y 2) conocer la prevalencia del VHC, características clínicas, efectividad y seguridad del tratamiento en esta población.
MétodosSe analizaron retrospectivamente 1.300 serologías solicitadas por el CAID entre 1998-2018, se calculó la seroprevalencia de VHC y se valoró la eficiencia del circuito clásico de derivación CAID-atención especializada. Se diseñó un plan asistencial coordinado entre especialistas implicados en el diagnóstico y tratamiento. Desde octubre de 2018 se incluyeron 11 pacientes en el nuevo plan y se comparó el rendimiento de ambos circuitos de derivación.
ResultadosCon el circuito clásico, se perdió un 48,2% (83/172) de los pacientes. Un 14,5% (172/1.300) presentaron serología VHC positiva, en comparación con población general OR = 19; IC 95% 14,3-25. La prevalencia de infección activa fue del 80,3% (90/112). Con el nuevo circuito acudieron el 100% (11/11) (p = 0,0003). De los 11 pacientes derivados mediante el nuevo plan, 76,9% (8/11) tenían infección activa y el 100% (8/8) fueron tratados con agentes antivirales directos con éxito.
ConclusionesEl nuevo plan asistencial coordinado CAID-atención especializada presenta alta efectividad, en comparación con el circuito clásico de derivación. La seroprevalencia y prevalencia de infección activa en la población del CAID es muy elevada. Los tratamientos con agentes antivirales directos son efectivos y seguros.
The drug-injecting population has a high prevalence of hepatitis C virus (HCV) and high risk of transmission. It is a priority to establish an agile diagnostic and treatment plan.
Objectives1) Assess the effectiveness of a new coordinated care plan of referral from the Comprehensive Care Centre for Drug Addicts (CAID) to specialised care and 2) Determine the prevalence of HCV, clinical characteristics, effectiveness and safety of treatment in this population.
Methods1,300 serologies requested by the CAID between 1998 and 2018 were retrospectively analysed, the seroprevalence of HCV was calculated and the efficiency of the traditional CAID-specialised care referral system was evaluated. A care plan was designed and coordinated among specialists involved in diagnosis and treatment. Since October 2018, 11 patients have been included in the new plan and the performance of both referral systems was compared.
ResultsWith the traditional system, 48.2% (83/172) of the patients were lost. 14.5% (172/1,300) presented positive HCV serology, compared to the general population OR = 19; 95% CI 14.3-25. The prevalence of active infection was 80.3% (90/112). The prevalence of active infection was 80.3% (90/112). Of the 11 patients referred by the new plan, 76.9% (8/11) had active infection and 100% (8/8) were treated with Direct Antiviral Agents successfully.
ConclusionsThe new coordinated CAID-specialised care plan presents high effectiveness in comparison with the traditional referral system. The seroprevalence and prevalence of active infection in the CAID population is very high. Treatments with Direct Antiviral Agents are effective and safe.
La eficacia de los nuevos regímenes de tratamiento con agentes antivirales directos (AAD) impulsó en 2016 a la Organización Mundial de la Salud (OMS) a adoptar el ambicioso objetivo de la eliminación del virus de la hepatitis C (VHC) como una amenaza para la salud pública en el 20301. Diferentes países han puesto en marcha planes de acción específicos; en España, se ha publicado recientemente un documento de posicionamiento por parte de la Asociación Española para el Estudio del Hígado (AEEH)2,3.
En 2017, se sugirió como estrategia para afrontar el complejo reto de la eliminación, establecer metas de microeliminación4, que consisten en aumentar la eficiencia de esta acción a través de la eliminación del VHC en poblaciones específicas, como son las personas que se inyectan drogas (PID) o practican otras conductas de riesgo, inmigrantes de áreas de alta prevalencia y presos4.
La población PID supone el 8% de las infecciones crónicas por VHC5, presenta una elevada prevalencia de VHC, que en España se estima entre 47-85%6–8 y con un alto riesgo para la transmisión del virus, dado que son responsables del 23% de las nuevas infecciones a nivel mundial9, entendiéndose, por tanto, el tratamiento también como prevención. En esta población, además de las medidas de reducción de daño (provisión de agujas/jeringuillas y terapia de sustitución de opiáceos (TSO), que contribuyen a la reducción de la transmisión del VHC10-12, debe establecerse un plan de diagnóstico y tratamiento a todos los pacientes en un corto periodo de tiempo, que se desarrolle a través de un proceso que incluya a todas las partes implicadas, personalizado, y con objetivos alcanzables13. Existen publicados algunos modelos de atención a esta población que mejoran el acceso a la atención y logran resultados exitosos del tratamiento14,15.
Hemos diseñado un plan asistencial para tratar, en un corto periodo de tiempo, a los pacientes de nuestra área con VHC atendidos en el CAID de Alcorcón.
Una barrera importante para alcanzar estos objetivos es la imposibilidad de derivación directa de estos pacientes desde los CAID a los centros especializados para el tratamiento, dado que deben ser valorados previamente en los centros de salud y una vez confirmada la seropositividad, derivarlos a las consultas especializadas. Estos múltiples pasos favorecen las incomparecencias y pérdida de seguimiento por la idiosincrasia de esta población.
Los objetivos del estudio fueron: 1) valorar la efectividad del nuevo plan asistencial coordinado para la derivación directa desde el CAID a atención especializada (AE) y 2) conocer la prevalencia del VHC, características clínicas, efectividad y seguridad terapéuticas en esta población.
Material y métodosSe realizó un estudio ambispectivo, el periodo retrospectivo comprendió el registro de los datos desde 1998 hasta septiembre de 2018. A partir de octubre de 2018, se realizó un seguimiento prospectivo.
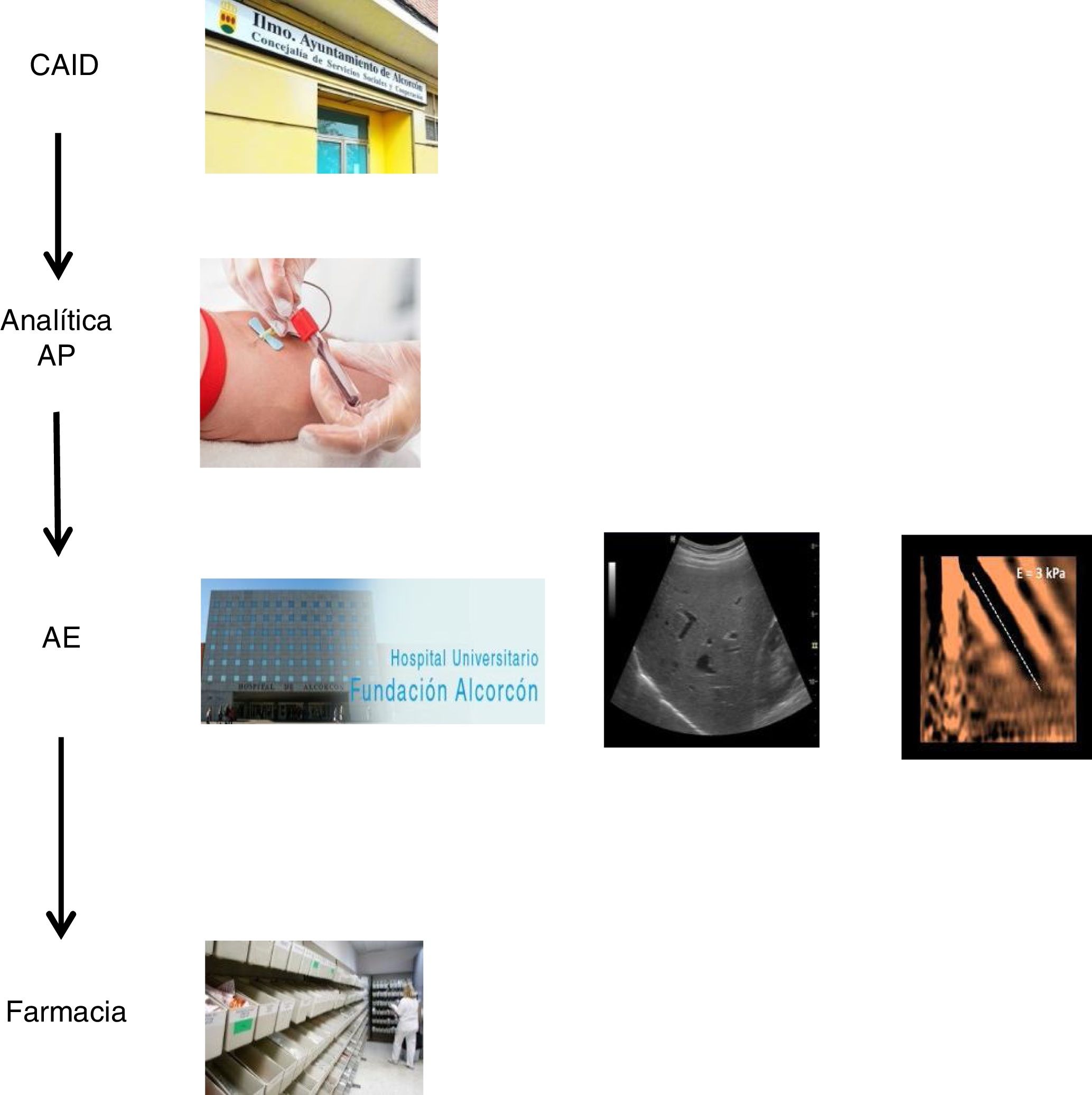
En un primer tiempo, se evaluó el circuito clásico de derivación desde el CAID a AE, que consistía en un total de nueve pasos y se calculó la efectividad del circuito, entendiendo como circuito efectivo, aquel que no presenta pérdidas de pacientes a lo largo del mismo. Se analizaron las pérdidas de pacientes en los diferentes pasos del circuito: número de pacientes derivados a AE a través de atención primaria (AP), número de pacientes que acudieron a la consulta de AE del total de pacientes derivados, número de pacientes en los que se realizó el estudio solicitado por AE, y número de pacientes que finalmente recibieron tratamiento antiviral.
Para ello se revisaron de forma retrospectiva 1.300 resultados de serología frente al VHC, solicitadas desde el CAID de Alcorcón, desde la apertura del hospital hasta el inicio del estudio (entre los años 1998-2018), para calcular la seroprevalencia, la prevalencia de infección activa (RNA-VHC positivos) y la efectividad del circuito clásico.Con el objeto de mejorar la efectividad del circuito y evitar las pérdidas de los pacientes a lo largo del mismo, se decidió diseñar un plan coordinado. En colaboración con los especialistas implicados en la atención de estos pacientes y de la Dirección de Continuidad Asistencial, se diseñó un plan asistencial que coordinaba a los diferentes especialistas implicados en el diagnóstico y tratamiento del VHC (médicos del CAID, analistas/microbiólogos, hepatólogos y farmacéuticos), aplicando además, la técnica para el diagnóstico del VHC «en un solo paso».
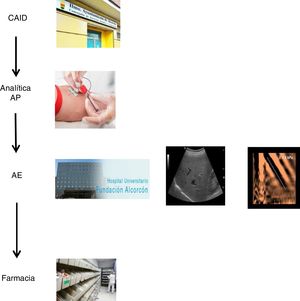
El plan coordinado consistió en tres pasos: 1) se decidió realizar una única extracción analítica en el centro de referencia de AP a todos los pacientes con serología VHC positiva conocida, que no habían sido valorados/tratados previamente, y a aquellos con serología positiva no conocida previamente, con el objetivo de analizar en la misma muestra la viremia, y en casos de resultado positivo, ampliar el estudio con genotipado y carga viral. El servicio de microbiología informaba mediante correo electrónico a los hepatólogos de aquellos casos con infección activa. 2) Los casos con infección activa fueron citados en la consulta de hepatología para valoración clínica, realización de ecografía abdominal/fibroscan, y prescripción del tratamiento antiviral en el mismo día. Se programó control clínico-analítico a las 12 semanas de seguimiento, una vez finalizado el tratamiento. 3) El tratamiento pautado completo se recogería en la farmacia hospitalaria el mismo día de la valoración por el hepatólogo, y se llevaría al CAID, donde se realizarían los controles de toma de medicación presencial para garantizar la correcta adherencia. Además los médicos del CAID se encargaron del seguimiento de los pacientes, en cuanto a efectos secundarios/interacciones farmacológicas (fig. 1).
Una vez aprobado el circuito coordinado de derivación, se realizó la segunda parte del estudio, que consistió en el estudio prospectivo de los pacientes incluidos en el nuevo circuito desde octubre de 2018 hasta la actualidad.
El estudio fue aprobado por el Comité Ético (CEIC) del Hospital Universitario Fundación Alcorcón. Los pacientes incluidos en el nuevo circuito de derivación fueron informados y firmaron un consentimiento informado, en el caso de los pacientes valorados de forma retrospectiva en el circuito clásico, se obtuvo una exención del CEIC para la obtención del consentimiento informado, al tratarse de práctica clínica real.
Para valorar el impacto del plan de asistencia coordinada, sobre la derivación de los pacientes a AE, se comparó la efectividad del nuevo circuito coordinado de derivación frente al plan tradicional de derivación.
Para valorar las características clínicas de los pacientes con VHC del CAID, se recogieron variables antropométricas, demográficas, comportamientos de riesgo, y comorbilidades, parámetros habitualmente recogidos en la clínica real. Como variables analíticas se recogieron: serología virus de la hepatitis (VHB), serología del virus de la inmunodeficiencia humana (VIH), tipificación y carga viral del VHC, estadio de fibrosis, tipo y duración de tratamiento con AAD.
Los análisis de los datos se analizaron mediante el programa estadístico SPSS 21.0. Las variables categóricas se expresaron mediantes frecuencias, y las cuantitativas por la media y desviación estándar o la mediana y rangos.
ResultadosUn 14,5% (172/1.300) presentaron una serología VHC positiva, en comparación con población general OR = 19; IC 95% 14,3-2516.
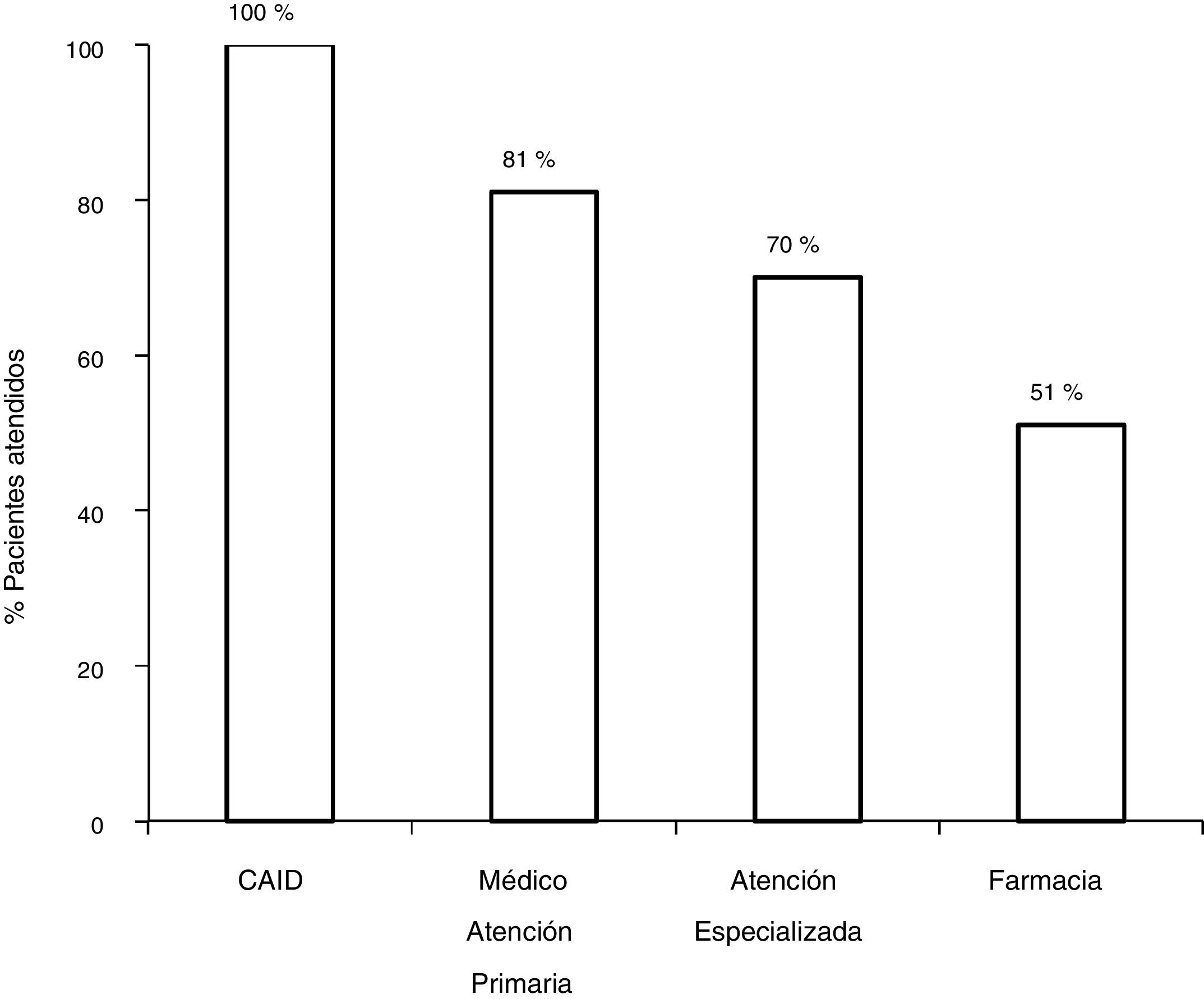
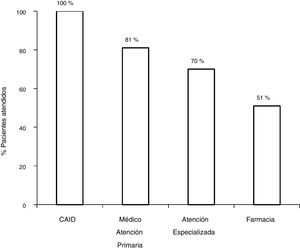
Con el circuito antiguo, de los 172 pacientes con serología positiva, 81,3% (140/172) fueron derivados a AE, y acudieron a la visita con el especialista el 70,3% (121/172). De los 121 pacientes valorados por el especialista, un 7,5% (9/121) no se realizó el estudio solicitado por el especialista. De los 112 con serología positiva que concluyeron el estudio, el 80,3% (90/112) presentó viremia positiva, y el 19,7% (22/112) presentaban viremia negativa. De los 90 pacientes con infección activa, 75,5% (67/90) fueron tratados obteniendo respuesta virológica sostenida (RVS), 27 con interferón (IFN) y 40 con AAD (fig. 2).
Con el esquema tradicional de derivación, del total de pacientes con serología positiva, se perdieron un 48,2% (83/172) en los diferentes pasos del circuito. El 18,6% (32/172) no fueron derivados, 11% (19/172) no acudieron a la primera cita con el especialista, 5,2% (9/172) no se realizó el estudio solicitado por el especialista o no acudió a los resultados, y un 13,3% (23/172) no fueron tratados.
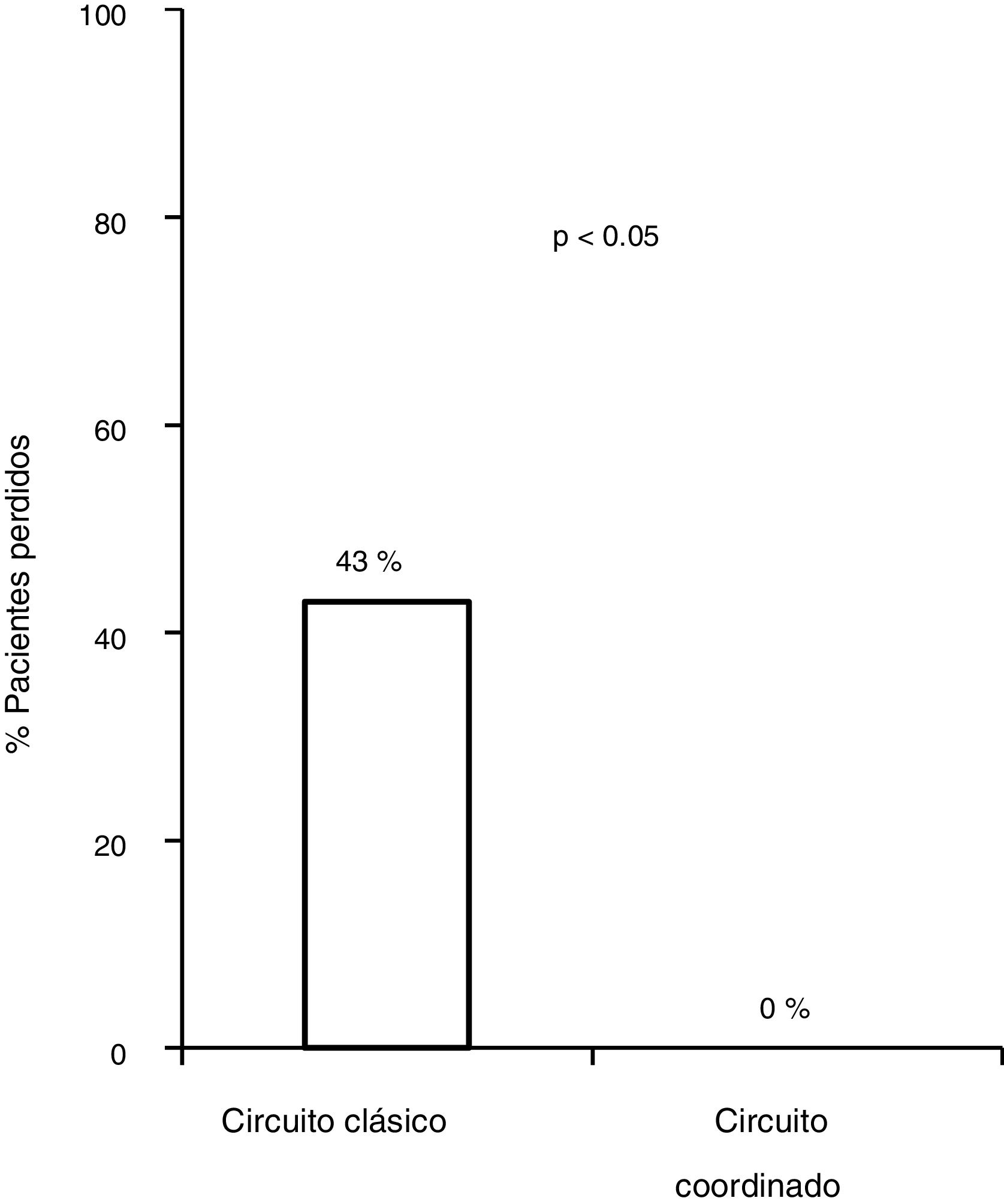
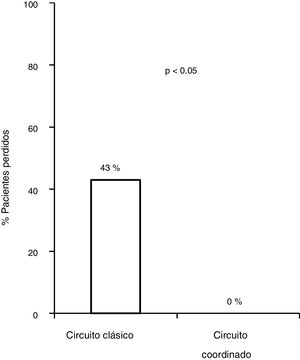
De los 83 pacientes perdidos, 11 fueron derivados por los médicos del CAID aplicando el nuevo plan de asistencia coordinada, 8 (76%) presentaban infección activa. Los ocho (100%) fueron diagnosticados y tratados según el plan diseñado sin ninguna pérdida durante el circuito, frente a las 83/172 (43,8%) pérdidas del circuito clásico, siendo por tanto, la tasa de derivación más alta del circuito coordinado cuando se comparó con el circuito clásico (p = 0,0008). Los ocho (100%) recibieron tratamiento con AAD, obteniendo respuesta virológica sostenida (RVS), con unas cifras de adherencia cercanas al 100%, sin haberse descrito efectos adversos graves (fig. 3).
Cuando se revisaron las historias clínicas de los 72 pacientes perdidos y que no se encontraban en seguimiento por el CAID, 14 (20%) pacientes habían fallecido, 49 (70%) se encontraban en otras áreas de la comunidad de Madrid, o en otras CC. AA., y solo 9 (10%) permanecían en nuestra área. Una vez informados a sus MAP, contactamos con los nueve pacientes que permanecían en el área, y solo conseguimos respuesta de dos de ellos, de los cuales, uno presentó viremia positiva.
En total, incluyendo ambos circuitos de derivación, 75 pacientes fueron tratados obteniendo RVS, de los cuales 27 (36%) fueron tratados con IFN y 48 (64%) con AAD. De estos 75 pacientes, 64 eran varones (85%), con una edad media de 44 años (rango 30-62). En cuanto a comorbilidades, 62 (82%) reconocían haber usado drogas por vía parenteral y 28 (35%) presentaban patología dual, ocho (10%) esquizofrenia, cuatro (5%) depresión, tres (4%) trastornos de la personalidad, tres (4%) trastornos adaptativos, nueve (12%) ansiedad y uno (1,3%) otra no especificada.
En el momento de iniciar tratamiento antiviral, 12 (16%) reconocían consumo activo de drogas, 27 (36%) recibían TSO, 66 (88%) eran fumadores activos y 47 (62%) reconocían consumo de alcohol.
Como era de esperar en la población infectada, el genotipo predominante fue el 1a y el 3 (60%), 21% presentaba estadios de fibrosis avanzada (F3-F4), 36% presentaban anti- HBc positivo y 16% eran VIH positivos.
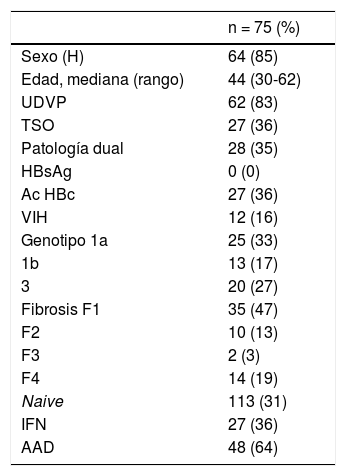
Las características clínicas de los pacientes tratados aparecen representadas en la tabla 1.
Características de los pacientes del CAID tratados
| n = 75 (%) | |
|---|---|
| Sexo (H) | 64 (85) |
| Edad, mediana (rango) | 44 (30-62) |
| UDVP | 62 (83) |
| TSO | 27 (36) |
| Patología dual | 28 (35) |
| HBsAg | 0 (0) |
| Ac HBc | 27 (36) |
| VIH | 12 (16) |
| Genotipo 1a | 25 (33) |
| 1b | 13 (17) |
| 3 | 20 (27) |
| Fibrosis F1 | 35 (47) |
| F2 | 10 (13) |
| F3 | 2 (3) |
| F4 | 14 (19) |
| Naive | 113 (31) |
| IFN | 27 (36) |
| AAD | 48 (64) |
El concepto de microeliminación del VHC en poblaciones específicas como PID, es una estrategia para afrontar el complejo reto de la eliminación del VHC de la OMS1,2. Las PID son una población estigmatizada, en ocasiones ilegal, reacia a buscar o a aceptar ayuda médica, a quienes el propio sistema de salud impone barreras como la atención en lugares alejados, con horarios y citas inflexibles. Es importante establecer planes que se desarrollen a través de un proceso de múltiples partes interesadas, adaptando las intervenciones a las necesidades de estas poblaciones. Existen publicados algunos modelos de atención a esta población que han demostrado ser eficaces para mejorar el acceso a la atención y lograr resultados exitosos14,15.
Diseñamos un plan asistencial para tratar, en un corto periodo de tiempo, a los pacientes de nuestra área atendidos en el CAID de Alcorcón con VHC, plan que coordinaba la asistencia de los diferentes especialistas implicados en el diagnóstico y tratamiento del VHC (médicos del CAID, analistas/microbiólogos, hepatólogos y farmacéuticos), empleando además, la técnica para el diagnóstico del VHC «en un solo paso».
El presente trabajo muestra que el nuevo plan asistencial coordinado CAID-AE presenta una alta efectividad en cuanto a tasas de derivación, cuando se compara con el circuito clásico de derivación. La seroprevalencia y prevalencia de infección activa en la población del CAID son muy elevadas. Se trata de una población más joven, con gran predominio de varones, en ocasiones con consumo activo de drogas, con frecuencia en TSO, y con patología dual en tratamiento concomitante con psicofármacos. Los tratamientos con AAD en esta población son efectivos y seguros.
Nuestro estudio demuestra la inefectividad del circuito clásico de derivación CAID-AE, tratándose de un circuito largo que consistía en un total de nueve pasos, y demuestra la pérdida de los pacientes en las diferentes escalas del circuito, de tal forma que casi la mitad de los pacientes finalmente no alcanzaron el objetivo final de recibir tratamiento antiviral. Cuando analizamos el circuito, vimos que casi 2/3 partes de las pérdidas tuvieron lugar en el acceso a AE, y que el 1/3 restante no recibió tratamiento antiviral, bien por no haber completado el estudio solicitado por AE, bien por la existencia de contraindicaciones, ya que se trata de un estudio retrospectivo donde se valoraba en la mayor parte de los pacientes el tratamiento con IFN. Se demuestra, por tanto, la necesidad de establecer circuitos ágiles y rápidos que faciliten el acceso a AE, consigan vincular al paciente en el sistema evitando pérdidas, en los que se emplee diagnóstico en un solo paso, se emplee ubicación conjunta de servicios y la externalización del tratamiento.
El nuevo circuito de derivación quedó simplificado en tres pasos; sin duda, uno de los puntos de mayor fortaleza del nuevo circuito es el empleo de la técnica del diagnóstico en un solo paso, seguido por la realización en una sola visita de la valoración clínica, estadificación de la enfermedad, y prescripción del tratamiento. Por último, la externalización del tratamiento antiviral en el CAID, mediante la toma presencial del mismo y el seguimiento por sus médicos habituales, aprovechando sus revisiones y sin necesidad de citas duplicadas.
Se pudo comprobar la eficacia del nuevo plan asistencial coordinado CAID-AE, ya que todos los pacientes completaron el estudio y realizaron el tratamiento en un corto periodo de tiempo y es superior al circuito clásico de derivación.
En cuanto a la prevalencia del VHC en la PID, los datos de nuestro estudio coinciden con series publicadas previamente que describen una elevada tasa de seroprevalencia y prevalencia de infección activa en esta población, quizá nuestro estudio refleja cifras de seroprevalencia algo menores que en otras series, es probable que tenga que ver con la inclusión de la totalidad de los pacientes del CAID, que no necesariamente son todos consumidores de droga por vía parenteral.
En cuanto a las características clínicas de los pacientes con VHC del CAID de nuestra área, si se compara con el resto de la población con VHC, se trata de una población más joven, con predominio de varones, menor grado de fibrosis, con patología dual, en ocasiones con consumo activo de drogas, en terapia sustitutiva con metadona y en tratamiento con psicofármacos. Dadas las características de esta población, es de gran importancia simplificar circuitos asistenciales que faciliten el acceso al sistema, al tratarse de una población estigmatizada, con poca tendencia a buscar ayuda médica, con un entorno social, laboral y familiar muy inestable, muy desinformada en lo referente a su enfermedad en cuanto a diagnóstico, pronóstico, y a la existencia actual de tratamientos actuales seguros y eficaces.
A pesar de estas características, los pacientes fueron adherentes, presentaron buena tolerancia, y no presentaron efectos secundarios graves. El tratamiento con AAD es seguro y efectivo en población en TSO y con consumo activo de drogas17, siendo además pautas de tratamiento sencillas y cortas, lo cual permite la participación de más profesionales en su prescripción (médicos del CAID, MAP, farmacéuticos).
Aparte de los beneficios relacionados, la curación de VHC, existen otros en la PID, como son la reducción de las conductas de riesgo de uso de drogas18 y la prevención de la transmisión de la infección de los que mantienen conductas de riesgo. Es muy importante aprovechar el contacto de estos pacientes con el sistema para informar del riesgo de reinfección (0-5% personas/año) si se mantienen conductas de riesgo19,20, informar sobre la reducción de daños, como son la existencia de equipos estériles y abordar otros temas de salud como son el riesgo de transmisión de otras infecciones (VHB/VIH).Dentro de las limitaciones de nuestro estudio está el escaso número de pacientes incluidos en el nuevo circuito, y dentro de las fortalezas está el diseño del nuevo circuito de derivación, en el cual se han establecido mejoras en diferentes puntos del mismo, como son el diagnóstico en un solo paso, la ubicación conjunta de servicios, y la externalización del tratamiento. Gracias al diseño del estudio y los resultados, este modelos de salud que se implementa en el contexto de la investigación y se convierte en la práctica clínica habitual, resulta un buen ejemplo de «Implementation Science».
El actual trabajo muestra que el nuevo plan asistencial coordinado CAID-AE presenta una alta efectividad cuando se compara con el circuito clásico de derivación, que la seroprevalencia y prevalencia de infección activa en la población del CAID es muy elevada y que los tratamientos actuales con AAD son efectivos y seguros. En cuanto a las características de la población, se trata de una población más joven, con menos fibrosis, con patología dual, en ocasiones con consumo activo, en terapia sustitutiva con metadona y con psicofármacos.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A los autores por la recogida de datos y la lectura crítica del artículo.