El síndrome de Leriche, consecuencia de la oclusión de la aorta abdominal o de ambas ilíacas, puede producirse de forma aguda, lo que conlleva un aumento de la morbimortalidad asociada. Aunque poco frecuente, el cuadro clínico en ocasiones es solo neurológico, manifestándose como una paraparesia aguda sin dolor asociado, lo cual generalmente produce un retraso diagnóstico y terapéutico, con el consecuente empeoramiento en el pronóstico del paciente. La cirugía abierta de forma urgente continúa siendo la primera opción terapéutica, aunque hay casos descritos de reparación endovascular. A pesar de ello, esta enfermedad presenta un mal pronóstico, con una mortalidad en torno al 30-50% en los primeros 30 días. Presentamos 3 casos clínicos de síndrome de Leriche agudo que se manifestaron como paraparesia aguda.
Leriche syndrome, a consequence of occlusion of the abdominal aorta and/or iliac, can occur acutely, leading to an increase in the associated morbidity and mortality. Although uncommon, the symptomatology is sometimes only neurological, manifesting itself as an acute paraparesis without associated pain. This generally leads to a diagnostic and therapeutic delay, with the consequent worsening of patient prognosis. Urgent open surgery continues to be the first therapeutic option, although there are reported cases of endovascular repair. Despite this, the condition has a poor prognosis with a 30-day mortality of around 30-50%. The clinical cases are presented of 3 patients with acute Leriche syndrome that manifested as acute paraparesis.
El síndrome de Leriche es una manifestación poco frecuente de la enfermedad arterial periférica (EAP) que se produce por la oclusión de aorta abdominal o ambas ilíacas. Su presentación habitual es de forma crónica con la tríada clásica: claudicación intermitente gemelar, claudicación glútea y disfunción eréctil; presenta una elevada morbimortalidad asociada (30% de mortalidad en los primeros 30 días)1. En ocasiones, puede iniciar de manera aguda, generalmente mediante isquemia aguda de miembros inferiores (MMII) o intestinal (isquemia mesentérica o perforación). La presentación con síntomas neurológicos se da en <10% de los casos1,2 y cursa con clínica de paraparesia aguda, disminución de reflejos osteotendinosos (ROT) o alteraciones del equilibrio. En estos casos, el pronóstico del paciente empeora y se le añade dificultad a su diagnóstico, con el consecuente retraso en el tratamiento3.
Se presentan 3pacientes que acuden a urgencias de nuestro centro con un cuadro clínico de paraparesia aguda secundaria a síndrome de Leriche, que todos precisaron intervención quirúrgica urgente.
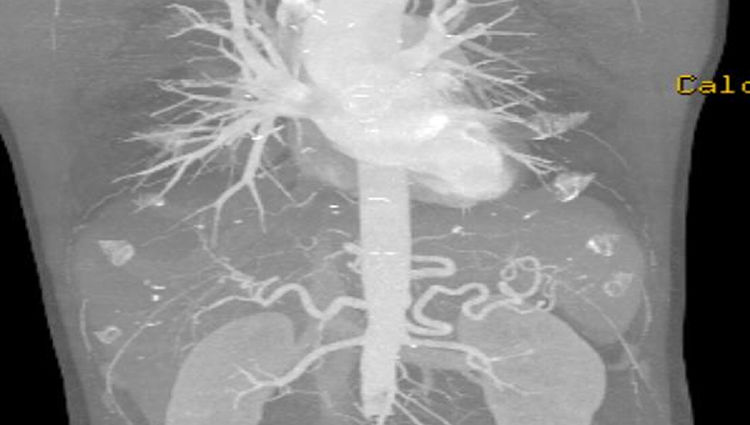
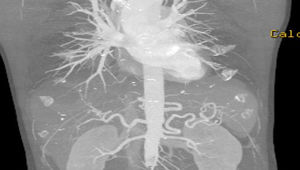
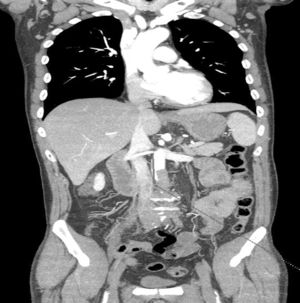
Casos clínicosCaso clínico 1Varón de 54 años, hipertenso, diabético, sin arritmia conocida, con claudicación neurógena por estenosis de canal lumbar, en seguimiento por neurocirugía y cardiopatía isquémica crónica revascularizada percutáneamente con fracción de eyección conservada en el último estudio ecográfico. El paciente acude a Urgencias por un cuadro de diarrea de una semana de evolución, con aparición brusca de déficit sensitivo-motor de ambos MMII. En la exploración física presenta mal estado general, con paraparesia, hipoestesia y ROT disminuidos en ambos MMII. Destaca pulso femoral izquierdo débil, con ausencia del resto, leve cianosis reversible en pulpejos y enlentecimiento del relleno venocapilar. En la analítica se observa leucocitosis (18×103/μl con 85% de neutrófilos), empeoramiento de la función renal y pancreática: 4,71mg/dl de creatinina, 3,371 UI/l de CPK, 1,153 UI/l de amilasa y 3,415 UI/l de lipasa. Se solicitó angiotomografía computarizada (angio-TC) urgente que evidenció la oclusión ilíaca izquierda en todo su trayecto y la ilíaca común derecha debido trombosis arterial aguda sobre un lecho crónico de lesiones por arterioesclerosis, además de datos compatibles con pancreatitis aguda (fig. 1). Tras comentar el caso con el Servicio de Cirugía Vascular, se decidió realizar intervención quirúrgica urgente mediante trombectomía transfemoral bilateral y plastia de arteria femoral común izquierda con parche de dacrón. Tras la intervención, el paciente recuperó el pulso femoral bilateral, sin recuperación completa de motilidad ni sensibilidad, permaneciendo en la Unidad de Reanimación durante 15 días por el episodio de pancreatitis. Además, presentó un cuadro de colitis isquémica derecha que precisó una hemicolectomía derecha; esta clínica isquémica se debe a la oclusión hipogástrica izquierda y a la afectación de regiones distales mesentéricas por el cuadro de bajo gasto cardiaco secundario a la administración de fármacos vasoactivos durante su estancia en la Unidad de Reanimación. Fue dado de alta a los 30 días tras iniciar tratamiento por rehabilitación, que completó de forma ambulatoria hasta lograr la recuperación neurológica completa a los 2 meses. A los 2años el paciente continúa con el sector aortoilíaco permeable, con pulsos femorales palpables y buena perfusión distal, sin otras complicaciones.
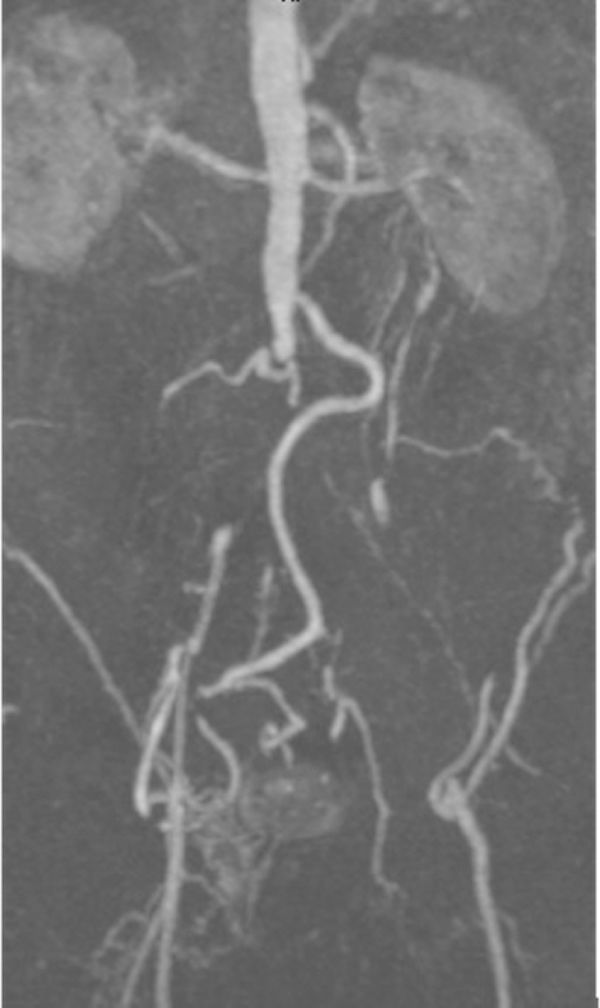
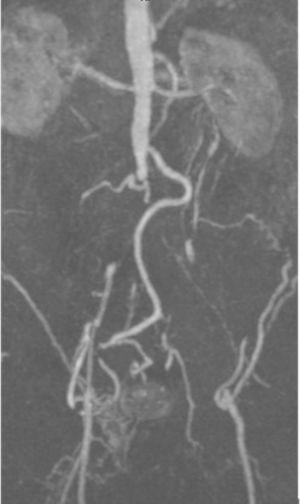
Caso clínico 2Varón de 58 años, diabético, dislipidémico, sin cardiopatía conocida y fumador activo de 20 cigarrillos al día, en seguimiento en consultas externas de Cirugía Vascular por isquemia crónica de grado iia de la escala de Fontaine de ambos MMII, sin pulsos en MMII. El paciente acudió a Urgencias por un cuadro de 15 días de evolución de imposibilidad para la bipedestación, con dolor leve en ambos MMII. En la exploración física presentaba paraparesia de ambos MMII con hipoestesia, alteración del equilibrio y disminución de reflejos osteotendinosos, ausencia de pulsos a todos los niveles, con leve enlentecimiento del relleno capilar y venoso. En la analítica se observa ausencia de leucocitosis, leve empeoramiento de la función renal: 1,98mg/dl de creatinina y 608 UI/l de CPK. Fue ingresado a cargo del Servicio de Neurología diagnosticado de paraparesia idiopática. En las siguientes horas, el paciente presentó empeoramiento clínico con aumento del dolor y, ante la sospecha de amiotrofia diabética, se solicitó resonancia magnética medular (RM) y angio-TC, donde se visualizó oclusión completa de la luz aórtica a nivel yuxtarrenal, con repermeabilización en ambas arterias femorales comunes, y se descartó enfermedad medular, hallazgos compatibles con trombosis arterial aguda en un paciente con arterioesclerosis previa ya conocida (fig. 2). Ante dichos hallazgos, se consultó con el Servicio de Cirugía Vascular, practicándose de forma urgente trombectomía aórtica con pinzamiento suprarrenal y bypass aortobifemoral con prótesis de dacrón (16×8mm) a arterias femorales profundas. Tras la intervención, el paciente evolucionó favorablemente, recuperó el pulso femoral bilateral y también recuperó la motilidad y la sensibilidad de ambos MMII. Fue dado de alta a los 13días y en el control a los 2 años presenta bypass permeable, sin déficits neurológicos residuales.
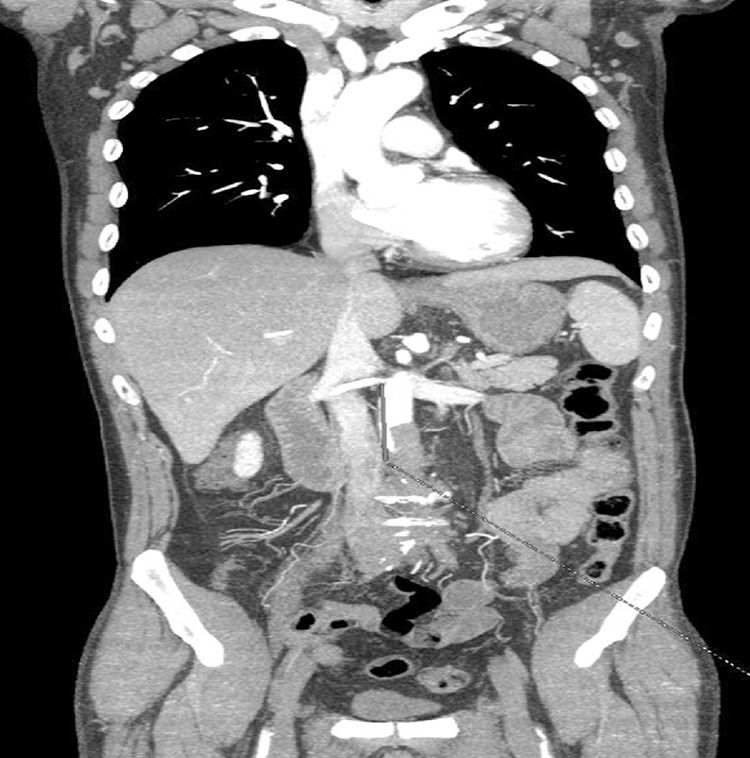
Caso clínico 3Varón de 55 años, exfumador y sin otros antecedentes personales de interés. Acudió a Urgencias por un cuadro brusco de 6 h de evolución caracterizado por dolor tipo «latigazo» en la región lumbar, dolor leve y paraparesia de ambos MMII. En la exploración física presentaba paraparesia de MMII con anestesia de los mismos y abolición completa de reflejos osteotendinosos, además de ausencia de pulsos a todos los niveles, con palidez y leve enlentecimiento del relleno capilar y venoso en ambos MMII. En la analítica se observa leucocitosis (14×103/μl con 92% de neutrófilos), empeoramiento de la función renal: 2,15mg/dl de creatinina, 1,245 UI/l de CPK. El paciente presentaba un brote de virus varicela zóster a nivel costal derecho de una semana de evolución, por lo que fue ingresado con sospecha de síndrome de Guillain-Barré y se solicitó una RM medular que descartó lesión nerviosa. Posteriormente, ante el empeoramiento del dolor, se solicitó una angio-TC que mostró oclusión completa aórtica a nivel infrarrenal con repermeabilización en ambas arterias ilíacas externas, y se diagnosticó de síndrome de Leriche agudo sin causa etiológica demostrada (fig. 3). Tras la valoración por el Servicio de Cirugía Vascular, se decidió la realización de una intervención quirúrgica urgente, mediante trombectomía transfemoral bilateral simultánea, con control radiológico, sin lograr la completa extracción de material trombótico a nivel infrarrenal, por lo que se realizó bypass aortobifemoral con prótesis de dacrón (16×8mm) y fasciotomía muscular bilateral infragenicular. Tras la intervención, el paciente recuperó el pulso pedio y presentó remisión completa de la paraparesia y la anestesia de MMII. A pesar de ello, desarrolló un síndrome de isquemia pélvica y fracaso multiorgánico, con mala evolución a pesar de manejo sistémico intensivo y fasciotomías glúteas, falleciendo a las 72 h. En el caso de este paciente, creemos que la mala evolución puede ser secundaria tanto al tiempo de retraso en el diagnóstico que conlleva un mayor estado isquémico, como también al nivel de afectación de oclusión aórtica y ambas arterias hipogástricas.
DiscusiónEl síndrome de Leriche es una manifestación poco frecuente de la EAP (< 1%)1, que se caracteriza por la oclusión total de la luz aórtica o ilíacas de manera aguda o crónica. La manifestación aguda se presenta en <0,01% de los casos de EAP1 y conlleva una alta morbimortalidad. Fue descrito por primera vez por Quain en 1847, pero no fue hasta 1923 cuando Rene Leriche desarrolló su estudio más profundamente2. Su etiología principal es la ateroesclerosis, aunque se ha relacionado también con la hipoplasia aórtica, la radiación, la infección congénita de la rubéola, la sífilis aórtica, la enfermedad de Ormond (fibrosis retroperitoneal), la enfermedad de Buerger y la arteritis de Takayasu. Los casos agudos habitualmente se deben a trombosis arterial sobre un lecho con lesiones por arterioesclerosis, como 2de los casos descritos en nuestro trabajo. También hay casos secundarios a embolias, disecciones y trombosis agudas, como en nuestro tercer paciente, cuya etiología concreta no se esclareció3-5.
La presentación clínica dependerá tanto de la localización de la oclusión aórtica como del tiempo de evolución. Respecto a la localización, lo habitual es que se produzca a nivel perirrenal (52%): suprarrenal (11%), infrarrenal (25%) o difuso (14%). Y esta localización influirá en la gravedad clínica, ya que en los casos con oclusión más proximal existirá una mayor afectación orgánica. En lo que se refiere a la clínica habitual, esta se suele presentar mediante la tríada clásica de claudicación intermitente glútea o gemelar de MMII, disfunción eréctil y ausencia o disminución de pulsos femorales. En ocasiones se asocia a hiperetensión arterial refractaria, dolor de reposo o lesiones tróficas en MMII. En cambio, en los casos de síndrome de Leriche agudo la presentación generalmente es de isquemia aguda de MMII. Si la clínica de presentación es de tipo neurológico, manifestación que es muy ocasional (0,01% de los casos de EAP), esta se caracteriza por paraparesia o paraplejía de MMII, arreflexia, disminución de la percepción del dolor a nivel espinotalámico y alteraciones del sistema nervioso autónomo (incontinencia de esfínteres, íleo paralítico). En algunas publicaciones, el cuadro clínico agudo se engloba dentro del «síndrome espinal arterial anterior» por oclusión de la arteria anterior espinal, aunque actualmente se cree que esta manifestación se deba a un cuadro de isquemia aguda a nivel de la circulación colateral pélvica (arteria mesentérica inferior, arterias hipogástricas y arterias femorales). La presentación neurológica del síndrome de Leriche agudo precisa una alta sospecha diagnóstica, ya que el retraso en su tratamiento empeora el pronóstico con aumento de la afectación isquémica. Habitualmente, no se incluye en el diagnóstico diferencial de la clínica, lo que conlleva un retraso diagnóstico que implica un aumento de la morbimortalidad6,7. En el diagnóstico diferencial es importante conocer las características de cada entidad clínica para poder adelantar el diagnóstico: la mielopatía aguda espinal cursa con dolor agudo lumbar o torácico de moderada cuantía, ROT presentes y buena perfusión distal, mientras que el síndrome de Leriche agudo cursa con dolor glúteo o de MMII intolerable, ROT disminuidos y mala perfusión periférica8. Para su diagnóstico, la arteriografía continúa siendo el «gold standard», pero rara vez se realiza, recomendándose pruebas menos invasivas, como eco-Doppler, angio-TC (de referencia) o angio-RM (según las disponibilidades del centro). Todas estas pruebas deberán ir precedidas de una aproximación diagnóstica clara, ya que lo habitual es que el diagnóstico de la oclusión aórtica sea un hallazgo incidental9,10. El tratamiento de revascularización se debe realizar de forma urgente para reducir el riesgo de complicaciones. Disponemos de técnicas de cirugía abierta, como trombectomía transfemoral, bypass aortobifemoral o derivación extraanatómica, en pacientes de alto riesgo quirúrgico sin posibilidad de abordaje endoluminal. En el primer caso descrito se logró un buen resultado con la trombectomía, como el publicado por Chien-Hung et al., aunque precisó de reparación femoral izquierda mediante plastia por la presencia de placas ateroescleróticas estenosantes. En el segundo caso, se decidió la realización de bypass aortobifemoral por presentar una oclusión aórtica conocida desde hace años, descartándose por ello la posibilidad de tratamiento endovascular.
La terapia endovascular ofrece menor agresividad y continúa en desarrollo. Generalmente, se realiza un tratamiento híbrido mediante trombectomía transfemoral o aórtica con implantación de endoprótesis o stents, aunque es necesario que las características anatómicas de las lesiones lo permitan. Destacamos que, a pesar de las múltiples opciones técnicas, la presentación aguda con paraparesia del síndrome de Leriche conlleva una alta morbimortalidad en los primeros 30 días por: síndrome de respuesta inflamatoria sistémica, rabdomiólisis masiva o fallo multiorgánico11.
ConclusiónLa inclusión de esta entidad en el diagnóstico diferencial conlleva un diagnóstico precoz y es un marcador pronóstico clave para disminuir la elevada morbimortalidad que presenta. Así pues, una exploración física vascular básica en todo paciente con clínica de paraparesia es imprescindible para adelantar su diagnóstico y con ello la revascularización urgente.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.