Circulating RNAs (cfRNAs) have emerged as promising biomarkers in liquid biopsy for prostate cancer (PCa). However, the lack of standardization in their analysis and the heterogeneity across available studies limit clinical application.
ObjectiveTo evaluate the diagnostic and prognostic utility of the total concentration of cell-free circulating small RNA (cf-sRNA) and microRNA (cf-miRNA) in plasma and urine from PCa patients using accessible techniques, without identifying specific miRNAs.
Materials and methodsProspective, longitudinal study including 143 men (111 with PCa and 32 healthy controls). Plasma and urine cf-sRNA and cf-miRNA levels were quantified with an Agilent 2100 Bioanalyzer. Levels were correlated with clinical features, tumor stage, and progression to metastatic castration-resistant PCa (mCRPC). A longitudinal follow-up was conducted in a metastatic subgroup.
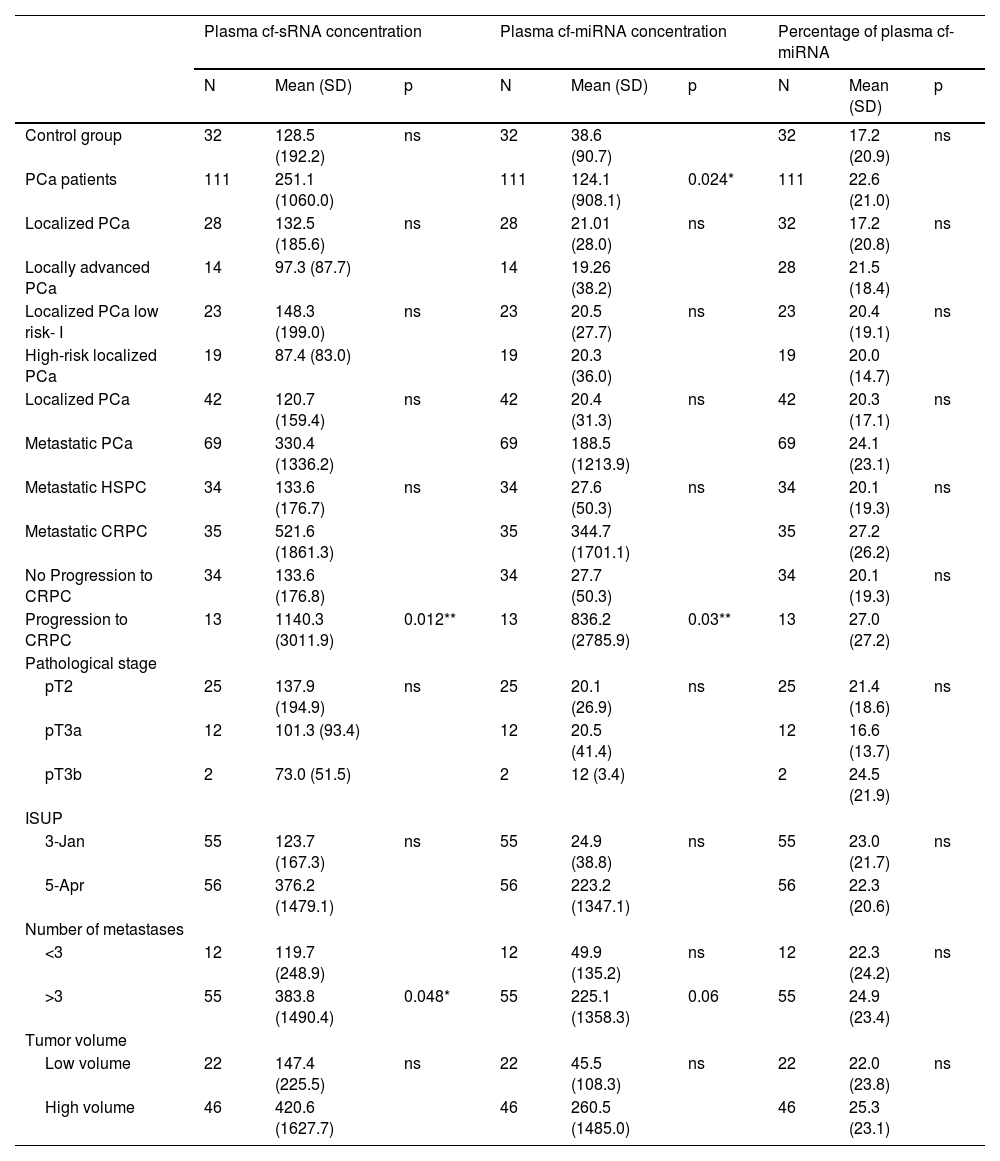
ResultsPlasma and urine levels of cf-miRNA and cf-sRNA were significantly higher in patients with advanced PCa, particularly in those who progressed to mCRPC (p < 0.05). During follow-up, a significant increase in plasma cf-miRNA was observed after treatment (p = 0.031), as well as an increase in the relative percentage of cf-miRNA in urine (p = 0.012).
ConclusionsTotal quantification of cf-miRNA in plasma and urine is an accessible strategy with potential value as a dynamic biomarker for PCa monitoring and prognosis. Its use could complement current diagnostic tools, although further studies are required to validate its utility in clinical practice.
Los ARN circulantes (cfRNA) han emergido como biomarcadores, en biopsia líquida, prometedores en el cáncer de próstata (CaP). Sin embargo, la falta de estandarización en su análisis y la heterogeneidad en los distintos estudios disponibles limita su aplicación clínica.
ObjetivoEvaluar la utilidad diagnóstica y pronóstica de la concentración total de smallRNA (cf-sRNA) y microRNA (cf-miRNA) libres circulantes en plasma y orina de pacientes con cáncer de próstata (CaP), mediante técnicas accesibles, sin identificación de miRNA específicos.
Material y métodosEstudio prospectivo, longitudinal, que incluyó 143 varones (111 con CaP y 32 controles sanos). Se cuantificaron los niveles de cf-sRNA y cf-miRNA en plasma y orina mediante bioanalizador Agilent 2100. Se correlacionaron los niveles con características clínicas, estadio tumoral y progresión a CaP resistente a la castración (CPRCm). Se realizó seguimiento longitudinal en un subgrupo de pacientes metastásicos.
ResultadosLos niveles plasmáticos y urinarios de cf-miRNA y cf-sRNA fueron significativamente superiores en pacientes con CaP avanzado, particularmente en aquellos que progresaron a CPRCm (p < 0,05). En el seguimiento, se observó un incremento significativo del cf-miRNA plasmático tras el tratamiento (p = 0,031), así como un aumento del porcentaje relativo de cf-miRNA en orina (p = 0,012).
ConclusionesLa cuantificación total de cf-miRNA en plasma y orina representa una estrategia accesible, con potencial valor como biomarcador dinámico en el seguimiento y pronóstico del CaP. Su uso podría complementar las herramientas diagnósticas actuales, aunque se requieren estudios adicionales para validar su utilidad en la práctica clínica.