Clostridium difficile es la primera causa de diarrea nosocomial en los países desarrollados y uno de los principales agentes etiológicos de diarrea comunitaria. La irrupción de la cepa hipervirulenta BI/NAP1/027 ha dado lugar a un incremento de la morbimortalidad de la infección por C.difficile (ICD). Este documento pretende revisar tanto los principales cuadros clínicos de la ICD como el diagnóstico de laboratorio, incluyendo la toma de la muestra, su transporte y conservación, su procesamiento, los distintos procedimientos diagnósticos disponibles, las pruebas de sensibilidad a antibióticos y la caracterización molecular de los aislados. El propósito principal de los autores ha sido elaborar un documento eminentemente práctico que dé respuesta a las principales dudas que surgen en el diagnóstico de laboratorio de la ICD.
Clostridium difficile is the leading cause of nosocomial diarrhoea in developed countries, and is one of the main aetiologic agents of community diarrhea. The eruption of the hypervirulent strain BI/NAP1/027 has given rise to an increase in the morbidity and mortality of C.difficile infection (CDI). This document aims to review the main clinical pictures of CDI and the laboratory diagnosis, including sampling, transport and storage of specimens, specimen processing, diagnostic procedures, antimicrobial susceptibility testing, and molecular characterisation of the isolates. The main purpose of the article is to develop a practical document that provides answers to the main questions that arise in the laboratory diagnosis of CDI.
Clostridium difficile es la primera causa de diarrea hospitalaria en los países desarrollados y una etiología cada vez más frecuente de diarrea comunitaria. La irrupción de la cepa hipervirulenta de C.difficile NAP1/BI/027 en Canadá a principios de este siglo y su rápida propagación al resto de países ha contribuido enormemente al aumento de la morbimortalidad de la infección por C.difficile (ICD)1. La prevención, factor clave en la reducción de la incidencia de la ICD, ha de estar basada en un óptimo diagnóstico de esta infección y, por tanto, en una correcta sospecha clínica del episodio y un diagnóstico de laboratorio rápido y certero que se acompañe de una información rápida del resultado tanto al clínico como al preventivista y al personal de enfermería2. El presente documento realiza una revisión de los aspectos clínicos de la ICD y profundiza en las diferentes etapas del diagnóstico de laboratorio de la ICD, incluyendo la toma inicial de la muestra, su procesamiento en el laboratorio, la caracterización fenotípica de los aislados toxigénicos, incluida la realización de pruebas de sensibilidad, y, finalmente, su caracterización molecular.
Consideraciones clínicasLa ICD puede cursar con diferentes manifestaciones clínicas que comprenden desde una diarrea leve o moderada a colitis pseudomembranosa fulminante, megacolon tóxico y muerte3,4. El tipo de enfermedad y su gravedad dependerán tanto de factores del microorganismo como del paciente, principalmente de la virulencia de la cepa infectiva y de la respuesta inmune del hospedador. El contacto con esporas de una cepa de C.difficile junto con la alteración de la microbiota colónica permite la colonización y posterior infección por este microorganismo. Las cepas toxigénicas de C.difficile poseen un locus de patogenicidad (PaLoc) con los genes de las toxinas A y B (tcdA y tcdB), exotoxinas que principalmente causan la sintomatología de la ICD. Además, algunas cepas producen la denominada toxina binaria, cuyo papel en la patogénesis no está todavía muy claro5. Otros factores de virulencia importantes que contribuyen a la patogénesis incluyen adhesinas, fimbrias, flagelos, cápsula y proteínas de la capa superficial. En torno al 1-3% de la población general y el 20% de los pacientes hospitalizados son portadores sanos de cepas toxigénicas. Además, más del 50% de los niños menores de 2años pueden ser portadores asintomáticos de este patógeno, probablemente por la falta de receptores para las toxinas en su intestino, por lo que se debe realizar el diagnóstico solamente en aquellos pacientes con diarrea en los que se hayan descartado razonablemente otras etiologías y que presenten ciertas condiciones que predispongan a la ICD, como un alto grado de inmunodepresión3. Los principales factores de riesgo para desarrollar ICD son la exposición a antibióticos de amplio espectro, la hospitalización prolongada, el ingreso en una unidad de cuidados intensivos, la proximidad física de un individuo infectado, la edad avanzada, la gravedad de enfermedades subyacentes, la inmunosupresión, una escasa respuesta inmune a las toxinas, los procedimientos gastrointestinales no quirúrgicos y el uso de antiácidos3,4. Aunque el contacto con centros sociosanitarios es un factor de riesgo muy importante de desarrollo de la ICD, las infecciones adquiridas en la comunidad (infecciones producidas en pacientes que no han pernoctado en un centro sociosanitario en las últimas 12 semanas previas al comienzo de la infección) constituyen en torno al 25% del total de casos de ICD y se dan en pacientes que no presentan los factores de riesgo tradicionales, ya que suele afectar a pacientes jóvenes y sin tratamiento antibiótico.
La ICD de origen intestinal se clasifica según diferentes criterios de gravedad (tabla 1) con el fin de poder valorar la necesidad de tratamiento, el tipo de terapia antimicrobiana o la necesidad de cirugía o ingreso en una unidad de cuidados intensivos3,4. Las manifestaciones clínicas van desde una diarrea leve-moderada a cuadros más severos con presencia de dolor abdominal, fiebre y leucocitosis. La enfermedad leve se caracteriza por presentar diarrea en ausencia de síntomas y signos de colitis, mientras que los pacientes con enfermedad moderada suelen presentar diarrea con evidencia de colitis caracterizada por fiebre y cólico abdominal. Algunos signos típicos de la ICD leve-moderada son leucocitosis <15.000cel/μl y niveles de creatinina sérica por debajo de 1,5 veces los niveles premorbilidad. Las manifestaciones sistémicas suelen aparecer en caso de enfermedad moderada o grave. La evidencia de colitis grave incluye fiebre (de hasta 40°C), cólico abdominal, leucocitosis ≥15.000cel/μl, hipoalbuminemia (con niveles de albúmina sérica <2,5mg/dl), presencia de leucocitos en heces e inflamación colónica visualizada por endoscopia (para pseudomembranas) o tomografía axial computarizada (para observar el engrosamiento de la pared del colon). La presencia de colitis pseudomembranosa puede ser suficiente para el diagnóstico de la ICD en ausencia de otra causa evidente y se diagnostica mediante endoscopia, tras colectomía o bien en la autopsia. La enfermedad fulminante por C.difficile ocurre en menos del 5% de los pacientes y cursa con dolor abdominal severo, diarrea abundante (aunque en ocasiones puede cursar sin diarrea), mientras el paciente progresa rápidamente al desarrollo de íleo o megacolon tóxico que puede llevar a sepsis, shock o muerte.
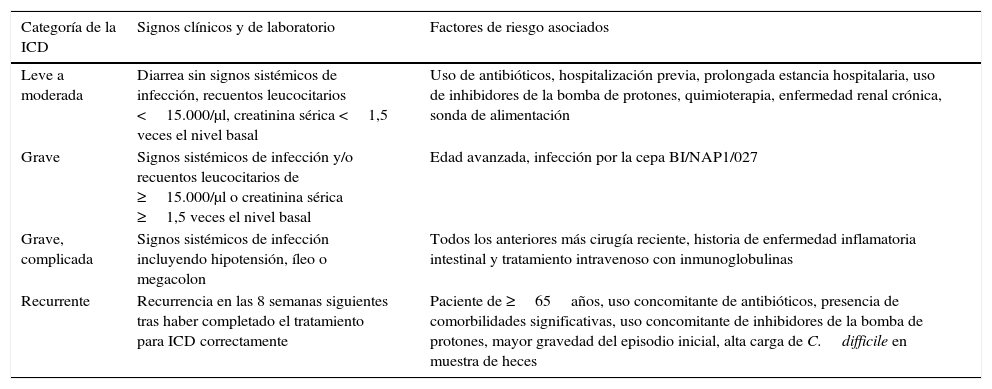
Clasificación de la infección por Clostridium difficile (ICD)según la gravedad de la enfermedad
| Categoría de la ICD | Signos clínicos y de laboratorio | Factores de riesgo asociados |
|---|---|---|
| Leve a moderada | Diarrea sin signos sistémicos de infección, recuentos leucocitarios <15.000/μl, creatinina sérica <1,5 veces el nivel basal | Uso de antibióticos, hospitalización previa, prolongada estancia hospitalaria, uso de inhibidores de la bomba de protones, quimioterapia, enfermedad renal crónica, sonda de alimentación |
| Grave | Signos sistémicos de infección y/o recuentos leucocitarios de ≥15.000/μl o creatinina sérica ≥1,5 veces el nivel basal | Edad avanzada, infección por la cepa BI/NAP1/027 |
| Grave, complicada | Signos sistémicos de infección incluyendo hipotensión, íleo o megacolon | Todos los anteriores más cirugía reciente, historia de enfermedad inflamatoria intestinal y tratamiento intravenoso con inmunoglobulinas |
| Recurrente | Recurrencia en las 8 semanas siguientes tras haber completado el tratamiento para ICD correctamente | Paciente de ≥65años, uso concomitante de antibióticos, presencia de comorbilidades significativas, uso concomitante de inhibidores de la bomba de protones, mayor gravedad del episodio inicial, alta carga de C.difficile en muestra de heces |
Fuente: adaptado de Bagdasarian et al.25.
El riesgo de recurrencia oscila entre un 20% tras la infección inicial a un 60% tras la primera recurrencia y es mayor en pacientes con edad avanzada, en episodios iniciales graves de ICD, el uso concomitante de antibióticos y una alta carga de C.difficile en muestra de heces2.
Las manifestaciones extraintestinales representan menos del 1% de las ICD y afectan principalmente a pacientes hospitalizados que han sufrido una manipulación quirúrgica reciente del tracto gastrointestinal y con factores de riesgo comunes a la ICD intestinal6. Los factores de virulencia responsables de las infecciones extraintestinales no se conocen bien, aunque se han descrito numerosos casos en los que la infección está causada por cepas de C.difficile no toxigénicas sugiriendo la implicación de otros factores distintos de las toxinasA y B. La mayoría de las infecciones se caracterizan por afectar a la región abdominopélvica debido, generalmente, a una perforación intestinal a partir de una infección o a una filtración tras cirugía. También se han descrito casos de infección de herida por contaminación por heces, o de bacteriemia, pudiendo producirse infecciones en otras localizaciones mediante diseminación por bacteriemias transitorias.
Recogida de la muestraLas muestras adecuadas para el diagnóstico de laboratorio de la diarrea producida por C.difficile son heces acuosas, sueltas o no formes. Se recomienda recoger una sola muestra de heces durante el curso de un mismo episodio de ICD, ya que la detección rutinaria de múltiples muestras apenas aumenta el rendimiento y puede generar falsos positivos. No se recomienda la detección de C.difficile para la confirmación de la curación postratamiento de la ICD, ya que no tiene correlación con la resolución de los síntomas. Por tanto, se han de rechazar las muestras de heces pertenecientes a todo paciente tratado diagnosticado microbiológicamente de ICD en los 7días previos. Únicamente en aquellos casos en los que no sea posible obtener muestra de heces (íleo, megacolon tóxico o distensión abdominal sin diarrea) se pueden aceptar muestras rectales. En pacientes que presentan colitis la detección de C.difficile en biopsias colónicas es menos sensible que en muestras de heces2-4.
Transporte y conservación de la muestraLas muestras de heces deben transportarse en recipientes estériles, de cierre hermético y sin medio de transporte. También son aceptables las muestras recogidas en recipientes con medio de transporte para enteropatógenos aerobios como, por ejemplo, el medio de Cary-Blair. Las muestras transportadas en medios esporicidas, como algunos medios de transporte para parásitos que contienen formaldehído, deben ser rechazadas. El transporte de las muestras debe realizarse lo antes posible al laboratorio de microbiología. En general, se recomienda conservar la muestra en frío (2-8°C) durante las primeras 48-72h o congelada (de −60 a −80°C) si no se va a procesar la muestra durante las 72h posteriores a su recogida2-4.
Manejo de la muestra en su recepción en el laboratorio de microbiologíaLas muestras deben procesarse lo antes posible. Dado que existe un importante infradiagnóstico clínico de la ICD, especialmente en aquellos pacientes sin ningún factor de riesgo tradicional, se recomienda procesar para diagnóstico de la ICD todas las muestras procedentes de pacientes con diarrea independientemente de su edad (salvo menores de 2años), su origen (hospitalizado o no) o la petición microbiológica del clínico demandante2,7. Las muestras de heces deben filtrarse mediante un filtro de membrana en caso de que se vaya a realizar el ensayo directo de citotoxicidad. Si se va a realizar un cultivo de las muestras puede realizarse optativamente un pretratamiento de las heces mediante shock con etanol absoluto homogeneizando volúmenes iguales de muestra durante 5min (son tan eficaces como 60min), o mediante choque térmico (15min/80°C) con el fin de incrementar la selectividad de la siembra. Se recomienda realizar el diagnóstico de la ICD al menos una vez al día, incluidos los fines de semana y los festivos, aunque lo ideal es realizar el diagnóstico conforme la muestra se recibe en el laboratorio.
Pruebas diagnósticas de la infección por Clostridium difficileEl diagnóstico de la ICD suele basarse en, al menos, 2 criterios: por un lado, la detección de la toxina y/o aislamiento de C.difficile toxigénico en heces en ausencia de otra causa para la diarrea o la evidencia colonoscópica o histopatológica de colitis pseudomembranosa y, por otro, la presencia de diarrea (≥3 deposiciones no formes/24h) o la existencia de íleo o megacolon tóxico. El diagnóstico de laboratorio debe realizarse solamente en los pacientes sintomáticos (diarrea y/o dolor abdominal, frecuentemente acompañados de leucocitosis y fiebre) y en heces no formes (niveles 5 a 7 de la escala de Bristol), con la importante excepción de los casos en que haya sospecha de íleo paralítico o megacolon tóxico donde la diarrea puede no estar presente y las heces pueden estar formadas3,4.
La detección rápida de las toxinasA y/o B se lleva a cabo mediante técnicas de inmunoanálisis (IA) como, por ejemplo, técnicas inmunocromatográficas basadas en flujo lateral o técnicas de enzimoinmunoanálisis basadas en una lectura final mediante espectrofotometría o quimioluminiscencia4,8. La principal desventaja de estas técnicas es su falta de sensibilidad, con valores del 40-60% cuando se comparan con el cultivo toxigénico. Por el contrario, la especificidad de los IA suele ser superior al 90%. El comportamiento de estas técnicas puede dar lugar a un importante número de falsos positivos y falsos negativos. Los falsos positivos pueden conducir a tratamientos innecesarios de la ICD, a la retirada de otros antibióticos y al aislamiento inadecuado del paciente que, a veces, puede compartir habitación con un verdadero caso de ICD. Por otra parte, los falsos negativos pueden impedir el tratamiento de los pacientes con ICD y favorecer la diseminación del patógeno en el medio hospitalario.
Una alternativa diagnóstica es la detección de la enzima glutamato deshidrogenasa (GDH), una proteína producida de forma constitutiva y en grandes cantidades por la mayoría de las cepas de C.difficile9. La sensibilidad de su detección es elevada, con valores cercanos al 90% cuando se compara con el cultivo toxigénico; sin embargo, posee una especificidad y un valor predictivo positivo relativamente bajos debido a que detecta tanto cepas productoras como no productoras de toxinas.
Se han comercializado pruebas de inmunocromatografía para la detección simultánea de antígeno GDH y la toxinaA y/o B, cuya principal ventaja es ofrecer ambos resultados al mismo tiempo. También existen pruebas de inmunocromatografía para detectar de forma independiente las toxinasA y B en el mismo ensayo, aunque la sensibilidad global suele ser menor y el hecho de determinarlas por separado tampoco añade valor diagnóstico.
Los ensayos basados en la amplificación de los genes de las toxinas de C.difficile son pruebas bastante rápidas (entre 45min y 3h) que suelen tener como diana el gen de la toxinaB (tcdB), aunque algunos detectan el gen de la toxinaA (tcdA). Algunos equipos son capaces de detectar, además, uno o ambos genes de la toxina binaria e incluso las cepas hipervirulentas del ribotipo 027 aprovechando el hecho de que poseen mutaciones o deleciones en el gen represor tcdC10,11. Los métodos basados únicamente en la amplificación del gen tcdA pueden detectar algunas cepas A−/B+ que conserven regiones de este gen. La sensibilidad de la mayoría de los métodos moleculares suele ser superior al 90% tanto para los métodos que utilizan PCR a tiempo real como los que realizan amplificación isotérmica, mientras que la especificidad suele alcanzar el 94-99%. Por otra parte, sus valores predictivos positivo y negativo son elevados (80-95 y 95-99%, respectivamente) cuando se comparan con el cultivo toxigénico. Un resultado positivo en un paciente sintomático indica con alta probabilidad que estamos frente a un paciente con ICD, aunque podría tratarse de un paciente portador de C.difficile con el gen de la toxinaB pero que no es capaz de expresar la toxina (opción muy improbable, ya que en la actualidad existen muy pocas cepas de este tipo) y que tiene diarrea por otra causa, o bien de una mera colonización. Un resultado negativo prácticamente excluye la ICD. Su principal limitación es su elevado precio.
El ensayo de citotoxicidad, que detecta la toxinaB preformada en heces mediante la detección de su efecto citopático sobre cultivo celular, ha sido considerado durante muchos años la técnica de referencia para el diagnóstico de la ICD2. Para su realización es necesaria la utilización de una antitoxina frente a la toxinaB de C.difficile para neutralizar los efectos citopáticos inespecíficos. La principal ventaja de esta técnica es su excelente especificidad, cercana al 100%, mientras que sus principales inconvenientes son sus bajos valores de sensibilidad (50-70%), la necesidad de mantener líneas celulares (MRC-5, CHO, Vero, HEp2, HeLa, riñón de mono, etc.), su demora diagnóstica (18-72h) y, como método basado en microscopia, la subjetividad de sus resultados.
El cultivo toxigénico consiste en el cultivo de las muestras de heces y la detección de las toxinas en los aislados de C.difficile1,12. Los medios selectivos tradicionales (agar CCFA, Brazier o CCEY, con cicloserina, cefoxitina y yema de huevo) han sido desplazados por medios selectivos con sangre que, a menudo, llevan taurocolato o lisozima como favorecedores de la germinación de las esporas de C.difficile2. El pretratamiento de la muestra mediante calor o alcohol con el fin de reducir el crecimiento de la microbiota habitual es recomendable cuando los medios de cultivo tienen una baja o nula concentración de antibióticos. En medios con sangre y tras 48h de incubación, las colonias de C.difficile presentan un aspecto de un color verde-grisáceo con apariencia de vidrio esmerilado y con un olor muy característico a «cuadra de caballo» debido a la producción de p-cresol. En la tinción de Gram se observan bacilos grampositivos con esporas ovales subterminales. La detección de toxinas a partir de los aislados puede hacerse mediante el ensayo de citotoxicidad, aunque es preferible el uso de técnicas más rápidas como los IA o de técnicas de amplificación molecular. El uso de una lupa en el laboratorio resulta muy aconsejable para incrementar la sensibilidad del cultivo, ya que permite detectar tanto colonias de C.difficile ocultas entre colonias de otros microorganismos como la diferenciación entre distintos morfotipos de C.difficile. El cultivo toxigénico es una técnica muy sensible y con una alta especificidad, aunque es lenta (1-3días), laboriosa y requiere personal preparado. El cultivo toxigénico es necesario para realizar tanto monitorización de técnicas implantadas en la rutina diagnóstica como evaluaciones de otras técnicas de diagnóstico nuevas y, además, se trata de una técnica fundamental para poder realizar estudios de epidemiología molecular o sensibilidad antibiótica.
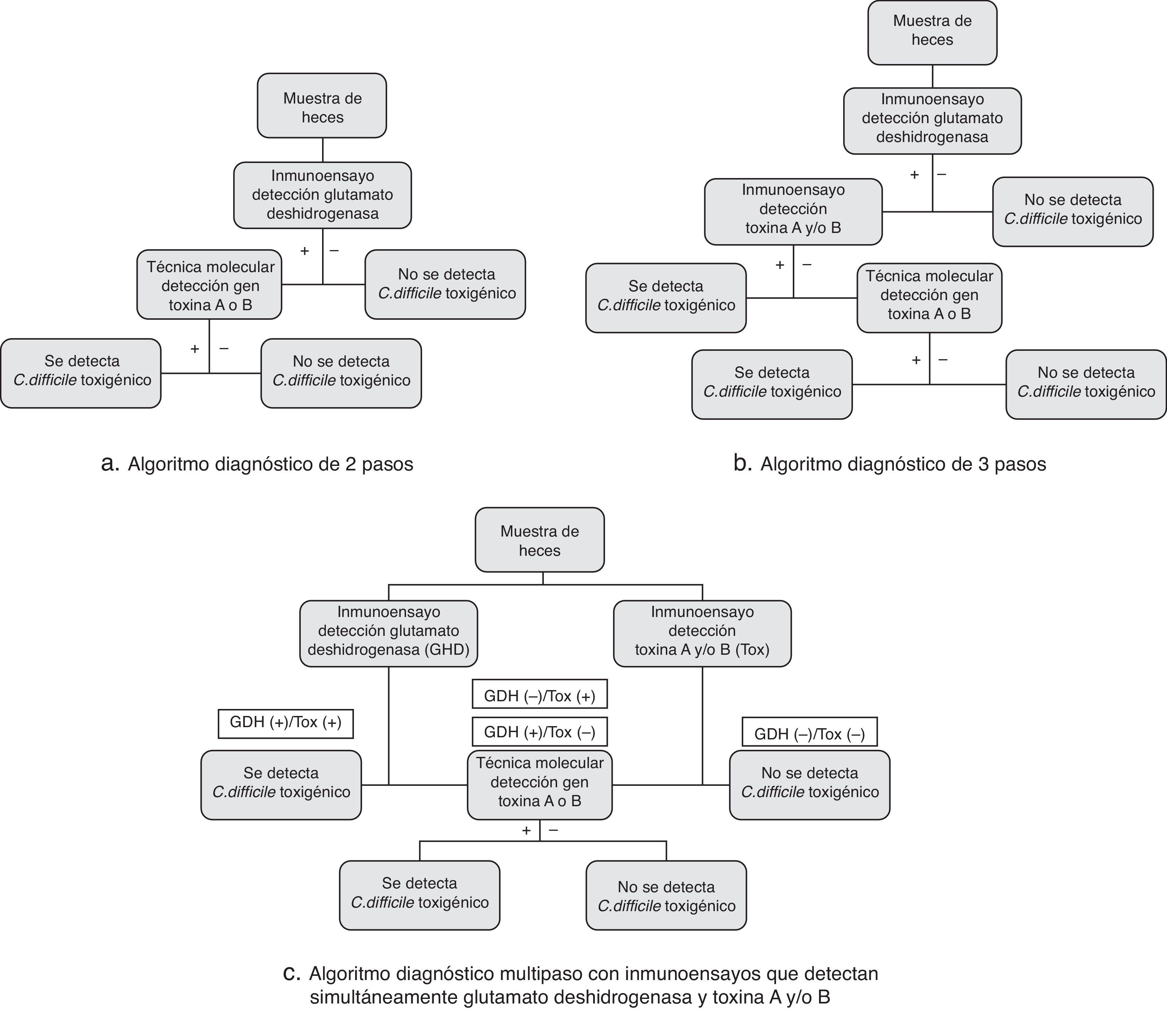
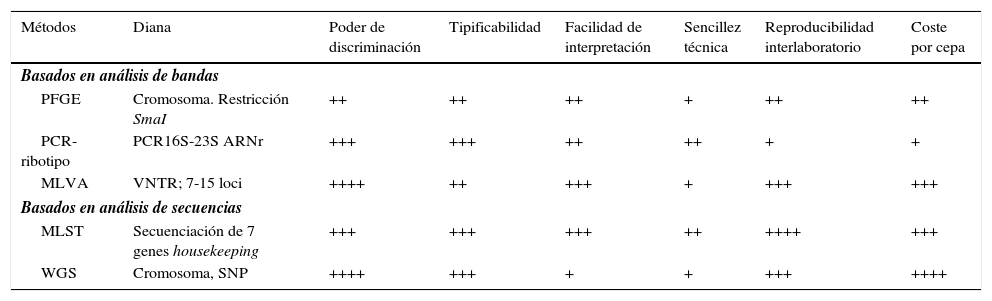
Procedimientos diagnósticos de la infección por Clostridium difficileNo existe en el momento actual ninguna técnica diagnóstica de la ICD que, por sí misma, pueda ser lo suficientemente coste-eficaz como para poder ser utilizada para el diagnóstico rápido de la ICD. Como consecuencia, se han diseñado varios algoritmos diagnósticos que aprovechan lo mejor de cada una de estas técnicas (fig. 1)13-15. La mayoría utilizan como método inicial la detección de GDH mediante IA debido a su alta sensibilidad diagnóstica, y como técnicas confirmatorias de los resultados positivos las técnicas moleculares por su elevada sensibilidad y especificidad. Estos algoritmos, denominados de 2 pasos, poseen valores de sensibilidad cercanos al 90% (sensibilidad limitada por la detección de GDH) y valores de especificidad mayores del 99%, con un precio final cercano al de las técnicas basadas en IA.
Los denominados algoritmos de 3 pasos introducen un IA que detecta las toxinasA y/o B entre la detección de GDH y la técnica molecular; de esta forma, los resultados GDH(+) son confirmados mediante este IA usándose las técnicas moleculares para las muestras con resultados discordantes [GDH(+)/Toxinas(−) o GDH(−)/Toxinas (+)]. Estos algoritmos logran reducir en casi un 50% el número de pruebas moleculares necesarias, aunque a costa del gasto añadido de los IA de las toxinas.
El uso de mezcla de muestras para analizarlas mediante técnicas moleculares es un procedimiento interesante para el diagnóstico molecular de la ICD a bajo coste16. Esta estrategia consiste en agrupar muestras de heces para analizarlas conjuntamente con una prueba molecular y así abaratar costes. Si el resultado de la prueba molecular es negativo se asigna a cada una de las muestras de la mezcla un resultado negativo, mientras que si el resultado es positivo hay que analizar individualmente cada una de las muestras. Esta estrategia, que alcanza valores de sensibilidad y especificidad cercanos a los obtenidos por las técnicas moleculares convencionales, reduce en un 40-60% el número de pruebas moleculares necesarias para el diagnóstico de la ICD.
Aunque los procedimientos diagnósticos basados en algoritmos o en análisis de mezcla de muestras constituyen las pruebas rápidas más coste-eficaces de la actualidad, su sensibilidad (90-95%) las excluye como métodos de referencia para el diagnóstico de la ICD frente a las cuales poder comparar otras técnicas2,15. Aunque el ensayo de citotoxicidad fue la primera técnica diagnóstica de la ICD considerada como método de referencia, pronto se comprobó que el cultivo toxigénico era más sensible e igual de específico. En estos últimos años se ha establecido un interesante debate entre expertos acerca del significado clínico de los resultados positivos mediante cultivo toxigénico pero negativos a partir del ensayo de citotoxicidad. Por una parte, algunos expertos consideran que solo las muestras con citotoxicidad positiva tienen toxinaB libre y, por lo tanto, pertenecen a pacientes con ICD, es decir, consideran que aquellos pacientes con muestras con citotoxicidad negativa y cultivo toxigénico positivo son pacientes sin ICD aunque colonizados por cepas «potenciales productoras de toxinaB»17. Estos expertos recomiendan que este último grupo de pacientes no sea tratado, aunque sugieren como posibilidad que sean aislados para evitar la transmisión de las cepas potencialmente patógenas a otros pacientes. Por otra parte, un número creciente de expertos considera que un resultado del ensayo de citotoxicidad negativo y del cultivo toxigénico positivo no indican tanto una ausencia de toxina libre en las heces como una concentración de toxina libre en las heces lo suficientemente baja como para no poder ser detectada por el ensayo de citotoxicidad y sí por el cultivo toxigénico2,15,18. Esta hipótesis se apoya en el hecho de la baja sensibilidad del ensayo de citotoxicidad, de la capacidad de estas cepas de producir toxinas in vitro y de la variabilidad sensitiva del ensayo de citotoxicidad en muestras seriadas de un mismo paciente. Esta teoría está siendo cada vez más aceptada y conlleva la idea de que todo paciente con un cultivo toxigénico positivo, independientemente del resultado de citotoxicidad, debe ser considerado como un posible caso de ICD que debe ser evaluado en último término por el clínico responsable del paciente.
En conclusión, no existe en la actualidad un método de referencia universalmente aceptado por todos los expertos para el diagnóstico de la ICD. Sin embargo, y aunque algunos expertos siguen considerando al ensayo de citotoxicidad como el estándar de oro del diagnóstico de la ICD, la mayor sensibilidad global del cultivo toxigénico y las cada vez más evidentes implicaciones clínicas de los resultados positivos de esta técnica (incluidos aquellos con resultado negativos del ensayo de citotoxicidad) hacen del cultivo toxigénico la técnica recomendada como estándar de oro para el diagnóstico de la ICD en este procedimiento.
Procedimientos diagnósticos en situaciones especialesAunque no existe un consenso para el diagnóstico de la ICD en pacientes con íleo o megacolon tóxico en los que no se puede obtener muestras de heces, el uso de 2 torundas rectales y la realización, si es posible, de técnicas moleculares directamente sobre una de ellas y cultivo toxigénico sobre la otra constituye un buen procedimiento diagnóstico de la ICD en este tipo de situaciones. Por otra parte, se ha demostrado que las muestras de heces son mucho más rentables que las biopsias de colon para el diagnóstico de la ICD en pacientes con colitis inespecífica, por lo que se recomienda su uso en estos pacientes2.
Debido a que las infecciones producidas por aislados de C.difficile del ribotipo 027 suelen ser más graves, transmisibles y recurrentes que las producidas por otros ribotipos, se recomienda establecer una especial vigilancia para detectarlas y, así, optimizar su tratamiento y evitar la diseminación de este clon en el ambiente hospitalario. Por tanto, en instituciones en las que exista una sospecha fundada de alto riesgo de brote (casos aislados detectados recientemente, existencia de alguna institución cercana en situación epidémica, etc.) o en el seno de un brote por este ribotipo es muy recomendable, siempre y cuando sea posible, modificar el algoritmo diagnóstico para facilitar su detección. Por una parte, conviene realizar alguna técnica molecular rápida que detecte específicamente este ribotipo, y por otra, es recomendable aplicar esta técnica a todos los resultados GDH positivos, independientemente del resultado del IA para este IA (en el caso de que el algoritmo incluya la detección de toxinas), con el fin de diagnosticar el mayor número de casos rápidamente. Otra posibilidad es la implantación de un procedimiento diagnóstico basado en un análisis mediante mezcla de muestras utilizando como técnica molecular alguna que detecte tanto el gen de la toxinaA y/o B como al ribotipo 027, aunque son necesarios más estudios para validar esta técnica en este tipo de situaciones.
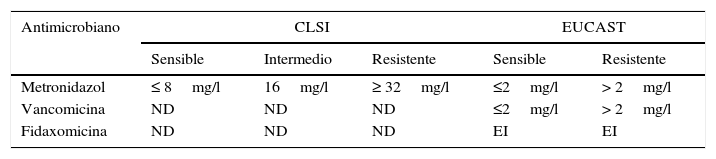
Estudios de sensibilidad in vitro a los antimicrobianosMetronidazol, vancomicina y fidaxomicina son los fármacos de elección para el tratamiento de la ICD19. Las concentraciones que alcanzan metronidazol y su metabolito (hidroximetronidazol) en la mucosa colónica son tan bajas (media de 9,3μg/g de heces acuosas y de 1,2μg/g de heces formes) que han motivado que el European Committee on Antimicrobial Susceptibility Testing (EUCAST) haya decidido reducir el punto de corte tradicional de metronidazol para C.difficile (16mg/l, recomendado por el Clinical and Laboratory Standards Institute [CLSI]) a 4mg/l (tabla 2)20. En cambio, los niveles colónicos de vancomicina y de fidaxomicina son mucho más elevados (en torno a 500mg/l para vancomicina y 3.000mg/l para fidaxomicina). Las guías internacionales recomiendan realizar estudios periódicos de vigilancia y seguimiento con el fin de conocer los patrones locales de sensibilidad a los fármacos de elección (especialmente metronidazol) y detectar cepas con CMI anormalmente altas o la aparición de resistencias21. Estos estudios de sensibilidad se deben realizar en el laboratorio de origen de los aislados si existe personal preparado o, en su defecto, por un laboratorio de referencia a un mínimo de 50-100 cepas de C.difficile. El método recomendado es el de dilución en agar, aunque el épsilon test y el método del gradiente en espiral se correlacionan muy bien con este método, por lo que pueden ser un alternativa al método de referencia.
Puntos de corte de los fármacos usados en clínica para el tratamiento de la infección por Clostridium difficile según las guías del CLSI y del EUCAST
| Antimicrobiano | CLSI | EUCAST | |||
|---|---|---|---|---|---|
| Sensible | Intermedio | Resistente | Sensible | Resistente | |
| Metronidazol | ≤ 8mg/l | 16mg/l | ≥ 32mg/l | ≤2mg/l | > 2mg/l |
| Vancomicina | ND | ND | ND | ≤2mg/l | > 2mg/l |
| Fidaxomicina | ND | ND | ND | EI | EI |
CLSI: Clinical and Laboratory Standards Institute; EI: evidencia insuficiente; EUCAST: European Committee on Antimicrobial Susceptibility Testing; ND: no datos.
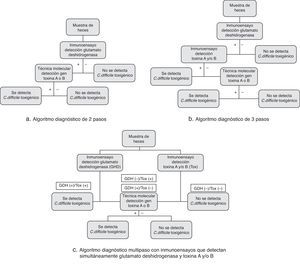
Las cepas de C.difficile son prácticamente indistinguibles fenotípicamente, por lo que, para su diferenciación, son necesarios estudios moleculares que permitan detectar brotes de la enfermedad, reconocer la diseminación de cepas de alta virulencia o transmisibilidad, establecer las cadenas de transmisión y diferenciar si una recurrencia es una recidiva causada por la misma cepa o si se debe a una reinfección con una cepa distinta. Para que un método de tipificación sea adecuado para abordar estudios de epidemiología molecular debe tener suficiente poder de discriminación, adecuada tipificabilidad (capacidad inequívoca de caracterizar la mayoría de los aislados de una población), buena reproducibilidad y exportabilidad (capacidad para obtener los mismos resultados en diferentes laboratorios y en diferentes momentos)22. Además, es deseable que sean fáciles de realizar y que su coste no sea muy elevado. Los métodos más usados para la tipificación molecular de C.difficile se pueden clasificar dependiendo de si se basan en el análisis de bandas o de secuencias (tabla 3). El método más usado en Europa y Australia es el ribotipado, mientras que en Norteamérica es la PFGE, aunque cada vez se utiliza más el ribotipado.
Características técnicas y coste de los métodos más utilizados para la tipificación molecular de Clostridium difficile
| Métodos | Diana | Poder de discriminación | Tipificabilidad | Facilidad de interpretación | Sencillez técnica | Reproducibilidad interlaboratorio | Coste por cepa |
|---|---|---|---|---|---|---|---|
| Basados en análisis de bandas | |||||||
| PFGE | Cromosoma. Restricción SmaI | ++ | ++ | ++ | + | ++ | ++ |
| PCR-ribotipo | PCR16S-23S ARNr | +++ | +++ | ++ | ++ | + | + |
| MLVA | VNTR; 7-15 loci | ++++ | ++ | +++ | + | +++ | +++ |
| Basados en análisis de secuencias | |||||||
| MLST | Secuenciación de 7 genes housekeeping | +++ | +++ | +++ | ++ | ++++ | +++ |
| WGS | Cromosoma, SNP | ++++ | +++ | + | + | +++ | ++++ |
MLST: multilocus sequence typing; MLVA: multilocus variable number of tandem DNA repeats (VNTR); PFGE: pulse field gel electrophoresis; SNP: single nucleotide polymorphisms; WGS: whole genome sequencing.
+: bajo; ++: moderado; +++; bueno; ++++: excelente.
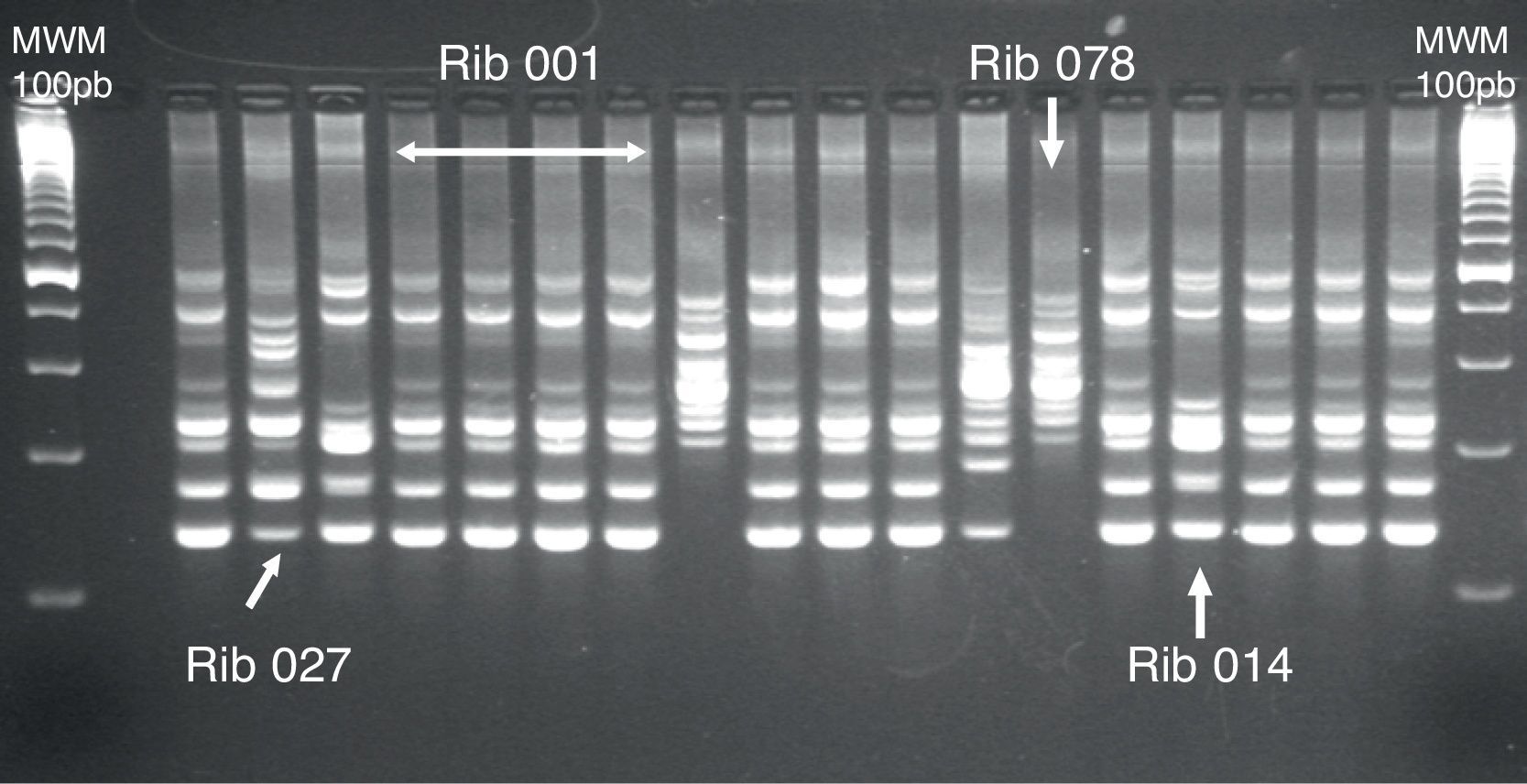
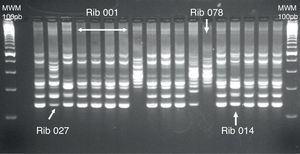
La técnica de PCR-ribotipado se basa en la amplificación mediante PCR del espacio intergénico (ISR) existente entre los genes 16S y 23S que codifican para el ARN ribosómico. Estos genes son multicopia en C.difficile, y su disposición, número y tamaño varía entre unas cepas y otras dentro del cromosoma. Los distintos fragmentos de la amplificación por PCR se separan por electroforesis en geles de agarosa, obteniéndose un patrón de bandas. El análisis de los patrones de bandas se realiza mediante la construcción de dendrogramas de similitud. En cada patrón se considera el número de bandas y su posición, siendo 2 patrones diferentes si tienen más de una banda de diferencia o están distintas posiciones (fig. 2). El ribotipado es un método sencillo con adecuada reproducibilidad intralaboratorio, pero poca reproducibilidad interlaboratorio22,23, lo que obliga a utilizar cepas de referencia de los principales ribotipos. Los ribotipos mayoritarios en España son los ribotipos 014/020, 001/072 y 078/1267. El ribotipo 027 (pulsotipo NAP1) no ha sido muy prevalente en España durante los últimos años (3,5% en 2013), aunque parece que su incidencia está aumentando desde 2014 en algunas regiones españolas.
La electroforesis en campo pulsado (pulsed fied gel electroforesis [PFGE]) se basa en la separación mediante electroforesis en campo pulsado de los fragmentos generados al digerir el cromosoma de C.difficile con la enzima de restricción SmaI, que es de corte poco frecuente. Ya que se obtienen fragmentos de ADN de tamaño grande, la separación de estos requiere una electroforesis a altos voltajes y con cambio de orientación del campo eléctrico (pulsos) característica de ciertos sistemas de electroforesis como el sistema contour clampled homogeneus electric field (CHEF). Esta técnica es laboriosa y plantea problemas por la facilidad de degradación del ADN de C.difficile y por la dificultad para lisar sus esporas; además, es algo menos discriminativa que el ribotipado y con similar reproducibilidad interlaboratorio.
La técnica de variabilidad del número de repeticiones en tándem en múltiples locus (MLVA) consiste en la amplificación mediante PCR de varias regiones de ADN (multilocus) en las que hay secuencias cortas repetidas en tándem denominadas microsatélites. El número de las repeticiones que hay en cada uno de los locus es variable en las distintas cepas de C.difficile. El método consiste en la amplificación de cada locus mediante PCR, usando iniciadores marcados con fluorescencia, seguido del análisis del tamaño de los amplicones obtenidos mediante electroforesis capilar en secuenciador de ácidos nucleicos. El número de repeticiones que una determinada cepa tiene en cada locus se determina relacionando el tamaño del fragmento amplificado con el tamaño que tendría el locus con una sola repetición y considerando los pares de bases de cada repetición. Las relaciones filogenéticas que existen entre las cepas analizadas se estudian mediante la construcción de un diagrama de similitud del tipo minimun spanning tree, que mide la distancia genética entre los distintos aislados, utilizando la diferencia entre las sumas de las repeticiones en tándem de todos los loci analizados (summed tandem repeats difference o STRD) y el número de loci variantes. Normalmente, se considera que forman parte de un complejo clonal los aislados con STRD ≤2. El MLVA es una técnica rápida muy discriminativa que proporciona resultados comparables a la secuenciación del genoma completo. Hoy día se utiliza como método de subtipado asociado al ribotipo, sobre todo para investigar brotes causados por cepas del mismo ribotipo e identificar rutas de transmisión entre pacientes. Además, es una técnica que, al realizarse en secuenciadores e interpretarse mediante perfiles numéricos, permite un análisis más reproducible y objetivo que los métodos basados en análisis de bandas.
La técnica de tipado mediante análisis de secuencias de múltiples locus (MLST) se basa en la amplificación y secuenciación de entre 300 y 500pb de 7 genes conservados en C.difficile (genes housekeeping). A cada variante de secuencia se le asigna un número, y la combinación de los 7 números obtenidos (cada uno correspondiente a la secuencia de un gen) da lugar a un perfil alélico al que se asigna una secuencia tipo o ST. La comparación de los ST de cada cepa se realiza de forma sencilla y objetiva a través de bases de datos públicas depositadas en Internet, en las que actualmente hay descritos 295 ST para C.difficile (http://pubmlst.org/cdifficile/) (última actualización 13 de marzo de 2015). El poder de discriminación del MLST es similar al del ribotipo pero, al contrario que este, permite un análisis objetivo, más sencillo e intercambiable entre laboratorios. Sin embargo, hay que tener en cuenta que es más costoso, al tener que hacer 7 secuencias por cada cepa, lo que quizá determina que el ribotipo siga siendo el método de tipificación más usado en los laboratorios europeos. Otra de las ventajas del MLST con respecto a otros métodos es que permite establecer relaciones evolutivas entre distintas cepas, lo que ha permitido estudiar la filogenia de C.difficile, que parece haber evolucionado en 6 linajes diferentes (clades), siendo el linaje1 el que agrupa a la mayoría de los ST descritos.
La técnica de secuenciación del genoma completo (WGS) es una metodología novedosa de caracterización molecular de microorganismos con un alto poder de discriminación24. En la WGS se realiza la «lectura» de todo el genoma de C.difficile y permite, entre otras muchas utilidades, estudiar diferencias a nivel de un solo nucleótido en las secuencias de cepas diferentes, lo que mejora mucho el poder de discriminación. Con la WGS se pueden establecer las cadenas epidemiológicas de transmisión con gran precisión y, además, se pueden definir linajes epidemiológicos, deducir el perfil de MLST e incluso distinguir entre cepas estrechamente relacionadas por el «simple» cambio de un nucleótido. Sin embargo, en lo referente a la tipificación de C.difficile queda por establecer cuántos SNP de diferencia tiene que haber para considerar si 2 cepas están genéticamente relacionadas o no. En la actualidad, su elevado coste y la complejidad del análisis bioinformático hacen que su uso esté restringido a centros de investigación o a laboratorios de referencia nacionales o supranacionales.
Requerimientos necesarios para los estudios de tipificación molecular de Clostridium difficileEn general, la tipificación molecular de C.difficile toxigénico se debe realizar a partir de cultivos recientes y puros que se deben mantener refrigerados hasta la extracción de ADN. Para ello, se pueden utilizar distintos métodos: hervido, resinas de extracción tipo Chelex, purificación con columnas, extracción automatizada, etc. Si se desea conservar el ADN extraído es conveniente la purificación con columnas (tipo Quiagen o similar) o el empleo de extractores automáticos (ADN más puro y más resistente a la degradación). En el caso de las técnicas PFGE o WGS, hay que utilizar otras metodologías específicas.
El ADN extraído puede conservarse a 4°C si se va a procesar en un periodo de tiempo corto y a −20 o −70°C en caso contrario (los ciclos de congelación-descongelación favorecen mucho la degradación del ADN). El método molecular de tipificación a elegir dependerá sobre todo del número de cepas a analizar, del material de laboratorio disponible (secuenciador principalmente) y del nivel de discriminación requerido. Si se quiere hacer un análisis descriptivo de la epidemiología local de C.difficile y no se dispone de secuenciador de ácidos nucleicos, quizás el ribotipo es la técnica de elección. Si se dispone de secuenciador se puede emplear el ribotipo o el MLST. Cuando el estudio molecular se utilice para caracterizar un brote, es conveniente asociar una técnica de alta discriminación como el MLVA.
Información de resultadosLa información de los resultados obtenidos en el laboratorio al personal sanitario responsable del paciente y al preventivista constituye uno de los pasos más importantes para optimizar el tratamiento y el control de la transmisión2. La rápida información de un resultado positivo en el laboratorio es fundamental para conseguir un adecuado tratamiento del episodio de ICD y para poner en marcha las medidas de aislamiento necesarias para evitar la transmisión de la infección a otro paciente; además, puede evitar que el paciente quede expuesto a fármacos innecesarios, como agentes antiperistálticos o narcóticos, que pueden complicar el episodio de ICD. Por otra parte, una rápida información de un resultado negativo puede evitar tratamientos empíricos innecesarios y facilitar la identificación de la verdadera causa de los síntomas.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.