Introducción
La pancreatectomía corporocaudal (PCC) es una conocida técnica quirúrgica que se utiliza en el tratamiento de una amplia gama de enfermedades pancreáticas (tumores, pancreatitis crónica, traumatismos, etc.). Sin embargo, en las últimas 2 décadas, sus indicaciones han variado de forma considerable. Ha dejado de realizarse tras la gastrectomía total ampliada1 , se ha abandonado su realización a ciegas en el insulinoma2 y su empleo ha disminuido llamativamente en la pancreatitis crónica, al haber surgido otras alternativas quirúrgicas, como la duodenopancreatectomía o la técnica de Beger3 . Por el contrario, se ha ampliado su indicación a nuevas enfermedades, como los tumores quísticos, la pancreatitis focal, los traumatismos y otros tumores del páncreas4 . En la actualidad, son objeto de debate algunos aspectos técnicos, como la posibilidad de realizar la PCC por laparoscopia5 , las ventajas de la conservación esplénica6 , la forma de sección pancreática7 y el tipo de cierre del muñón pancreático8 . Por ello, presentamos un estudio retrospectivo de 14 casos de PCC y estudiamos cuáles han sido las indicaciones, los aspectos técnicos más relevantes y la morbilidad de la técnica en nuestra experiencia.
Pacientes y método
Estudio retrospectivo de los pacientes a los que se ha practicado una PCC clásica con esplenectomía asociada (CIE: 52.52) en nuestro servicio durante los años 1998-2003. En dicho período se practicaron 14 PCC, el 75% de ellas en el trienio 2000-2002. Se consideró que había fístula pancreática ante la presencia de valores de amilasa > 5.000 U/l en el líquido de drenaje.
Resultados
La edad media fue de 52,6 años (rango, 21-78). El 36% fue varón (5/14). Las lesiones se localizaron en cuerpo (n = 2) y en cola (n = 12). Los diagnósticos preoperatorios fueron: tumor quístico mucinoso pancreático (n = 5), tumor neuroendocrino (n = 3), con 1 insulinoma y 2 tumores malignos no funcionantes, pancreatitis focal sobre pancreatitis crónica (n = 2), cáncer de páncreas en cuerpo-cola de 4 y 5 cm (T3N0M0) (n = 2), traumatismo pancreático por herida con arma blanca de grado III (n = 1) y metástasis pancreática de cáncer renal (n = 1). Las pruebas diagnósticas más utilizadas fueron la tomografía computarizada (TC) abdominal (13/14) y la ecografía (11/14). Otras pruebas efectuadas ocasionalmente fueron colangiopancreatografía retrógrada endoscópica (CPRE) en 1 caso, colangiorresonancia en 1 y tomografía por emisión de positrones (PET) en 1. La cirugía fue electiva en el 86% (12/14). Dos pacientes fueron intervenidos de forma urgente: 1 por traumatismo abdominal por arma blanca y 1 paciente con neoplasia primaria que presentó una obstrucción intestinal. Se efectuó PCC con esplenectomía en todos los casos. El tiempo medio de la intervención quirúrgica fue de 232 min (rango, 120-360). En 5 (35%) de 14 pacientes se trasfundió una media de 1,36 concentrados (rango, 2-4; mediana, 0). La técnica utilizada para el cierre del muñón distal fue: sutura manual en 4 casos (29%), grapado mecánico en 9 (64%) y grapado más sutura posterior en 1 caso (7%). En los casos en que se realizó sutura manual, el conducto de Wirsung fue ligado de forma independiente. En el 50% de los pacientes (7/14) se asoció otro gesto quirúrgico (4 colecistectomías, 1 colectomía, 1 adrenalectomía y 1 gastrectomía).
La concordancia diagnóstica pre y postoperatoria fue del 86% (12/14). Los diagnósticos incorrectos correspondieron a 1 paciente con obstrucción intestinal en el que se sospechó inicialmente una neoplasia obstructiva de colon y que en realidad correspondía a una neoplasia pancreática que invadía al colon, y 1 paciente en el que se sospechó una neoplasia gástrica con invasión pancreática y era un tumor primario pancreático con invasión gástrica.
Se determinó la amilasa en el líquido del drenaje a las 24 h de la intervención en todos los pacientes y se encontró elevada en 5 casos, con un valor medio de 2.796 U (rango, 16-7.100). En 4 de los 5 pacientes en los que se detectaron valores elevados de amilasa en el drenaje se desarrolló una fístula pancreática (FP) asociada a un absceso intraabdominal (3 localizadas en la celda esplénica y 1 en las interasas). La morbilidad total fue del 35% (5/14): 2 pacientes presentaron fístula pancreática (FP), derrame pleural, absceso intraabdominal en la celda esplénica e infección de la herida quirúrgica; otros 2 tuvieron FP y absceso intraabdominal (1 en la celda esplénica y otro entre las asas) y 1 paciente presentó retraso del vaciamiento gástrico. El 80% de la morbilidad estuvo relacionada con la FP. Se colocó drenaje percutáneo en celda esplénica en 3 pacientes (21% del total), con una efectividad terapéutica del 66% (2/3). Se reoperó a 2 pacientes para efectuar drenaje y lavado de la cavidad abdominal: 1 tras el fracaso del drenaje percutáneo y 1 con un absceso no puncionable por su localización interasas. Todas las fístulas cerraron espontáneamente. No hemos observado ninguna relación estadística entre la técnica empleada para el cierre del muñón y el desarrollo de la fístula pancreática. La mortalidad fue del 0%. La estancia media fue de 18 días (rango, 7-42). La tasa de diabetes postoperatoria ha sido del 28% (4/14).
En la evolución a largo plazo se ha observado que los pacientes con tumor quístico mucinoso, traumatismo pancreático y pancreatitis focal se encuentran bien; la paciente con una metástasis pancreática falleció a los 4 años de la intervención por progresión de la enfermedad; de los 2 pacientes con neoplasia primaria de páncreas, 1 murió a los 4 meses por una embolia pulmonar y 1 está vivo y libre de enfermedad a los 17 meses de la operación. De los 2 pacientes con tumores endocrinos malignos no funcionantes, 1 falleció a los 11 meses y 1 está vivo y libre de enfermedad 36 meses después.
Discusión
La PCC, también llamada pancreatectomía distal en el mundo anglosajón, es la técnica de elección para múltiples enfermedades benignas y malignas que afectan al cuerpo y a la cola del páncreas6,9 . Fue realizada por primera vez por Billroth en 18849 . En Europa, se entiende por PCC la resección pancreática que se inicia en la unión entre la cabeza y el cuerpo pancreáticos y se extiende hasta la cola, lo que supone la exéresis de cerca del 70% del parénquima pancreático. No está plenamente definido si la PCC se realiza a la derecha o izquierda de la vena mesentérica superior. Muchos autores también denominan PCC a resecciones más extensas, de hasta el 95% del parénquima, o menores (sólo la cola pancreática)8,9 . Esta discrepancia dificulta la interpretación de los resultados publicados, ya que mayor resección implica más morbilidad.
Las indicaciones por las que se realiza la PCC han cambiado considerablemente en la últimas 2 décadas. Ha disminuido la indicación por cáncer gástrico, pancreatitis crónica e insulinoma y se ha incrementado la de las tumoraciones quísticas pancreáticas, los traumatismos abdominales, las metástasis pancreáticas y otras lesiones infrecuentes3,10 . Los excelentes resultados publicados por grupos dedicados en exclusiva a la cirugía pancreática han demostrado que es posible realizar una PCC con una mortalidad prácticamente nula, lo que ha contribuido a la ampliación de las indicaciones.
En los años ochenta se realizaba PCC de forma sistemática en toda gastrectomía total ampliada por considerarse que implicaba una mayor radicalidad oncológica. Numerosos estudios han demostrado que la realización de PCC asociada a la gastrectomía incrementa el número de ganglios extirpados, pero no aumenta la supervivencia y sí la morbilidad postoperatoria, por lo que actualmente se realiza con poca frecuencia1 .
La PCC realizada antaño de manera habitual en enfermos con pancreatitis crónica ha caído en desuso. La indicación más aceptada hoy día de PCC por pancreatitis crónica es la realizada en pacientes con enfermedad localizada exclusivamente en el páncreas izquierdo (sólo el 5-15% de los enfermos)11 . La indicación más frecuente de cirugía (PCC) en estos pacientes concretos es el dolor no tratable médicamente (71%)12 ; sin embargo, los resultados obtenidos fueron sólo aceptables12 . Los mejores resultados se obtienen cuando la indicación de PCC en la pancreatitis crónica es debida a un seudoquiste11,13 , una pancreatitis focal, una estenosis aislada del ducto pancreático13 o una pancreopatía crónica obstructiva14 ; los peores se obtienen en la pancreatitis crónica atrófica sin calcificaciones y en la pancreatitis difusa 11,12 .En nuestra serie, los pacientes con pancreatitis crónica fueron intervenidos para descartar una posible neoplasia. Histológicamente se demostró en ambos casos que eran pancreatitis focales de la cola pancreática.
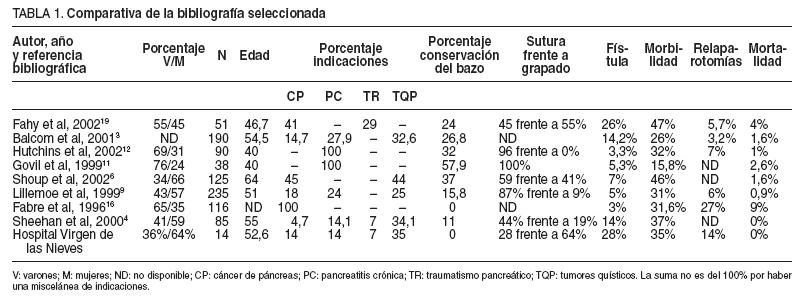
TABLA 1. Comparativa de la bibliografía seleccionada
Los tumores neuroendocrinos pancreáticos constituyen una indicación de PCC que también ha presentado modificaciones. Se ha incrementado el número de pacientes diagnosticados gracias a la mejora de los métodos de imagen; sin embargo, ha disminuido el número de PCC realizadas debido a la aparición de técnicas alternativas (pancreatectomías mediales15 , enucleaciones laparoscópicas5 ).
En la actualidad se ha incrementado de manera sustancial el diagnóstico de tumores quísticos de páncreas. Por ello, esta indicación se ha convertido progresivamente en la primera indicación de PCC, como ocurre en serie3,9.
El cáncer primario de páncreas susceptible de ser tratado por PCC es el que se encuentra localizado en el cuerpo y la cola del páncreas. Sin embargo, su tasa de resecabilidad es cercana al 15-20%9,16 , ya que en el momento del diagnóstico es habitual que haya afección vascular y metástasis a distancia que desaconsejan un tratamiento quirúrgico16 . Sólo los pacientes con tumores pequeños sin invasión ganglionar (estadios I y II de la AJCC) se benefician de la resección16 . La invasión de órganos vecinos resecables, como en nuestros casos (colon y estómago), es un factor de mal pronóstico.
El traumatismo pancreático (abierto o cerrado) se produce habitualmente en pacientes con grandes traumatismos y múltiples lesiones concomitantes. La técnica quirúrgica dependerá de la extensión de la lesión. En pacientes con lesiones de grado III de la AAST (rotura del parénquima con lesión ductal), como era nuestro caso, la PCC es la técnica de elección17 . Debido a las lesiones asociadas que presentan estos pacientes, en estas PCC se observa la mayor morbimortalidad.
La presencia de metástasis pancreáticas (MP) parece ser más frecuente de lo que se creía y aparecen en el contexto de una enfermedad tumoral diseminada. Entre el 2 y el 4,5% de los tumores pancreáticos son MP18 .La MP aislada es excepcional, puede ser causada por diversos tumores (colon, riñon, piel, pulmón y ovario)18 y es infrecuente la presencia de una lesión única localizada en la cola pancreática, como ocurrió en nuestro caso.
La PCC se considera una técnica con una morbilidad elevada (15,8-47%) pero una baja mortalidad (1-4%) (tabla 1)3,6,8,11,12,19.Nuestra serie presenta una mortalidad nula y una morbilidad del 37%, similar a la de otras series más amplias.
La complicación más grave y frecuente es la aparición de una FP20 . En nuestra serie se obtiene una tasa de FP elevada (28%) que se concentra en los pacientes neoplásicos y con traumatismo. La FP supone el 80% del total nuestras complicaciones, ya que las complicaciones extrapancreáticas fueron poco habituales. La frecuencia de fístula pancreática post-PCC en las series consultadas (tabla 1) oscila entre el 3,3 y el 26%3,6,8,11,12,19 . Debemos recalcar la falta de un criterio homogéneo para definir la 19,20 , por lo que Fahy et al19 han propuesto una clasificación de las FP post-PCC que esperamos permita realizar en el futuro comparaciones entre las diferentes casuísticas.
Los factores que han sido implicados en la aparición de FP son: el tipo de cierre del muñón pancreático (grapado frente a suturado), la enfermedad por la que se ha efectuado la PCC8 , la realización de una esplenectomía concomitante19 y la presencia de un páncreas blando no fibrótico8,20 . Varios estudios no prospectivos no han conseguido confirmar que el tipo de cierre tenga una relación directa con la aparición de la FP, aunque cuando el páncreas es blando se recomienda el grapado19 . Tampoco se ha conseguido demostrar ninguna asociación estadísticamente significativa entre la enfermedad por la que se realiza la PCC y la aparición de FP, aunque las efectuadas por un traumatismo pancreático sí parecen tener una incidencia levemente superior8,19 . La no realización de esplenectomía también se ha asociado con el desarrollo de FP19 . En nuestra serie no hay relación entre el tipo de cierre del muñón y la aparición de FP.
En la serie de Fahy et al19 , un 23% de los pacientes con FP tuvo que ser relaparotomizado (el 7% en nuestra serie). La tasa media de reoperación oscila entre el 3,2 y el 7% (el 14% en nuestra serie)3,6,8,11,12,19 . Cabe destacar que todos nuestros casos de FP presentaron un absceso intraabdominal secundario al mal drenaje de la FP que requirió tratamiento mediante drenaje percutáneo o laparotomía. En las series consultadas se recogen también casos con abscesos intraabdominales, pero no se especifica si éstos acompañan a una FP3,6,8,11,12,19 . Habitualmente, la FP se cierra sin necesidad de nutrición parenteral total8 .
Otra complicación importante es la diabetes postoperatoria de novo, que oscila entre el 20 y el 70% (el 28% en nuestra serie)11 . Se ha observado que hay una relación directa entre la cantidad de páncreas resecado y el porcentaje de enfermos que desarrollan diabetes. La PCC con preservación esplénica parece presentar tasas inferiores de diabetes postoperatoria11,12 .
Uno de los puntos técnicos de debate es cómo efectuar el cierre del muñón del páncreas. Tras la sección pancreática, clásicamente se realizaba una ligadura del ducto principal y se suturaba el tejido del muñón pancreático. Así se obtenía una tasa de FP que oscilaba entre el 10 y el 27%7 . Otra opción es la sección con grapadora del parénquima, que es una técnica sencilla y fiable20,21 . Más recientemente se ha comunicado la posibilidad de seccionar el parénquima con el bisturí ultrasónico7 . Además, se han utilizado diversos productos (fibrina, prolamina, etc.) para sellar el ducto del muñón pancreático, siempre con la intención de disminuir la tasa de FP22 . Las series consultadas demuestran una gran disparidad de datos que no permite llegar a ninguna conclusión sobre cuál es el mejor cierre a realizar3,6,8,11,12,19 . En nuestra serie, la sección del páncreas fue efectuada en la mayoría de los pacientes (9/14) mediante grapadora. Debido al reducido número de casos, no se han obtenido diferencias estadísticamente significativas entre el tipo de cierre y la aparición de FP. En nuestras últimas 4 PCC hemos sellado el muñón con fibrina y los pacientes no han presentado FP, pero no podemos recomendar su empleo sistemático por el número reducido de casos.
La PCC se ha realizado clásicamente asociada a una esplenectomía6 . En 1943, el cirujano francés Mallet-Guy realizó por primera vez la PCC con la conservación del bazo. Pero es en la última década cuando se han publicado varias series donde se exponen los resultados de esta modificación técnica6,10,11 . La tasa de preservación del bazo en distintas series oscila entre el 16 y el 58% (tabla 1). Las razones por las que no se practica la exéresis del bazo son su dificultad quirúrgica, el mayor tiempo quirúrgico y las mayores perdidas sanguíneas6 , pero se sustenta en que su preservación elimina la infrecuente, pero gravísima, infección por bacterias encapsuladas. La tasa de complicaciones por preservar el bazo es baja3 :se ha descrito infarto esplénico, absceso esplénico y hemorragia. Shoup et al6 observaron una tasa global de infecciones y complicaciones muy inferior si se preserva el bazo. La aplicabilidad de la técnica es alta (50%) y no se recomienda en tumores malignos cercanos al hilio esplénico6 . Warshaw10 describió una variante técnica de preservación con transección de los vasos esplénicos basándose en que el bazo se nutre por los vasos cortos gástricos. Esto puede ser útil en los pacientes con pancreatitis crónica que presentan adherencias muy consistentes entre la vena esplénica y el tejido pancreático10 . En nuestra serie aún no hemos podido aplicarla, ya que no era posible por tratarse de tumores cercanos al hilio.
La cirugía pancreática por laparoscopia es una alternativa técnica que requiere gran destreza. La PCC por laparoscopia probablemente sea, en un futuro, la técnica de elección en tumores benignos de cuerpo y la cola de páncreas (cistoadenomas serosos y mucinosos) y en tumores neuroendocrinos no malignos y no localizados en la cabeza del páncreas5 . Fernández Cruz et al5 presentan una serie de cirugía laparoscópica pancreática en la que incluyen 12 pancreatectomías distales. En 1 caso fue preciso seccionar los vasos pancreáticos y el paciente desarrolló un absceso pancreático. La tasa de FP fue del 25% y la estancia media, de 5,75 días5 . Actualmente no creemos que sea una técnica de aplicación universal, pero cabe prever que se consolide en las indicaciones comentadas.
En conclusión, la PCC es una técnica con indicaciones cambiantes en la última década. No hay aún consenso sobre cuál es la mejor técnica de cierre del muñón pancreático. La PCC presenta una baja mortalidad y una alta morbilidad, habitualmente relacionada con la aparición de una FP. Los centros con mayor volumen de cirugía pancreática obtienen mejores resultados y menores costes3 . La aplicación de vías clínicas y la estandarización de los cuidados postoperatorios en la PCC suponen un descenso de la estancia media de los pacientes sometidos a cirugía pancreática3 , por lo que creemos aconsejable centralizar la PCC en unidades con gran experiencia en cirugía pancreática.
Correspondencia: J.M. Ramia . Buensuceso, 6, 4. o D. 18002 Granada. España. Correo electrónico: jose_ramia@hotmail.com
Manuscrito recibido el 11-12-2003 y aceptado el 28-6-2004.