INTRODUCCION
En la mayoría de centros de Medicina Nuclear en los que se realizan exploraciones PET no disponen de un ciclotrón propio para la producción de 2-[18F]-Fluoruro-2-deoxi-D-Glucosa (18F-FDG). La 18F-FDG es habitualmente suministrada por un Laboratorio de radiofármacos PET (LPET) en forma de vial multidosis a la Unidad de Radiofarmacia (UR) donde se realiza la preparación extemporánea individualizada de 18F-FDG. En algunos casos su concentración radiactiva (CR) es muy elevada, lo que obstaculiza su uso directo y hace necesaria una dilución a una concentración adecuada para la preparación de dosis individualizadas para cada paciente. Esta elevada concentración radiactiva puede producir autorradiolisis del radiofármaco debido a la elevada energía de los positrones emitidos por el 18F, que disminuiría su estabilidad, favoreciendo la liberación del anión fluoruro1. Estas preparaciones son usadas durante algunas horas, de ahí el interés en determinar si su pureza radioquímica disminuye durante este periodo. La dilución de la 18F-FDG debe aumentar la estabilidad de las preparaciones, disminuyendo el fenómeno de autorradiolisis. A la Unidad de Radiofarmacia le corresponde el establecimiento del plan de control de calidad de los radiofármacos que permita asegurar el uso en las condiciones adecuadas de los mismos. La legislación española establece que cada radiofármaco tendrá su propio plan de garantía de calidad2,3, aunque en el caso de radiofármacos listos para su uso no es necesario que se incluya necesariamente la determinación de pureza radioquímica4. Una guía de la European Association of Nuclear Medicine menciona que puede confirmarse la pureza radioquímica por cromatografía en capa fina (TLC) en el caso de una Unidad de Radiofarmacia que reciba la 18F-FDG de un centro productor5. Según esta misma guía la dilución de las preparaciones de 18F-FDG con salina fisiológica estéril puede realizarse en caso de necesidad. El determinar la influencia del tiempo y la concentración radiactiva sobre la pureza radioquímica permitiría establecer el plan de trabajo adecuado para asegurar la calidad de las preparaciones de 18F-FDG.
El objetivo de este estudio consiste en determinar la influencia de la concentración radiactiva de la 18F-FDG y el tiempo de almacenamiento máximo habitual del radiofármaco en la Unidad de Radiofarmacia sobre su pureza radioquímica.
MATERIAL Y MÉTODOS
18F-FDG
Fabricada por un Laboratorio de radiofármacos PET cercano al Hospital, producida por sustitución nucleofílica SN2 del 18F sobre el triflato de manosa, asistida por aminopoliéter, posterior hidrólisis básica, y purificación en columnas de intercambio iónico, alúmina y fase reversa. El producto se formuló isotónicamente mediante cloruro sódico inyectable y tampón fosfato hasta pH 5,5 y se esterilizó en autoclave en el vial final (135 °C, 3,5 minutos, F0 mínimo = 60 minutos). Se suministra en viales multidosis, listos para su uso en la Unidad de Radiofarmacia. Se estudiaron 30 preparaciones de 18F-FDG procedentes de distintos lotes de fabricación, con una concentración radiactiva comprendida entre 17 y 294 mCi/ml (media: 80 mCi/ml; desviación estándar: 52 mCi/ml) en el momento de su dispensación a viales multidosis y entre 14 y 130 mCi/ml (media: 36 mCi/ml; desviación estándar: 25 mCi/ml) a su recepción en la Unidad de Radiofarmacia.
Pureza radioquímica
- En la Unidad de Radiofarmacia: a la recepción de la preparación se extrajeron aproximadamente 50 μl en una jeringa de 1 μl y se introdujeron en un tubo de ensayo de vidrio. Inmediatamente se pipetearon 10 μl a otro tubo, se le añadieron 90 μl de suero fisiológico y se agitó suavemente 10 segundos en un vórtex. Dentro de los 30 minutos de su recepción y a las 5 horas se realizó, para cada muestra, un ensayo de TLC en placa de Silicagel 60 de 10 cm con marcas de lápiz a 1,5 cm (Rf 0) y a 9,5 cm (Rf 1). La fase móvil utilizada estaba constituida con una mezcla acetonitrilo: agua (95:5), de acuerdo con el procedimiento descrito en la Real Farmacopea Española6. Los posibles contaminantes detectados con este método son el 18F-Fluoruro (Rf 0,0) y los derivados parcialmente acetilados de la 18F-FDG (Rf 0,8-0,95). La 18F-FDG se encontraría en Rf 0,45. Se cuantificaron todas las especies citadas. La cuantificación se realizó con un radiocromatógrafo BioScan Imaging Scanner System 200-IBM (1000).
- En el Laboratorio de radiofármacos PET: dentro de la primera hora posterior a su dispensación a viales multidosis, se realizó un ensayo de cromatografía líquida a alta presión (HPLC) según el procedimiento descrito en la Real Farmacopea Española6. Con este método se cuantificó la proporción de 18F-fluoruro, 18F-FDG y 2-[18F]-Fluoruro-2-desoxi-D-Manosa (18F-FDM). El método fue validado utilizando como fase móvil NaOH 0,1 M con un flujo de 0,9 ml/min. Se obtuvieron los siguientes tiempos de retención: 4,8 min, 8,6 min y 9,5 min para 18F-Fluoruro, 18F-FDM y 18F-FDG, respectivamente. La separación se realizó con una bomba HPLC Sykam S-1021 con una columna CarboPac PA10 (Dionex) de 4 x 250 mm y la detección con un detector isotópico NaI (Tl) Nuclear Interface (con un ratio de contaje a 370 KBq de 137Cs, 63.800 cps) y un detector UV Kanauer k-2001 con longitud de onda 220 nm.
Análisis estadístico
Los resultados se compararon mediante la prueba de la "t" de Student para muestras apareadas. Las rectas de regresión se calcularon mediante un ajuste por mínimos cuadrados y el coeficiente de correlación se determinó por la R de Pearson.
RESULTADOS
Derivados parcialmente acetilados
En el ensayo de TLC realizado tanto a la preparación recibida como a la diluida, a su recepción y a las 5 horas, no se apreció la presencia de derivados parcialmente acetilados marcados con 18F.
Aumento del porcentaje de 18F-Fluoruro entre las 5 horas y los 30 minutos
Se calculó la diferencia entre el porcentaje de 18F-Fluoruro a las 5 horas y a los 30 minutos para todas las muestras y se compararon los incrementos obtenidos en las muestras sin diluir con los de las muestras diluidas.
La media del incremento de porcentaje de 18F-Fluoruro en las muestras diluidas fue del 0,17 % (desviación estándar: 0,05; rango: [0,2]-0,8) y en las sin diluir 0,42 % (de: 0,06; rango: [0,2]-1,4). Observamos que este incremento fue significativamente mayor en las muestras sin diluir que en las diluidas (p < 0,0001) (tabla 1).
Regresión del porcentaje de 18F-Fluoruro con la concentración radiactiva
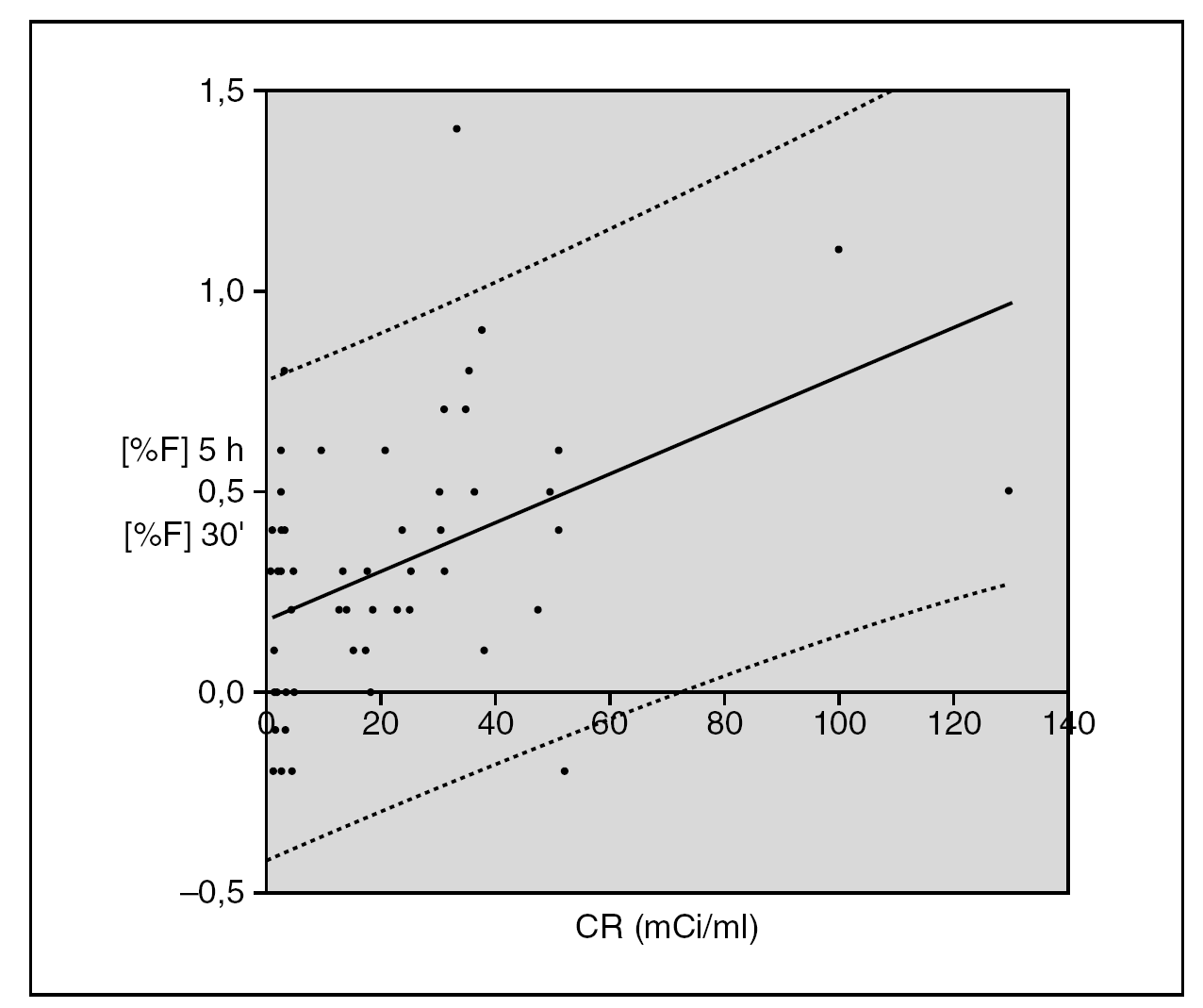
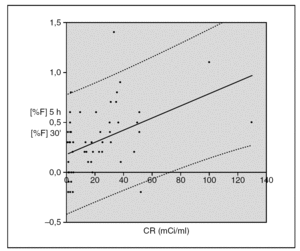
Estudiamos la regresión entre el incremento de porcentaje de 18F-Fluoruro entre las 5 horas y los 30 minutos con la concentración radiactiva. Los datos de las muestras y la ecuación de regresión se presentan en la figura 1.
Fig. 1.-- Representación gráfica de la diferencia de porcentaje de 18F-Fluoruro a las 5 horas después de su recepción y a los 30 minutos de su recepción frente a la concentración radiactiva (CR) en el momento de su recepción. (--) Recta de regresión con la siguiente ecuación: y = 0,0061x + 0,1759 (R 2 = 0,1977) (n = 60). (····) Intervalo de confianza para el 95 %.
La recta de regresión que se obtuvo es la siguiente: y = 0,0061x + 0,1759 (R 2 = 0,1977). Se encontró una correlación significativa entre este aumento de porcentaje de 18F-Fluoruro con el tiempo respecto a la concentración radiactiva de las muestras (p < 0,0005).
Muestras con el porcentaje de 18F-Fluoruro superior al 5 %
De las 30 muestras sin diluir, sólo en una muestra dentro de los 30 minutos posteriores a su llegada a la Unidad de Radiofarmacia, el porcentaje 18F-Fluoruro fue superior al 5 % (6,6 %, resultado repetido y verificado). A pesar de esto, no se observaron diferencias en la calidad de las imágenes obtenidas. Sin embargo, el porcentaje de 18F-Fluoruro determinado por el Laboratorio de radiofármacos PET fue 1,3 %. El tiempo transcurrido desde la dispensación en el Laboratorio de radiofármacos PET hasta su control en la Unidad de Radiofarmacia fue de 3,5 horas y la concentración radiactiva en el momento de su dispensación 126,7 mCi/ml.
Diferencia entre el porcentaje de 18F-Fluoruro determinado en la UR y en el LPET
Se comparó el porcentaje de 18F-Fluoruro determinado por TLC en la Unidad de Radiofarmacia y el obtenido en el Laboratorio de radiofármacos PET por HPLC.
La media del porcentaje de 18F-Fluoruro determinado en la Unidad de Radiofarmacia fue de 2,02 (desviación estándar: 0,22; rango: 0,8-6,6) y en el Laboratorio de radiofármacos PET de 0,74 (de: 0,06; rango: 0,3-1,4). El porcentaje determinado en la Unidad de Radiofarmacia fue significativamente mayor que el determinado en el Laboratorio de radiofármacos PET (p < 0,0001) (tabla 2).
El tiempo medio transcurrido entre la dispensación en el Laboratorio de radiofármacos PET y el ensayo de TLC en la Unidad de Radiofarmacia fue de 127 minutos (desviación estándar: 15 minutos; rango: 28-330 minutos).
Regresión entre el aumento de porcentaje de 18F-Fluoruro con la concentración radiactiva
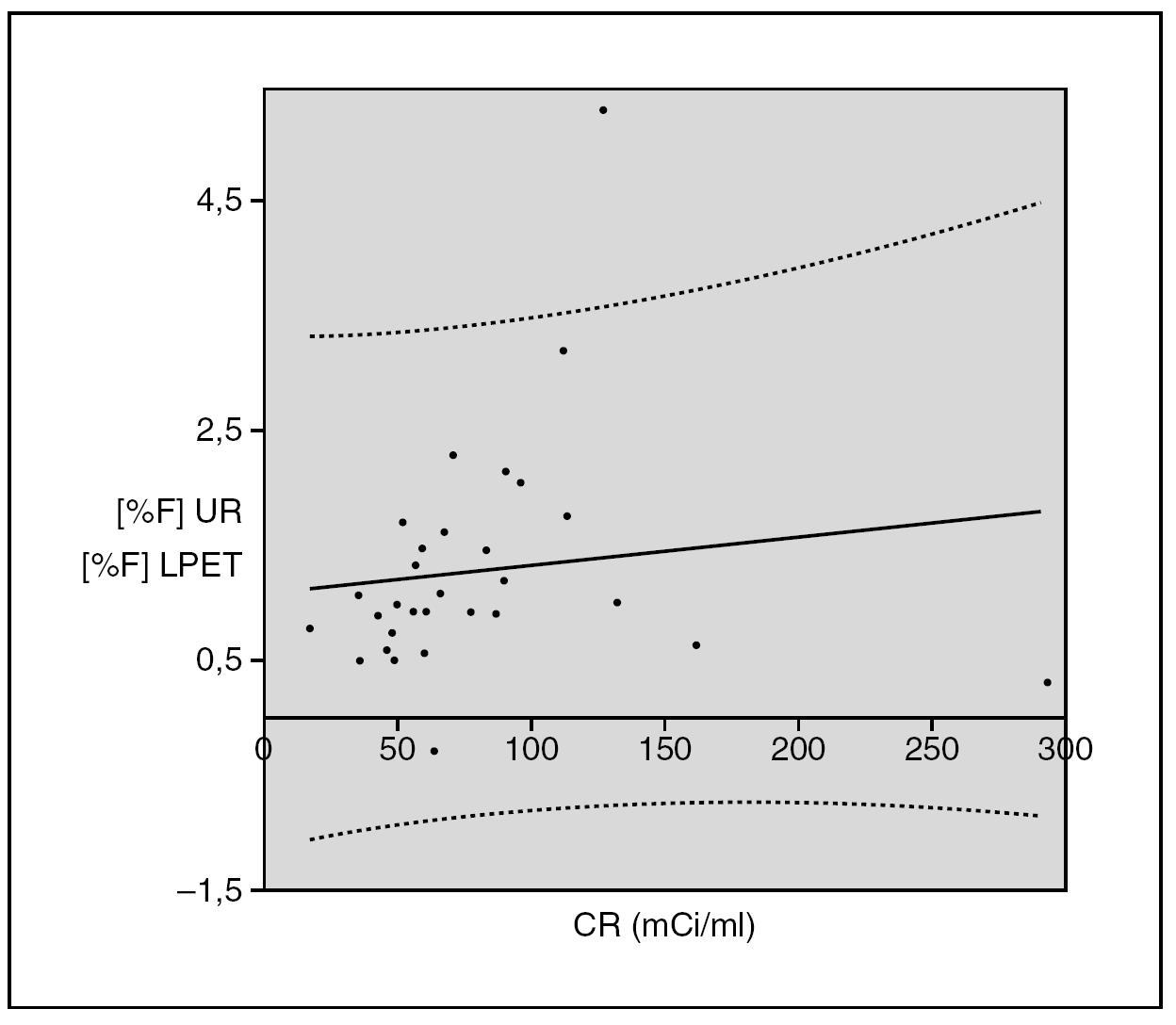
Estudiamos la regresión entre el aumento del porcentaje de 18F-Fluoruro (y) con la concentración radiactiva a la hora de su dispensación (x). Los datos y la ecuación de regresión se presentan en la figura 2.
Fig. 2.--Representación gráfica de la diferencia de porcentaje de 18F-Fluoruro determinado en la Unidad de Radiofarmacia (UR) y la determinada en el laboratorio PET (LPET) frente a la concentración radiactiva (CR) en el momento de su dispensación. (--) Recta de regresión con la siguiente ecuación: y = 0,0026x + 1,0833 (R 2 = 0,0167) (n = 30). (····) Intervalo de confianza para el 95 %.
La recta de regresión que se obtiene es: y = 0,0026x + 1,0833 (R 2 = 0,016). No se obtuvo correlación significativa entre este aumento y la concentración radiactiva en el momento de su dispensación (p = 0,496).
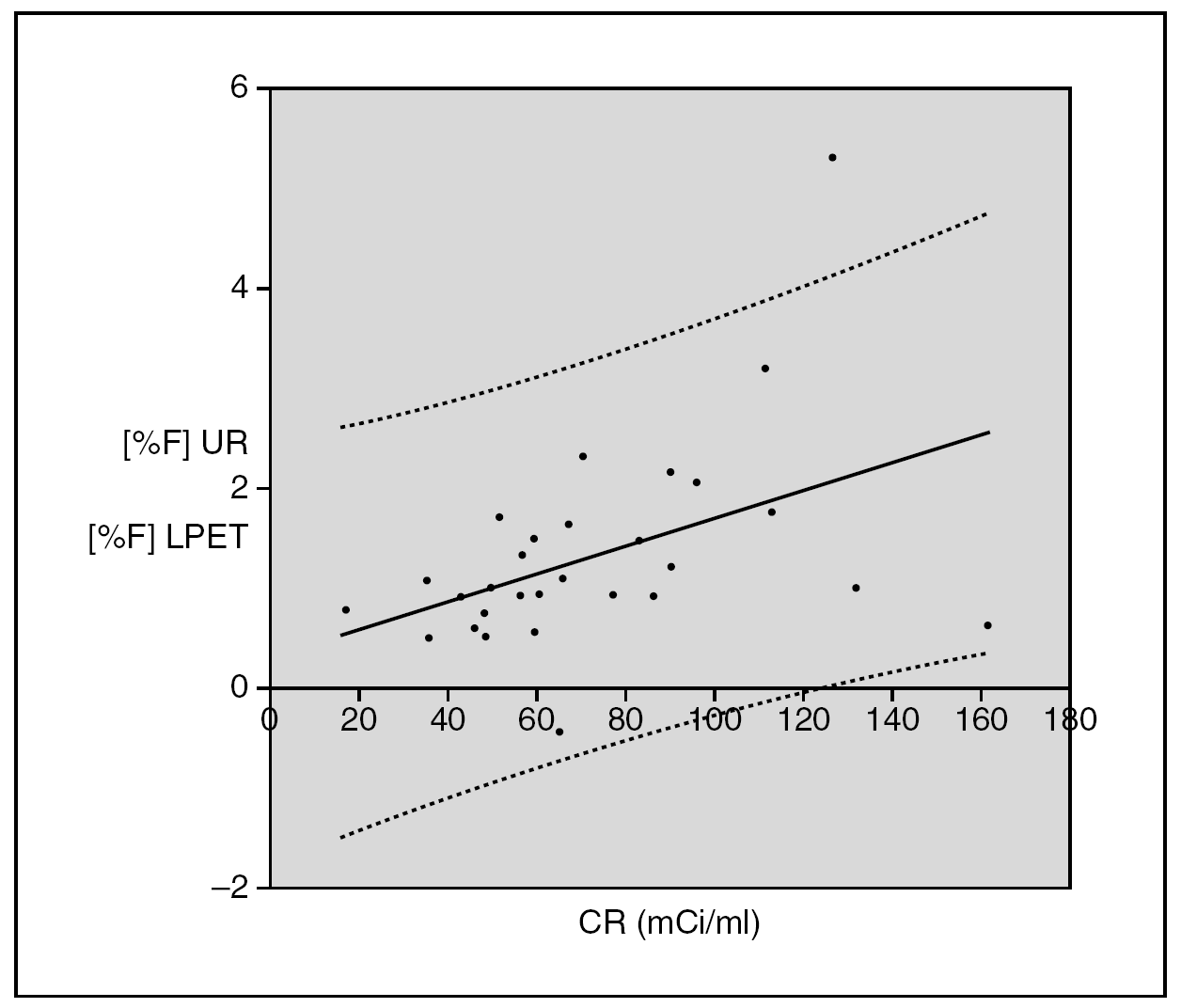
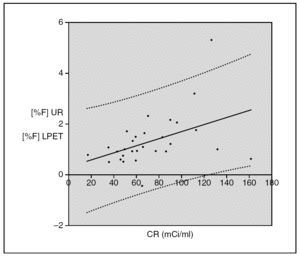
Eliminando el dato de mayor concentración radiactiva a la hora de estudiar la correlación obtenemos la representación de los datos y la ecuación de regresión mostrada en la figura 3. No tenemos en cuenta este resultado debido a que en la figura 3 se puede observar que la tendencia es un mayor aumento de porcentaje de fluoruro al aumentar la concentración radiactiva (como cabría esperar por el fenómeno de la autorradiolisis) y este dato no concordaría con esta tendencia.
Fig. 3.--Representación gráfica de la diferencia de porcentaje de 18F-Fluoruro determinado en la Unidad de Radiofarmacia (UR) y la determinada en el laboratorio PET (LPET) frente a la concentración radiactiva (CR) en el momento de su dispensación, sin el dato correspondiente a la mayor concentración. (--) Recta de regresión con la siguiente ecuación: y = 0,0139x + 0,3146 (R 2 = 0,1961) (n = 29). (····) Intervalo de confianza para el 95 %.
Con estos datos estudiamos la regresión y se obtuvo la siguiente recta: y = 0,0139x + 0,3146 (R 2 = 0,196). De esta manera sí se encontró una correlación significativa entre el aumento de %F- y la concentración radiactiva (p = 0,016).
Regresión del aumento de porcentaje de 18F-Fluoruro con la concentración radiactiva y el tiempo
Estudiamos la correlación entre el aumento de porcentaje de 18F-Fluoruro ([ %F] UR [ %F] LPET), la concentración radiactiva (CR) y el tiempo transcurrido desde la dispensación hasta el momento de realizar el control en la Unidad de Radiofarmacia (t). Se obtiene la siguiente curva de regresión: [ %F] UR [ %F] LPET = 0,01159*CR (mCi/ml) + 0,250*t (h) 0,01903 (R 2 = 0,226). Se obtuvo una correlación significativa entre el aumento de porcentaje de 18F-Fluoruro, la concentración radiactiva y el tiempo desde la dispensación (p = 0,014).
Correlación entre la concentración radiactiva y el tiempo transcurrido desde la dispensación
Estudiamos la correlación entre la concentración radiactiva (y) y el tiempo transcurrido desde su dispensación (x) para los 30 datos. Los datos y la ecuación de regresión se encuentran representados en la figura 4.
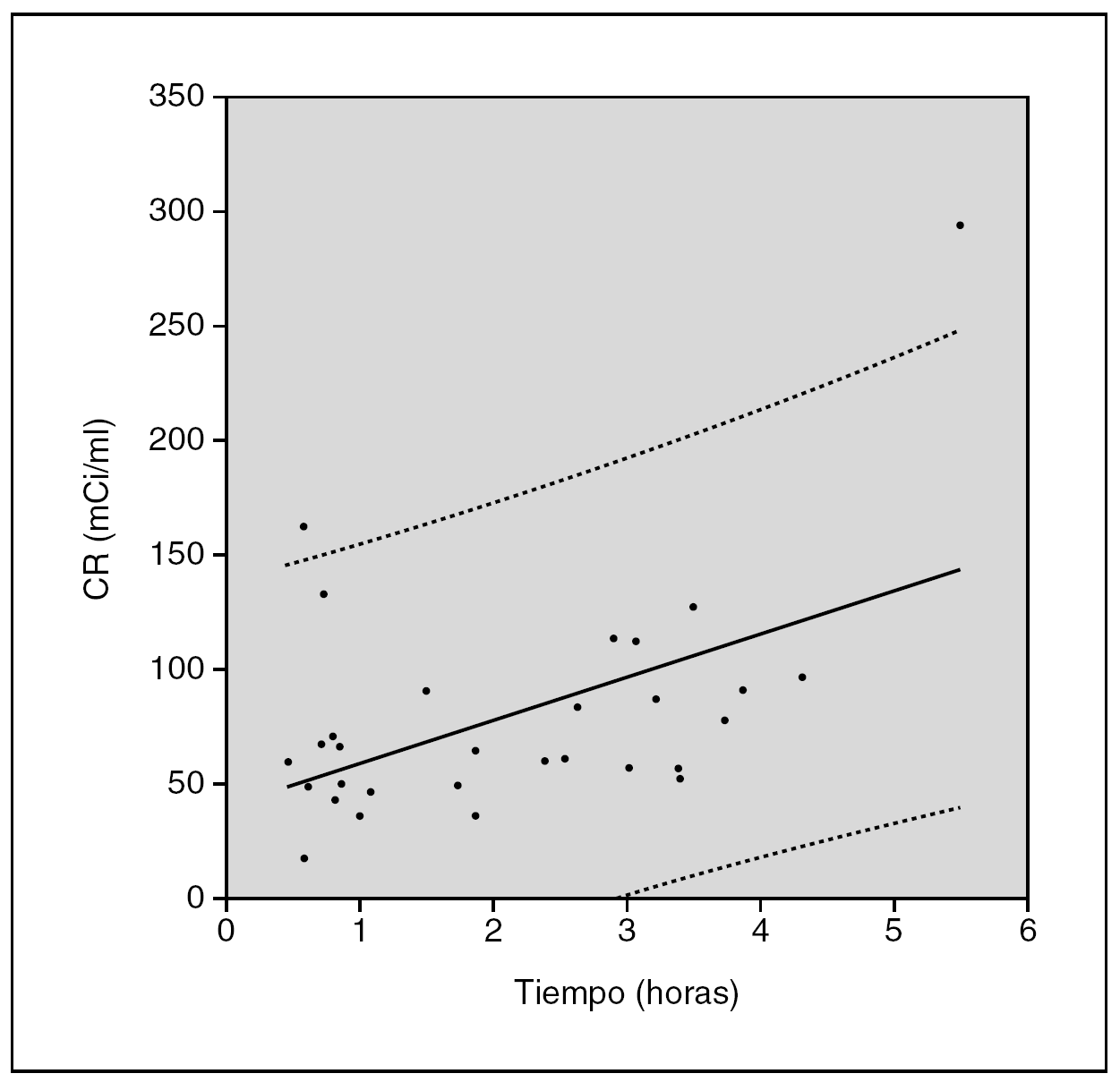
Fig. 4.--Representación gráfica de la concentración radiactiva (CR) frente al tiempo transcurrido desde su dispensación. (--) Recta de regresión con la siguiente ecuación: y = 18,798x + 40,175 (R 2 = 0,249) (n = 30). (····) Intervalo de confianza para el 95 %.
La recta de regresión obtenida es: y = 18,798x + 40,175 (R 2 = 0,249). Se encontró una correlación significativa entre la concentración radiactiva y el tiempo transcurrido (p = 0,005).
DISCUSION
El aumento de porcentaje de 18F-Fluoruro determinado en la Unidad de Radiofarmacia con el tiempo y su correlación con la concentración radiactiva está de acuerdo con estudios anteriores en los que se observó un aumento de porcentaje de 18F-Fluoruro con el tiempo y la concentración radiactiva debido a la autorradiolisis1. La existencia de valores negativos (es decir, una disminución de porcentaje de 18F-Fluoruro) podría ser explicado por la incertidumbre asociada a este método de determinación.
La correlación del aumento de porcentaje de 18F-Fluoruro con la concentración radiactiva no nos permite predecir este aumento a partir de la concentración radiactiva (R 2 = 0,1977).
Las diferencias encontradas entre los resultados obtenidos en la Unidad de Radiofarmacia y los obtenidos en el Laboratorio de radiofármacos PET, se explican en parte por la concentración radiactiva y el tiempo transcurrido desde la dispensación, aunque este último factor en menor medida debido a que el aumento de correlación al tener en cuenta el tiempo es poco significativo (p = 0,014 y en el caso de considerar sólo la concentración radiactiva p = 0,016), que puede ser debido a la correlación observada entre esta concentración radiactiva y el tiempo transcurrido desde su dispensación. En ambos casos, la correlación no nos permite predecir la diferencia que esperamos encontrar a partir de la concentración radiactiva y el tiempo (R 2 = 0,196 y R 2 = 0,226). Por otro lado, este aumento no significativo de la correlación al tener en cuenta el tiempo podría ser debido a la incertidumbre en el tiempo transcurrido desde la dispensación, ya que este tiempo podría llegar a ser hasta una hora menor mientras que el tiempo medio fue de 127 minutos. Otro factor que puede explicar esta diferencia entre los resultados obtenidos en la Unidad de Radiofarmacia y el Laboratorio de radiofármacos PET puede ser la diferente metodología empleada (HPLC en el LPET y TLC en la UR). La separación por TLC da lugar a un mayor factor "arrastre" de las especies a separar, que en ocasiones puede sobreestimar las áreas de los picos en el origen que en nuestro caso es la zona crítica por tener el pico menor.
En nuestro estudio comprobamos que la dilución de la 18F-FDG con solución salina fisiológica minimiza la posible pérdida de pureza radioquímica por efecto de la radiolisis durante el tiempo de almacenamiento hasta su utilización. En la mayoría de las Unidades de Radiofarmacia no se realiza habitualmente el control radioquímico de las preparaciones de 18F-FDG. En general, basta el certificado de calidad expedido por el LPET y el periodo de validez garantizado por el mismo. Asimismo, una guía de procedimiento FDG-PET permite la posibilidad de diluir el radiofármaco con suero salino fisiológico5. El estudio realizado por nosotros demuestra que la dilución de 18F-FDG con suero salino fisiológico, además de facilitar el manejo y la preparación de dosis individuales, aumenta la estabilidad del radiofármaco. En el caso de que el LPET se encuentre más alejado de la UR, el tiempo transcurrido desde la dispensación de la FDG hasta su llegada a la UR puede ser mucho mayor que el presentado en este estudio. En estos casos la concentración del radiofármaco al finalizar su preparación puede ser mucho mayor que las concentraciones más altas incluidas en este trabajo. De este modo, podría ser aconsejable realizar la dilución en el propio LPET y/o realizar el control de la pureza radioquímica a su recepción en la UR.
CONCLUSIONES
La estabilidad de las preparaciones de 18F-FDG aumenta al disminuir su concentración. Debido a este aumento de la estabilidad se puede aconsejar la dilución del vial multidosis con solución salina fisiológica, sobre todo en aquellos con alta concentración radiactiva y en los que el tiempo transcurrido entre la preparación y la dispensación para su uso inmediato pueda ser elevado.
Recibido: 7/4/05.
Aceptado: 14/7/05.
Correspondencia:
I.R. Jiménez Romero
Medicina Nuclear
Hospital Universitari de Bellvitge-IDIBELL
Feixa Llarga, s/n
08907 L'Hospitalet de Llobregat. Barcelona.
Correo electrónico: ijimenez@csub.scs.es