Los aloinjertos óseos estructurales han supuesto una alternativa al tratamiento de los tumores óseos de miembros, con posibilidad de cirugía de conservación del mismo. Presentamos un estudio retrospectivo observacional del manejo de los aloinjertos óseos estructurales en tumores óseos de huesos largos en nuestro hospital, durante los años 1993 a 2010, en el que obtenemos una muestra de 37 pacientes subsidiarios de esta técnica quirúrgica. Mediante la obtención de datos clínicos de la muestra aplicamos las escalas de funcionalidad de Mankin y EVACOM HUVA con resultados excelentes, muy buenos o buenos del 84%, y con los datos radiológicos aplicamos la escala de osteointegración ISOLS con un 95,6% de resultados excelentes a los 24 meses. Estos resultados nos muestran que los aloinjertos óseos estructurales constituyen una técnica válida y reproducible en pacientes con tumores óseos destructivos de huesos largos.
Structural bone allografts have become an alternative in the treatment of limb bone tumours with a chance of limb-saving surgery. We present an observational retrospective study on the use of structural bone allografts in bone tumours of the long bones in our hospital between January 1993 and January 2010, with a sample of 37 patients subjected to this surgical technique. After obtaining clinical information from our sample we applied the Mankin and EVACOM HUVA functional scales with excellent, very good and good results in 84%, and with the radiological information we applied the ISOLS osseointegration scale, with 95.6% of excellent results after 24 months. These results demonstrate that structural bone allografts are a valid and reproducible technique in patients with destructive long bone tumours.
La evolución constante de la medicina ha supuesto la aparición y el desarrollo de nuevas tecnologías que han permitido mejorar los resultados obtenidos en el tratamiento de las diferentes afecciones. Al igual que en otras disciplinas médicas, el enfoque inicial en el manejo de la cirugía oncológica consiste en preservar la vida y limitar el daño ocasionado manteniendo la funcionalidad del miembro afecto en la medida de lo posible. Sin embargo, la medicina actual exige, además, la optimización de la calidad de vida evitando al máximo las complicaciones atribuibles a los tratamientos y el minimizar el uso de procedimientos de mutilación como las amputaciones1. En este sentido, uno de los avances más importantes de los últimos 50 años ha sido el desarrollo de los bancos de huesos y tejidos, cuyo impacto es de tal magnitud que una gran cantidad de las cirugías que se realizan hoy en día en los mejores centros de cirugía ortopédica son posibles gracias a la disponibilidad de aloinjertos óseos y tendinosos2. De este modo, en los últimos años, con el avance de la quimioterapia, las nuevas tecnologías de criopreservación de tejidos y el desarrollo de nuevos instrumentos y técnicas quirúrgicas en el tratamiento de los tumores, han cambiado los planteamientos de la cirugía oncológica ósea, lo que hace que la amputación sea cada vez menos frecuente y prosperen técnicas que permiten preservar la extremidad3.
En la cirugía tumoral se requieren resecciones extensas que precisan de una compleja reconstrucción, para la cual se pueden proponer diferentes alternativas como las endoprótesis y el trasplante óseo, autólogo o alogénico1.
En el año 1993 se inician en nuestro centro estas técnicas de reconstrucción de los defectos óseos mediante el uso de aloinjertos estructurales, siendo el tratamiento de elección en la cirugía reconstructiva tumoral debido a los resultados satisfactorios desde el punto de vista funcional. Nuestro objetivo es mediante un estudio descriptivo, valorar nuestra experiencia y los resultados obtenidos en el manejo de los aloinjertos óseos estructurales, tanto en lo que se refiere a la técnica quirúrgica empleada como a la propia afección tumoral.
Material y métodosTodos los pacientes incluidos en el estudio fueron diagnosticados de tumoración ósea destructiva benigna o maligna, tratados mediante el uso de aloinjertos óseos estructurales para suplir el defecto óseo creado tras la resección y seguidos en nuestro centro durante un período medio de de 60 meses (rango: 5-153). Realizamos un estudio de series de casos clínicos descriptivo, retrospectivo, observacional y longitudinal, a lo largo de un período de tiempo desde el 1 de enero de 1993 a 1 de enero de 2010, en un grupo de 37 pacientes diagnosticados y tratados íntegramente en el Hospital Universitario Virgen de la Arrixaca, analizando los resultados del tratamiento con aloinjertos en función de la técnica quirúrgica utilizada, morbilidad, complicaciones, escalas de funcionalidad y satisfacción de Mankin4 y EVACOM HUVA (tablas 1 y 2), escala de osteointegración de ISOLS5 (tabla 3), tasas de recidiva tumorales, supervivencia de los pacientes y supervivencia de los aloinjertos en función de sus factores de riesgo, siguiendo los protocolos establecidos por el hospital para acceder a los datos de las historias clínicas con la finalidad de poder realizar este tipo de publicación para la investigación y divulgación para la comunidad científica.
Variables a medir según la escala de Mankin y su puntuación
| Variables | 1 | 2 | 3 |
| Dolor | Diario | Ocasional | Ninguno |
| Movilidad | 1/3 del normal | 2/3 del normal | Completa |
| Deambulación | Dos bastones | Un bastón o alza | Sin bastones |
| Calidad de vida | Mala | Con restricciones | Integrado |
| Psicología | No aceptación-introversión | Secuelas | Aceptado-vida normal |
Excelente: 13-15 puntos; bueno: 9-13 puntos; regular: 6-8 puntos; malo: 3-5 puntos.
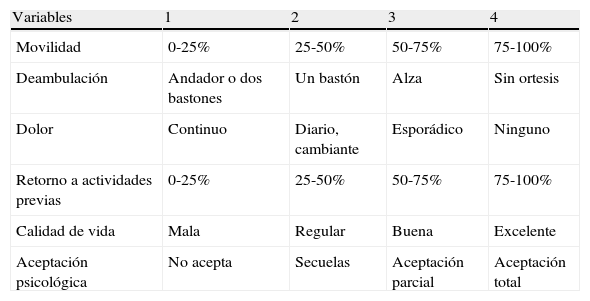
Variables a medir según la escala EVACOM HUVA y su puntuación
| Variables | 1 | 2 | 3 | 4 |
| Movilidad | 0-25% | 25-50% | 50-75% | 75-100% |
| Deambulación | Andador o dos bastones | Un bastón | Alza | Sin ortesis |
| Dolor | Continuo | Diario, cambiante | Esporádico | Ninguno |
| Retorno a actividades previas | 0-25% | 25-50% | 50-75% | 75-100% |
| Calidad de vida | Mala | Regular | Buena | Excelente |
| Aceptación psicológica | No acepta | Secuelas | Aceptación parcial | Aceptación total |
Excelente: 22-24 puntos; muy bueno: 19-21 puntos; bueno: 15-18 puntos; regular: 12-14 puntos; malo: 8-11 puntos; muy malo: 4-7 puntos.
Para calcular las diferencias entre los distintos aspectos estudiados se utilizó la prueba Log-Rank (Mantel-Cox) mientras que otras estimaciones fueron calculadas a través del método exacto de Fisher y Chi-cuadrado de Pearson, considerando un valor de p<0,05 como estadísticamente significativo.
Se descartaron en el estudio aquellos pacientes con tumores óseos malignos de miembros que no fueron subsidiarios de cirugía de conservación de la extremidad y aquellos diagnosticados pero no tratados en nuestro centro.
La casuística comprendió 41 casos, de los que 4 pacientes fueron desestimados, dos por ser derivados a otro centro para su tratamiento (osteosarcomas ilíacos susceptibles, a priori, de cirugía conservadora), otro por ser intervenido en un centro de otra comunidad autónoma y otro que sufrió cardiotoxicidad en el tratamiento quimioterápico neoadyuvante, falleciendo al inicio del mismo.
De los 37 pacientes de la serie, 18 fueron varones (48,6%) y 19 fueron mujeres (51,4%), con una edad media de 29,27 años (rango: 14-74 años), siendo la década más frecuente la segunda con un 35,13%.
No existieron antecedentes oncológicos familiares en el grupo de pacientes de nuestro estudio salvo en un caso de osteosarcoma condroblástico con un antecedente en un familiar de primer grado de osteosarcoma óseo no filiado. En cuanto a los antecedentes personales, solo destacan las metástasis de carcinoma de mama con antecedente, en los 4 casos de nuestra serie, de carcinoma mamario primario tratado mediante mastectomía radical y quimioterapia- radioterapia según protocolo.
Clínicamente, el 94,6% de los pacientes presentaron dolor en la primera consulta, un 45,9% refirió aumento subjetivo de tamaño del miembros y un 78,4% presentaba alteración funcional. En la exploración física, un 37,8% de los pacientes presentaba inflamación a la exploración física, un 48,6% presentaba aumento de tamaño del miembro afecto y un 81,1% tenía alteración funcional con respecto al miembro contralateral.
Se localizaron tres casos en húmero (8,1%), 18 casos en fémur (48,6%), 11 casos en tibia (29,7%) y 5 casos en radio (13,5%). Los casos desarrollados en húmero fueron todos en la región proximal (tres casos, 8,10%); en fémur, tres casos en fémur proximal (8,10%), tres casos en fémur medio (8,10%) y 12 casos en fémur distal (32,43%) siendo ésta la localización tumoral más frecuente; en tibia, los 11 casos se localizaron en tibia proximal (29,72%) y los casos que se desarrollaron en radio fueron todos en radio distal (5 casos, 13,51%).
El tiempo hasta la primera consulta en nuestra especialidad fue de 3,69 meses (rango: 0,1-12 meses), el tiempo medio hasta el diagnóstico de neoplasia ósea fue de 2,13 meses (rango: 0,1-24 meses), mientras que el tiempo medio hasta la realización del tratamiento quirúrgico fue de 6,89 meses (rango: 0,3-48 meses).
Desde el punto de visto de las exploraciones complementarias, en la radiología convencional la insuflación de la cortical fue el hallazgo radiológico más frecuente en un 94,6%; en la tomografía axial computarizada (TAC), hubo rotura cortical en un 89,2% y destrucción medular en un 64,9%, mientras que en la resonancia magnética (RM) la media de longitud tumoral fue de 7,81 centímetros (rango: 3,5-15 centímetros), con infiltración de partes blandas en un 37,8% y afectación fisaria en un 50% de los pacientes menores de 17 años, sin pacientes con afectación neurovascular.
Referente al estudio de extensión de los tumores óseos primarios del estudio, fue negativo en el 100% de los casos en radiología convencional, TAC, RM y gammagrafía ósea.
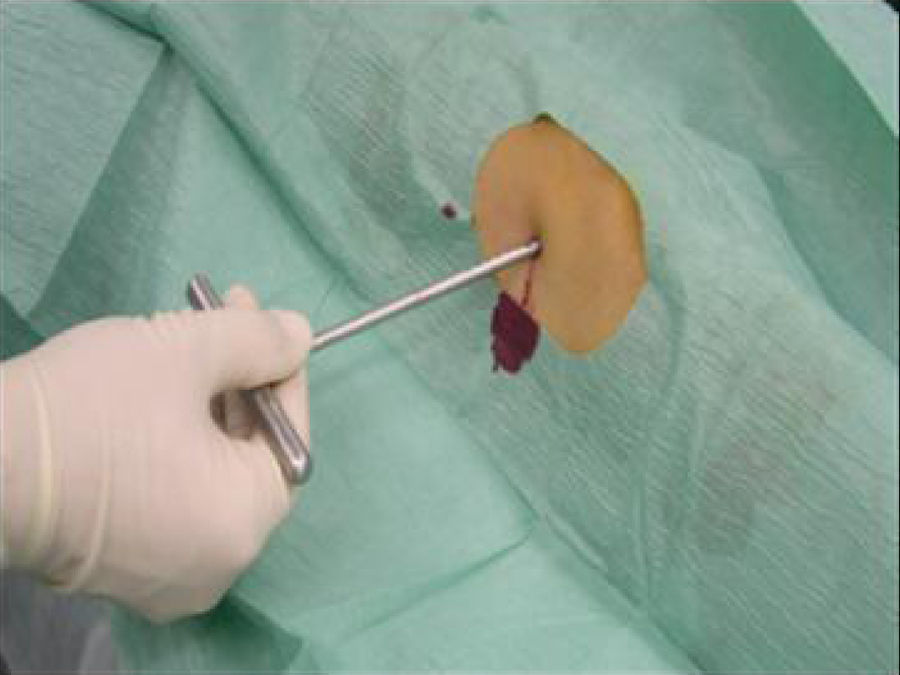
Desde el punto de vista anatomopatológico, a un 97,3% de los pacientes se les practicó una biopsia preoperatoria percutánea mediante trócar guiada con radioescopia bajo anestesia local y sedación (figs. 1 y 2). Solo un caso precisó la realización de biopsia abierta (2,7%), por no lograr obtener material suficiente para el diagnóstico.
Nuestra serie comprendió 17 osteosarcomas (45,9%) de los cuales 6 eran osteosarcomas convencionales (16,2%), 7 osteosarcomas parostales (18,9%), dos osteosarcomas condroblásticos (5,4%), un osteosarcoma periostal (2,7%) y un osteosarcoma telangiectásico (2,7%). Hubo 10 casos de tumor de células gigantes (27%), de los cuales 5 casos fueron convencionales (13,5%) y 5 casos asociados a componente aneurismático (13,5%). Hubo 4 casos de metástasis de carcinoma mamario (10,8%), tres casos de condrosarcoma (8,1%), dos casos de sarcoma de Ewing (5,4%) y un caso de osteoblastoma maligno (2,7%).
Según el estadio de Enneking6, clasificamos a los 23 sarcomas óseos de nuestro estudio con estadío IB en un 13,1%, estadío IIA en un 17,4%, estadío IIB en un 65,2% y estadío III en un 4,3% (tabla 4).
Solo 24 tumores de la serie fueron subsidiarios de quimioterapia (62,2%): 17 osteosarcomas, 4 casos de metástasis de carcinoma mamario, dos sarcomas de Ewing y un condrosarcoma de alto grado. Se excluyeron los 10 tumores de células gigantes de la serie (27%), dos condrosarcomas no subsidiarios de quimioterapia (8,1%) y el osteoblastoma maligno (2,7%).
Los tipos de quimioterapia (QT) fueron: neoadyuvante en un 4,2%, adyuvante en un 20,8% y neoadyuvante + adyuvante en un 75% (tabla 5). La complicación derivada de la QT más frecuente fueron las náuseas y vómitos en un 95,8%, con una media de 11 días de ingreso por las complicaciones.
En cuanto al método empleado, todos los aloinjertos de nuestra serie fueron aloinjertos de hueso estructural procedentes de donantes multiorgánicos y fueron remitidos desde el Banco de Tejidos de Alicante, perteneciente a la Red del Banco de Órganos y Tejidos de la Comunidad Valenciana, el cual es el encargado del procesamiento y conservación de las piezas.
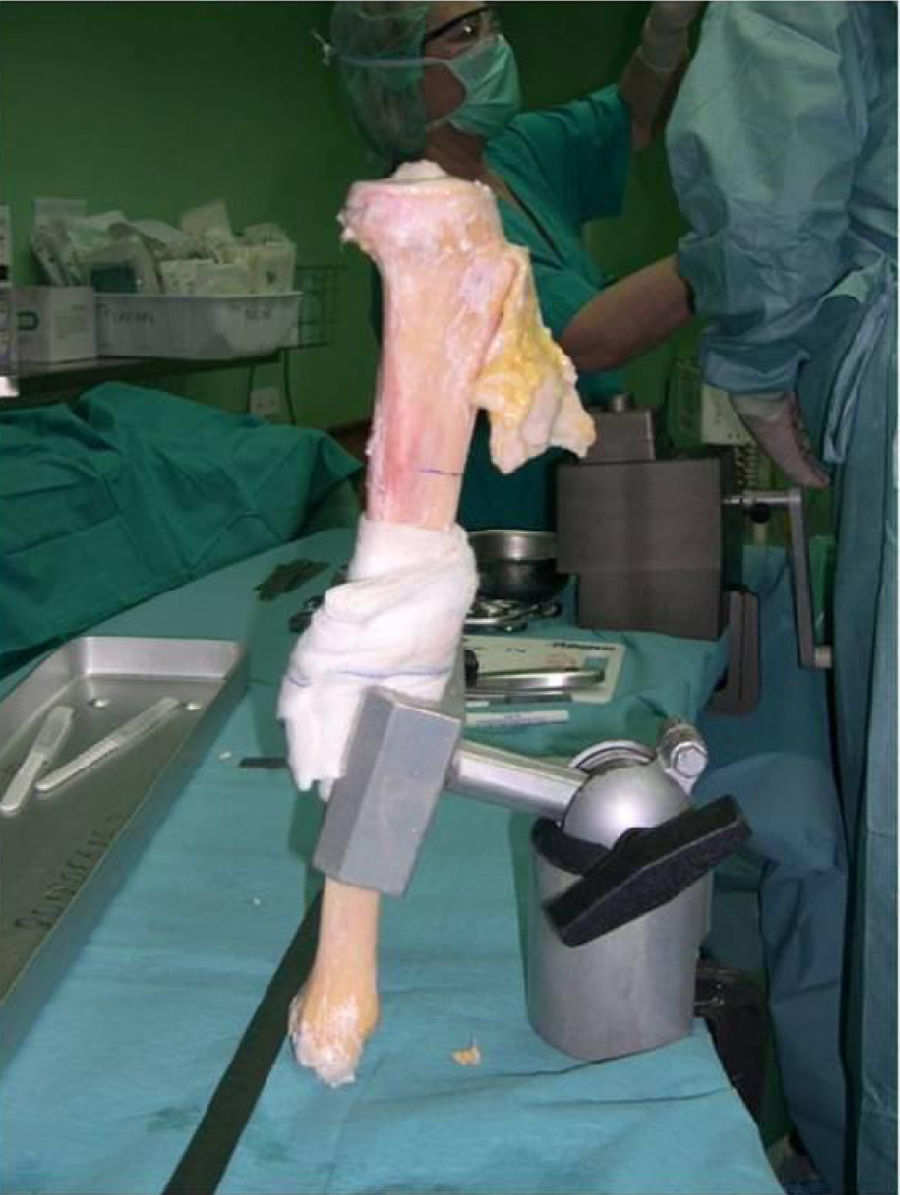
Una vez diagnosticado el paciente de un tumor óseo destructivo de huesos largos, a continuación es valorado en un Comité de Tumores para decidir conjuntamente la decisión que se ha de adoptar, valorando si es subsidiario de cirugía de conservación de la extremidad. En este caso, tras una planificación preoperatoria minuciosa y la obtención del consentimiento informado, se realiza una resección en bloque del tumor con unos márgenes quirúrgicos amplios entre 2,5-5 centímetros, incluyendo en la incisión la zona de biopsia, y una toma de biopsia de la zona intramedular adyacente a la osteotomía, la cual se presupone sana. En otro campo quirúrgico, un segundo equipo realiza la confección del aloinjerto óseo estructural, una vez medido con exactitud el defecto. Una vez confeccionado, se utilizan distintas técnicas para la estabilización del mismo según la localización del tumor óseo (figs. 3-9).
En nuestra serie, la media de resección tumoral fue de 14,7 centímetros, con un rango de 4,5-30 centímetros, con un margen de seguridad de resección ósea proximal de 4,3 centímetros de media (rango: 1-10 centímetros), y un margen de seguridad de resección ósea distal de 4,9 centímetros de media (rango: 1-10 centímetros). La biopsia del canal medular adyacente a la osteotomía en todos los tumores malignos resultó negativa en el 100% de los casos.
La estabilización del aloinjerto se realizó con endoprótesis en un 59,5%, con clavo intramedular en un 5,4%, con placa en un 16,2%, con endoprótesis más clavo intramedular en un 10,8% y con endoprótesis más placa en un 8,1%.
Se realizó aporte de injerto de cadáver en la zona de interfase huésped-aloinjerto en un 54,1%, mientras que en un 24,3% se asoció aloinjerto liofilizado al injerto de cadáver, no aportándose injerto en un 21,6%. Se realizó cobertura plástica en un 13,5%, siendo 4 casos en tibia proximal mediante colgajo muscular de rotación del gastrocnemio medial y un caso en fémur distal mediante un colgajo miocutáneo de vasto lateral.
Se precisó de una media de 3 UI de necesidades transfusionales (rango: 1-9 UI), con una media de tiempo de cirugía de 6,3 horas (rango: 4-7,5 horas) y una estancia hospitalaria media de 11 días (rango: 4-40 días).
Como complicaciones de los pacientes de nuestro estudio tuvimos:
- a)
Infecciones herida quirúrgica en el postoperatorio inmediato: se evidenciaron en dos pacientes (5,4%), siendo infecciones cutáneas superficiales producidas en ambos casos por Staphylococcus epidermidis, tratadas mediante antibioterapia intravenosa con vancomicina y curas locales diarias.
- b)
Fracturas: siendo incompletas en dos casos de tibia proximal (5,4%) y completa en un caso de fémur distal (2,7%), produciéndose todas por discrepancia de diámetro entre aloinjerto-endoprótesis-hueso receptor. Se resolvieron con un mayor tiempo de espera para la carga completa del miembro (4 meses en las fracturas incompletas y 5 meses en la fractura completa).
- c)
Pseudoartrosis (no evidencia de unión entre aloinjerto-receptor después de 6-8 meses o movilidad de foco con callo atrófico o hipertrófico): se desarrolló en 5 pacientes (13,5%), precisando 4 pacientes de reintervención para curetaje, aporte de injerto y nueva estabilización, mientras que uno de ellos se mantuvo en abstención terapéutica por estar asintomático, falleciendo por causas oncológicas a los 10 meses.
- d)
Rotura de material: en dos casos (5,4%), ambos precisaron de reintervención quirúrgica.
- e)
Aflojamiento protésico: en 5 casos (13,5%), precisando todos ellos de recambio protésico.
En cuanto a los resultados en términos de funcionalidad, se aplicaron las siguientes escalas:
- –
Escala de Mankin4: con un 8,1% de resultados malos (retirada del aloinjerto, amputación del miembro o fallecimiento como consecuencia directa de una recidiva local), un 8,1% de resultados regulares (requerimiento de soporte externo para deambular, dolor o limitación funcional que interfiere en la vida laboral y de hogar), un 32,4% de resultados buenos (no evidencia de enfermedad, modesta limitación de la función, sin dolor y sin necesidad de soportes externos) y un 51,4% de resultados excelentes (no evidencia de enfermedad ni de dolor, función normal y sin limitaciones).
- –
Escala de Evaluación de Aloinjertos Óseos en Cirugía Oncológica Musculoesquelética del Hospital Univeristario Virgen de la Arrixaca (EVACOM HUVA): escala de uso interno hospitalario con unos resultados muy malos (4-7 puntos) en un 5,4%, malos (8-11 puntos) en un 2,7%, regulares (12-14 puntos) en un 8,1%, buenos (15-18 puntos) en un 18,9%, muy buenos (19-21 puntos) en un 13,5% y excelentes (22-24 puntos) en un 51,4%.
En función de la osteointegración radiológica aloinjerto-huésped, clasificamos los resultados en función de la escala ISOLS5 (International Symposium on Limb Salvage), la cual clasifica la unión aloinjerto-hueso en referencia al porcentaje de línea radioluciente visible radiográficamente como: excelente (línea de osteotomía no visible), buena (unión >75% con una línea de osteotomía todavía visible), aceptable (unión entre el 25-75%) y pobre (no evidencia de callo o unión <25%). Los resultados que obtuvimos fueron los siguientes:
- •
A los tres meses, un 83,8% de los pacientes muestran un resultado pobre en la radiología convencional, con un 16,2% con un resultado aceptable.
- •
A los 6 meses, un 46,7% muestran un resultado bueno en cuanto a osteointegración del aloinjerto, con un 37,2% de resultados aceptables y un 16,1% de resultados pobres que incluyen los pacientes con pseudoartrosis y un paciente con retardo de consolidación. En dos pacientes no se pudo hacer la medición ya que fallecieron por causas oncológicas.
- •
A los 12 meses, un 50% muestra un resultado excelente, con un 37,5% de resultado bueno, un 9,4% con resultado aceptable y un 3,1% con resultado pobre que incluye un paciente con pseudoartrosis inicial reintervenido a los 9 meses y sin evidencia de osteointegración radiológica. En 5 casos no se pudo hacer la medición, tres casos por fallecimiento por causas oncológicas y dos casos por cambio de país de residencia.
- •
A los 18 meses, un 88,5% muestra resultados excelentes, por un 11,5% con un resultado bueno. En 11 pacientes no se pudo medir la consolidación radiológica, 5 de ellos por fallecimiento por causas oncológicas, dos pacientes por cambio de residencia y 4 pacientes por no acudir a revisión.
- •
A los 24 meses, un 95,6% muestra resultados excelentes, con 4,4% con resultado bueno. Catorce pacientes no pudieron ser medidos, 6 por fallecimiento por causas oncológicas, dos pacientes por cambio de residencia y 6 pacientes por no acudir a revisión.
En cuanto a la tasa de recidiva tumoral, la tasa global de recidiva tumoral fue del 29,7% (11 pacientes), siendo sarcomas óseos en 8 pacientes. De ellos, en 7 casos (87,5%) el estadio era IIB, por un caso (12,5%) de osteosarcoma parostal con estadio III. El tiempo medio hasta la recidiva fue de 11 meses, con un rango de 3-42 meses, observándose que el fracaso de los aloinjertos ocurre principalmente en el primer año tras la cirugía, manteniéndose estables posteriormente.
La tasa global de metástasis fue del 29,7%, con un tiempo medio transcurrido desde el diagnóstico de 21 meses (rango: 5-54 meses) y de 17 meses de media desde el tratamiento quirúrgico (rango: 3-52 meses). Se produjeron en dos casos de osteosarcoma convencional, dos casos de osteosarcoma parostal, dos casos de sarcoma de Ewing, tres casos de metástasis por carcinoma mamario, un caso de osteosarcoma periostal y un caso de condrosarcoma, siendo la localización más frecuente el pulmón con un 63,6% y recibiendo tratamiento paliativo en un 72,7% por un 29,7% de tratamiento quirúrgico de las metástasis. En los 8 sarcomas óseos de los 11 pacientes con metástasis, el estadio predominante fue el IIB en un 75% (6 casos), por un caso (12,5%) con estadio III de un osteosarcoma parostal (12,5%) y un caso (12,5%) estadio IIA de un condrosarcoma.
En relación a la supervivencia de los pacientes de nuestra serie, a día 1 de enero de 2010 y tras un período medio de seguimiento de 60 meses (rango: 5-153 meses), la tasa global de fallecimiento de los pacientes fue de 32,4% (12 casos), con un 67,6% (25 casos) de los pacientes vivos. El 100% de los casos de exitus fue por causas oncológicas en tumores malignos, sin relación alguna con el tratamiento mediante aloinjertos óseos, produciéndose un 70% de los fallecimientos entre los tres y 5 años postcirugía.
La supervivencia global de los aloinjertos de nuestra serie fue del 70,3%, con un mayor porcentaje de fracasos de la técnica en el primer año para posteriormente mantenerse estables y con ausencias de fracasos.
En relación a los resultados en términos de supervivencia de los aloinjertos según los distintos factores de riesgo, en función del estadio de Enneking obtuvimos una peor supervivencia global de los aloinjertos en sarcomas óseos con estadio de Enneking ≥IIB con mayores tasas de recidiva tumoral, siendo estadísticamente significativo (p<0,05). Del mismo modo, no obtuvimos resultados estadísticamente significativos en función de la agresividad tumoral (benigno-maligno), infección postoperatoria, fisura periprotésica, fracturas, pseudoartrosis, rotura del material, aflojamiento protésico, estabilización del aloinjerto mediante endoprótesis, placa o clavo o tipo de quimioterapia empleado, probablemente debido a la baja potencia de la muestra.
DiscusiónLos aloinjertos óseos estructurales han supuesto una alternativa al tratamiento de los tumores óseos de miembros con posibilidad de cirugía de conservación del miembro. En nuestro estudio, no hubo diferencias en los estudios revisados con respecto a la proporción varón/mujer, edad de presentación, antecedentes personales, presentación clínica y exploración física.
En nuestra serie, el tiempo medio desde que el paciente refiere el inicio de la sintomatología hasta que consulta con el médico especialista en Traumatología fue de 3,6 meses, con un rango de 0,1-12 meses. Así mismo, el tiempo medio desde que el médico especialista valora al paciente hasta que realiza el diagnóstico anatomopatológico definitivo fue de 2,1 meses, con un rango de 0,1-24 meses, lo cual hace un tiempo medio desde el comienzo de la clínica hasta el diagnóstico de 5,7 meses. Esta cifra de retraso en el diagnóstico va en descenso con respecto a la revisión de las publicaciones7 y con respecto a las series publicadas en el Hospital Virgen de la Arrixaca de Murcia8,9, lo cual muestra la mejoría en el diagnóstico precoz de estas lesiones. Esta mejoría va íntimamente unida a la creación de centros de referencia en tumores óseos y a la constitución en dichos centros de Comités de Tumores de Expertos en Patología Tumoral de las distintas especialidades, que planifican individualmente la táctica de obtención del diagnóstico definitivo y su posterior tratamiento con la mayor premura posible. Pero, a pesar de esta mejoría, estas cifras de retraso diagnóstico nos deben hacer reflexionar aún más acerca de cómo reforzar la conciencia del médico de Atención Primaria para la sospecha y diagnóstico precoz de estas lesiones, ya que en nuestra serie el 65% de los casos eran un estadio IIB de Enneking, al igual que en la literatura publicada10, implicando éste un peor pronóstico y una mayor agresividad del tumor que en estadios iniciales.
La articulación afectada con mayor frecuencia fue la rodilla en un 62% de los casos, lo cual corresponde con los datos aportados por autores como Mankin11 o Muscolo12, con tasas de tumoraciones alrededor de la rodilla del 60-70%. Esta localización, muy probablemente se relacione con el hecho de la existencia de la asociación edad-localización-período de crecimiento óseo, afectando normalmente a gente joven y con un mayor crecimiento óseo en las fisis yuxtaarticulares de la rodilla, donde este crecimiento es mayor.
El tratamiento mediante aloinjertos óseos aplicados a los pacientes de nuestra serie precisó de una adecuada estabilización quirúrgica según la localización tumoral, siendo la estabilización mediante endoprótesis la más frecuente de nuestra serie, con un 78%, por ser la rodilla la localización más frecuente de los tumores estudiados, obteniendo resultados similares a las distintas series13.
En cuanto a la funcionalidad de los aloinjertos implantados en los pacientes de nuestro estudio, aplicamos para su valoración las escalas de Mankin y EVACOM HUVA. Según la escala de Mankin, y tras un período de seguimiento medio de 60 meses con un 67,6% de los pacientes vivos (25 casos), en nuestro estudio se obtuvieron unos resultados excelentes y buenos en prácticamente en un 84%, obteniéndose solo en un 16,2% un resultado regular o malo, que fueron debidos a causas oncológicas de recidiva local y no derivadas del aloinjerto. Sin los citados problemas oncológicos obtendríamos hipotéticamente unos resultados excelentes y buenos cercanos al 100% en nuestra serie, superiores a los obtenidos por Mankin en su serie con un 85% de resultados excelentes14, pero no superponibles debido a la baja potencia muestral.
En cuanto a la escala EVACOM HUVA, la suma de los resultados excelentes, muy buenos y buenos fue de un 84%. Al igual que en la escala de Mankin, los resultados negativos del uso de aloinjerto fueron debidos a causas oncológicas en forma de recidiva tumoral. Estos resultados de la escala EVACOM HUVA no son comparables a otras series de evaluación de la funcionalidad de los aloinjertos debido a que es una escala de uso interno hospitalario, aunque con muy buena correlación con la escala de Mankin y con el aporte de mayor información en cuanto a satisfacción del paciente y calidad de vida.
En relación a la funcionalidad de los aloinjertos medida en las escalas de Mankin y EVACOM HUVA, no encontramos diferencias estadísticamente significativas con respecto a los protocolos y tipo de quimioterapia utilizados ni con respecto a la agresividad tumoral (benigno-maligno) o el tipo de estabilización del aloinjerto utilizada, sí encontrando relación estadísticamente significativa (p<0,05) con mejores resultados en ambas escalas a mayor supervivencia del aloinjerto y a mayor valoración radiológica del aloinjerto en la escala ISOLS. Sí hubo relación, aunque no estadísticamente significativa por la baja potencia muestral, entre los resultados funcionales y el estadiaje de Enneking, siendo peores los resultados en las escalas de Mankin y EVACOM HUVA en estadios de Enneking iguales o superiores a IIB, por la mayor tasa de recidivas tumorales y peor supervivencia del aloinjerto.
Estos resultados en cuanto a funcionalidad del paciente en el que se ha implantado un aloinjerto estructural, unido a la similitud de resultados de las grandes series de Enneking15, Muscolo12, Fox16 o Donati13, nos muestran que los aloinjertos óseos constituyen una técnica válida y reproducible en pacientes con tumores óseos destructivos de huesos largos, permitiendo una mejor calidad de vida y aceptación psicológica que otras técnicas de cirugía tumoral como la amputación del miembro o la reconstrucción con megaprótesis, como se muestra en el estudio publicado por DiCaprio y Friedlaender17.
Del mismo modo, al igual que se realiza la valoración de la funcionalidad de los pacientes, realizamos la valoración de la osteointegración de los aloinjertos medida radiológicamente según la escala del International Symposium on Limb Salvage (ISOLS) en función de la línea radiolucente visible en la radiología convencional. Tras un seguimiento medio de 60 meses, en nuestra serie obtuvimos unos resultados que fueron mejorando sustancialmente con el paso del tiempo, con ningún resultado excelente a los tres meses (aceptable en un 16%), ningún resultado excelente a los 6 meses (bueno en un 47% y aceptable en un 37%), 50% de resultados excelentes a los 12 meses (37,5% buenos), 88,5% de resultados excelentes a los 18 meses y un 95,6% de resultados excelentes a los 24 meses. Estos resultados son similares a los obtenidos por San Julián18 en sus publicaciones y nos muestran que el aloinjerto óseo precisa de un tiempo mínimo de 6 meses para evidenciarse radiológicamente signos de buen pronóstico en cuanto a osteointegración, consiguiendo los mejores resultados radiológicos a partir de los 12 meses de la cirugía.
Estos resultados radiológicos muestran diferencias estadísticamente significativas (p<0,05) en relación a:
- a)
Resultados funcionales obtenidos en las escalas de Mankin y EVACOM HUVA: con mejor funcionalidad del paciente intervenido en relación a la mejor osteointegración radiológica del aloinjerto.
- b)
Localización: siendo la consolidación radiológica, entendida como un ISOLS bueno o excelente, una media de 4 meses más rápida en los aloinjertos colocados a nivel metafisoepifisario que en los aloinjertos colocados a nivel diafisario.
Con resultados similares a las distintas series, encontramos diferencias, aunque no estadísticamente significativas por la baja potencia muestral, en cuanto a la administración o no de quimioterapia, siendo más rápida la consolidación del aloinjerto en aquellos tumores que no recibieron quimioterapia.
En función de los resultados oncológicos obtenidos medimos la supervivencia de los aloinjertos, obteniendo en nuestro estudio un 30% de recidiva tumoral a los 11 meses de media, lo que nos muestra que el mayor porcentaje de recidivas ocurre dentro del primer año, precisando por ello revisiones periódicas, con una supervivencia de los aloinjertos muy alta tras este primer año.
En los pacientes con recidiva local tumoral de nuestro estudio, se encontraron diferencias estadísticamente significativas (p<0,05) en cuanto a la probabilidad de recidiva tumoral en estadios de Enneking iguales o mayores de IIB, mientras que hubo diferencias, pero no estadísticamente significativas por la baja potencia de la muestra, en la probabilidad de metástasis según el estadio de Enneking, con mayores tasas en estadios iguales a superiores al IIB. Estas consideraciones, unidas a lo previamente comentado en cuanto a retrasos en el diagnóstico de los tumores óseos, nos muestran la importancia de una adecuada selección de los pacientes19 y de la realización de un diagnóstico y tratamiento precoz con el fin de comenzar el tratamiento conservador de la extremidad en estadios precoces y disminuir la tasa de recidivas de la técnica.
En cuanto a la supervivencia de los pacientes de nuestra serie, y tras un seguimiento medio de 60 meses, la tasa global de supervivencia a día 1 de enero de 2010 fue del 68%, con una tasa de fallecimiento del 32%, de los cuales, el 100% fueron por causas oncológicas. Solo en un caso de los supervivientes había presencia de enfermedad por metástasis recidivadas, obteniendo en nuestra serie un intervalo libre de enfermedad de 50 meses y un intervalo de supervivencia (desde el diagnóstico de afección tumoral) de 58 meses. Estos datos son similares a las grandes series de Muscolo12, Mankin14 y Fox16 y muestran mejores tasas de supervivencia que las series de Donati13, lo que nos muestra que la técnica de reconstrucción mediante aloinjertos óseos es una opción quirúrgica válida en aquellos pacientes con las condiciones adecuadas que no afecta a la supervivencia de los pacientes en comparación con técnicas más agresivas como la amputación1,17.
Nivel de evidenciaNivel de evidencia IV.
Responsabilidades éticasProtección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.