Introdução
Entre janeiro de 2005 e junho de 2015, 410.101 casos de AIDS foram registrados no Brasil, numa distribuição que se expandiu para todo o território nacional de acordo com o último boletim epidemiológico do Ministério da Saúde.1 A média nacional para o registro anual nos últimos cinco anos foi de 40,6 mil casos de AIDS. A maior concentração de casos está na faixa etária entre 25 e 39 anos para ambos os sexos.1 Ou seja, a maioria das pessoas vivendo com HIV/AIDS (PVHA) estão no ápice de sua capacidade vital e passarão pelo processo de envelhecimento natural no cenário de uma doença crônica. Destaca-se a diminuição da proporção de PVHA com diagnóstico tardio da infecção em todas as faixas etárias, entre janeiro de 2009 e outubro de 2015, e um declínio contínuo, ao longo de todo o período, do diagnóstico tardio na faixa dos 25 a 39 anos.
Infelizmente, porém, nos estratos de idade mais avançada, o atraso no diagnóstico persiste – as maiores proporções de diagnóstico tardio foram observadas entre aqueles com 60 anos e mais. Essa proporção entre idosos chega a ser três vezes maior do que a observada entre os jovens de 18 a 24 anos, em outubro de 2015.
Nos últimos 10 anos, houve aumento na taxa de detecção de casos de AIDS na faixa dos 60 anos ou mais de idade.1 Isso significa que precisamos definir medidas específicas de prevenção e enfrentar as particularidades da terapia antirretroviral (TARV) para essa população.
Contextualizando o envelhecimento
O mundo está envelhecendo porque as pessoas estão vivendo mais tempo e morrendo menos. A população mundial está envelhecendo devido ao aumento da expectativa de vida e à diminuição da taxa de mortalidade. Precisamos nos preparar para as diferentes exigências desse processo. É fundamental sabermos se o envelhecimento se dá em boas condições de saúde.
Se os anos adicionais são vividos em boa saúde, a população que está envelhecendo estará associada ao crescimento humano como fonte de contribuição para a sociedade – por exemplo, como força de trabalho até os 70 anos de idade (considerados hoje os “antigos 60”).2 Contrariamente, se as pessoas estiverem envelhecendo com limitações em sua capacidade laboral, isso poderá significar que estarão contribuindo menos, socialmente.
Até o ano de 2025, teremos aproximadamente 2 bilhões de idosos no planeta, a maioria (80%) vivendo nos países em desenvolvimento.2 No Brasil, estima-se que em 2030 o número de pessoas com 60 anos de idade ou mais ultrapasse os 40 milhões.3
Esse é um contexto que deve interessar a cada um de nós como pessoas envelhecendo e como profissionais de saúde.
O acesso à TARV é o mais importante fator associado à sobrevida entre pacientes diagnosticados com infecção pelo HIV após os 50 anos de idade.
O envelhecimento na infecção pelo HIV
A partir da disponibilização da TARV combinada, em meados dos anos 1990, a expectativa de vida das PVHA cresceu significativamente. O Centers for Disease Control and Prevention (CDC) considera “idoso” a PVHA com 50 anos de idade ou mais.4 O aumento da prevalência do HIV em grupos etários mais velhos não foi acompanhado da criação de guias terapêuticos ou recomendações adequadas a essa população, e apenas recentemente esse tópico foi inserido nas pautas de discussão.
O acesso à TARV é o mais importante fator associado à sobrevida entre pacientes diagnosticados com infecção pelo HIV após os 50 anos de idade.5 A expectativa de vida atual para aqueles iniciando a TARV precocemente pode ser próxima à da população geral.6 Para pessoas não tratadas, o risco de eventos associados ou não ao HIV e o risco de morte são maiores quando comparadas àquelas em uso de ARV apresentando supressão viral.7-9
Além do benefício clínico, a TARV está também associada à redução do risco de transmissão do HIV.10 Assim, o benefício do tratamento suplanta, sem dúvida, seus malefícios; desse modo, hoje está indicado o início da TARV para todas as pessoas diagnosticadas com infecção pelo HIV, no momento de sua identificação, independentemente de idade e sem restrições de contagem de CD4.11,12
No contexto da TARV e do envelhecimento, a presença de morbidades associadas e, consequentemente, a necessidade de múltiplos tratamentos concomitantes constituem os principais desafios.
Fisiopatologia do envelhecimento na infecção pelo HIV
A velocidade do envelhecimento e a suscetibilidade para morrer jovem dependem de fatores genéticos e são definidas pelo DNA. Fatores ambientais, biológicos e o estilo de vida também influenciam na idade biológica ou fenotípica. A idade cronológica é aquela que mensuramos por anos de vida a partir do nascimento. A senescência é o aumento da idade cronológica de uma população de células, uma definição essencialmente biológica que corresponde à evolução natural.13
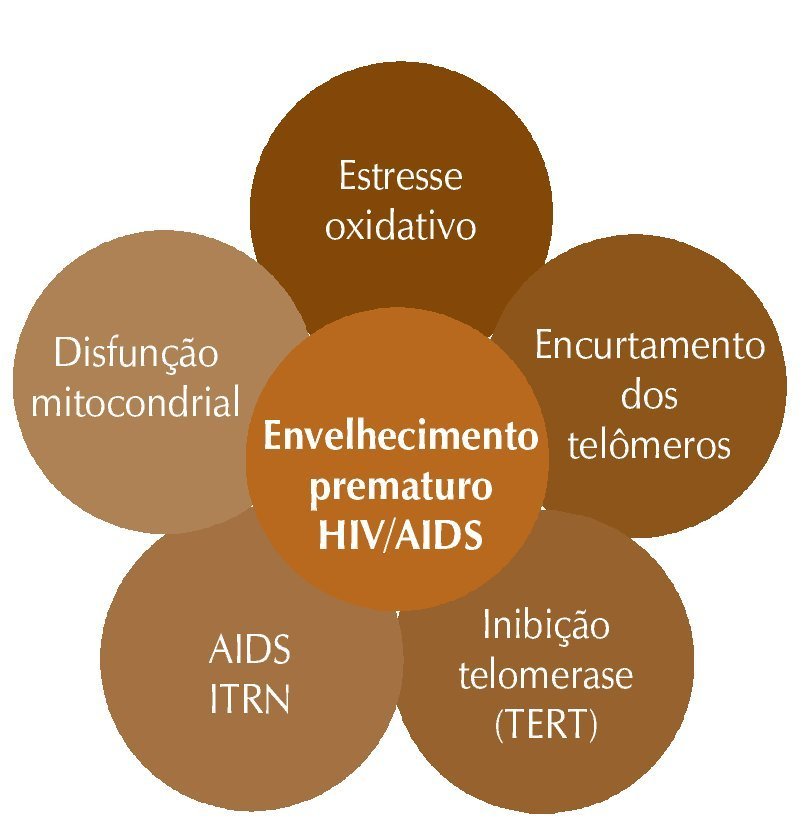
Todos os cromossomos das células eucariontes apresentam uma estrutura denominada telômero, um marcador de divisão celular cuja função é manter a estabilidade estrutural do cromossomo. Em condições normais de envelhecimento, toda vez que uma célula se replica, os telômeros encurtam até que a célula perca completa ou parcialmente a sua capacidade de divisão, culminando com a doença e a morte. A síntese de telômeros depende da enzima telomerase, uma transcriptase reversa (TR). Essa síntese ocorre ao final da replicação do DNA. Teorias que ajudam a explicar o envelhecimento biológico incluem o estresse oxidativo (lesão oxidativa mitocondrial excede a capacidade de defesa antioxidante) e o encurtamento dos telômeros, com consequente senescência celular, além do acúmulo de pré-lamina A – molécula que participa do processo de maturação, que tem a função de proporcionar um arcabouço para o núcleo celular e cuja anormalidade está associada à síndrome de progeria, caracterizada pela ocorrência de envelhecimento acelerado.14 Esses fatores podem ser potencializados ou causados pelo HIV per si, pela TARV ou pela associação de ambos.13 Os inibidores da transcriptase reversa do HIV-1 análogos de nucleosídios (ITRN) causam disfunção mitocondrial, estresse oxidativo e defeitos no DNA mitocondrial, que ocorrem tanto nos eventos não definidores de AIDS quanto no envelhecimento natural. Evidências apontam para o encurtamento dos telômeros associado aos ITRN por meio da inibição da TR da telomerase (TRT), sugerindo que isso contribua para o envelhecimento prematuro no HIV.15 Inibidores de protease (IP) também podem ter um papel no envelhecimento prematuro, pois estão associados ao acúmulo de pré-lamina A.14 A figura 1 mostra o complexo de interações envolvendo mecanismos para o envelhecimento na infecção pelo HIV.
Figura 1 Complexo de interações envolvendo mecanismos para o envelhecimento na infecção pelo HIV. Adaptado de: Torres RA, Lewis W. Aging and HIV/AIDS: pathogenetic role of therapeutic side effects. Lab Invest. 2014;94:120-8.
A semelhança estrutural entre análogos de nucleosídios nativos permite que os ITRN interfiram com a TR do HIV e inibam sua replicação.
Inibidores da transcriptase reversa do HIV-1 análogos de nucleosídios
A semelhança estrutural entre análogos de nucleosídios nativos permite que os ITRN interfiram com a TR do HIV e inibam sua replicação. Apesar de a toxicidade mitocondrial dos ITRN ser reconhecida, seus efeitos de longo prazo, como aqueles vistos em pacientes envelhecendo e tratados por décadas (infarto agudo do miocárdio, insuficiência cardíaca congestiva, insuficiência renal ou hepática, neuropatia, acidose lática e miopatia), ainda são pouco compreendidos e fazem parte do espectro de doença visto em pacientes envelhecendo, independentemente do HIV.14 Algumas evidências recentes associam a inibição da TRT pelos ITRN trifosfatos, e outras evidências sugerem o encurtamento do telômero como resultado da administração de zidovudina (AZT).14,16-19
Inibidores da protease
A lâmina A madura é gerada após vários passos da maturação celular e depois é removida por clivagem proteolítica.20 Defeitos na lâmina podem resultar de efeito colateral de IP no processo de inibição da protease do HIV. O indinavir e nelfinavir impedem a maturação da pré-lamina A in vitro em adipócitos. Eles causam acúmulo de pré-lamina A, como visto no envelhecimento precoce.21 Não sabemos se podemos extrapolar esses efeitos aos outros IP. Combinações com IP provavelmente contribuem para o envelhecimento por meio de um mecanismo que soma acúmulo de prélamina A com estresse oxidativo.21,22 Essas observações defendem uma relação até então não previamente reconhecida entre os IP e o desenvolvimento de doenças com a identificação de características de senescência nos tecidos afetados entre pacientes com HIV/AIDS.21
Inibidores da integrasse
Apesar da sua crescente utilização, efeitos colaterais dos INI não parecem diretamente envolvidos nos mecanismos de envelhecimento descritos anteriormente23 – talvez porque apenas recentemente passaram a fazer parte do arsenal terapêutico. Existe evidência para dislipidemia, geralmente aceitável para uso clínico.23,24
Uma vez que existe benefício em tratar e todos deverão ser tratados, a TARV não pode ser desvinculada do processo crônico da infecção pelo HIV e, consequentemente, do envelhecimento dessa população.
Estudos que explorem eventos celulares na interseção de doenças ou condições biológicas complexas como o envelhecimento são necessários para se obter dados da natureza de cada condição clínica que relaciona o HIV/AIDS ao envelhecimento.14 Essas abordagens poderão facilitar a busca por intervenções que minimizem ou anulem esses efeitos e promovam melhor qualidade de vida e saúde.
Estudos que explorem eventos celulares na interseção de doenças ou condições biológicas complexas, são necessários para se obter dados da natureza de cada condição clínica que relaciona o HIV/AIDS ao envelhecimento.
Múltiplas morbidades
A infecção pelo HIV parece aumentar o risco de múltiplas morbidades. Dados sugerem que PVHA, mesmo as adequadamente tratadas e controladas, têm risco cinco vezes maior do que outras doenças crônicas associadas.25,26 Quanto
maior o número de morbidades crônicas associadas, maior o risco de declínio na capacidade funcional.27,28 O impacto de múltiplas morbidades nas pessoas mais velhas também depende do tipo particular de doenças envolvidas.26-28
Considerando a importância desse cenário, a individualização da TARV deve ser pensada para os pacientes mais idosos apresentando múltiplas morbidades, além de uma abordagem multidisciplinar. Essa abordagem deve, minimamente, incluir avaliações metabólicas, pressão arterial, função renal, triagem para depressão e avaliação regular da doença hepática em indivíduos coinfectados por hepatite viral com ultrassom e estadiamento de fibrose.29 Além disso, talvez sejam necessárias avaliações mais amplas ou mais frequentes no processo de acompanhamento de pacientes com infecção pelo HIV e com 50 anos de idade ou mais, ainda que inicialmente não apresentem morbidades associadas.30
Escolha da TARV
Se a tendência atual das recomendações é simplificar a TARV, essa estratégia deve ser considerada ainda mais importante para os pacientes mais idosos com múltiplas morbidades, nos quais se somam medicamentos concomitantes e se sobrepõem toxicidades e maior risco de interações entre drogas. A OMS sugeriu a simplificação, recomendando um número limitado de opções preferenciais e dando prioridade aos ARV com eficácia e tolerabilidade superiores, considerando conveniência, disponibilidade de dose fixa e compatibilidade com tratamento de morbidades comumente associadas, além de potencial para serem utilizados em todas as populações (tabela 1).11 O guia da sociedade europeia (EACS) reduziu suas opções iniciais de 13 para seis, incluindo quatro inibidores de integrase (INI), um ITRNN e um IP reforçado com ritonavir (IP/r); essas alterações foram recomendadas com base nos resultados dos estudos com INI.29 O protocolo clínico e as diretrizes terapêuticas do Ministério da Saúde do Brasil12 atualmente recomenda o esquema 3 em 1 como preferencial, e não considera o uso dos INI em primeira linha como alternativos, como o faz o guia da OMS.
A experiência em escolher e iniciar a TARV para os pacientes se apresentando para o diagnóstico nas faixas etárias acima dos 50-60 anos é provavelmente algo novo para a maioria dos clínicos.
Individualizando a TARV entre pacientes mais velhos
A escolha da TARV deve levar em conta o estilo de vida e a idade do paciente, entre outros fatores. O uso de AZT, muitas vezes considerado opção ao tenofovir (TDF), é sabidamente associado a um maior risco de toxicidade. Pacientes mais idosos podem, por sua vez, apresentar função renal reduzida e menor massa óssea já no início do tratamento.
A experiência em escolher e iniciar a TARV para os pacientes se apresentando para o diagnóstico nas faixas etárias acima dos 50-60 anos é provavelmente algo novo para a maioria dos clínicos. Esses pacientes também tendem a apresentar mais depressão e distúrbios cognitivos.
Para o tratamento inicial, consensos terapêuticos de países desenvolvidos propõem esquemas de primeira linha baseados em INI. A OMS, embora ainda considere como primeira opção a combinação de TDF/lamivudina (3TC) ou emtricitabina (FTC) e efavirenz (EFV) coformulados, sugere o dolutegravir (DTG) como alternativa. No Brasil, os esquemas iniciais são baseados em EFV, prioritariamente.
Qual seria, realmente, o melhor esquema para os indivíduos mais idosos? A terapia de base proposta atualmente é composta de TDF/3TC ou FTC, drogas com melhor perfil para toxicidade mitocondrial. Entretanto, TDF pode ter pior perfil de toxicidade renal e óssea. Resultados recentes de 96 semanas de TARV dos estudos GS 104 e 111 e uma análise post hoc com a utilização de tenofovir alafenamida (TAF), em comparação com TDF em pacientes virgens de tratamento, mostraram melhores desfechos com TAF – i.e., menor incidência de doença renal crônica (DRC) e mudanças favoráveis na proteinúria. As taxas de supressão viral foram elevadas em ambos os braços.31,32 Em pacientes com alto risco para DRC, a incidência geral da doença na semana 96 foi de 0,1% com TAF vs. 1,6% com TDF; nenhum dos pacientes interrompeu o tratamento devido à piora da função renal no braço TAF, enquanto 3% interromperam no braço contendo TDF.
A maioria dos estudos avaliando perda óssea com ARV identifica uma estabilização após um período de 2-3 anos; recentemente, o estudo START confirmou esse dado.33 A recomendação do Department for Health and Human Services (DHHS, Departamento de Saúde e Serviços Humanos dos Estados Unidos) é de que o TDF seja evitado em pacientes com diagnóstico estabelecido de osteoporose.34 Não existem dados avaliando as opções sem nucleosídios em indivíduos mais velhos. Em estudos prospectivos de pacientes, tanto em terapia inicial como switch, reduções de densidade mineral óssea (DMO) foram menores em pacientes que receberam TAF; na verdade, semelhante ao esquemas sem nucleosídios, e há uma melhora na DMO em pessoas que mudaram de esquemas baseados em TDF para os baseados em TAF.35,36 Com os resultados desses estudos, pode-se esperar que em breve as formulações com TAF substituam as com TDF. Um tempo mais longo de observação pode ser necessário para se estabelecer a segurança do TAF entre pacientes mais velhos e com uso de longo prazo. Na análise post hoc, feita de acordo com a distribuição de risco para DRC, a maioria dos pacientes tinha idade ≤ 35 anos, e somente 2% em cada braço tinha 60 anos ou mais.
Na 15ª Conferência da European AIDS Clinical Society foram apresentados os resultados de 24 semanas do estudo PADDLE,37,38 estudo piloto, aberto, fase IV de braço único avaliando uso da dupla DTG/3TC como terapia inicial em 20 pacientes virgens de tratamento. Todos atingiram carga viral < 50 cópias/mL na semana 24 do tratamento. Essa ainda não é uma estratégia recomendada. Do mesmo modo que a maioria dos estudos clínicos avaliando estratégias de TARV, esse estudo também não incluiu um número significativo de pacientes mais velhos. A média de idade foi de 34 anos, e dados de longo prazo ainda estão sendo aguardados.
Indivíduos mais velhos vivendo com HIV utilizam mais medicamentos para doenças cardiovasculares, agentes gastrointestinais e hormonais do que os mais jovens, perfil semelhante ao observado para a população em geral.39 Importantes interações envolvem ARV e drogas rotineiramente utilizadas, muitas vezes como automedicação, tais como antiácidos e inibidores de bomba, como omeprazol. Interações importantes ocorrem com corticosteroides fluorados, estatinas e outros agentes hipolipemiantes, anticoagulantes, anti-hipertensivos, alfa-antagonistas usados para distúrbios urinários, antidepressivos e anticonvulsivantes e quimioterápicos, arsenal não incomum entre pacientes idosos.40 Especial atenção precisa ser tomada no tratamento de coinfecções, como a tuberculose e a hepatite C, nas quais a combinação com certos ARV pode resultar tanto em maior toxicidade quanto em redução da eficácia.
A incidência de desordens cognitivas também aumenta com a idade do paciente, e nesse cenário talvez seja interessante evitar o EFV. Apesar disso, quando não disponíveis outras opções em uma única pílula diária, a coformulação 3 em 1 pode facilitar a vida de pacientes, inclusive os que desenvolvem demência, cenário possível quando estamos tratando de pacientes com HIV e idade avançada.
No cenário das múltiplas morbidades, pode ser mais prudente a escolha de esquemas baseados em INI. Cabe lembrar que, ainda assim, algumas interações precisam ser consideradas.41 Entre os INI, o DTG tem a vantagem de não precisar do adjuvante farmacológico, ter menor número de interações, ser bem-tolerado e poder ser usado em dose única diária. Os INI, de um modo geral, são vantajosos para mulheres mais velhas em terapia de reposição hormonal.
O uso do abacavir (ABC) permanece discutível, uma vez que parece estar envolvido nos mecanismos moduladores de função plaquetária, e ainda não está claro seu papel no risco cardiovascular.
O protocolo clínico e as diretrizes terapêuticas brasileiros12 atualmente recomendam o esquema 3 em 1 como preferencial. Esse esquema é adequado à maioria de nossos pacientes iniciando a TARV. O protocolo menciona a importância da avaliação de múltiplas morbidades entre pacientes com 50 anos de idade ou mais e chama a atenção para o risco de toxicidades e interações medicamentosas. Entretanto, nenhuma recomendação especial para TARV em pacientes idosos é sugerida. Certamente, questões individuais no âmbito do envelhecimento e das múltiplas morbidades precisam ainda ser discutidas nesse contexto.
Em resumo, não há um esquema que seja igualmente perfeito para todos os pacientes envelhecendo com HIV ou iniciando TARV em idade mais avançada. Qualquer que seja a escolha final, é fundamental considerar a facilidade de uso (menos comprimidos), o perfil de tolerabilidade e a avaliação muito cuidadosa das interações medicamentosas.