La ecografía hepática es actualmente la primera técnica diagnóstica para la detección y caracterización de la mayoría de las lesiones del hígado, especialmente en la detección de lesiones focales o en el seguimiento de las enfermedades hepáticas crónicas.
No solo se utiliza el modoB, sino también el doppler color y más recientemente la ecografía con contraste. Se usa principalmente en el diagnóstico de enfermedades hepáticas difusas como la esteatosis, la hepatopatía crónica y la cirrosis.
En este artículo se van a revisar las características principales de las lesiones focales fundamentales y los principales signos de enfermedades difusas.
Liver ultrasound is frequently used as a first-line technique for the detection and characterization of the most common liver lesions, especially those incidentally found focal liver lesions, and for monitoring of chronic liver diseases.
Ultrasound is not only used in the Bmode, but also with Doppler and, more recently, contrast-enhanced ultrasound. It is mainly used in the diagnosis of diffuse liver diseases, such as steatosis or cirrhosis.
This article presents a practical approach for diagnosis workup, in which the different characteristics of the main focal liver lesions and diffuse liver diseases are reviewed.
El hígado es un órgano sólido intraabdominal con una ecoestructura homogénea, de grano fino y característicamente iso o hiperecocoica respecto a la corteza renal, hipoecocia respecto al parénquima pancreático y ligeramente hipoecoica respecto al bazo. Su parénquima está salpicado de estructuras anecoicas (vasos) y ecoicas (ligamentos y cisuras) no patológicas.
En el estudio de la patología hepática nos enfrentamos ante el órgano de mayor tamaño del organismo, y debido a la función que desempeña se puede ver afectado por enfermedades tanto locales como sistémicas. Por este motivo, y desde un punto de vista didáctico, realizaremos una clasificación del estudio de la patología hepática según afecte al parénquima de forma localizada (patología focal) o de forma extensa (hepatopatía difusa)1.
Patología focalSe entiende por lesión focal una estructura intraparenquimatosa de naturaleza líquida (anecoica) o sólida (con ecos internos) que altera la estructura hepática normal, pudiendo desplazar las estructuras vecinas y en superficie deformar los contornos hepáticas. En ocasiones resulta complicado diferenciar entre lesiones benignas y malignas, teniendo que recurrir a diferentes datos característicos que nos informen sobre la sospecha de su estirpe.
Podemos establecer la siguiente clasificación:
- 1.
Lesiones focales de naturaleza líquida.
- A.
Quiste congénito hepático.
- B.
Enfermedad poliquística hepatorenal.
- C.
Pseudoquiste parasitario.
- D.
Absceso hepático.
- E.
Hematomas hepáticos.
- F.
Enfermedad metastásica quística.
- A.
- 2.
Lesiones focales de naturaleza sólida.
- A.
Benignas.
- I.
Hemangioma cavernoso.
- II.
Hiperplasia nodular focal.
- III.
Adenoma hepático.
- IV.
Lipomas y angiolipomas hepáticos.
- V.
Hígado graso focal.
- VI.
Granuloma calcificado.
- I.
- B.
Malignas.
- I.
Carcinoma hepatocelular.
- II.
Hemangiosarcoma o angiosarcoma.
- III.
Enfermedad metastásica sólida.
- I.
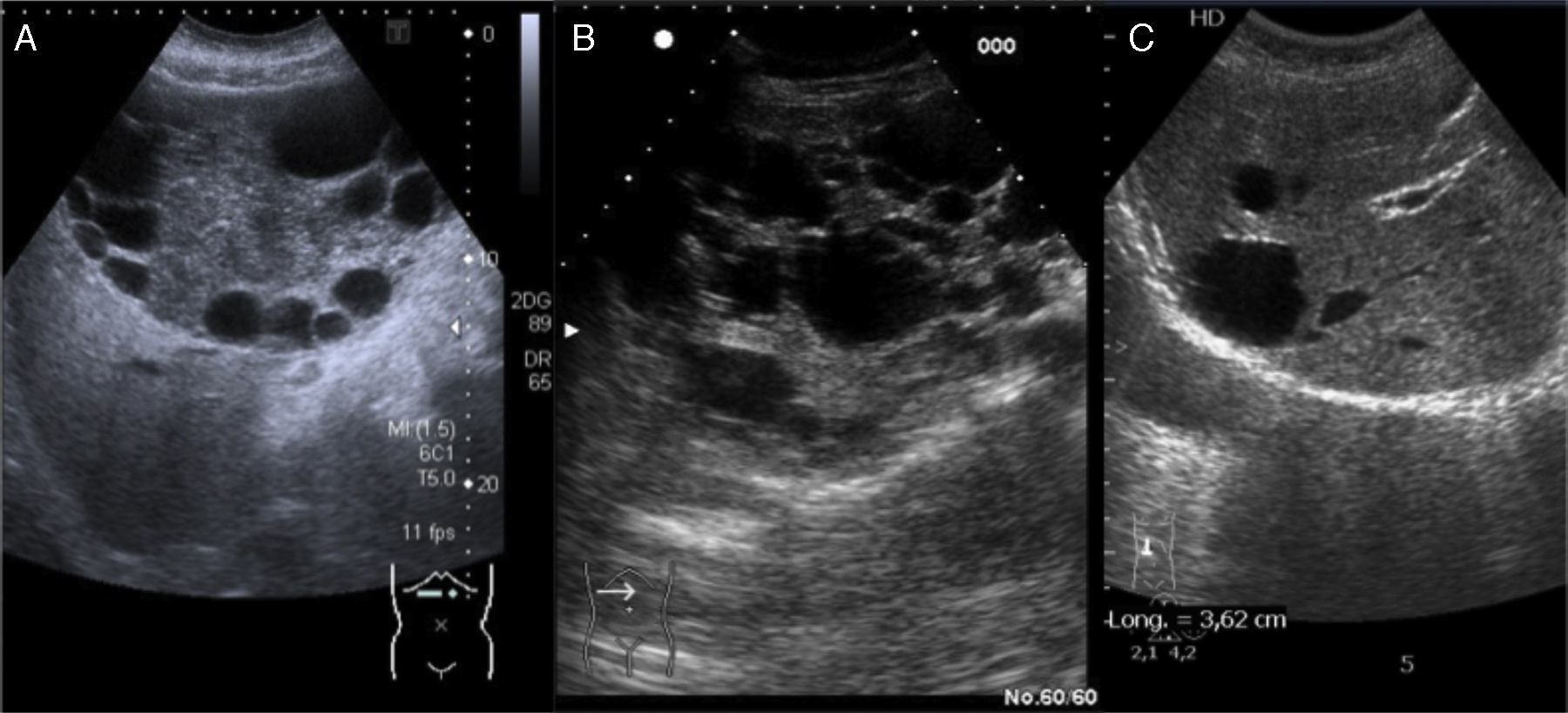
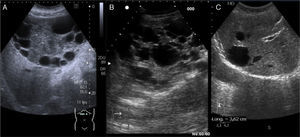
Se trata de un quiste verdadero (posee un recubrimiento epitelial) que surge como una anomalía en el desarrollo de la vía biliar intrahepática. Ecográficamente se define como una lesión anecoica, sin ecos internos, bien delimitada por una pared fina y con refuerzo acústico posterior (quiste simple) (fig. 1C). En ocasiones puede contener ecos internos, septos de diferente grosor, adelgazamiento o irregularidad parietal, e incluso puede parecer sólido, obligándonos a establecer un diagnóstico diferencial entre la posible complicación de un quiste simple por infección o hemorragia o la existencia de un quiste complejo de otra naturaleza.
Enfermedad poliquística hepatorrenal2Con diferente implicación pronóstica según se trate de la enfermedad autosómica recesiva infantil o enfermedad autosómica dominante del adulto. En el estudio ecográfico hallamos la presencia de múltiples quistes simples con la semiología antes descrita, a nivel renal y hepático (con discreta predilección por el lóbulo hepático izquierdo) (fig. 1B).
Pseudoquiste parasitarioLa hidatidosis3 es la zoonosis más importante en nuestro medio, y la ecografía es la técnica más rentable para realizar su diagnóstico y valorar la localización (principalmente afecta al lóbulo hepático derecho), la cantidad, la relación con estructuras vecinas (vasculares y biliares) y el estadio de las lesiones. Esta última valoración permite clasificar las lesiones en 5 tipos4:
- •
Quiste univesicular. Es un quiste simple pero que característicamente presenta una membrana externa gruesa que constituye su pared, pudiendo estar más o menos calcificada, y que aunque no contiene una arquitectura interna, presenta material ecogénico en su interior denominado arena hidatídica, que es el reflejo del escólex.
- •
Quiste con membrana desprendida, conocido como signo del nenúfar. Presenta despegamiento de la membrana germinativa (tabique ecogénico con forma ondulada) flotando en el interior de la cavidad quística.
- •
Quiste multivesicular. Imagen patognomónica, caracterizada por la presencia interna de múltiples cavidades que constituyen las vesículas hijas (cada uno de ellos delimitados por una pared gruesa y con material ecogénico en su interior) (fig. 1A).
- •
Quiste con patrón sólido, imagen en nevada. Se corresponde con quistes evolucionados, sometidos a tratamiento farmacológico o sobreinfectados. El quiste adquiere un patrón de lesión sólida, ya que está ocupado por material ecogénico que se distribuye de forma más o menos homogénea.
- •
Quiste calcificado. Tan solo se observa una estructura hiperecogénica y curvilínea de convexidad anterior que deja una sombra acústica posterior.
No debemos olvidar que los hallazgos ecográficos refuerzan la sospecha clínica de esta entidad. Su apariencia se asemeja a un quiste complicado con una ecogenicidad variable (principalmente anecoicos o hipoecoicos), delimitados por una pared irregular, dejando su refuerzo acústico y con presencia en su interior de forma variable de ecos, septos, niveles y focos ecogénicos por presencia de gas. Su etiología y su mecanismo fisiopatológico son variables, siendo los más frecuentes los bacterianos y encontrando particularidades ecográficas características en alguno de ellos. Podemos destacar:
- •
El absceso amebiano5 suele presentarse como lesión única, ovalada o redondeada, ausencia de una pared prominente, con ecos internos finos de forma homogénea, hipoecoica en comparación con parénquima hepático no afectado y localizado predominantemente en lóbulo hepático derecho, contiguo al diafragma.
- •
El absceso candidiásico, cuya imagen ecográfica recuerda al ojo de toro (lesión en anillo hipoecoica con un centro hiperecoico). Importante en señalar y recordar ya que la visualización de esta imagen debe siempre conducir hacia el diagnóstico diferencial con la enfermedad metastásica hepática.
Si nos encontramos con un antecedente de traumatismo o biopsia hepática, tenemos que valorar en primera instancia el tiempo de evolución del mismo, ya que determinará las características ecográficas de los hallazgos. De manera que la hemorragia reciente (24-48h) se presenta como una lesión ecógena mal definida; a medida que evoluciona durante la primera semana (debido a la reabsorción del tejido y la llegada de líquido intersticial) adquiere cierta hipoecogenicidad con mejor delimitación, y durante las 2-3semanas siguientes termina presentando las características de un hematoma evolucionado (presencia de áreas ecogénicas, tabiques y pared engrosada).
Enfermedad metastásica quísticaSu etiología es variable, pudiendo encontrar lesiones quísticas complejas en neoplasias primarias con componente quístico (cistoadenocarcinoma de ovario y páncreas, carcinoma mucinoso de colon), secundarias a necrosis extensa intratumoral (sarcoma metastásico) o por degeneración quística (tumores neuroendocrinos y carcinoides metastásicos). Se distinguirá de los quistes benignos por la presencia de una o varias lesiones complejas con nódulos ecogénicos murales, engrosamiento e irregularidad de la pared y tabiques y niveles hidroaéreos internos.
Previo a comenzar con la descripción de las lesiones focales sólidas6, debemos recordar que su ecogenicidad se expresa de forma relativa a la ecogenicidad del parénquima sano circundante y debemos prestar atención al reconocimiento de ciertas características ecográficas, que aunque no son patognomónicas de malignidad, sí nos obligan a realizar un diagnóstico definitivo de la/s lesión/es con la utilización de otras técnicas diagnósticas7,8. Estas son: halo hipoecoico periférico, masa sólida e hipoecoica, masas sólidas múltiples y, sin ser ecográfico, antecedente de neoplasia y/o hepatopatía previa9.
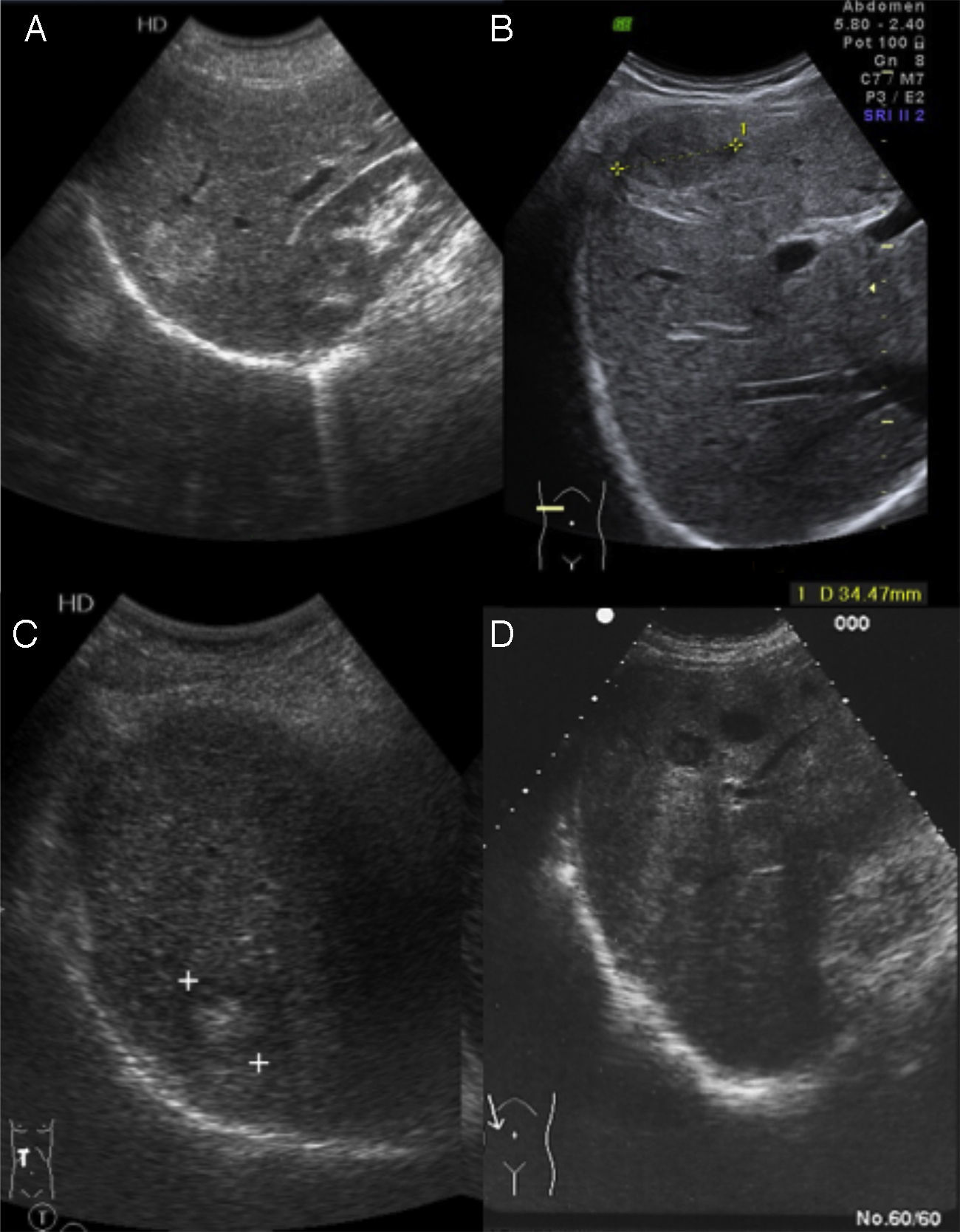
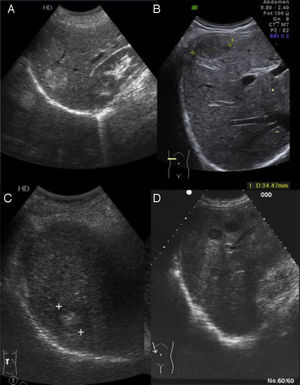
Hemangioma cavernosoTumor benigno hepático más frecuente, con mayor prevalencia en población adulta femenina. El aspecto ecográfico típico10 es reflejo de su histología, mostrándose como una lesión de pequeño tamaño (inferior a 30mm), hiperecoica, bien delimitada, homogénea, con refuerzo acústico posterior y sin captación en el estudio Doppler (fig. 2A). Estas características requieren seguimiento en los siguientes 3-6meses para confirmar la estabilidad de la lesión. En cambio, el aspecto ecográfico atípico (mayor tamaño, heteroecoico con zona central hipoecoica y límites irregulares o mal definidos) requiere de otras técnicas, entre las que encontramos la ecografía con contraste de microburbujas (fig. 2B)11.
Hiperplasia nodular focalSegunda masa hepática benigna, con cierta influencia hormonal, por lo cual también es más frecuente en población femenina. Debido a que se considera una malformación vascular congénita12, se presenta como una masa bien circunscrita, solitaria, hipo/isoecoica respecto el parénquima hepático, no encapsulada y con la presencia de una cicatriz central lineal o estrellada, hiper/hipoecoica y que tiene flujo Doppler arterial13.
Adenoma hepático14Posee una relación clara con el uso de anticonceptivos orales. Su aspecto ecográfico es inespecífico, presentándose como una masa solitaria de gran tamaño, encapsulada pero sin refuerzo acústico posterior y de ecogenicidad variable dependiendo del grado de infiltración grasa, hemorragia, necrosis o calcificación que presente. En el estudio Doppler se muestra como un tumor hipervascular.
Lipomas y angiomiolipomas hepáticosSe presentan como una masa ecogénica bien definida similar a otras lesiones focales pero que característicamente presentan artefacto de propagación del ultrasonido.
Hígado graso focalSe puede presentar como una infiltración grasa focal (regiones de mayor ecogenicidad dentro de un parénquima hepático sano) o como un respeto graso focal (los islotes de parénquima hepático sano aparecen como masas hipoecoicas dentro de un hígado infiltrado). La localización habitual es el segmento IV (por delante de la bifurcación de la vena porta en el hilio hepático), sin olvidar la localización en la fosa vesicular. Y de forma característica presenta bordes geográficos, no ejerce efecto masa en vasos intrahepáticos ni en contorno hepático y que pueden modificarse con la supresión del agente causante (obesidad, malnutrición, hábito enólico, etc.).
Granuloma calcificadoSuele tratarse de lesiones pequeñas (<20mm), solitarias o múltiples, hiperecoicas, con marcada sombra acústica posterior. Etiológicamente están relacionados con procesos infecciosos previos.
Carcinoma hepatocelular15,16Considerado el tumor primario maligno más frecuente, asienta principalmente sobre un hígado cirrótico. Desde el punto de vista histológico tiene 3 formas de presentación (tumor solitario, múltiples nódulos e infiltración difusa), por lo cual su aspecto ecográfico es variable, pudiendo describirse como:
- •
Una masa de pequeño tamaño (5cm), bien delimitada, hipoecoica y con un halo fino de menor ecogenicidad (pseudocápsula) (fig. 2C).
- •
Una masa compleja, de gran tamaño (>5cm) y heterogénea por procesos de necrosis y/o fibrosis, que suele invadir estructuras vasculares con trombosis secundaria.
- •
Una masa pequeña hiperecoica, debido a infiltración grasa o dilatación sinusoidal.
El estudio Doppler muestra señales de alta velocidad y también muestra la neovascularización interna de los trombos murales de los vasos portales (signo diagnóstico de esta entidad tumoral). Destaca nuevamente la gran utilidad de la ecografía de contraste con microburbujas17.
Existe una variante de carcinoma fibrolaminar, que aparece sin hepatopatía previa, en pacientes jóvenes y que ecográficamente se presenta como una lesión única, bien diferenciada, a menudo encapsulada, de gran tamaño (entre 6 y 22cm), y ocasionalmente con calcificación en punteado y cicatriz ecogénica central.
HemangiosarcomaSu relevancia se debe a la relación que tiene con carcinógenos específicos como el arsénico y el cloruro de polivinilo. Es de muy baja incidencia, y su aspecto ecográfico corresponde a una masa de gran tamaño y ecogenicidad mixta.
Enfermedad metastásica sólida18Constituye la primera causa de lesión maligna en el hígado. La procedencia es diversa, y entre las más frecuentes se encuentran: vesícula biliar, colon, estómago, páncreas, mama y pulmón. Las imágenes ecográficas que ofrecen no son características de cada uno de los tumores primarios, aunque pueden orientar la secuencia diagnóstica. De manera que la relevancia de la ecografía no reside en ser el estudio principal para el diagnóstico, sino en ser un método de estudio para el hallazgo de las lesiones ocupantes de espacio.
Hay diferentes patrones ecográficos19,20:
- •
Metástasis ecógenas. Cuanto mayor grado de vascularización posea el tumor primario, mayor probabilidad de que la lesión sea ecógena. Su origen tiende a ser digestivo, principalmente colon.
- •
Metástasis hipoecoicas. Generalmente hipovascularizadas. Patrón típico del cáncer de mama o pulmón no tratados. También recordar estómago, páncreas, esófago y linfoma.
- •
Patrón en ojo de toro o en diana. Presenta una zona hipoecoica periférica. Se suele identificar con carcinoma broncógeno (fig. 2D).
- •
Metástasis calcificadas. Podemos encontrar un patrón de calcificaciones grandes, ecógenas y con fuerte sombra acústica posterior (adenocarcinoma mucinoso de colon) o un patrón de múltiples y pequeñas ecogenicidades puntiformes sin clara sombra acústica posterior.
- •
Desorganización difusa del parénquima, reflejo de la forma infiltrativa de la enfermedad metastásica y que supone un reto diagnóstico, al no poseer parénquima sano hepático que nos sirva de referencia para la comparación. Los más frecuentes: mama, pulmón y melanoma.
Queda definida como la afectación más o menos extensa de la estructura del parénquima hepático. Determinadas patologías pueden adquirir ciertos signos o patrones ecográficos más o menos característicos que orientan a su correcta valoración.
Dentro de estas se desmarcan:
- 1.
Hepatitis agudas.
- 2.
Hígado graso difuso o esteatosis.
- 3.
Cirrosis hepática.
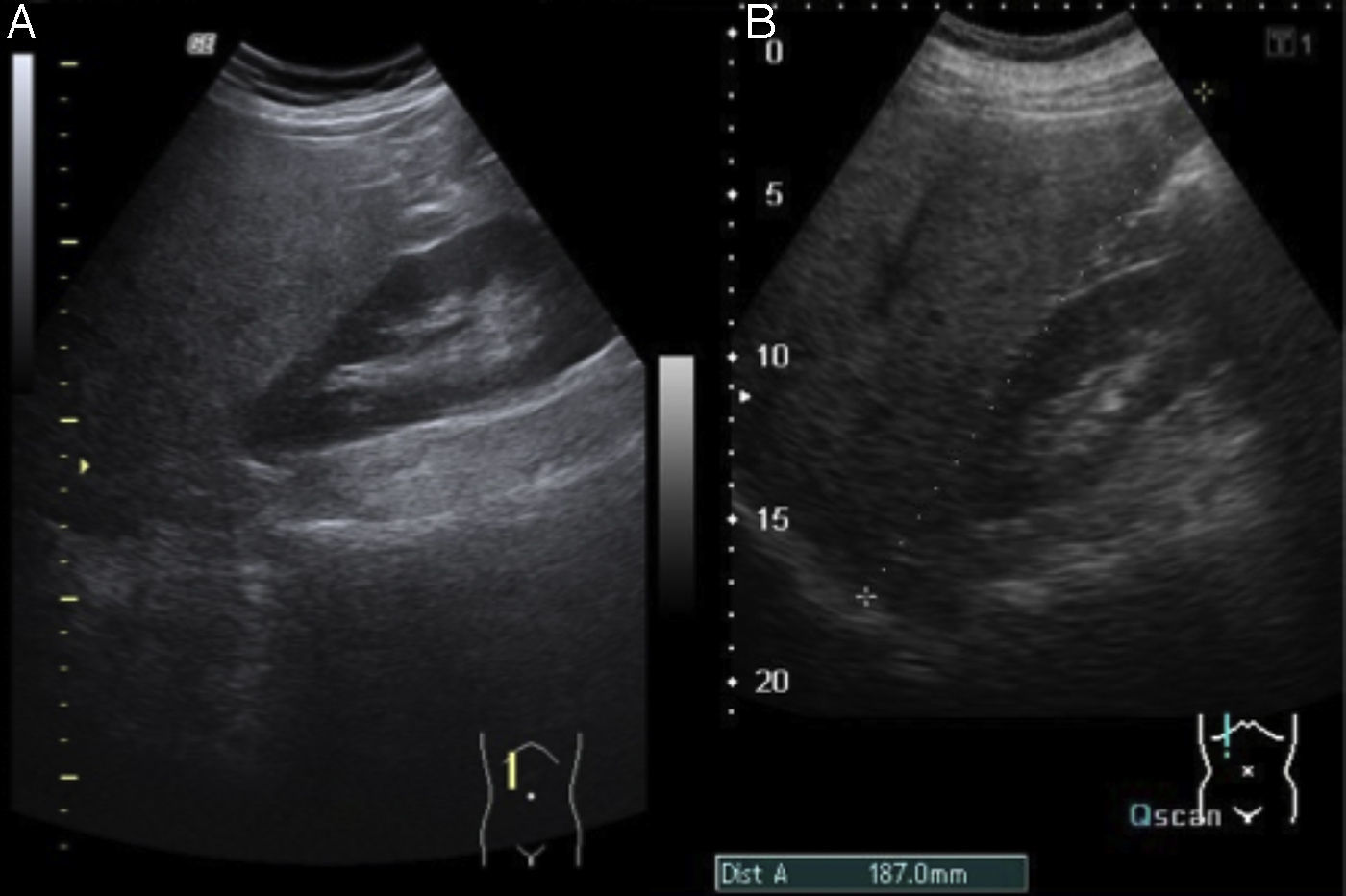
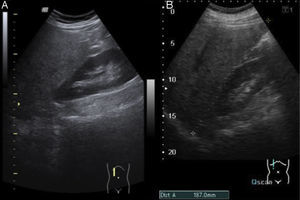
Las características ecográficas, difíciles de observar, son reflejo de los cambios histológicos, pudiendo aparecer: alteración difusa de la ecogenicidad, con brillo acentuado en las triadas portales, diferente grado de hepatomegalia homogénea y engrosamiento de la pared vesicular con contenido de barro biliar (colecistitis aguda alitiásica) (fig. 3B).
Hígado graso difuso21Los hallazgos ecográficos dependen de la cantidad de triglicéridos acumulados que poseen una alta reflectividad, lo cual conduce a un aumento de la ecogenicidad hepática (hígado brillante) en relación con el riñón derecho y el páncreas y a una atenuación del ultrasonido que se traduce en una pérdida de visualización correcta de las estructuras intrahepáticas profundas. Según la severidad de los hallazgos22:
- •
Esteatosis leve. Aumento difuso mínimo de la ecogenicidad hepática (fig. 3A).
- •
Esteatosis moderada. Aumento difuso moderado de la ecogenicidad hepática con ligera pérdida de la visualización de los vasos intrahepáticos.
- •
Esteatosis severa. Aumento acentuado de la ecogenicidad hepática y mala/nula visualización de campos posteriores y del diafragma.
Se caracteriza a nivel histológico por una afectación difusa con fibrosis y conversión de la estructura parenquimatosa en nódulos23. El estudio ecográfico no solo objetiva unos patrones asociados, sino que también es capaz de realizar un diagnóstico precoz de las complicaciones que puede asociar, la hipertensión portal y el carcinoma hepatocelular24.
A continuación se describen los patrones ecográficos25:
- •
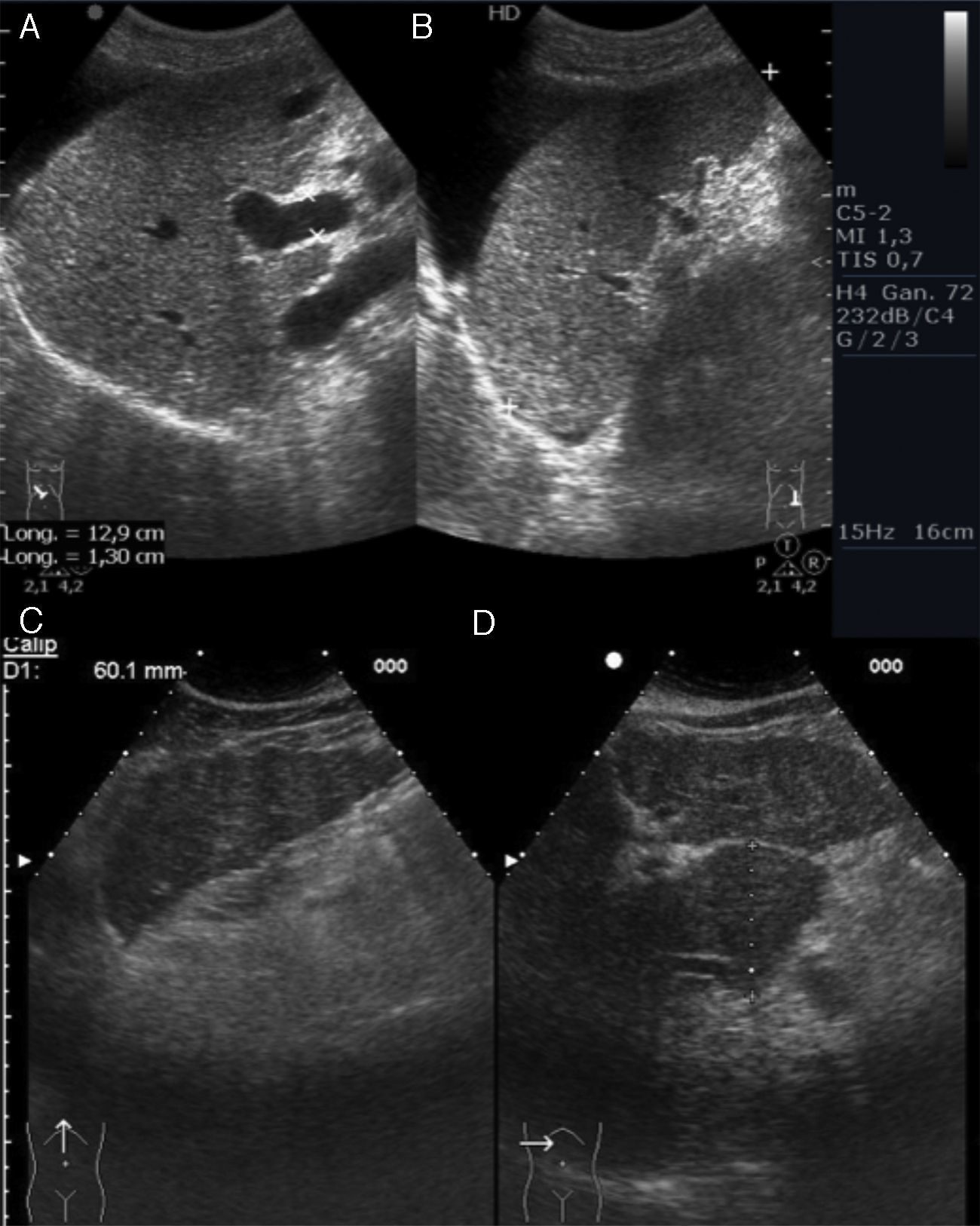
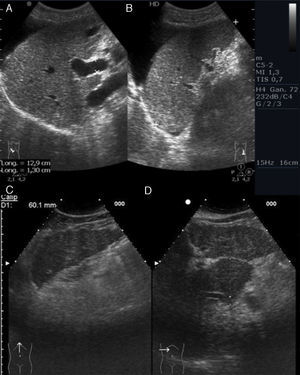
Redistribución del volumen. En fases iniciales el hígado puede aumentar de tamaño, pero su tendencia es hacia un hígado de tamaño reducido (atrófico) con un aumento relativo del lóbulo izquierdo y/o del lóbulo caudado (presentando un tamaño >35mm en el eje anteroposterior y una relación LC/LHD>0,65) (fig. 4D)26,27.
Figura 4.Signos de hepatopatía crónica. A)Corte oblicuo de hipocondrio derecho. Dilatación de la porta y ascitis. B)Corte longitudinal de hipocondrio izquierdo. Esplenomegalia y ascitis. C)Corte longitudinal de epigastrio. Bordes irregulares del lóbulo hepático izquierdo. D)Corte transversal de hipocondrio derecho. Hipertrofia del lóbulo caudado.
(0,21MB). - •
Ecoestructura grosera. Aumento heterogéneo en la ecogenicidad del parénquima con una estructura grosera (apariencia de grano grueso).
- •
Superficie nodular. Visualizada como irregularidad del contorno hepático, evidenciándose mejor ante la presencia de ascitis y causada por nódulos regenerativos y fibrosis (fig. 4C).
La cirrosis se considera la causa más frecuente de hipertensión portal intrahepática, y su traducción a nivel ecográfico está basada en objetivar:
- •
Alteraciones de la vena porta y del eje esplenoportal28-30. Medición de la vena porta a nivel del hilio hepático superior a 13mm, nula o pobre modificación de su volumen con los cambios de presión abdominal secundarios a la dinámica respiratoria (aumento inferior al 20% de su volumen durante la inspiración)31 y disminución de la velocidad32 e inversión del flujo venoso (hepatófugo) (fig. 4A)33.
- •
Esplenomegalia. Volumen aumentado (diámetro bipolar >13cm o la superficie del eje en el corte longitudinal del órgano >60cc), siempre relativo al peso del paciente. Y medición de la vena esplénica, a nivel del hilio, mayor de 9mm (fig. 4B).
- •
Ascitis. Presencia de líquido libre (sonoluscente) en la cavidad peritoneal rodeando a órganos y asas intestinales, en mayor o menor medida en función del volumen (figs. 4A y B).
- •
Colaterales venosas portosistémicas. Se encuentran 4 principales localizaciones: unión gastroesofágica (si vena coronaria >7mm sugiere HTP grave), vena paraumbilical (a través del ligamento falciforme), espleno y gastrorrenal e intestinal34.
Los autores declaran no tener ningún conflicto de intereses.