Es preciso desarrollar nuevas estrategias que permitan una identificación precoz y una inmediata instauración de medidas efectivas en el abordaje de la sepsis. La unidad multidisciplinar de sepsis (UMS) desarrolló una herramienta: el Protocolo Informático de Manejo Integral de la Sepsis (PIMIS). El objetivo de este estudio es evaluar la intervención de la UMS y la utilidad del PIMIS.
MétodosSe analizaron las intervenciones según fueran realizadas por consulta directamente solicitada (activación de PIMIS o consulta telefónica) o no solicitada (aislamientos microbiológicos y el Sistema Informático de Detección de Constantes Vitales [SIDCV]), los servicios, el tipo de infección, la recomendación de cambio de antibiótico y el grado de aceptación.
ResultadosDe las 1.581 consultas, el 65,1% se solicitaron directamente: un 84,1% por activación del PIMIS por el médico responsable y un 15,9% por contacto telefónico directo. Entre las consultas no solicitadas, el 95,2% procedían de microbiología y el 4,8% del SIDCV. Las consultas directamente solicitadas se realizaron más precozmente que las no solicitadas (5,63días vs. 8,47días; p<0,001) y la frecuencia fue mayor en los servicios médicos frente a los quirúrgicos (73,0% vs. 39,1%; p<0,001). Se recomendó un cambio de antibiótico en el 32% de las primeras consultas y se aceptó en el 78,1% de los casos.
ConclusionesLa elevada proporción de consultas directamente solicitadas y aceptación de las recomendaciones demuestra que la intervención de la UMS es valorada y respetada. El PIMIS es el principal mecanismo de consulta, lo que lo convierte en una herramienta útil y conveniente para la identificación precoz y el abordaje de la sepsis.
New strategies need to be developed for the early recognition and rapid response for the management of sepsis. To achieve this purpose, the Multidisciplinary Sepsis Team (MST) developed the Computerised Sepsis Protocol Management (PIMIS). The aim of this study was to evaluate the convenience of using PIMIS, as well as the activity of the MST.
MethodsAn analysis was performed on the data collected from solicited MST consultations (direct activation of PIMIS by attending physician or telephone request) and unsolicited ones (by referral from the microbiology laboratory or an automatic referral via the hospital vital signs recording software [SIDCV]), as well as the hospital department, source of infection, treatment recommendation, and acceptance of this.
ResultsOf the 1,581 first consultations, 65.1% were solicited consultations (84.1% activation of PIMIS and 15.9% by telephone). The majority of unsolicited consultations were generated by the microbiology laboratory (95.2%), and 4.8% from the SIDCV. Referral from solicited consultations were generated sooner (5.63days vs 8.47days; P<.001) and came from clinical specialties rather than from the surgical ward (73.0% vs 39.1%; P<.001). A recommendation was made for antimicrobial prescription change in 32% of first consultations. The treating physician accepted 78.1% of recommendations.
ConclusionsThe high rate of solicited consultations and acceptance of recommended prescription changes suggest that a MST is seen as a helpful resource, and that PIMIS software is perceived to be useful and convenient to use, as it is the main source of referral.
La sepsis continúa siendo una de las principales causas de muerte en pacientes hospitalizados. En España los últimos estudios indican un aumento en la incidencia1. Por ello, es preciso el desarrollo de mecanismos y herramientas que permitan su reconocimiento precoz para prevenir así el desarrollo de complicaciones.
A lo largo de los últimos años se han creado diversas estrategias para intentar mejorar el abordaje de la sepsis, algunas originadas a partir del servicio de medicina intensiva o medicina interna2,3. Además, se ha destacado el papel primordial que juega la enfermería en el reconocimiento y seguimiento4,5.
En un intento de mejorar la atención integral al paciente con sepsis, en nuestro centro se creó en el año 2006 la primera unidad multidisciplinar de sepsis (UMS) en nuestro país. El equipo estaba compuesto por un médico con formación específica en enfermedades infecciosas y una enfermera con dedicación exclusiva, así como por un equipo multidisciplinar con dedicación parcial, compuesto por especialistas de: medicina intensiva, urgencias, neumología, medicina interna, farmacia, microbiología y cirugía general.
La UMS tiene un triple objetivo. En primer lugar, promover el reconocimiento precoz de la sepsis grave. Segundo, conseguir la implementación de las medidas de abordaje y tratamiento de la sepsis según las guías de la Surviving Sepsis Campaing6. El tercer objetivo va dirigido a la optimización del tratamiento antibiótico.
La intervención de un especialista en enfermedades infecciosas se ha demostrado que mejora el pronóstico de estos pacientes7,8. En algunos centros se están implementando programas para la optimización del tratamiento antibiótico por parte de equipos multidisciplinares que han logrado mejorar los resultados en la prescripción y consumo de antibióticos9,10.
Para asegurar una intervención precoz, la UMS creó una herramienta informática: el Protocolo Informático de Manejo Integral de la Sepsis (PIMIS). Sus objetivos son: permitir una identificación precoz de la sepsis y la implementación inmediata de un conjunto de medidas eficaces, que puedan prevenir el desarrollo de complicaciones, mejorando el pronóstico del paciente.
El presente estudio describe el desarrollo e implantación del PIMIS.
MétodosSe realizó un análisis observacional, descriptivo y retrospectivo entre el 1 de enero de 2011 y el 30 de junio de 2012, en el que se recogieron las siguientes variables: los diferentes mecanismos de inclusión de un paciente en el PIMIS, el servicio de procedencia, los días transcurridos desde el ingreso hasta la consulta (DC), el foco de infección, el origen (nosocomial), el tipo de recomendación en el cambio del tratamiento antibiótico, así como el grado de aceptación de los pacientes adultos incluidos en el PIMIS ingresados en el Hospital Son Llàtzer. El hospital ofrece cobertura sanitaria a una población de unos 225.000 habitantes y dispone de 400 camas.
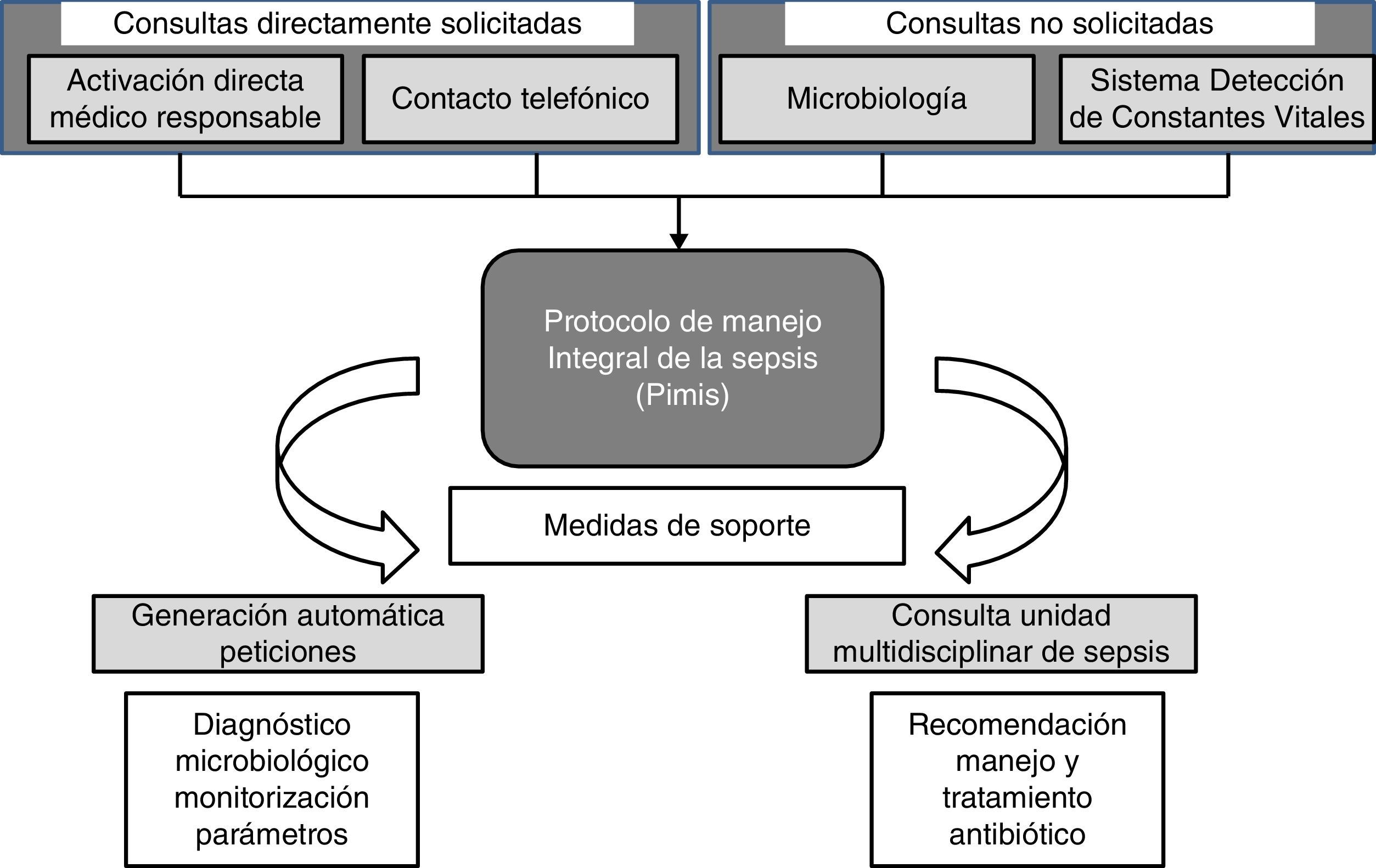
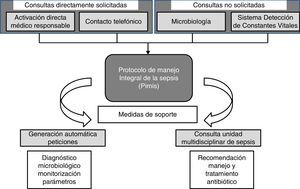
Un paciente puede ser incluido en el PIMIS a partir de 4 mecanismos: 1) mediante la activación informática directa por su médico responsable; 2) por consulta telefónica directa a la UMS; 3) tras conocerse un aislamiento microbiológico significativo, y 4) tras la alerta del Sistema Informático de Detección de Constantes Vitales (SIDCV). Consideramos que la consulta es directamente solicitada (CDS) cuando se realiza por la inclusión del paciente por su médico en el PIMIS o telefónicamente, y no solicitada (CNS) cuando se incluye a partir de la información de microbiología o del SIDCV (fig. 1).
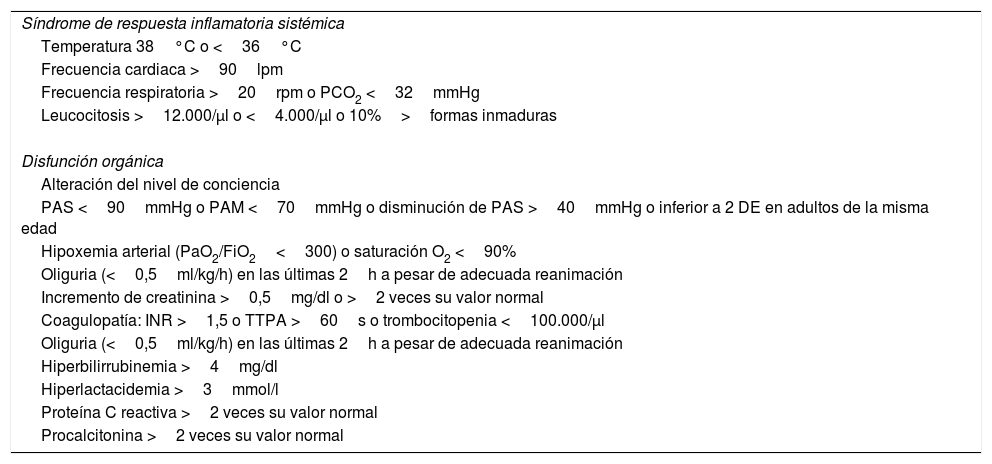
Cuando un paciente tiene sospecha de sepsis grave, al seleccionar la herramienta del PIMIS se despliegan en un check-list los criterios de respuesta inflamatoria sistémica (SIRS), disfunción orgánica y marcadores inflamatorios (proteína C reactiva; normal <5mg/l y procalcitonina; normal <0-05ng/ml) (tabla 1). Cuando se cumplen al menos 2 criterios de SIRS y uno de disfunción orgánica, o elevación de marcadores, el paciente se identifica como sepsis grave y, validando el check-list, se genera la activación automática del protocolo. Una vez incluido el paciente, se genera un aviso automático a la UMS a través de la generación de un listado que identifica al paciente y sus criterios de inclusión. A partir de este momento el paciente es valorado por un miembro de la UMS que se encargará de realizar las recomendaciones correspondientes en cuanto al abordaje y tratamiento específico. El PIMIS está disponible para su activación desde cualquier servicio del hospital.
Criterios de activación del Protocolo de manejo integral de la sepsis
| Síndrome de respuesta inflamatoria sistémica |
| Temperatura 38°C o <36°C |
| Frecuencia cardiaca >90lpm |
| Frecuencia respiratoria >20rpm o PCO2 <32mmHg |
| Leucocitosis >12.000/μl o <4.000/μl o 10%>formas inmaduras |
| Disfunción orgánica |
| Alteración del nivel de conciencia |
| PAS <90mmHg o PAM <70mmHg o disminución de PAS >40mmHg o inferior a 2 DE en adultos de la misma edad |
| Hipoxemia arterial (PaO2/FiO2<300) o saturación O2 <90% |
| Oliguria (<0,5ml/kg/h) en las últimas 2h a pesar de adecuada reanimación |
| Incremento de creatinina >0,5mg/dl o >2 veces su valor normal |
| Coagulopatía: INR >1,5 o TTPA >60s o trombocitopenia <100.000/μl |
| Oliguria (<0,5ml/kg/h) en las últimas 2h a pesar de adecuada reanimación |
| Hiperbilirrubinemia >4mg/dl |
| Hiperlactacidemia >3mmol/l |
| Proteína C reactiva >2 veces su valor normal |
| Procalcitonina >2 veces su valor normal |
DE: desviación estándar; FiO2: fracción inspirada de oxígeno; INR: cociente internacional normalizado; PAM: presión arterial media; PaO2: presión parcial de oxígeno; PAS: presión arterial sistólica; PCO2: presión parcial carbónico; SIRS: síndrome inflamatorio de respuesta sistémica; TTPA: tiempo de tromboplastina parcial activado.
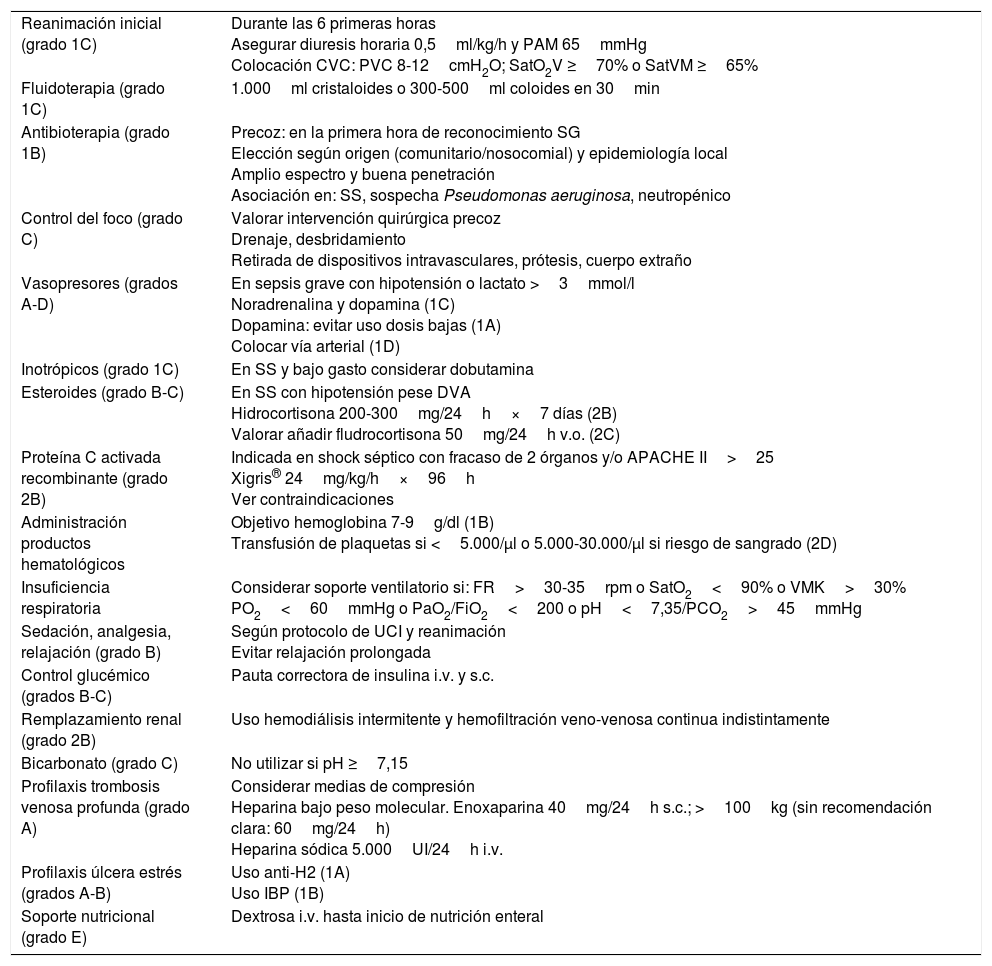
Paralelamente a la generación de un listado de los pacientes incluidos, se visualizan para su posible consulta una serie de recomendaciones sobre el abordaje terapéutico en cuanto a: reanimación inicial, soporte hemodinámico, y tratamientos asociados, adaptadas y según las recomendaciones de la Surviving Sepsis Campaing11 (tabla 2), así como una serie de peticiones: extracción de hemocultivos, radiografía de tórax, y extracción de análisis para monitorización de lactato y parámetros de disfunción orgánica, PCR y PCT a las 6 y 24h siguientes a la inclusión (siempre) y muestras microbiológicas (según proceda).
Recomendaciones de tratamiento de la sepsis grave y shock séptico
| Reanimación inicial (grado 1C) | Durante las 6 primeras horas Asegurar diuresis horaria 0,5ml/kg/h y PAM 65mmHg Colocación CVC: PVC 8-12cmH2O; SatO2V ≥70% o SatVM ≥65% |
| Fluidoterapia (grado 1C) | 1.000ml cristaloides o 300-500ml coloides en 30min |
| Antibioterapia (grado 1B) | Precoz: en la primera hora de reconocimiento SG Elección según origen (comunitario/nosocomial) y epidemiología local Amplio espectro y buena penetración Asociación en: SS, sospecha Pseudomonas aeruginosa, neutropénico |
| Control del foco (grado C) | Valorar intervención quirúrgica precoz Drenaje, desbridamiento Retirada de dispositivos intravasculares, prótesis, cuerpo extraño |
| Vasopresores (grados A-D) | En sepsis grave con hipotensión o lactato >3mmol/l Noradrenalina y dopamina (1C) Dopamina: evitar uso dosis bajas (1A) Colocar vía arterial (1D) |
| Inotrópicos (grado 1C) | En SS y bajo gasto considerar dobutamina |
| Esteroides (grado B-C) | En SS con hipotensión pese DVA Hidrocortisona 200-300mg/24h×7 días (2B) Valorar añadir fludrocortisona 50mg/24h v.o. (2C) |
| Proteína C activada recombinante (grado 2B) | Indicada en shock séptico con fracaso de 2 órganos y/o APACHE II>25 Xigris® 24mg/kg/h×96h Ver contraindicaciones |
| Administración productos hematológicos | Objetivo hemoglobina 7-9g/dl (1B) Transfusión de plaquetas si <5.000/μl o 5.000-30.000/μl si riesgo de sangrado (2D) |
| Insuficiencia respiratoria | Considerar soporte ventilatorio si: FR>30-35rpm o SatO2<90% o VMK>30% PO2<60mmHg o PaO2/FiO2<200 o pH<7,35/PCO2>45mmHg |
| Sedación, analgesia, relajación (grado B) | Según protocolo de UCI y reanimación Evitar relajación prolongada |
| Control glucémico (grados B-C) | Pauta correctora de insulina i.v. y s.c. |
| Remplazamiento renal (grado 2B) | Uso hemodiálisis intermitente y hemofiltración veno-venosa continua indistintamente |
| Bicarbonato (grado C) | No utilizar si pH ≥7,15 |
| Profilaxis trombosis venosa profunda (grado A) | Considerar medias de compresión Heparina bajo peso molecular. Enoxaparina 40mg/24h s.c.; >100kg (sin recomendación clara: 60mg/24h) Heparina sódica 5.000UI/24h i.v. |
| Profilaxis úlcera estrés (grados A-B) | Uso anti-H2 (1A) Uso IBP (1B) |
| Soporte nutricional (grado E) | Dextrosa i.v. hasta inicio de nutrición enteral |
CVC: catéter venoso central; DVA: drogas vasoactivas; FR: frecuencia respiratoria; IBP: inhibidores de la bomba de protones; i.v.: intravenoso; PAM: presión arterial media; PCO2: presión parcial carbónico; PO2: presión parcial de oxígeno; PVC: presión venosa central; s.c.: subcutánea; SatO2: saturación oxígeno; SatO2V: saturación venosa de oxígeno central; SatVM: saturación venosa mixta; SG: sepsis grave; SS: shock séptico; UCI: unidad de cuidados intensivos; VMK: ventimask; v.o.: vía oral.
La activación de un paciente en el PIMIS a partir del aislamiento microbiológico se realiza cuando, tras la reunión diaria con microbiología, se facilitan los resultados de las muestras significativas. Con el resultado se realiza una valoración clínica del paciente, y si cumple criterios de sepsis, es introducido y activado a través del PIMIS.
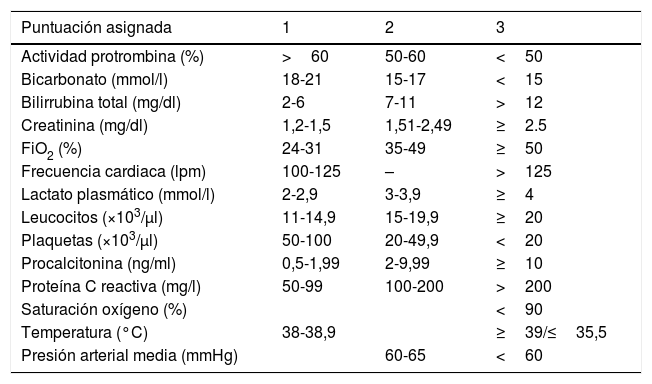
La otra herramienta empleada para la detección de pacientes con sospecha de sepsis es el SIDCV. Con los parámetros hemodinámicos introducidos en el sistema informático de enfermería, junto con valores predefinidos de laboratorio, se genera una puntuación que clasifica al paciente como sospecha de sepsis si la puntuación es mayor de 6 puntos (tabla 3). La puntuación obtenida siempre será de las últimas 24h. La UMS recibe una alerta con el listado de pacientes que superan esta puntuación cada 24h a la UMS. Este sistema estaba siendo sometido a un ensayo piloto de validez interna durante los últimos meses del estudio.
Criterios de puntuación en el Sistema Informático de Detección de Constantes Vitales (SIDCV)
| Puntuación asignada | 1 | 2 | 3 |
|---|---|---|---|
| Actividad protrombina (%) | >60 | 50-60 | <50 |
| Bicarbonato (mmol/l) | 18-21 | 15-17 | <15 |
| Bilirrubina total (mg/dl) | 2-6 | 7-11 | >12 |
| Creatinina (mg/dl) | 1,2-1,5 | 1,51-2,49 | ≥2.5 |
| FiO2 (%) | 24-31 | 35-49 | ≥50 |
| Frecuencia cardiaca (lpm) | 100-125 | – | >125 |
| Lactato plasmático (mmol/l) | 2-2,9 | 3-3,9 | ≥4 |
| Leucocitos (×103/μl) | 11-14,9 | 15-19,9 | ≥20 |
| Plaquetas (×103/μl) | 50-100 | 20-49,9 | <20 |
| Procalcitonina (ng/ml) | 0,5-1,99 | 2-9,99 | ≥10 |
| Proteína C reactiva (mg/l) | 50-99 | 100-200 | >200 |
| Saturación oxígeno (%) | <90 | ||
| Temperatura (°C) | 38-38,9 | ≥39/≤35,5 | |
| Presión arterial media (mmHg) | 60-65 | <60 |
FiO2: fracción inspirada de oxígeno.
Los miembros de la UMS se distribuyen y valoran diariamente los pacientes incluidos en el PIMIS y/o seleccionados por el SIDCV para asegurarse de que cumplen criterios clínicos de sepsis, en cuyo caso se continúa el seguimiento hasta el final del proceso. En la primera consulta se establecen unas recomendaciones terapéuticas que son comunicadas directamente al médico responsable, así como reflejadas en un informe de interconsulta.
Las recomendaciones de cambio en el tratamiento antibiótico pueden ser de 4 tipos: a) desescalada, cuando el número o el espectro antibiótico se reduce de acuerdo con el patrón de resistencias; b) cambio por mala evolución, cuando existen criterios clínicos y/o analíticos de SIRS o disfunción orgánica que persisten más allá de las primeras 72h; c) ajuste de dosis o tratamiento inadecuado, cuando el antibiótico carece de actividad in vitro o es inadecuado para el foco de la infección, o su administración puede conllevar efectos adversos que exceden a los beneficios esperados, y d) terapia secuencial, cuando se pasa de la vía de administración intravenosa a la oral. La optimización del tratamiento antibiótico es supervisada por un farmacéutico miembro de la UMS.
Una recomendación se considera aceptada cuando el cambio en el tratamiento antibiótico se ajusta a la recomendación realizada por la UMS.
Las variables categóricas se expresan como frecuencias relativas y absolutas. Las variables continuas se expresan como media y desviación estándar (DE) y se comparan utilizando la t-Student o el test ANOVA para variables con distribución normal y el test U de Mann-Whitney para las de distribución no normal. El análisis estadístico se realizó con SPSS 17.0 (Chicago, IL, EE.UU.) y EPIDAT v.3.1.
ResultadosDurante el periodo de estudio se registraron 1.581 nuevas consultas a la UMS correspondientes a 1.340 pacientes, lo que supone una media de 89 consultas nuevas por mes. El 78,5% de los episodios fueron comunitarios.
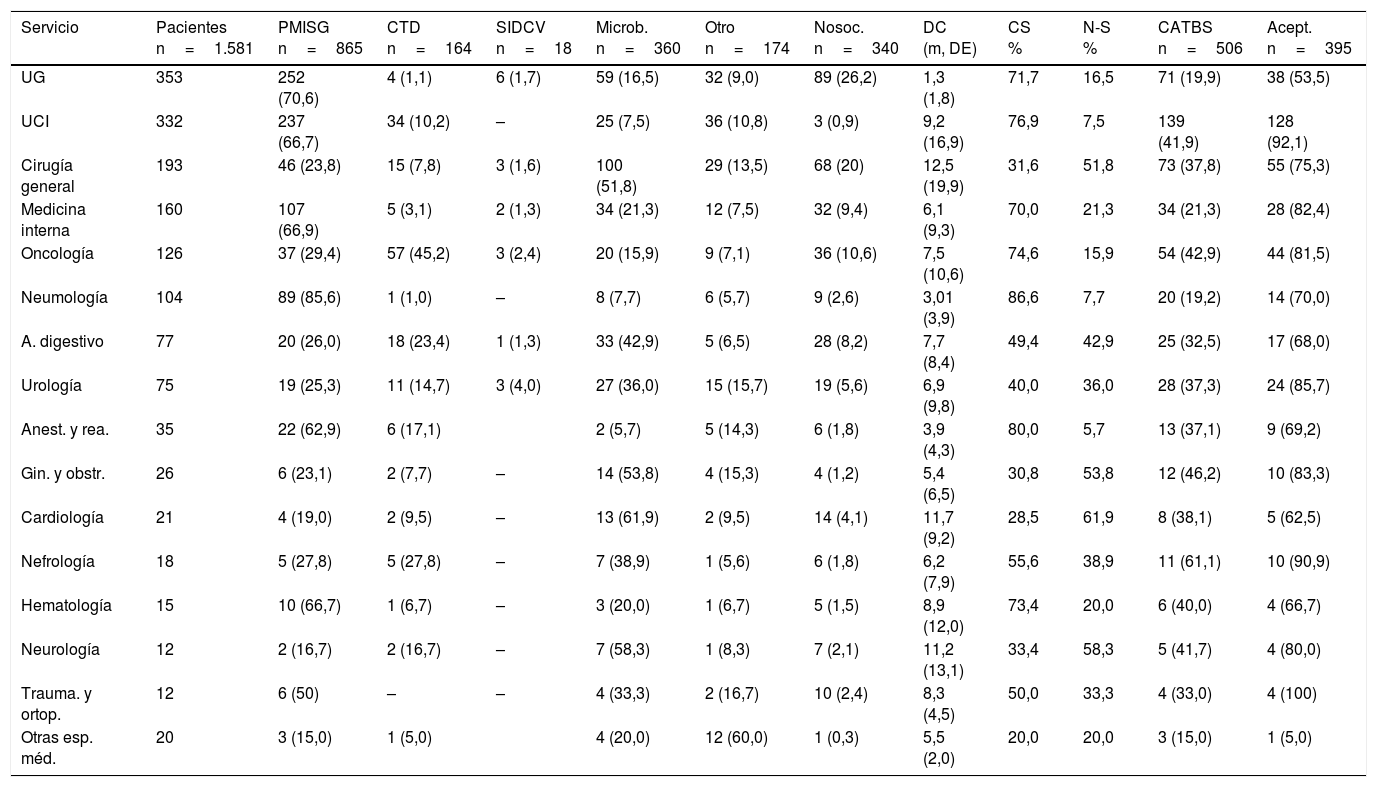
El servicio de procedencia del paciente y el tipo de consulta realizada se recogen en la tabla 4. El servicio de urgencias (22,6%) y la UCI (21%) fueron los servicios que realizaron un mayor número de consultas.
Mecanismo de consulta y modificación de tratamiento por servicio
| Servicio | Pacientes n=1.581 | PMISG n=865 | CTD n=164 | SIDCV n=18 | Microb. n=360 | Otro n=174 | Nosoc. n=340 | DC (m, DE) | CS % | N-S % | CATBS n=506 | Acept. n=395 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| UG | 353 | 252 (70,6) | 4 (1,1) | 6 (1,7) | 59 (16,5) | 32 (9,0) | 89 (26,2) | 1,3 (1,8) | 71,7 | 16,5 | 71 (19,9) | 38 (53,5) |
| UCI | 332 | 237 (66,7) | 34 (10,2) | – | 25 (7,5) | 36 (10,8) | 3 (0,9) | 9,2 (16,9) | 76,9 | 7,5 | 139 (41,9) | 128 (92,1) |
| Cirugía general | 193 | 46 (23,8) | 15 (7,8) | 3 (1,6) | 100 (51,8) | 29 (13,5) | 68 (20) | 12,5 (19,9) | 31,6 | 51,8 | 73 (37,8) | 55 (75,3) |
| Medicina interna | 160 | 107 (66,9) | 5 (3,1) | 2 (1,3) | 34 (21,3) | 12 (7,5) | 32 (9,4) | 6,1 (9,3) | 70,0 | 21,3 | 34 (21,3) | 28 (82,4) |
| Oncología | 126 | 37 (29,4) | 57 (45,2) | 3 (2,4) | 20 (15,9) | 9 (7,1) | 36 (10,6) | 7,5 (10,6) | 74,6 | 15,9 | 54 (42,9) | 44 (81,5) |
| Neumología | 104 | 89 (85,6) | 1 (1,0) | – | 8 (7,7) | 6 (5,7) | 9 (2,6) | 3,01 (3,9) | 86,6 | 7,7 | 20 (19,2) | 14 (70,0) |
| A. digestivo | 77 | 20 (26,0) | 18 (23,4) | 1 (1,3) | 33 (42,9) | 5 (6,5) | 28 (8,2) | 7,7 (8,4) | 49,4 | 42,9 | 25 (32,5) | 17 (68,0) |
| Urología | 75 | 19 (25,3) | 11 (14,7) | 3 (4,0) | 27 (36,0) | 15 (15,7) | 19 (5,6) | 6,9 (9,8) | 40,0 | 36,0 | 28 (37,3) | 24 (85,7) |
| Anest. y rea. | 35 | 22 (62,9) | 6 (17,1) | 2 (5,7) | 5 (14,3) | 6 (1,8) | 3,9 (4,3) | 80,0 | 5,7 | 13 (37,1) | 9 (69,2) | |
| Gin. y obstr. | 26 | 6 (23,1) | 2 (7,7) | – | 14 (53,8) | 4 (15,3) | 4 (1,2) | 5,4 (6,5) | 30,8 | 53,8 | 12 (46,2) | 10 (83,3) |
| Cardiología | 21 | 4 (19,0) | 2 (9,5) | – | 13 (61,9) | 2 (9,5) | 14 (4,1) | 11,7 (9,2) | 28,5 | 61,9 | 8 (38,1) | 5 (62,5) |
| Nefrología | 18 | 5 (27,8) | 5 (27,8) | – | 7 (38,9) | 1 (5,6) | 6 (1,8) | 6,2 (7,9) | 55,6 | 38,9 | 11 (61,1) | 10 (90,9) |
| Hematología | 15 | 10 (66,7) | 1 (6,7) | – | 3 (20,0) | 1 (6,7) | 5 (1,5) | 8,9 (12,0) | 73,4 | 20,0 | 6 (40,0) | 4 (66,7) |
| Neurología | 12 | 2 (16,7) | 2 (16,7) | – | 7 (58,3) | 1 (8,3) | 7 (2,1) | 11,2 (13,1) | 33,4 | 58,3 | 5 (41,7) | 4 (80,0) |
| Trauma. y ortop. | 12 | 6 (50) | – | – | 4 (33,3) | 2 (16,7) | 10 (2,4) | 8,3 (4,5) | 50,0 | 33,3 | 4 (33,0) | 4 (100) |
| Otras esp. méd. | 20 | 3 (15,0) | 1 (5,0) | 4 (20,0) | 12 (60,0) | 1 (0,3) | 5,5 (2,0) | 20,0 | 20,0 | 3 (15,0) | 1 (5,0) |
Acept.: cambio de antibiótico aceptado; Anest. y rea.: anestesia y reanimación; CATBS: cambio de antibiótico sugerido; CS: consulta solicitada; CTD: contacto telefónico directo; DC: días hasta consulta; Gin. y obstr.: ginecología y obstetricia; Microb.: aislamiento microbiológico; N-S: consulta no solicitada; Nosoc.: nosocomial; PMISG: protocolo de manejo integral de la sepsis grave; SIDCV: Sistema Informático de Detección de Constantes Vitales; Solic.: consulta solicitada; Trauma. y ortop.: traumatología y ortopedia; UCI: unidad de cuidados intensivos; UG: urgencias generales.
El principal mecanismo de consulta fue por activación directa del PIMIS por el médico responsable (54,7%). Los pacientes procedían fundamentalmente de servicios médicos (91,1%): urgencias (29,1%), seguido por la UCI (27,4%), medicina interna (12,4%) y neumología (10,3%), respectivamente.
El segundo mecanismo de inclusión en el PIMIS fue tras la información microbiológica (22,8%). Existen servicios en los cuales más de la mitad de los pacientes valorados eran incluidos a través de este mecanismo: cardiología (61,9%), neurología (58,3%), ginecología y obstetricia (53,8%), y cirugía general (51,8%).
Por contacto telefónico directo se realizaron un 10,4% de las inclusiones en el PIMIS, procedentes principalmente de oncología (34,7%), UCI (20.7%) y aparato digestivo (10,9%). El SIDCV identificó tan solo 18 pacientes con sepsis, correspondiendo solamente al 1,1% del total de consultas.
Consultas directamente solicitadas (CDS) vs. consultas no solicitadas (CNS)La mayoría de las consultas fueron CDS (65,1%). De ellas, el 84,1% fueron por activación del PIMIS por el médico responsable y el 15,9% por contacto telefónico directo. La proporción fue significativamente mayor en los servicios médicos que en los quirúrgicos (73,0% vs. 39,1%; p<0,001). Así mismo, las CDS se realizaron significativamente de forma más precoz (5,63días vs. 8,47días; p<0,001). Entre las CNS, el 95,2% procedían de microbiología y el 4,8% del SIDCV. El tiempo transcurrido entre la admisión del paciente en el hospital y la consulta con la UMS se presenta en la tabla 4 (días hasta consulta [DC]). Las CDS por activación directa del PIMIS se realizaron antes que las que se hicieron por contacto telefónico directo (4,93días vs. 9,33días; p<0,001).
Foco de infecciónEn la primera consulta la infección más frecuente fue de origen respiratorio (34,4%), seguida de la de origen abdominal (22,4%) y urinaria (18,2%). En un 23,9% de los casos no fue posible identificar el foco de la infección.
Recomendación de cambio de antibióticoSe recomendó un cambio en 506 (32%) de las primeras consultas y fue aceptado en 398 casos (78,1%). La frecuencia de aceptación fue muy variable entre las especialidades. El porcentaje de aceptación fue significativamente mayor en las CDS (80,6% vs. 72,4%; p=0,04).
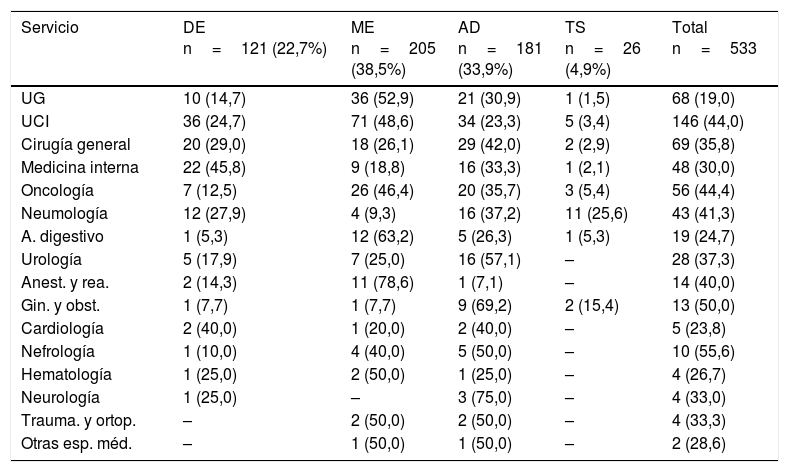
Tipos de recomendaciónLa principal causa de recomendación de cambio de antibiótico fue por mala evolución (38,5%), seguido por tratamiento inadecuado (33,9%) (tabla 5). Los servicios donde se realizó el cambio por mala evolución fueron principalmente anestesia y reanimación (78,6%), aparato digestivo (63,2%), urgencias (52,9%) y UCI (48,6%). El ajuste de dosis fue la intervención más frecuente en los servicios quirúrgicos (cirugía general, ginecología y obstetricia, urología, traumatología), así como en cardiología y neurología. La desescalada fue la principal intervención en medicina interna (45,8%) y la terapia secuencial lo fue en neumología (25,6%).
Tipo de intervención realizada por servicio
| Servicio | DE n=121 (22,7%) | ME n=205 (38,5%) | AD n=181 (33,9%) | TS n=26 (4,9%) | Total n=533 |
|---|---|---|---|---|---|
| UG | 10 (14,7) | 36 (52,9) | 21 (30,9) | 1 (1,5) | 68 (19,0) |
| UCI | 36 (24,7) | 71 (48,6) | 34 (23,3) | 5 (3,4) | 146 (44,0) |
| Cirugía general | 20 (29,0) | 18 (26,1) | 29 (42,0) | 2 (2,9) | 69 (35,8) |
| Medicina interna | 22 (45,8) | 9 (18,8) | 16 (33,3) | 1 (2,1) | 48 (30,0) |
| Oncología | 7 (12,5) | 26 (46,4) | 20 (35,7) | 3 (5,4) | 56 (44,4) |
| Neumología | 12 (27,9) | 4 (9,3) | 16 (37,2) | 11 (25,6) | 43 (41,3) |
| A. digestivo | 1 (5,3) | 12 (63,2) | 5 (26,3) | 1 (5,3) | 19 (24,7) |
| Urología | 5 (17,9) | 7 (25,0) | 16 (57,1) | – | 28 (37,3) |
| Anest. y rea. | 2 (14,3) | 11 (78,6) | 1 (7,1) | – | 14 (40,0) |
| Gin. y obst. | 1 (7,7) | 1 (7,7) | 9 (69,2) | 2 (15,4) | 13 (50,0) |
| Cardiología | 2 (40,0) | 1 (20,0) | 2 (40,0) | – | 5 (23,8) |
| Nefrología | 1 (10,0) | 4 (40,0) | 5 (50,0) | – | 10 (55,6) |
| Hematología | 1 (25,0) | 2 (50,0) | 1 (25,0) | – | 4 (26,7) |
| Neurología | 1 (25,0) | – | 3 (75,0) | – | 4 (33,0) |
| Trauma. y ortop. | – | 2 (50,0) | 2 (50,0) | – | 4 (33,3) |
| Otras esp. méd. | – | 1 (50,0) | 1 (50,0) | – | 2 (28,6) |
AD: ajuste de dosis; Anest. y rea.: anestesia y reanimación; DE: desescalada; Gin. y obstr.: ginecología y obstetricia; ME: mala evolución; Trauma. y ortop.: traumatología y ortopedia; TS: terapia secuencial; UCI: unidad de cuidados intensivos; UG: urgencias generales.
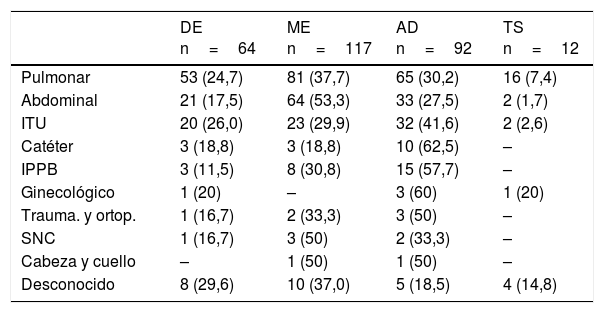
El ajuste de dosis de antibiótico fue la intervención más frecuente en algunas infecciones como en la infección del tracto urinario (ITU), infección asociada a catéter, o de piel y partes blandas (tabla 6). La ITU fue la infección en que se realizó desescalada antibiótica en un mayor número de ocasiones. Por el contrario, la infección abdominal y la respiratoria fueron las localizaciones donde mayormente se realizó cambio de antibiótico por mala evolución.
Tipo de intervención según el foco de infección
| DE n=64 | ME n=117 | AD n=92 | TS n=12 | |
|---|---|---|---|---|
| Pulmonar | 53 (24,7) | 81 (37,7) | 65 (30,2) | 16 (7,4) |
| Abdominal | 21 (17,5) | 64 (53,3) | 33 (27,5) | 2 (1,7) |
| ITU | 20 (26,0) | 23 (29,9) | 32 (41,6) | 2 (2,6) |
| Catéter | 3 (18,8) | 3 (18,8) | 10 (62,5) | – |
| IPPB | 3 (11,5) | 8 (30,8) | 15 (57,7) | – |
| Ginecológico | 1 (20) | – | 3 (60) | 1 (20) |
| Trauma. y ortop. | 1 (16,7) | 2 (33,3) | 3 (50) | – |
| SNC | 1 (16,7) | 3 (50) | 2 (33,3) | – |
| Cabeza y cuello | – | 1 (50) | 1 (50) | – |
| Desconocido | 8 (29,6) | 10 (37,0) | 5 (18,5) | 4 (14,8) |
AD: ajuste de dosis; DE: desescalada; IPPB: infección de piel y partes blandas; ITU: infección del tracto urinario; ME: mala evolución; SNC: sistema nervioso central; Trauma. y ortop.: traumatología y ortopedia; TS: terapia secuencial.
Hay 2 aspectos importantes que diferencian el abordaje de la sepsis en nuestro centro. Por un lado, la existencia de una UMS, compuesta por especialistas médicos y quirúrgicos. Por otro lado, la existencia de una herramienta informática que permite la identificación, evaluación y registro de pacientes potencialmente afectos de sepsis grave: el PIMIS, pionero en España.
Se han desarrollado sistemas de alerta informáticos para promover la identificación e implementación de medidas de abordaje de la sepsis en unidades distintas de la UCI3,5,12,13. La idea que comparten todos ellos es permitir la identificación precoz y facilitar un abordaje integral e intensivo de patologías potencialmente críticas. A diferencia de la herramienta informática desarrollada por Ferreras et al.14, con implantación en el servicio de urgencias, nuestro protocolo permite la activación desde cualquier servicio del hospital.
Nuestro análisis refleja la actividad pormenorizada por servicio, mientras que estudios previos se limitan a comparar las diferencias entre los servicios médicos y los quirúrgicos15. Esto nos permite reconocer aquellos servicios con los que necesitamos mejorar nuestra asistencia.
La mayoría de las consultas realizadas a la UMS se llevaron a cabo mediante la activación directa del PIMIS, lo que demuestra su aceptación y reconocimiento. Así mismo, es probable que la generación automática de un paquete de recomendaciones sea percibida como una ayuda útil para el abordaje del paciente. Sin embargo, algunos profesionales prefieren recurrir a la consulta telefónica directa. Esto podría deberse a diversas causas, como mayor confianza en la comunicación verbal directa, desconocimiento o falta de información acerca de la existencia del PIMIS o desconfianza en la tecnología.
En conjunto, las CDS constituyen el principal mecanismo de consulta, lo que demuestra que las recomendaciones sobre el abordaje de la sepsis por parte de la UMS son consideradas y aceptadas. Uno de los principales retos a los que se enfrentan los profesionales de estas unidades es que su labor sea aceptada y reconocida por los especialistas de sus propios centros. Esto es un requisito que permite asegurar la cooperación con las distintas especialidades y la eficacia de estos programas.
La mayoría de los pacientes valorados mediante CNS fueron aquellos procedentes de los aislamientos microbiológicos. Esto podría implicar un retraso en el reconocimiento de la sepsis y la prescripción de antibiótico adecuado, dado que la valoración se hace al menos en las 24h posteriores al envío de la muestra, sin haberse consultado acerca del abordaje precoz o del tratamiento empírico. De hecho, existe en estos casos una diferencia significativa en los días que transcurren desde el ingreso del paciente hasta la valoración por la UMS. En el futuro, pensamos que los esfuerzos deberán ser dirigidos a la promoción del reconocimiento precoz y a hacer más accesible el PIMIS.
Actualmente se han desarrollado estrategias institucionales para promover la implementación de programas que optimicen la prescripción antibiótica16-18, ya que se ha demostrado que en ocasiones hasta un 50% de las prescripciones antibióticas eran inapropiadas19. En nuestro estudio el 32% de las prescripciones iniciales se consideraron inapropiadas. Gómez et al.3 demostraron que la consulta con un especialista en enfermedades infecciosas aumentaba la proporción de tratamientos apropiados en las prescripciones iniciales.
En comparación con estudios previos, la frecuencia de modificación de la prescripción antibiótica fue mayor20-22. Los resultados son especialmente relevantes en los servicios quirúrgicos19,23,24. Uno de los motivos que podría explicar estos resultados podría ser la integración de miembros de los servicios quirúrgicos en la UMS. Además, el hecho de que las recomendaciones sean comunicadas directamente al médico responsable, en lugar de ser simplemente reflejadas en la historia clínica, podría haber favorecido el grado de aceptación.
Es destacable la elevada proporción de cambios aceptados en la UCI de acuerdo con estudios previos25,26. Este hecho se debería a que la UMS fue creada en el servicio de medicina intensiva y una elevada proporción de sus miembros pertenecen a este servicio.
En cuanto al tipo de recomendación de cambio, el hecho de que el más frecuente sea por mala evolución podría sugerir que se solicita ayuda en un segundo tiempo, cuando el abordaje terapéutico puede ser más complejo, y se estima necesaria la intervención de un especialista en enfermedades infecciosas.
Es posible que nuestra intervención, además de conseguir optimizar el tratamiento antibiótico, disminuya su consumo al promover la desescalada y la terapia secuencial precoz, pero necesitamos confirmarlo con un estudio económico.
Aunque nuestro estudio refleja la experiencia de un solo centro, creemos que la exhaustiva descripción del funcionamiento de nuestra intervención puede alentar a otros grupos a definir y organizar estrategias en otros centros.
Recientemente, en el último documento de consenso acerca de las definiciones de la sepsis27, se cuestiona el uso de los criterios de SIRS en su diagnóstico, sugiriendo como nueva herramienta de valoración clínica el qSOFA. En el periodo de nuestro estudio todavía estaban vigentes las recomendaciones previas que incluían los criterios de SIRS, sin embargo, creemos que puede ser una escala que facilite la valoración e identificación de gravedad en los pacientes con sepsis.
Una de las limitaciones de nuestro estudio es que no hemos recogido el número de episodios de sepsis que no fueron consultados a nuestra unidad. A pesar de que no podemos conocer ni comparar el pronóstico de ambos grupos, el objetivo de nuestro estudio se centraba en señalar la importancia de organizar un abordaje coordinado con la implementación simultánea de unas medidas desde una perspectiva multidisciplinar. Esperamos poder examinar variables clínicas en próximos estudios. Por otra parte, las consultas realizadas para valoración diagnóstica u otra causa distinta a la prescripción antibiótica no han sido recogidas.
En resumen, este estudio revela que una herramienta informática como el PIMIS puede ser una estrategia válida para el reconocimiento de la sepsis. Además, la elevada proporción de aceptación de las recomendaciones realizadas implica que la actividad de la UMS es aceptada y valorada positivamente.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Al resto de componentes de la unidad multidisciplinar de sepsis: J Tarradas, B Comas, S Pons, J Bauzá, A Liébana, A Villoslada, MC Pérez, C Gallego, V Fernández-Baca, M Aranda, R Morales, O Gutiérrez, J Barceló, A Llompart, R Poyo-Guerrero, D Muñiz. Al equipo de informáticos de nuestro hospital: VM Estrada, A Hernández, F Velasco.