En este artículo comentamos los trabajos sobre trastornos funcionales y motores digestivos presentados en el Congreso de la Asociación Gastroenterológica Americana (Digestive Diseases Week, DDW) del año 2013 que nos han parecido de mayor interés. Se han aportado nuevos datos sobre la importancia clínica de los trastornos funcionales digestivos (TFD) y cómo pueden producir tantas molestias como la enfermedad inflamatoria intestinal, que se asocian con patología somática funcional y especialmente con fatiga. Además hay más datos sobre fisiopatología, de forma que se ha descrito que los factores ambientales y acontecimientos de la primera infancia pueden favorecer el desarrollo de un TFD. También se han presentado datos de cómo los ácidos biliares pueden favorecer la diarrea en pacientes con síndrome del intestino irritable (SII) y de cómo el tipo de ingesta puede favorecer el desarrollo de síntomas. Tenemos más datos de la presencia de enfermedad celíaca subyacente en pacientes con SII que nos deben motivar a investigarla en nuestros pacientes. Asimismo se ha demostrado que la dieta sin gluten aplicada de forma indiscriminada a los pacientes con SII no supone ninguna mejoría clara en ellos. Respecto a la fisiopatología de la dispepsia funcional (DF), se aportan resultados de cómo los factores psicológicos pueden modificar la acomodación gástrica y cómo esta, a su vez, se relaciona con la hipersensibilidad visceral o el vaciamiento gástrico. Desde el punto de vista terapéutico se ha constatado cómo la mirtazapina puede mejorar los síntomas y el peso en pacientes con DF grave con importante pérdida de peso. Se han presentado resultados de nuevos fármacos para el SII como el ibodutant, o de viejos fármacos con nuevas aplicaciones como la mesalazina o la ebastina. Se conoce mejor porque la linaclotida tiene un efecto antinociceptivo y se ha comunicado un metaanálisis en el que se demuestra su efectividad en el SII con predominio de estreñimiento. Respecto a los pacientes con estreñimiento hemos podido comprobar cómo la simple entrevista clínica y el tacto rectal permiten el diagnóstico de disinergia del suelo pélvico. Tenemos más datos de la eficacia de prucaloprida (que se demuestra que es capaz de acelerar el tiempo de tránsito de colon) y se presentan datos de plecanatida, un potencial nuevo fármaco útil en el estreñimiento. Finalmente se aportan resultados del uso de la inyección con toxina botulínica en pacientes con trastornos motores espásticos del esófago. En este sentido, también es remarcable un estudio en el que se confirma una mayor frecuencia de cáncer de esófago en pacientes tratados de acalasia.
This article discusses the most interesting studies on functional and motility gastrointestinal disorders presented in Digestive Diseases Week (DDW) in 2013. New data were reported on the clinical importance of functional gastrointestinal disorders (FGID) and on how they can produce numerous disturbances such as inflammatory bowel disease. These disturbances are associated with somatic functional disease and particularly with fatigue. In addition, new data have emerged on the physiopathology of these disorders, with some studies reporting that environmental factors and events in early infancy can favor their development. Data were also presented on how bile acids can increase susceptibility to diarrhea in patients with irritable bowel syndrome (IBS) and on how the type of food intake can favor the development of symptoms. More data are available on the presence of underlying celiac disease in patients with IBS, which should prompt us to investigate this disease in our patients. Likewise, indiscriminate application of a gluten-free diet in patients with IBS has been shown not to produce a clear improvement. Regarding the physiopathology of functional dyspepsia (FD), results have been presented on how psychological factors can modify gastric accommodation and how this is in turn related to visceral hypersensitivity and gastric emptying. Regarding therapy, mirtazapine can improve symptoms and lead to weight gain in patients with severe FD and substantial weight loss. Results were presented on new drugs for IBS such as ibodutant and on old drugs with new applications such as mesalazine and ebastine. The antinociceptive effect of linaclotide is now better understood and a meta-analysis has shown its effectiveness in IBS with constipation as the main symptom. In patients with constipation, pelvic floor dysynergy can be diagnosed by a simple clinical interview and rectal touch. More data are available on the efficacy of prucalopride (which has been shown to accelerate colon transit time) and data were provided on plecanatide, a potential new drug that could be useful in constipation. Finally, results were presented on the use of botulinum toxin injection in patients with spastic motility disorders of the esophagus. Also worthy of mention is a study confirming a higher frequency of esophageal cancer patients with achalasia who receive treatment.
Padecer un trastorno funcional digestivo (TFD) no es fácil. Muchos pacientes preferirían tener una enfermedad orgánica y un informe médico en el que se describiesen los resultados de alguna prueba concluyendo que se observa una lesión. Así podrían decir a sus familiares y amigos que les han encontrado una úlcera, una inflamación en el colon o una alteración en los análisis. No tendrían que llegar a casa y volver a decir: “No me han encontrado nada”.
Durante décadas, los médicos y la sociedad hemos dividido a los pacientes en 2 grupos diferenciados: “los que tienen algo” y los “que no tienen nada”. Hemos sido como el apóstol Tomás y necesitábamos ver para creer. Meter la mano en la llaga, o al menos ver la úlcera o la neoplasia en la endoscopia. Si no veíamos la lesión es que el paciente no tenía nada. Que conclusión tan ingenua y, al mismo tiempo, tan prepotente. No es el daño el ausente, es el método de observación el que falla. La mayoría de estrellas “no existieron” hasta que se inventó el telescopio, y la célula fue “un invento” del microscopio. La realidad es contundente y perseverante, pero se necesita cierta metodología para entenderla. Los neurotransmisores, los fenómenos de hipersensibilidad visceral, la microinflamación y los mecanismos de intercomunicación entre el sistema nervioso y digestivo no se ven a simple vista; pero no por eso dejan de existir.
En el pasado, el médico se ha preocupado de descartar “lesiones graves”. Así, el paciente se quedaba más tranquilo, pero igual de molesto. Sin riesgo a grandes equivocaciones se puede decir que la historia de los TFD se ha caracterizado por su escaso conocimiento fisiopatológico, por el poco interés por parte de la comunidad científica y por la incomprensión por parte de muchos profesionales sanitarios.
En el futuro es poco probable que se establezca alguna diferencia entre enfermedades orgánicas y no orgánicas, lesiones visibles y no visibles. Muy posiblemente resulte irrisoria la forma actual que tenemos de entender la fisiopatología, y la neuroinmunofisiopatología, junto con la medicina genética, posiblemente desplace a gran parte de los conocimientos que ahora creemos dogma de fe. El futuro descubrimiento de las claves concretas por las que los procesos de origen central activan mecanismos periféricos (y viceversa), el conocimiento de la inducción de los mecanismos postinfecciosos, los mecanismos inmunorreguladores, la activación de múltiples neurotransmisores y otras muchas cosas que ahora ni nos imaginamos, harán que los TFD formen parte del grupo general de las enfermedades digestivas (del que nunca debieron salir).
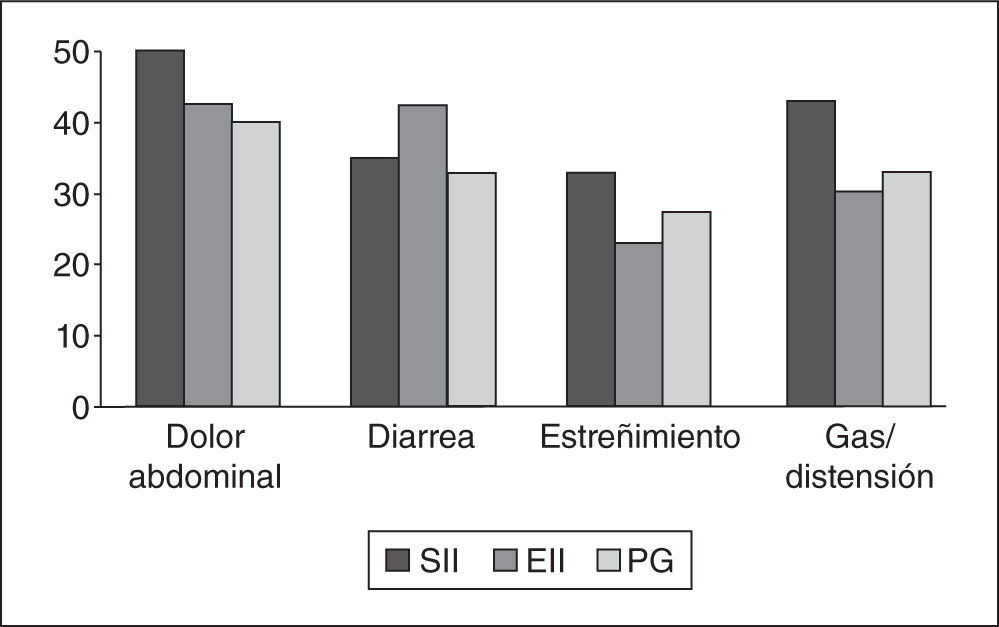
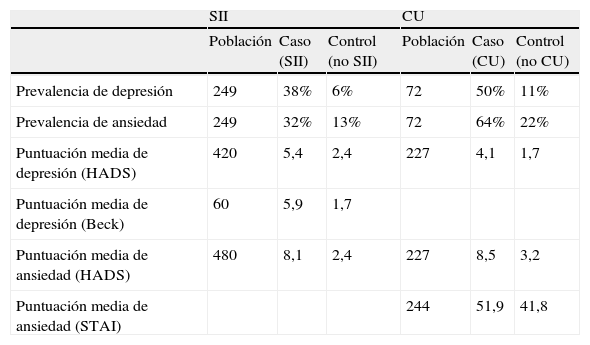
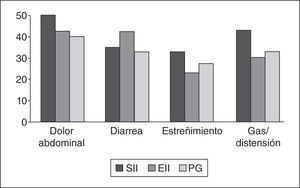
Síndrome del intestino irritable frente a enfermedad inflamatoria intestinal. ¿Cuál es peor?A este respecto se presentaron en la Digestive Diseases Week (DDW) 2013 varios estudios que comparaban pacientes con síndrome del intestino irritable (SII) y pacientes con enfermedad inflamatoria intestinal (EII). En un trabajo se comparó la intensidad de los síntomas digestivos en 231 casos de SII y 190 de EII1. Curiosamente (o no), los síntomas resultaron ser más intensos en los enfermos con SII incluyendo el dolor abdominal, la distensión y el estreñimiento; tan solo la diarrea fue peor en la EII (fig. 1). Pero quizá lo que ocurra es que los pacientes con SII se quejen más debido a sus trastornos psicológicos, ¿no? Otro estudio ha revisado y comparado las alteraciones psicológicas en el SII (n=668) y la EII (n=261)2. En esta revisión sistemática se seleccionaron publicaciones que habían utilizado la Hospital Anxiety and Depression Scale (HADS), el Beck Depression Inventor o el State-Trait Anxiety Index (STAI). Nuevamente, y de forma también curiosa (o no), se comprobó que el porcentaje de enfermos con ansiedad o con depresión fue semejante en ambas patologías (tabla 1). De estudios como este, que lógicamente deben ser confirmados, pueden sacarse 2 conclusiones a cuál más importante: a) no todo lo del SII es psicológico, y b) los aspectos psicológicos son importantes en cualquier enfermedad, incluyendo la EII.
Depresión y ansiedad en pacientes con síndrome del intestino irritable (SII), colitis ulcerosa (CU) y controles.
| SII | CU | |||||
| Población | Caso (SII) | Control (no SII) | Población | Caso (CU) | Control (no CU) | |
| Prevalencia de depresión | 249 | 38% | 6% | 72 | 50% | 11% |
| Prevalencia de ansiedad | 249 | 32% | 13% | 72 | 64% | 22% |
| Puntuación media de depresión (HADS) | 420 | 5,4 | 2,4 | 227 | 4,1 | 1,7 |
| Puntuación media de depresión (Beck) | 60 | 5,9 | 1,7 | |||
| Puntuación media de ansiedad (HADS) | 480 | 8,1 | 2,4 | 227 | 8,5 | 3,2 |
| Puntuación media de ansiedad (STAI) | 244 | 51,9 | 41,8 | |||
Beck: Beck Depression Inventor; CU: colitis ulcerosa; HADS: Hospital Anxiety and Depression Scale; STAI: State-Trait Anxiety Index.
Yendo un paso más adelante se comprueba de nuevo cómo, frecuentemente, los TFD forman parte de una alteración más generalizada. Así, su asociación con trastornos funcionales somáticos dolorosos es habitual. Jones et al3 presentaron los resultados de más de 20.000 pacientes atendidos en atención primaria con el diagnóstico de TFD. La asociación con migraña, cefalea tensional, dolor facial, pélvico o de espalda fue claramente superior a la de un grupo control sin TFD. Además, cuando se asocian varios TFD en un mismo sujeto el riesgo es mayor y cuando el TFD es único el mayor riesgo es para el SII. Quizá más importante es la comprobación de cómo el tipo, y no solo el número, de comorbilidades físicas y psicológicas altera de manera distinta la gravedad de los síntomas y la calidad de vida en pacientes con SII4. Siguiendo con este tema, hay síntomas que están ahí pero que pasan desapercibidos: por ejemplo, la fatiga. Lacker et al5 evaluaron de manera muy detallada a 176 pacientes que cumplían criterios de Roma III para SII; de los síntomas digestivos y extradigestivos, el tercero más frecuente fue la fatiga (61%), que se asoció de manera significativa tanto a molestias somáticas (SII más grave, mayor número de síntomas) como psicológicas (ansiedad, depresión).
En busca de la causa del síndrome del intestino irritableFactores ambientales en la infanciaSin duda, la patogénesis de los TFD es multifactorial: influyen factores genéticos, ambientales, familiares, dietéticos, etc. Estudios previos han comprobado que los acontecimientos de la infancia pueden predisponer al desarrollo de un TFD en la edad adulta. Para profundizar más en este sentido, Koloski et al6 analizaron tanto los aspectos emocionales como los higiénicos (“teoría de la higiene”) en la infancia de 670 sujetos con TFD y controles. Se evaluaron los factores ambientales precoces de riesgo como la forma de parto, la prematuridad, la lactancia materna y su duración. También se incluyeron otros como compartir el dormitorio, vivir en un área rural agrícola, convivir con animales domésticos, y el divorcio, separación o muerte de los padres. Se comprobó que los sujetos con SII habían tenido una menor duración de lactancia materna (5,6 frente a 8,1 meses), habían compartido habitación con menor frecuencia entre los 18 meses y los 5 años, y la separación de los padres (entre los 5 y 18 años) había sido más frecuente. A su vez, las personas que cumplían criterios de dispepsia funcional (DF) también habían tenido una menor duración de lactancia materna (5,5 frente a 7,9 meses), habían tenido una mayor exposición a animales domésticos entre el nacimiento y los 18 meses, y más divorcios paternos. El nacimiento por cesárea, aunque no llego a alcanzar significación estadística, fue más frecuente tanto en el SII como en la DF. Estos datos refuerzan “la teoría de la higiene”, así como de los traumas psicológicos en la infancia, como posibles mecanismos inductores de TFD.
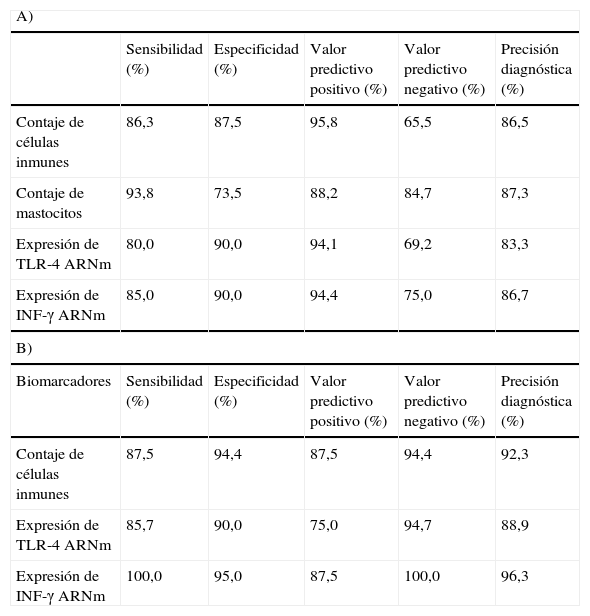
La microinflamación como biomarcadorUno de los problemas fundamentales en el diagnóstico del SII es que no hay un marcador biológico específico. No obstante, varios estudios han demostrado un aumento de células mastocitarias en el colon. El grupo de la Universidad de Bolonia ha investigado si la cuantificación de células inmunitarias puede servir como biomarcador en el SII7. Para ello se obtuvieron biopsias del colon de 144 pacientes con SII, 32 con colitis ulcerosa (CU) y 68 controles sanos (CS), con el fin de estudiar el número total de células inmunes, mastocitos, y expresión genética de inmunidad. Los resultados son de gran interés: los parámetros evaluados fueron significativamente superiores en pacientes con SII que en CS, aunque inferiores a los enfermos con CU. Los valores de sensibilidad, especificidad, valor predictivo positivo y valor predictivo negativo se muestran en la tabla 2. Como puede observarse, el contaje de células inmunes, mastocitos, y expresión genética de inmunidad tiene una buena sensibilidad y especificidad para distinguir pacientes con SII de CU y CS. No obstante, estos datos deben ser confirmados por otros investigadores, comparados con otras enfermedades que pueden producir microinflamación colónica, y valorados económicamente.
Precisión diagnóstica de los biomarcadores inmunes mucosos en distinguir controles sanos de pacientes con síndrome del intestino irritable (A), y en distinguir pacientes con síndrome del intestino irritable de pacientes con colitis ulcerosa (B).
| A) | |||||
| Sensibilidad (%) | Especificidad (%) | Valor predictivo positivo (%) | Valor predictivo negativo (%) | Precisión diagnóstica (%) | |
| Contaje de células inmunes | 86,3 | 87,5 | 95,8 | 65,5 | 86,5 |
| Contaje de mastocitos | 93,8 | 73,5 | 88,2 | 84,7 | 87,3 |
| Expresión de TLR-4 ARNm | 80,0 | 90,0 | 94,1 | 69,2 | 83,3 |
| Expresión de INF-γ ARNm | 85,0 | 90,0 | 94,4 | 75,0 | 86,7 |
| B) | |||||
| Biomarcadores | Sensibilidad (%) | Especificidad (%) | Valor predictivo positivo (%) | Valor predictivo negativo (%) | Precisión diagnóstica (%) |
| Contaje de células inmunes | 87,5 | 94,4 | 87,5 | 94,4 | 92,3 |
| Expresión de TLR-4 ARNm | 85,7 | 90,0 | 75,0 | 94,7 | 88,9 |
| Expresión de INF-γ ARNm | 100,0 | 95,0 | 87,5 | 100,0 | 96,3 |
Cada vez parece más importante el papel de los ácidos biliares en la patogénesis de los síntomas del SII. Su producción, secreción y absorción dentro del ciclo enterohepático pueden condicionar los síntomas. Además, su modulación puede utilizarse tanto para el tratamiento de la diarrea como del estreñimiento. Se ha establecido una relación entre la excreción de ácidos biliares, el tiempo de tránsito colónico (TTC) y los síntomas de pacientes con SII. El grupo de la Clínica Mayo (Rochester, MN) ha investigado la frecuencia deposicional (número) y la consistencia (forma) en relación con el TTC y la excreción de ácidos biliares en 30 pacientes con SII-estreñimiento, 31 con SII-diarrea y 31 CS8. En el análisis univariante se encontró una asociación entre el número y la forma de las heces con la excreción total de ácidos biliares, aunque la influencia del TTC fue mayor. Lo que parece es que el aumento de la excreción total de ácidos biliares secretores aumenta el efecto del TTC en las características de las heces. De tal forma, la correlación es mejor cuando se cuantifican específicamente los ácidos biliares primarios y secundarios que cuando se mide el total: se comprobó un aumento de ácidos biliares primarios secretores en pacientes con diarrea mientras que estuvieron disminuidos cuando predominaba el estreñimiento9.
La comida y la dieta (FODMAP)En un trabajo sueco se investigó qué grupo de alimentos y circunstancias dietéticas causan más síntomas en el SII10. Para ello, 197 pacientes rellenaron un cuestionario sobre 56 alimentos posiblemente relacionados con intolerancias/alergias alimentarias; también se cumplimentaron cuestionarios para valorar depresión y ansiedad (HAD), ansiedad GI-específica (VSI), síntomas de SII (IBS-SSS), síntomas somáticos (PHQ-15) y calidad de vida (IBSQOL). Los resultados más destacables fueron que el 84% de los pacientes relacionó al menos 1 de los alimentos con los síntomas. El 71% con carbohidratos de absorción incompleta, siendo los más frecuentes los lácteos (49%), alubias/lentejas (36%) y la manzana. El 56% relacionó los síntomas con alimentos ricos en aminas (vino, cerveza, salami) o con alimentos que liberan histamina (cerdo, chocolate y naranja). Los alimentos grasos fueron implicados en un 52%. Se encontró una correlación entre la gravedad de los síntomas de SII con más síntomas somáticos, una peor calidad de vida y más número de alimentos potencialmente inductores de molestias.
Además, parece claro que hay una correlación entre la ingesta y la aparición de síntomas en el SII (aunque parece haber pasado desapercibida y no se incluye en ningún criterio diagnóstico). Sin embargo, Lackner et al11 han comprobado que las manifestaciones clínicas se inducen al comer en el 59% de los pacientes con SII moderado o grave.
Por otro parte, se ha postulado que una dieta baja en FODMAP (oligo-, di- y mono-sacáridos fermentables y polioles) puede mejorar los síntomas de los pacientes con SII. El mecanismo puede ser tan solo la disminución de la fermentación colónica de los alimentos, pero Zhou et al12 han investigado si también tiene algún efecto en la microbiota y la inflamación intestinal así como en la nocicepción. Para ello realizaron un estudio en ratas Wistar que fueron alimentadas con una dieta rica, pobre o normal en FODMAP. Las conclusiones fueron que la primera puede causar disbiosis intestinal acompañada de inflamación, alteración de la permeabilidad e hipersensibilidad visceral. Por el contrario, una dieta pobre en FODMAP reduce la inflamación intestinal y mejora la función barrera; ello se acompaña de una normalización de la hipersensibilidad visceral. Estos datos obtenidos de la investigación en animales abren nuevas hipótesis sobre las interacciones entre alimentos, microbiota, mecanismos inmunoinflamatorios y síntomas (¡apasionante!).
Síndrome del intestino irritable, enfermedad celíaca y sensibilidad al gluten no celíacaSi bien es cierto que en un metaanálisis publicado en el año 2009, que incluía 4.202 pacientes, la prevalencia de enfermedad celíaca (EC) en sujetos con sospecha de SII fue 4 veces superior a la encontrada en una población control13, otros investigadores consideran que la prevalencia de EC no está aumentada en los pacientes con síntomas de SII. Así, algunos estudios caso-control, aunque con un escaso número de pacientes, no han encontrado diferencias estadísticamente significativas entre pacientes con síntomas de SII y controles sin síntomas gastrointestinales14,15. Más sólidos son los datos de un trabajo publicado en 2011 en el que se comparaban los datos de 492 pacientes con SII sin estreñimiento (es decir, con diarrea o ritmo deposicional mixto diarrea/estreñimiento) con los de 458 sujetos asintomáticos. La serología para EC fue positiva en el 7,3% de los pacientes con SII y el 4,8% de los controles; los anticuerpos positivos en los pacientes con SII fueron: 6,51% antigliadina, 1,22% antitransglutaminasa y 0,61% antiendomisio (en ningún caso estadísticamente diferentes a los resultados en controles)16. Se confirmó, mediante biopsia duodenal, EC en el 0,41% de los pacientes y en el 0,44% de los controles. No obstante, los propios autores comentan el posible significado de la elevada prevalencia de anticuerpos antigliadina en los casos de SII. Este fenómeno ya se había publicado tanto en sujetos que refieren tolerar mal el gluten (prevalencia de anticuerpos antigliadina del 40%)17 como en pacientes con SII (prevalencia del 17%), a pesar de ser normal la biopsia duodenal y negativos los anticuerpos antitransglutaminasa y antiendomisio18.
Las diferencias en los resultados de los distintos estudios que comprueban o no un aumento de la prevalencia de EC en pacientes que cumplen criterios de SII podrían deberse a diferencias poblacionales y geográficas. La mayoría de los estudios con resultados positivos, incluidos en el metaanálisis, proviene de Europa. Por el contrario, los que aportan resultados negativos y, en especial, el más determinante (por su calidad metodológica y número de enfermos incluidos) de Cash et al16 se realizaron en Estados Unidos.
Estos datos previos refuerzan el interés de un estudio realizado en Méjico (Norteamérica), en el que se analizó la presencia de anticuerpos antitransglutaminasa y antigliadina en 339 pacientes con SII y 339 CS19. En el 6,9% de los pacientes se detectó algún marcador positivo de enfermedad celíaca, frente al 2,91% de los controles; el 3,85% de los pacientes y el 0,88% de los controles tenían anticuerpos antitransglutaminasa positivos. En 11 pacientes y 3 controles se comprobó enfermedad celíaca histológicamente.
En cualquier caso, y hasta que haya datos más concluyentes, actualmente se aconseja realizar cribado de la EC mediante serología y, en caso positivo, biopsia duodenal en pacientes con síntomas de SII que no padezcan estreñimiento20.
¡Ah!, otra cosa interesante: la mayoría de pacientes que siguen una dieta sin gluten por decisión propia y sin indicación médica no cumple criterios de sensibilidad al gluten no celíaca; de hecho, no son capaces de diferenciar un período de dieta con o sin gluten cuando se realiza de forma ciega21.
Dispepsia funcionalIntentando mejorar la clasificación de la dispepsia funcionalLos criterios diagnósticos de Roma III para la DF la subdividen en 2 subtipos: síndrome de distrés posprandial (SDP), en el que los síntomas aparecen en relación con la ingesta, y síndrome de dolor epigástrico (SDE), en el que los síntomas no tienen una relación tan inmediata con la ingesta. El problema está en que más de la mitad de los pacientes con DF presenta un solapamiento de ambos subtipos. Uno de los grupos de investigadores más activos en DF, como es el de Lovaina, analizó cómo cambiaba la clasificación de los pa cientes si se tenía en cuenta si la aparición de los distintos síntomas se relacionaba con la ingesta de alimentos22. Así, a partir de 598 pacientes remitidos para estudio de síntomas dispépticos, pudieron reclutar a 80 pacientes con endoscopia normal que reunían criterios de Roma III de DF, y de ellos el 17% tenía SDE puro, el 29% tenía SDP puro y el 55% restante tenía solapamiento entre SDE y SDP. Analizaron la relación de los síntomas con la ingesta, entre ellos la pesadez posprandial o la saciedad precoz (síntomas reconocidos como parte del SDP), pero también síntomas como el dolor epigástrico posprandial, la náusea posprandial o los eructos (en los que la relación con la ingesta no está recogida en los cuestionarios de Roma III). Cuando compararon los pacientes con SDE puro con los pacientes con solapamiento entre SDE y SDP observaron que estos últimos tenían más náusea posprandial, eructos y dolor epigástrico posprandial, mientras que el dolor epigástrico entre comidas no era diferente entre ambos grupos de pacientes. El grupo de Lovaina planteaba que si se consideraban otros síntomas posprandiales como el dolor epigástrico o la náusea como parte del SDP, la clasificación de los pacientes con DF variaba sustancialmente, de forma que se mantenía, como es lógico, el 17% de pacientes con SDE, pero aumentaba el porcentaje de pacientes con SDP, que pasaba del 29 al 52%, y disminuía de forma notable el porcentaje de pacientes con solapamiento entre SDE y SDP, que pasaba del 55 al 31%.
Profundizando en la fisiopatología de la dispepsia funcionalUno de los mecanismos involucrados en la fisiopatología de la DF son las alteraciones en la acomodación gástrica. El grupo de Jan Tack estudió de forma precisa la acomodación gástrica determinando mediante barostato gástrico cuál era la curva de volumen gástrico que se obtenía en respuesta a una ingesta líquida. Obtenían así 4 partes en la curva de respuesta de volumen gástrico posprandial que correspondían a distintos momentos de la acomodación (la primera parte correspondía a la relajación gástrica inicial inducida por la ingesta, mientras que las otras partes correspondían a un lento incremento del volumen hasta alcanzar el máximo y posteriormente el retorno al nivel basal). Pues bien, aplicando esta metodología en 259 pacientes con DF (criterios de Roma II), valoraron en un trabajo presentado como comunicación oral el efecto de la ansiedad aguda y de la ansiedad crónica comórbida sobre la acomodación gástrica23, y pudieron observar que ambos estados de ansiedad comportaban una alteración de la acomodación gástrica significativa. Esto vendría a explicar, en parte, el ya conocido papel como agravante de la sintomatología de los pacientes dispépticos de la ansiedad.
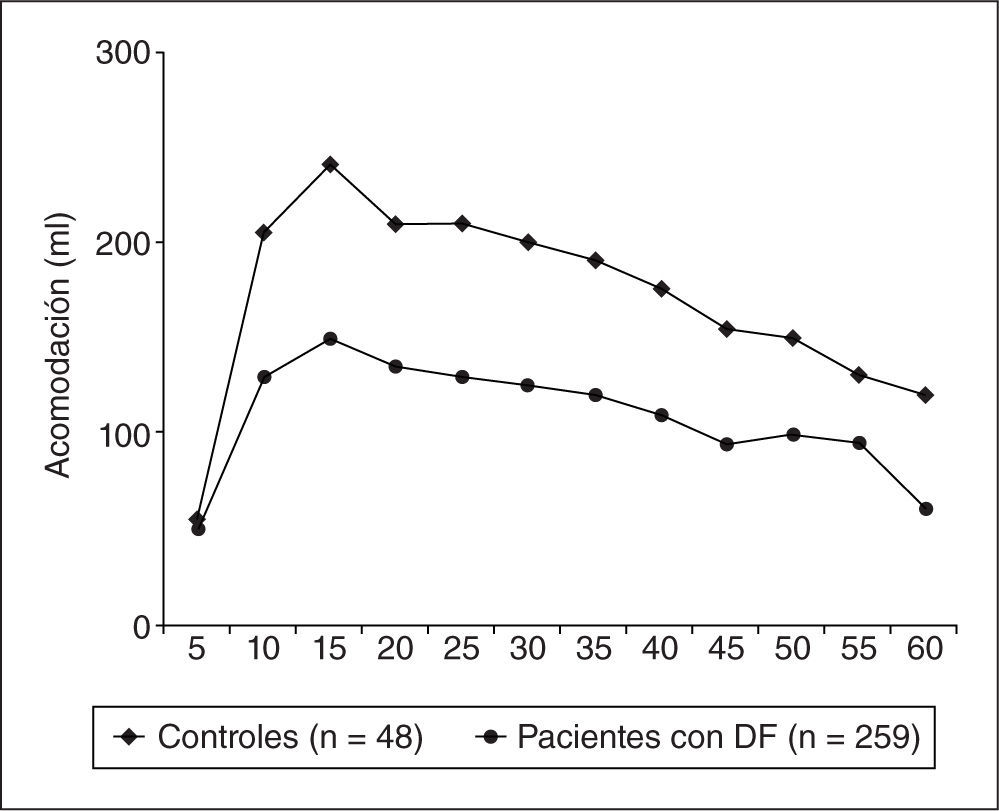
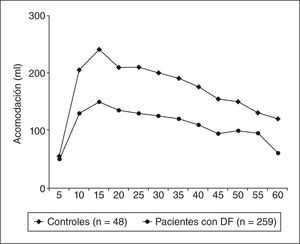
Aplicando esta misma metodología, el mismo grupo de investigadores comparó las curvas de acomodación gástrica de los 259 pacientes con DF con las obtenidas en 46 CS. Además valoró la acomodación gástrica en función de la sensibilidad gástrica (medida mediante el mismo barostato) y del vaciamiento gástrico (medido por prueba del aliento con ácido octanoico marcado con C13) de los pacientes con DF24. Comparados con los CS, los pacientes con DF presentan un más lento incremento del volumen gástrico hasta alcanzar un volumen máximo menor y un más lento retorno al valor basal (fig. 2). Cuando analizaron el efecto en la curva de acomodación de la hipersensibilidad gástrica observaron un incremento inicial más rápido en los pacientes con hipersensibilidad, así como un más rápido retorno a los valores basales. Cuando analizaron el efecto del retraso del vaciamiento gástrico observaron un incremento global en toda la curva de acomodación. Esto demuestra la forma compleja en que las distintas alteraciones sensoriales y motoras gástricas interactúan entre sí para explicar la fisiopatología de la DF.
Variaciones del volumen gástrico que reflejan las fases de la acomodación gástrica medidas por barostato rectal. Los pacientes con dispepsia funcional (DF) presentan un más lento incremento del volumen gástrico hasta alcanzar un volumen máximo menor y un más lento retorno al nivel basal.
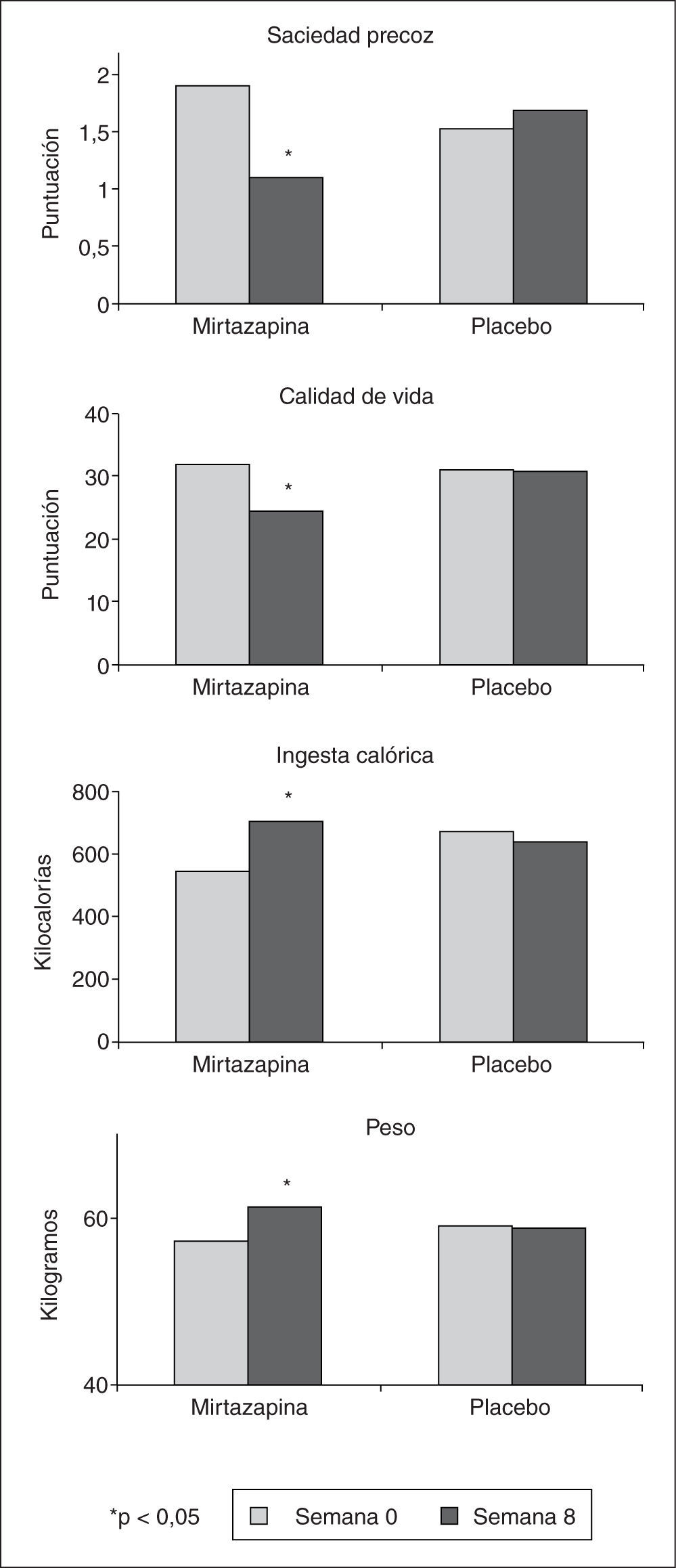
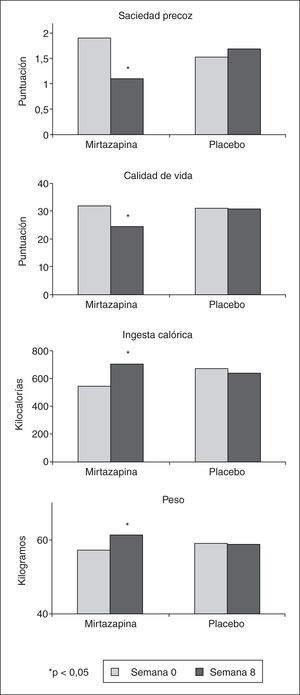
Un interesante trabajo presentado como comunicación oral demostró la eficacia de la mirtazapina, un antidepresivo de acción dual noradrenérgica y serotoninérgica, en pacientes con DF con pérdida de peso25. Para ello reclutaron 34 pacientes con DF que habían perdido al menos un 10% de su peso sin que estuviesen afectados de trastornos de ansiedad o depresión. Después de hacer un test de saciedad inicial, los pacientes fueron aleatorizados a recibir placebo o mirtazapina 15mg cada noche mediante técnica de doble ciego. Se hicieron evaluaciones con cuestionarios clínicos y con un cuestionario de calidad de vida relacionada con la salud específico para DF (Nepean Dyspepsia Index) en el momento de inclusión en el estudio y a las 8 semanas, momento en el que también se repitió el test de saciedad. Los resultados mostraron que la mirtazapina mejoró significativamente la saciedad precoz y la calidad de vida de estos pacientes. Esto se asoció a una mayor tolerancia a la ingesta (medida por el test de saciedad) y a un mayor incremento del peso, de forma que el grupo tratado con mirtazapina recuperó más de 4kg de peso de media mientras que el grupo tratado con placebo no recuperó nada de peso (fig. 3). Siempre es bueno añadir una opción más al arsenal terapéutico para manejar a nuestros pacientes, así que ¡bienvenida a la gastroenterología, mirtazapina!
Hace tiempo que se debate el papel de Helicobacter pylori en la DF, y este año un nuevo trabajo aportó más datos sobre la eficacia de su erradicación en la evolución a largo plazo de esta. En este estudio se evaluó el efecto de la erradicación al cabo de una media de 15 años en 141 pacientes con DF, comprobando que no se hubieran reinfectado en ningún caso26. Al cabo de 15 años, 109 pacientes seguían teniendo síntomas, de forma que tan solo el 23% de los pacientes permanecía asintomático. Esto enfría un poco los ánimos de los entusiastas de la erradicación como tratamiento de la DF, aunque visto por otro lado parece que una cuarta parte de los pacientes se puede beneficiar. ¿Cuáles?
Gastroparesia¿Qué novedades terapéuticas hay en la gastroparesia?El grupo de investigadores liderado por Henry P. Parkman, del que en años anteriores habíamos comentado distintos estudios, presentó este año un estudio que valoró la eficacia de la nortriptilina en el control de los síntomas de pacientes con gastroparesia idiopática27. El estudio fue diseñado a dosis progresivas durante 15 semanas. Se incluyeron 65 pacientes en cada grupo de tratamiento: nortriptilina o placebo. Pues bien, no se demostró una mejoría global en el grupo tratado con nortriptilina, aunque sí mejoraron síntomas como la náusea y el dolor abdominal a dosis bajas (a dosis elevadas no se observó este efecto). Mejoró además el apetito y hubo una mayor ganancia de peso corporal en los pacientes tratados con nortriptilina, por una mejor tolerancia a la ingesta evaluada por test de saciedad. Un inconveniente del tratamiento es que un 29% de los pacientes tuvo que interrumpirlo por efectos secundarios. En resumen, aunque no parece que la nortriptilina controle todos los síntomas de la gastroparesia idiopática, sí nos permite controlar algunos síntomas y, especialmente, mejorar el estado nutricional de estos pacientes, por lo que habrá que tenerla en cuenta en estos casos.
Aunque no se pueda considerar una novedad terapéutica, sí lo puede ser la forma de administración. Así, el mismo grupo de investigadores probó la eficacia de 2 dosis de metoclopramida administrada en forma de spray nasal comparándola con metoclopramida oral en pacientes con gastroparesia diabética28. Pues bien, en 89 pacientes con gastroparesia diabética la metoclopramida en spray nasal logró un mejor control, tanto a dosis de 10 como de 20mg, que la metoclopramida en comprimidos de 10mg oral, y puede ser, por tanto, una opción de administración muy útil en pacientes con gastroparesia diabética.
Diagnóstico diferencial del síndrome de intestino irritableLa malabsorción de ácidos biliares (MAB) y la insuficiencia pancreática exocrina son 2 entidades a descartar en pacientes con síndrome del intestino irritable con predominio de diarrea (SII-D). La insuficiencia pancreática exocrina puede presentar una clínica similar al SII-D y se ha comunicado un único estudio que señala una prevalencia del 6,1% entre pacientes con SII-D29. El grupo de Gotteborg presentó este año un estudio donde se evaluó la elastasa fecal en 2 ocasiones en una serie de 111 pacientes consecutivos con SII, registrando durante 2 semanas el hábito defecatorio. Se detectaron unos valores bajos de elastasa fecal en 7 pacientes, lo que representa una frecuencia del 6,3%, pero solo 1 de ellos mostró un claro predominio de diarrea30.
La MAB es otra de las entidades que se plantea ante un paciente con clínica de SII-D; las posibilidades para realizar el diagnóstico diferencial son el diagnóstico exjuvantibus con una prueba terapéutica con resincolestiramina o el test de retención con 75SeHCAT. Covington et al presentaron unos excelentes resultados de un estudio piloto con una novedosa técnica diagnóstica, la “e-nose”, para diferenciar los pacientes con MAB de los pacientes con SII, utilizando como patrón oro la retención de 75SeHCAT31. La e-nose detecta los compuestos orgánicos volátiles de la orina mediante una batería de sensores químicos. Esta técnica se perfila como una extraordinaria ayuda diagnóstica para múltiples problemas digestivos, incluyendo la MAB.
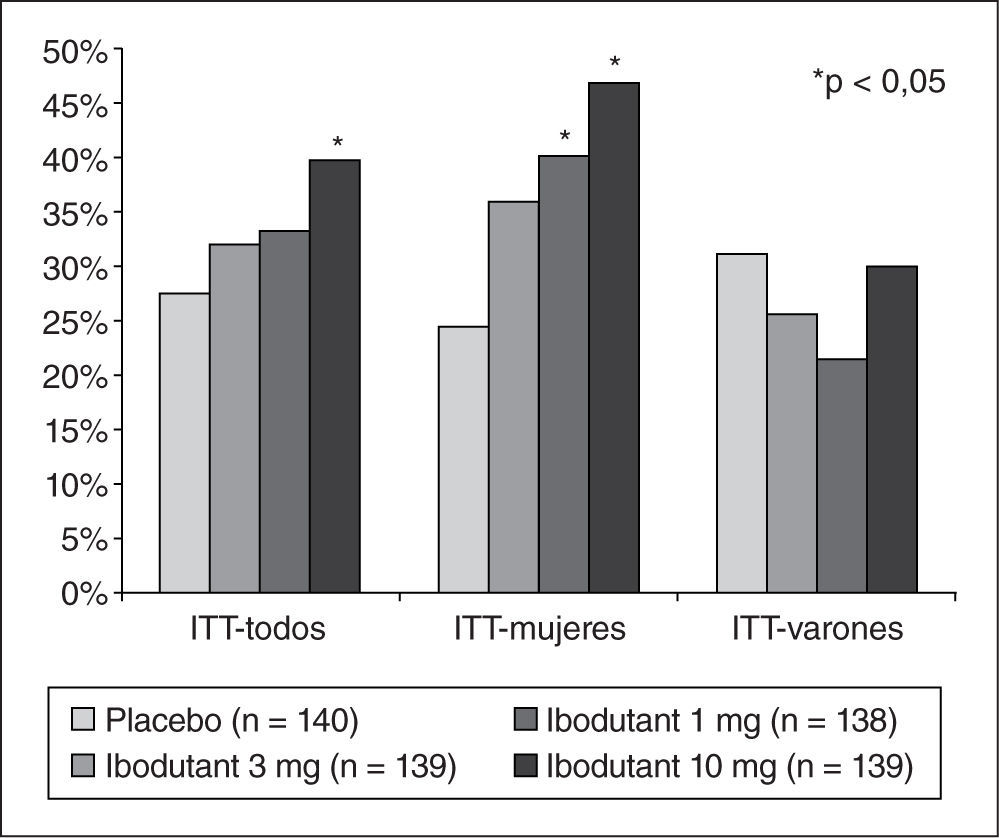
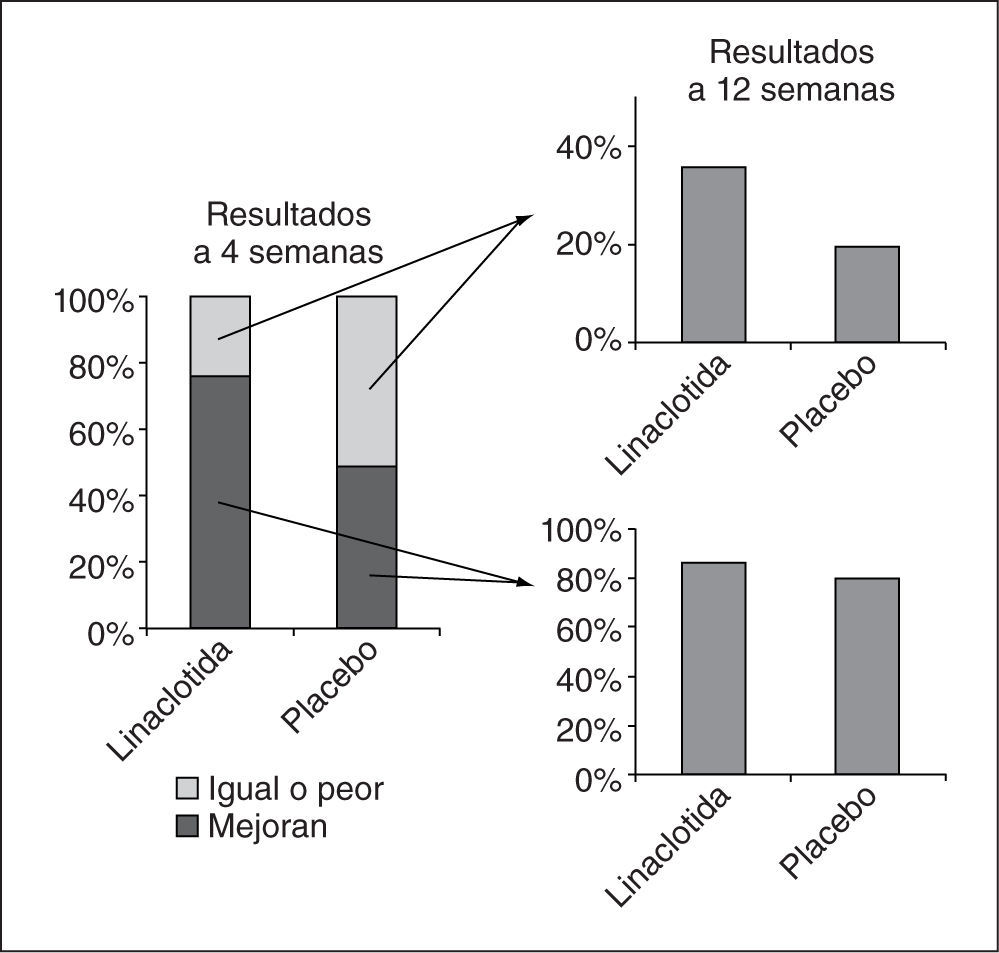
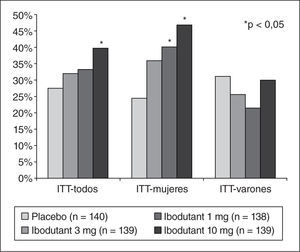
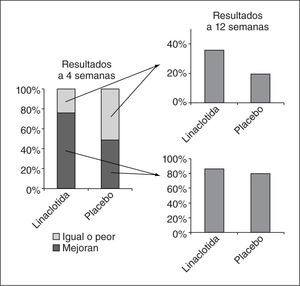
Tratamiento del síndrome de intestino irritableEl tratamiento del SII es complejo en la práctica y desafortunadamente no hay muchos fármacos que hayan demostrado claramente su eficacia en la clínica. Entre las novedades presentadas en la DDW cabe destacar la presentación de los resultados de un estudio doble ciego de fase II que comparaba ibodutant, un antagonista de los receptores NK2 a diferentes dosis, frente a placebo, incluyendo 559 pacientes con SII-D32. El ibodutant, a dosis de 10mg diarios, mostró una superioridad sobre el placebo con un perfil de seguridad excelente. Curiosamente, este beneficio se produjo solo entre las mujeres, con una ventaja del fármaco activo sobre el placebo superior al 20% de acuerdo al objetivo primario, sin que se observara ningún beneficio en los varones (fig. 4).La hipótesis de la microinflamacion subyacente al SII hace muy atractivo el tratamiento con antiinflamatorios, como la mesalazina. Son pocos los estudios realizados y con resultados discordantes, por lo que resulta de interés un pequeño ensayo con 21 pacientes en el que se muestra que la mesalazina a dosis de 800mg 3 veces al día es superior al placebo en pacientes con SII-D33.Con respecto al SII con predominio de estreñimiento destacan los datos sobre linaclotida, un fármaco recientemente aprobado por la Food and Drug Administration y la European Medicines Agency para esta indicación, cuya eficacia fue corroborada por un metaanálisis de 6 estudios presentado en la DDW34. Un estudio experimental en ratones ha demostrado claramente que es capaz de reducir la sensibilidad visceral y que este efecto es claramente dependiente de su capacidad para activar la guanilato ciclasa C35. Una de las preguntas clínicas de más interés es cuál es la mínima duración del tratamiento antes de decidir que ha fracasado; un análisis de 2 estudios de fase III mostró que la mayoría de los pacientes que obtuvieron respuesta a las 4 semanas seguía manteniendo la respuesta a las 12 semanas, mientras que hasta un 30% de los que no habían tenido respuesta a las 4 semanas alcanzaba una respuesta clínica a las 12 semanas (fig. 5)36; no queda claro, por tanto, si un tratamiento de 4 semanas es suficiente para decidir el fracaso del tratamiento.Se presentaron otros 2 estudios terapéuticos, con fundamentos muy diferentes, que resultan interesantes. El primero de ellos fue un estudio doble ciego controlado con placebo que evaluaba la eficacia clínica y el efecto sobre la sensibilidad visceral de la ebastina, un antagonista H1, en 55 pacientes con SII, con un diseño aleatorizado y doble ciego. La ebastina mostró ser superior al placebo para aliviar los síntomas de SII y para disminuir el dolor, aunque no modificó los parámetros de sensibilidad visceral37. El segundo estudio mostró los resultados de un estudio aleatorizado que comparaba los efectos de la glutamina y el placebo sobre los síntomas y la permeabilidad intestinal en 61 pacientes con SII-D. La glutamina, a dosis de 10mg 3 veces al día, mejoró todos los síntomas del SII y restauró las alteraciones de la permeabilidad intestinal38.Entre las nuevas dianas terapéuticas posibles cabe destacar la potencial utilidad de los antagonistas de los receptores H4 como analgésicos viscerales. Un estudio realizado en un modelo animal de hipersensibilidad postinflamatoria (colitis inducida por instilación de ácido 2,4,6-trinitrobencenosulfónico [TNBS]) demostró que un antagonista selectivo de los receptores H4 de la histamina, el JNJ 7777120, era capaz de modificar de forma dependiente de la dosis las respuestas visceromotoras a la distensión colónica39.
El estreñimiento crónico es un motivo de consulta frecuente, que en muchos casos es relativamente fácil de resolver con el arsenal disponible, pero hay pacientes con clínica especialmente grave y que plantean un importante problema clínico. Entre las novedades presentadas en la DDW destaca un ensayo en fase IIa de un nuevo agonista de los receptores de la GC-C, la plecanatida. En este ensayo doble ciego se compararon 3 dosis de plecanatida con placebo en 946 pacientes con estreñimiento crónico que cumplían criterios de Roma III y presentaban menos de 3 deposiciones espontáneas y completas semanales, durante 12 semanas, demostrándose que la plecanatida a la mayor dosis ensayada (3mg 1 vez al día) es superior al placebo para aliviar los síntomas de estreñimiento40.
Entre los fármacos actualmente disponibles para el tratamiento del estreñimiento crónico se encuentra prucaloprida, que ha mostrado una superioridad frente a placebo41. En la DDW se presentó un análisis conjunto de 280 pacientes incluidos en los ensayos clínicos realizados con prucaloprida frente a placebo y de los que se disponía estudio de TTC previo y posterior; los resultados muestran que prucaloprida es capaz de normalizar el TTC en una mayor proporción de pacientes, pero además señala que otros síntomas como esfuerzo defecatorio, distensión o flatulencia presentan una relación inversa con el TTC posterior, sugiriendo que la aceleración del tránsito es la responsable de la mejoría de estos síntomas42.
La estimulación de las raíces sacras es una de las opciones terapéuticas disponibles en pacientes con estreñimiento refractario con tiempo de tránsito enlentecido. Sin embargo, apenas hay estudios bien diseñados que sustenten su eficacia y hay una gran heterogeneidad de resultados en la práctica. De gran interés por ello es un estudio excelentemente diseñado en el que se incluyen 55 pacientes con estreñimiento crónico por TTC lento sin disinergia asociada que habían presentado respuesta a la estimulación periférica y en el que se implanta un estimulador de raíces sacras. La comparación cruzada y ciega de estimulación ficticia, estimulación no percibida y estimulación percibida no muestra ventajas de la estimulación activa frente a la ficticia43.
En los pacientes con disinergia defecatoria, el biofeedback representa la mejor opción terapéutica. Sin embargo, no está claro cuáles son los factores que predicen la respuesta al tratamiento. En este sentido es destacable un estudio coreano en el que se analizan los factores predictores de respuesta en una serie clínica muy amplia de 1.341 pacientes44. La tasa de respuesta al biofeedback en esta serie fue del 65% y los factores que predecían la respuesta fueron una adecuada prensa abdominal (definida por una elevación normal de la presión rectal durante el esfuerzo defecatorio), ausencia de hiposensibilidad rectal, capacidad para expulsar el balón en el test de expulsión y sexo femenino. No obstante, la hiposensibilidad puede mejorarse con el biofeedback, especialmente con el biofeedback asistido por barostato, como mostró otro estudio del grupo de Rao45.
Otros mensajes de utilidadRiesgo de padecer un cáncer de esófago en pacientes con acalasiaDiversos estudios han sugerido que la acalasia incrementa el riesgo de padecer un cáncer de esófago y que esta es una de las causas de aumento de mortalidad en estos pacientes. El diagnóstico suele demorarse al pensar que la disfagia es por recidiva de la acalasia en lugar de ser considerada como un síntoma de alarma. Por este motivo es interesante referir aquí los resultados de un estudio belga en el que se analizaron los datos de 372 enfermos con acalasia tratados mediante dilatación neumática desde el año 199246. Seis pacientes (media de 62±2 años) fueron diagnosticados de cáncer de esófago durante el seguimiento. La incidencia fue muy superior a la de la población general y los tiempos desde la primera dilatación neumática (87±23 frente a 29±2 meses; p<0,01) y desde los primeros síntomas (84±27 frente a 51±3 meses; p<0,05) fueron significativamente mayores en los pacientes que desarrollaron cáncer que en los que no lo desarrollaron. En todos los casos había dilatación esofágica y retención de líquido o comida previos al diagnóstico del tumor. Estos datos sirven para recordarnos la necesidad de realizar seguimiento en los pacientes con acalasia y extremar la vigilancia en los casos de mayor evolución y estasis esofágica.
Tratamiento con inyección de toxina botulínica de los trastornos motores del esófago de tipo no acalasiaEl tratamiento de los trastornos motores espásticos del esófago es difícil. Los resultados obtenidos con inyección de toxina botulínica son contradictorios y casi siempre se han valorado a corto plazo. En un estudio realizado en la Clínica Mayo de Jacksonville se analizaron los datos de 49 pacientes (edad media 70 años) con los siguientes diagnósticos: espasmo esofágico distal (55%), esófago en cascanueces (31%), esfínter esofágico inferior (EEI) hipertensivo (8%) y relajación incompleta del EEI (6%)47. Se realizó un total de 86 inyecciones de toxina botulínica y 17 pacientes recibieron más de 1 inyección. En el seguimiento, de 1 a 60 meses, se produjo mejoría en un 72-100% de los casos, con una duración media de 20±17 meses; no hubo complicaciones.
En otro trabajo, en este caso francés, los resultados no fueron tan esperanzadores48. Trataron mediante inyección de toxina botulínica en el EEI o en el esófago distal a pacientes con los siguientes diagnósticos (según la clasificación de Chicago): acalasia tipo III (n=9); “esófago en martillo neumático” (n=5); espasmo esofágico distal (n=1); esófago en cascanueces (n=1), y contracción excesiva del EEI posdeglución (n=1). Solo 7 pacientes (los 5 con “esófago en martillo neumático” y 2 con acalasia) estaban sin síntomas a los 5 meses de seguimiento (rango, 2–11 meses). Aunque no se produjeron efectos adversos graves, tras la inyección 9 pacientes tuvieron dolor torácico y 2 precisaron medicación con mórficos.
De estos estudios, y de datos previos, se puede inferir que el tratamiento con inyección de toxina botulínica de los trastornos motores del esófago de tipo no acalasia es una opción pero que los resultados son variables y parecen depender del tipo de trastorno.
Cómo diagnosticar el estreñimiento por disinergia de una manera sencillaLa disinergia defecatoria (contracción paradójica o ausencia de relajación del esfínter anal o del músculo puborrectal durante la defecación) es una causa frecuente de estreñimiento. Su diagnóstico y diferenciación de otras causas de estreñimiento es importante porque puede aplicarse un tratamiento específico: el biofeedback. Sin embargo, en muchas ocasiones no se realiza el diagnóstico por carecer de las pruebas complementarias precisas. Entonces, ¿cómo identificar a estos pacientes si no se dispone de manometría anorrectal, test de expulsión de balón o defecografía? En un estudio se ha evaluado la sensibilidad y la especificidad de la historia clínica y la exploración física en un grupo de 208 pacientes con estreñimiento que no respondía al tratamiento con fibra49. Mediante manometría anorrectal, test de expulsión del balón, defecografía y estudio del TTC se identificó a 102 pacientes con defecación disinérgica, 31 con tránsito colónico lento, 37 con obstrucción mecánica y 63 con tránsito colónico normal (5 fueron inclasificables). La elaboración de un cuestionario “ad hoc” demostró que la pregunta que mejor identificaba la defecación disinérgica era una sobre qué músculos se utilizaban para defecar: la respuesta “el ano” identificaba de manera correcta el 91% de las disinergias defecatorias mientras que cualquier otro tipo de respuesta indicaba otro tipo de estreñimiento en un 89%. El examen digital durante la maniobra defecatoria, comprobando si el esfínter anal se relajaba, identificó correctamente al 98% de los pacientes con disinergia defecatoria. En resumen, preguntando y haciendo un buen tacto rectal puede sospecharse muy fidedignamente la existencia de un estreñimiento por disinergia.
Conflicto de interesesEl Dr. Fermín Mearin es consultor de Almirall, Menarini, Novartis y Shire-Movetis. Ha impartido conferencias para Abbott, Alfa Wasserman, Almirall, Janssen, Menarini, Novartis y Shire-Movetis.
El Dr. Enrique Rey es consultor de Shire, Norgine y Almirall. Ha recibido fondos para investigación de Norgine y Almirall. Ha impartido conferencias para Shire, Norgine, Almirall, Menarini y Janssen-Cilag.
El Dr. Agustín Balboa declara no tener ningún conflicto de intereses.