INTRODUCCIÓN
La historia de los antidepresivos se inicia en 1957, al comprobar que 2 fármacos, la iproniazida y la imipramina, mejoraban el humor de los pacientes depresivos. Estos fármacos fueron inicialmente concebidos para otros fines terapéuticos, y fue mérito de sus descubridores confirmar su eficacia en un porcentaje elevado de depresivos. La iproniazida es el primer fármaco antidepresivo de la serie de los inhibidores de la monoaminooxidasa (IMAO), y la imipramina se considera el antidepresivo tricíclico patrón. En 1960 se descubría la amitriptilina y se sintetizaba la clorimipramina, y un año después se creaba la trimipramina, fármacos que iniciaron el grupo de los antidepresivos tricíclicos sedativos. En 1964 se evidenciaba que la imipramina y otros antidepresivos tricíclicos eran capaces de inhibir la recaptación presináptica de la noradrenalina (Glowinski y Axelrod, 1964). Un año más tarde, Joseph J. Schildkraut desarrollaría la hipótesis catecolamínica de los trastornos afectivos, que resaltaba el papel de la noradrenalina (Nad) en la aparición de los cuadros depresivos.
En la década de los setenta aparecieron los llamados antidepresivos de segunda generación (maprotilina, mianserina), de potencia antidepresiva igual o menor que los anteriores, pero en general mejor tolerados por su menor acción anticolinérgica. A este grupo también se añadirían los llamados antidepresivos atípicos (trazodona, nomifensin, alprazolam). El conjunto de antidepresivos: tricíclicos, de segunda generación y atípicos, se denominan antidepresivos heterocíclicos.
En 1972, el grupo de Copen, en Inglaterra, desarrolló la hipótesis indolamínica de la depresión, y destacó el papel de la serotonina (5HT). En la búsqueda de antidepresivos más seguros, el desarrollo de los inhibidores selectivos de la recaptación de serotonina (ISRS; fluoxetina, fluvoxamina, paroxetina, citalopram, sertralina) ha representado un avance significativo. Más recientemente ha aparecido una serie de antidepresivos que ha mejorado los perfiles de efectos secundarios, con mayor especificidad sobre los distintos sistemas neurotransmisores.
Los antidepresivos disponibles presentan estructuras químicas muy diversas, sin que pueda apreciarse ninguna correlación entre su estructura química y su especificidad terapéutica. Aunque el mecanismo de la acción antidepresiva todavía no se ha podido dilucidar, se sabe que los antidepresivos eficaces interactúan, de forma inmediata, con uno o más receptores o enzimas relacionados con los neurotransmisores monoaminérgicos. Estas acciones inmediatas proporcionan el fundamento farmacológico para la clasificación actual de los diferentes antidepresivos. Según este esquema de clasificación, existen, al menos, 8 mecanismos de acción farmacológicos distintos y más de 2 docenas de antidepresivos. La mayoría de los antidepresivos bloquean la recaptación de monoaminas, pero algunos de ellos bloquean los receptores alfa-2, y otros, la enzima monoaminooxidasa (MAO). Algunos antidepresivos tienen acciones directas sólo en un sistema neurotransmisor y otros actúan sobre varios sistemas (tabla 1)1.
PERFIL GENERAL DE LOS EFECTOS SECUNDARIOS DE LOS ANTIDEPRESIVOS
Los efectos secundarios de los antidepresivos, aparecen en un 15% de los pacientes, pero sólo en un 5% obligan a suspender la medicación. Es necesario distinguir entre la toxicidad del fármaco y los síntomas depresivos (astenia, ansiedad, alteraciones del sueño). El uso de dosis infraterapéuticas del fármaco expone a los efectos adversos sin tratar de forma adecuada la depresión. Estos efectos dependen de diversos factores2:
Las propiedades farmacológicas y sus efectos esencialmente alfaadrenolítico y anticolinérgico.
La posología y el ritmo de administración.
La sensibilidad individual de cada paciente.
Las eventuales asociaciones e interacciones medicamentosas.
En los apartados siguientes se describen los principales efectos secundarios de cada grupo farmacológico.
INHIBIDORES DE LA MONOAMINOOXIDASA
Fueron los primeros antidepresivos clínicamente eficaces descubiertos (Loomer et al, 1957). Los IMAO originales son todos inhibidores irreversibles de la MAO, y destruyen para siempre su función, de manera que la actividad enzimática sólo puede recuperarse por medio de la síntesis de una nueva enzima, para lo cual precisa de una a 3 semanas.
Existen 2 subtipos de MAO: la A y la B. Ambas formas son inhibidas por los IMAO originales, que no son selectivos. La forma A metaboliza los neurotransmisores monoaminérgicos más estrechamente relacionados con la depresión (5-HT y Nad). Asimismo, metaboliza la amina más estrechamente relacionada con la presión sanguínea (Nad). Por ello, la inhibición de la MAO A está asociada tanto a los efectos antidepresivos como a los secundarios hipertensivos no deseables. Dado que los IMAO inactivan también las MAO A intestinal y hepática, pueden incrementar las aminas ingeridas en la dieta (como la tiramina) y causar un aumento peligroso de la presión sanguínea, con el riesgo de hemorragias cerebrales. Por ello, requieren restricciones dietéticas y de ciertos medicamentos (meperidina, ISRS, tricíclicos, agentes simpaticomiméticos).
De los IMAO clásicos irreversibles y no selectivos (fenelcina, tranilcipromina, ixocarboxacida y nialamida), en España tan sólo se ha comercializado la tranilcipromina, y se utiliza a dosis de entre 10 y 40 mg/día. Los principales efectos adversos de los IMAO clásicos, son3-7:
Hepatotoxicidad.
Sobre el sistema nervioso central (SNC): excitabilidad, agitación, insomnio (50%), cuadros confusionales.
Sobre el sistema nervioso vegetativo: aumento de apetito y de peso (10-15%), impotencia y disminución de la libido (5-20%). Sobre todo, síntomas hiperadrenérgicos, aunque de menor intensidad que en los antidepresivos heterocíclicos (sequedad de boca [40%], visión borrosa, retención urinaria...). La hipotensión ortostática es el aspecto vegetativo más importante (del 40 al 60% de los sujetos), los cuadros de vértigo postural se observan en un 5 al 10% de los pacientes.
Cardiovasculares: sobre todo, crisis hipertensivas por interacción con otros fármacos (cefaleas, convulsiones, hemorragia intracraneal y colapso cardiovascular). El principal agente involucrado es la tiramina, pero también diversos fármacos, como la anfetamina, el metilfenidato, la efedrina, las aminas simpaticomiméticas y los antidepresivos tricíclicos). Más infrecuentes son las alteraciones de la acomodación visual (visión borrosa).
Crisis hipertérmicas por interacción con espasmos, mioclonías, vértigos, convulsiones y coma.
Síndrome de abstinencia en retirada brusca, con hipertensión arterial (HTA), taquicardia y dolor precordial.
Abuso por el efecto euforizante de la tranilcipromina.
Más raros: discrasias sanguíneas (anemia, leucopenia, agranulocitosis), reacciones cutáneas (erupciones, dermatitis), edemas.
De más reciente aparición son los Inhibidores selectivos y reversibles de los subtipos de la MAO. En psiquiatría, de interés son los IMAO reversibles de la MAO A (RIMA), y el principal producto es la moclobemida8. Los RIMA producen una inhibición reversible de la subunidad A de la MAO (cerebral y hepática), que desaparece en torno a las 16 h. Por ello, es mejor tolerado y no precisa restricciones dietéticas. Tiene efectos anticolinérgicos. Como reacciones adversas de los RIMA se han descrito las siguientes9:
Sequedad de boca.
Visión borrosa.
Taquicardia.
Hipotensión ortostática (en pacientes hipertensos).
Náuseas, vómitos, diarrea, dispepsia, estreñimiento.
Cefalea, insomnio, ansiedad, mareos, vértigos, astenia, temblor.
Sudación.
Aunque, en conjunto, se describe que la moclobemida, comparada con los antidepresivos tricíclicos patrón (imipramina), es mejor tolerado en cuanto a los efectos colinérgicos y la somnolencia8,9.
ANTIDEPRESIVOS TRICÍCLICOS Y HETEROCÍCLICOS
Este grupo de fármacos se denominó así porque su estructura química orgánica contenía 3 anillos. Posteriormente, se fueron incluyendo nuevos agentes con uno, 2, 3 y 4 anillos en sus estructuras. Por ello, se propuso el término heterocíclicos, aunque el término tricíclico se ha consagrado por el uso. Tienen en común que bloquean las bombas de recaptación de serotonina, noradrenalina y, en menor medida, la dopamina.
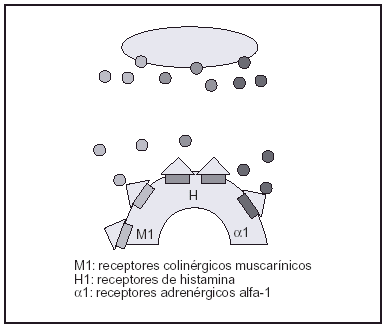
Mientras que el bloqueo de las bombas de recaptación de serotonina y noradrenalina da cuenta de las acciones terapéuticas de los antidepresivos tricíclicos, estos fármacos tienen otras acciones que explican sus efectos secundarios (fig. 1)1:
Figura 1. Acción de bloqueo de los antidepresivos tricíclicos y heterocíclicos sobre los receptores colinérgicos muscarínicos (M1), los receptores de histamina (H1) y los receptores adrenérgicos alfa-1 (α1).
1. Bloqueo de los receptores colinérgicos muscarínicos M1. Produce efectos anticolinérgicos (estreñimiento, visión borrosa, sequedad de boca, retención urinaria, sedación, taquicardia, sudación, así como trastornos de la memoria).
2. Bloqueo de los receptores de histamina H1. Produce somnolencia y aumento de peso.
3. Bloqueo de los receptores adrenérgicos alfa-1. Produce hipotensión ortostática, mareos, somnolencia.
Los antidepresivos tricíclicos bloquean también los canales de sodio en el corazón y en el cerebro, lo que puede provocar arritmias cardíacas y parada cardíaca por sobredosis, además de ataques.
EFECTOS ADVERSOS DE LOS ANTIDEPRESIVOS TRICÍCLICOS
Se han descrito diversos tipos2-6:
Efectos psíquicos
Astenia. Sobre todo con los antidepresivos de tipo sedativo.
Reactivación o descompensación delirante. En pacientes con psicosis crónicas, los antidepresivos tricíclicos pueden "reactivar cuadros de tipo psicótico" (efecto inespecífico activador).
Riesgo suicida. Presente, sobre todo, en las 2 primeras semanas del tratamiento. Puede producirse por una reactivación ansiosa u por una disminución rápida de la inhibición psicomotriz depresiva.
Efecto "inversor del humor" en pacientes bipolares (por alteraciones de la sensibilidad de los receptores).
Ansiedad. Sobre todo, por los antidepresivos más estimulantes (imipramina, desimipramina), al comienzo del tratamiento.
Efectos adversos de tipo central
Trastornos confusionales, relacionados principalmente con la acción anticolinérgica central, sobre todo en personas de mas de 50 años o con insuficiencia renal o hepática. Las alteraciones de la conciencia pueden acompañarse de ansiedad, agitación, e incluso con trastornos alucinatorios u oníricos. Una serie de factores pueden favorecerlos: productos fuertemente atropínicos, interacción con otros fármacos sedativos y/o anticolinérgicos, así como sustancias que lentifican el metabolismo de los antidepresivos.
Trastornos de la vigilancia (somnolencia diurna o insomnio).
Temblor, sobre todo en antidepresivos con actividad anticolinérgica. Consiste en un temblor fino de las extremidades, emocionalmente sensible y de intensidad variable. Es más frecuente
en personas mayores. Ocasionalmente, aparecen fasciculaciones, parestesias e incoordinación.
Disminución del umbral convulsionante. Sobre todo, con dosis muy elevadas de antidepresivos y en sujetos con antecedentes de alcoholismo, afección orgánica cerebral, abuso y abstinencia de benzodiazepinas.
Discinesias y síndromes extrapiramidales, con fuertes posologías y en personas de edad avanzada.
Disminución de las capacidades intelectuales, en sujetos de edad avanzada, con antidepresivos de tipo sedativo y efectos anticolinérgicos, a dosis altas.
Otros: disartria, nistagmo, hiper o hiporreflexia, alucinaciones o ilusiones visuales, y un cuadro de agitación psicomotriz paradójica, con insomnio, ansiedad y ligera confusión.
Efectos adversos de tipo periférico
Cardiovasculares
Los pacientes deprimidos pueden presentar fluctuaciones en la frecuencia cardíaca y la presión arterial, como resultado de disfunciones del sistema nervioso autónomo, que implican los sistemas simpático y parasimpático. Estas disfunciones cardiovasculares pueden agravarse aún más, según el perfil farmacológico del fármaco utilizado, sobre todo por los antidepresivos de acción alfaadrenolítica y anticolinérgica10.
Puede observarse:
Hipotensión ortostática, que puede acompañarse de sensación vertiginosa y raramente de pérdida de conciencia.
Crisis hipertensivas en tratamientos con IMAO no reversibles.
Síntomas cardiovasculares, la mayoría de los cuales son reversibles a corto plazo o inciden en pacientes con cardiopatía previa (riesgo de arritmias, bloqueos, taquicardia sinusal cardiomiopatía o agravamiento de insuficiencia cardíaca precia). Las alteraciones en el electrocardiograma (ECG) son: aplanamiento de la onda T, depresión del segmento ST, ensanchamiento del QRS, ondas U prominentes y retraso en la velocidad de conducción).
Digestivos
Sequedad de boca (con sabor agrio o metálico) y a veces infecciones bucales derivadas, sobre todo con los antidepresivos anticolinérgicos.
Estreñimiento, con disminución de la motilidad intestinal (puede llegar al íleo paralítico), con antidepresivos anticolinérgicos.
Toxicidad hepática, sobre todo con los IMAO, aunque también se han descrito con la imipramina, la amitriptilina y la amineptina.
Aumento de peso.
Genitourinarios
Disuria y retención urinaria, con o sin polaquiuria, y agravación de síndrome prostático en ancianos (infecciones urinarias recidivantes). Se observa, sobre todo, con los antidepresivos anticolinérgicos.
Disfunciones sexuales: retraso o inhibición de la eyaculación, disminución de la libido y retraso en el orgasmo y anorgasmia femenina.
Oculares
Debidos a la acción midriásica y ciciopléjica (visión borrosa, dificultad para la lectura). Deben controlarse los pacientes con glaucoma, especialmente los de ángulo cerrado.
Otros efectos adversos
De difícil catalogación y etiopatogenia incierta.
Amenorrea.
Hipersensibilidad alérgica (exantema, fotosensibilización, ictericia colostática...).
Alteraciones hematopoyéticas (leucocitosis/leucopenia, eosinofilia, agranulocitosis, anemia aplásica, púrpura trombocitopénica).
Prurito, urticaria, eritema.
Hipoglucemia.
Ginecomastia y galactorrea.
Alteraciones de la secreción de la hormona antidiurética.
Tolerancia y dependencia. Se ha descrito tolerancia en imipramínicos con efectos anticolinérgicos y dependencia con síntomas de abstinencia, en especial molestias gastrointestinales y somnolencia. Se sugiere que estos síntomas, o al menos parte de ellos, pueden deberse a un rebote colinérgico. Se recomienda controlar estrictamente a los pacientes durante el período de discontinuación11.
INHIBIDORES SELECTIVOS DE LA RECAPTACIÓN DE SEROTONINA
Son una clase de fármacos con 5 miembros prominentes: fluoxetina, sertralina, paroxetina, fluvoxamina y citalopram. Aunque cada uno de ellos pertenece a una familia químicamente distinta, todos tienen en común una potente y selectiva inhibición de la recaptación de serotonina, más fuerte que sus acciones sobre la recaptación de noradrenalina, receptores alfa-1, histamínicos H1 o colinérgicos muscarínicos.
Los ISRS producen sus acciones aumentando la serotonina en las sinapsis, donde se bloquea la recaptación y se desinhibe la liberación de serotonina. En síntesis, los ISRS ejercen sus acciones terapéuticas por un mecanismo farmacológico en cascada por el que se produce una potente desinhibición de la liberación de serotonina en las vías clave de todo el cerebro. Por otra parte, los efectos secundarios se deben, hipotéticamente, a las acciones agudas de la serotonina en receptores no deseables situados en vías no deseables. Estos efectos secundarios pueden atenuarse a la larga, debido a la desinhibición de los propios receptores que median estos efectos.
Los ISRS carecen de efectos secundarios anticolinérgicos, aunque pueden presentar secundarismos debido a su potente acción serotoninérgica. El síndrome de irritación serotoninérgica es la complicación más grave, y está caracterizado por:
Alteraciones digestivas
Náuseas, a veces con vómitos.
Diarreas, espasmos intestinales.
Estimulación del SNC
Incremento de la ansiedad, la inquietud motora y la irritabilidad.
Cefaleas.
Insomnio y mioclonías nocturnas.
Los ISRS no potencian los efectos del alcohol, los sedantes, los anticolinérgicos o los antihistamínicos. Se ha descrito una interacción negativa entre fluoxetina y litio (puede desarrollar manía y neurotoxicidad). El cuadro más grave se produce por la interacción de los ISRS con IMAO, y produce un grave síndrome confusional.
La discontinuación del tratamiento con ISRS puede provocar reacciones de abstinencia, como vértigos, parestesias, temblor, ansiedad y náuseas. Estos síntomas son más frecuentes con paroxetina y muy raras con fluoxetina. También se ha descrito, con la discontinuación de un tratamiento con fluvoxamina, un síndrome de abstinencia caracterizado por vértigos, cefaleas, náuseas, confusión y debilidad. El síndrome se atribuye a la vida media relativamente corta de la fluvoxamina y a su gran especificidad como inhibidor de la recaptación de serotonina. Aunque en conjunto no puede concluirse que exista un auténtico síndrome de abstinencia de los ISRS13,14.
Los diferentes estudios comparativos entre los ISRS y los antidepresivos tricíclicos, considerados como patrón, muestran un mejor perfil de efectos secundarios y una mejor tolerancia general.
Fluoxetina
El clorhidrato de fluoxetina ha sido uno de los ISRS más utilizado, y su peculiaridad resiste en la prolongada vida media de su metabolito activo (norfluoxetina) que puede llegar a 3 días.
Las náuseas y, en menor medida, los vómitos son los efectos más molestos (el 3,7% de los pacientes abandonan el tratamiento).
La anorexia y el adelgazamiento también aparecen con mayor frecuencia que en el placebo.
El efecto adverso potencialmente grave registrado más a menudo ha sido el exantema cutáneo, que aparece en las primeras semanas y se resuelve espontáneamente en una semana.
En comparación con los tricíclicos, la fluoxetina presenta menos efectos secundarios14-16. La evidencia sugiere que podría causar significativamente menos efectos colaterales anticolinérgicos, antihistaminérgicos y cardiotóxicos que los antidepresivos tricíclicos. No se ha comunicado que el tratamiento crónico con fluoxetina afecte al ECG. En pacientes con sobredosis se han comunicado muy pocos casos de afección cardíaca en comparación con los producidos por los antidepresivos tricíclicos. Los pacientes con enfermedad cardiovascular estable preexistente no experimentaron cambios en la presión arterial. Los datos demuestran una incidencia muy baja de hipertensión en la terapia a corto plazo con fluoxetina.
Paroxetina
Es el más potente inhibidor de la recaptación de serotonina. Su perfil de tolerancia también es mejor que el de los antidepresivos tricíclicos17,18. Los efectos secundarios más frecuentes parecen ser las náuseas y las alteraciones de la eyaculación. Otros síntomas han sido cefaleas, insomnio, inquietud, temblor. Efectos de tipo anticolinérgico, como sequedad de boca, estreñimiento, sudoración y visión borrosa, aparecen con menor frecuencia que en los antidepresivos tricíclicos. No se han registrado alteraciones de la función cardíaca, renal o hepática. Tampoco alteraciones metabólicas ni hematológicas. Asimismo, no produce alteración en el rendimiento psicomotor y en la conducción. Por otro lado, reduce el tiempo total del sueño REM, aumenta el sueño de ondas lentas y acorta el tiempo hasta su aparición19.
Fluvoxamina
Es un potente ISRS. Sus efectos secundarios más frecuentes son los gastrointestinales, como las náuseas, que pueden acompañarse de vómitos, la anorexia y el estreñimiento. También se han descrito somnolencia, agitación, astenia, disfunción sexual y cefalea. Ocasionalmente se han descrito ligeros descensos del recuento plaquetario, así como ligeros aumentos de la creatinina sérica y de la prolactina sérica. Se han detectado algunos casos con efectos secundarios extrapiramidales20-29. No causa alteraciones cardiovasculares, de los rendimientos psicomotores y conducción.
Sertralina
Presenta una potencia de inhibición de la recaptación de la serotonina muy próxima a la de la paroxetina, y superior a la de la fluoxetina y la fluvoxamina. Además, presenta una mayor capacidad inhibitoria sobre la recaptación de la dopamina (agonista dopaminérgico indirecto).
La incidencia de efectos secundarios es dependiente de la dosis, y entre elos destacan las náuseas y la diarrea. También se han descrito boca secua y alteraciones de la eyaculación30, síntomas que parecen atenuarse con el tratamiento. Frente a los antidepresivos tricíclicos presenta una menor incidencia de efectos anticolinérgicos31. Con respecto a otros ISRS, la sertralina presenta un perfil similar, y entre los efectos secundarios destaca la irritabilidad, la somnolencia, la anorexia y la cefalea32. También se han descrito efectos extrapiramidales, presumiblemente por interacción de las vías dopaminérgicas y serotoninérgicas, en algún caso aislado33. No tiene efectos cardiovasculares y presenta un bajo potencial de interacción con otros fármacos.
Citalopram
Es el ISRS de más reciente aparición (1989) y está considerado como el de acción más selectiva sobre la recaptación de serotonina. En ensayos controlados con placebo, las náuseas, la xerostomía, la somnolencia, la sudación, el temblor, la diarrea y los trastornos de la eyaculación han sido los efectos adversos más frecuentes (intensidad de leve a moderada). Menos frecuentes han sido el insomnio, la sedación, el temblor y el estreñimiento34,35.
En estudios comparativos, el perfil de tolerancia del citalopram fue similar al de otros ISRS y algo mejor que el de los antidepresivos tricíclicos; además, interactúa poco con otros fármacos36-38. La monitorización específica de efectos adversos ha revelado un potencial convulsionante bajo y pocos efectos extrapiramidales. No existe evidencia de fenómeno de retirada tras la discontinuación brusca del tratamiento, sin que hayan aparecido efectos cardíacos clínicamente relevantes o alteraciones en los parámetros bioquímicos, y se ha observado poco o ningún efecto sobre la función locomotora. Cuando se administra en sobredosis aislada parece tener un amplio margen de seguridad. Por otro lado, el citalopram tiene buena tolerancia a largo y corto plazo, y su perfil observado en los ensayos se observa también en la clínica.
En los estudios comparativos a corto plazo de los ISRS no se encuentran diferencias en la eficacia entre los compuestos individuales, aunque sí un inicio de acción más lento de la fluoxetina. En función de los resultados obtenidos y teniendo en cuenta los puntos fuertes y débiles de los métodos empleados para comparar los fármacos39 se ha observado que:
El citalopram debe evitarse en pacientes con tendencia a las sobredosis.
La fluoxetina puede no ser el fármaco de elección en pacientes en que se requieren efectos antidepresivos rápidos o que están agitados, pero tiene la ventaja sobre los demás de que es adecuado para personas con mala adherencia al tratamiento y con problemas tras el cese de fármacos.
La fluvoxamina y la paroxetina no deben ser de primera elección en pacientes con tendencia las reacciones adversas por ISRS.
Deben tenerse en cuenta el citalopram y la sertralina si se temen reacciones por interacción de fármacos, dado su teórico menor riesgo.
ANTIDEPRESIVOS RECIENTES
Recientemente se han sintetizado diferentes grupos de antidepresivos, que persiguen combinar una mayor eficacia con una mejor tolerancia40. En este sentido, el perfil de efectos secundarios es un factor que, ante una eficacia comparable, es determinante. Sin embargo, son escasos los estudios en que se comparen estos efectos colaterales, y los que hay adolecen de imprecisiones y fallos metodológicos41,42.
Mirtazapina
Es un agente noradrenérgico y serotoninérgico específico (NaSSA). Facilita la liberación de Nad y 5HT. No provoca prácticamente ninguna reacción adversa anticolinérgica, adrenolítica ni serotoninérgica, por su perfil farmacológico característico43,44.
Su perfil de efectos secundarios e interacciones es bastante reducido. Se han descrito: hipotensión, taquicardia, somnolencia, sedación, cefalea, agitación, inquietud, náuseas, dispepsia y estreñimiento.
En estudios comparativos con ISRS, se mostró un perfil de tolerancia comparable, salvo por los cambios en el peso corporal que fueron estadísticamente más pronunciados en el grupo con la mirtazapina45.
Nefazodona
Antagonista de los receptores 5HT2, junto a la inhibición de la recaptación de 5HT (AIRS). Por ello, tiene una menor incidencia de efectos secundarios que los ISRS (no interfiere la función sexual ni efectos serotoninérgicos). La nefazodona tiene un perfil farmacológico muy favorable frente a otros antidepresivos: no provoca activación psíquica, alteración sexual, cambios de peso o cardiotoxicidad, y sus efectos secundarios son leves y con frecuencia transitorios, lo que permite a los pacientes adaptarse a ellos en las primeras semanas del tratamiento46. Entre los efectos secundarios que se han descrito figuran:
Náuseas, vómitos, diarrea, cefalea, jaqueca.
Bloqueo excesivo 5HT2: somnolencia, astenia, palinopsia.
Pueden registrarse interacciones con los fármacos que actúan sobre la isolenzima P450 IIIA4, pero no sobre los que actúan sobre las isozimas P450 IID6 o IA2. La sobredosis no causa complicaciones graves y no se ha registrado ningún caso de muerte hasta el momento. La seguridad de la nefazodona a largo plazo se ha demostrado en una serie de 250 pacientes tratados durante un año, y en los que no se observaron nuevas experiencias adversas. Cuando existe alteración de la función hepática las dosis deben ser algo menores, al igual que en pacientes de edad avanzada; no es preciso modificar la dosis cuando hay alteración de la función renal.
El perfil adverso observado en pacientes mayores es similar al registrado en menores de 65 años. Los abandonos debidos a experiencias adversas son comparables a los de la fluoxetina y menores que los de la imipramina.
Venlafaxina
La venlafaxina es un antidepresivo, con un perfil farmacológico único. Tiene 2 sitios de acción primarios, inhibiendo la recaptación presináptica de serotonina y noradrenalina (ISRN), pero a diferencia de los tricíclicos no tiene acción sobre receptores y, por ello, sus reacciones adversas son menores que los antidepresivos tricíclicos. Es un fármaco antidepresivos y estimulante de las funciones cognitivas. Su efecto más potente tiene lugar sobre la recaptación de serotonina, y en un tercio de la noradrenalina. Parece que esta inhibición de los sistemas de recaptación de estas 2 aminas cuenta para la actividad farmacológica de la venlafaxina en los modelos neurofisiólogicos y de comportamiento sensibles a los antidepresivos, y presumiblemete también para su actividad clínica antidepresiva. La venlafaxina carece de afinidad por los neurorreceptores adrenérgicos, colinérgicos o histaminérgicos, lo que permitiría esperar un mejor perfil de tolerancia que el de los antidepresivos tricíclicos. Las ventajas clínicas predecibles a partir del mecanismo de acción de la venlafaxina incluyen una curva de dosis-respuesta positiva y un inicio de acción rápido47. Es un fármaco bien tolerado, con menores efectos anticolinérgicos; sus efectos secundarios son dependientes de la dosis:
Dosis bajas (los mismos que ISRS): por estimulación de los receptores 5HT2 y 5HT3 (náuseas, insomnio, ansiedad, disfunción sexual...).
Dosis medias (se añaden los de los sistemas Nad y Do): hipertensión, insomnio grave, agitación, vómitos, cefaleas... La interrupción brusca puede determinar síntomas de abstinencia (mareos, náuseas, sudoración...).
En estudios comparativos, los perfiles de seguridad y de tolerabilidad de la venlafaxina48 fueron similares a los observados anteriormente en ISRS, y aparecieron insomnio, mareos, cefaleas, sequedad de boca, somnolencia, constipación, sudación y náuseas, que se resolvieron rápidamente en la mayoría de los pacientes49,50. La administración de la venlafaxina produjo una menor aparición de efectos secundarios anticolinérgicos que los observados con antidepresivos tricíclicos, por la ausencia de una afinidad significativa de la venlafaxina por los receptores colinérgicos muscarínicos. En un pequeño porcentaje de pacientes se produjeron aumentos moderados, pero significativos, de la presión arterial, similares a los observados en pacientes tratados con imipramina51. En comparación con muchos de los antidepresivos de primera y segunda generación, parece ser relativamente bien tolerado y seguro en casos de sobredosis. Se considera que la venlafaxina podría presentar alguna interacción con el sistema de la citocromo P450, aunque estudios in vitro han demostrado que se trata de una modesta inhibición y, en general, los estudios clínicos han demostrado que posee mínimas interacciones con otros fármacos52. Los resultados de tolerabilidad y seguridad en pacientes ancianos no difirieron significativamente de los observados en pacientes más jóvenes. La venlafaxina es bien tolerada en los ancianos y en aquellos que requieren medicación concomitante. Si bien está contraindicada en el embarazo, la exposición accidental a este fármaco no parece asociarse con un riesgo aumentado de malformaciones fetales.
Roboxetina
La roboxetina es un inhibidor selectivo de la recaptación de noradrenalina. Su eficacia antidepresiva se aproxima al de la imipramina. No obstante, la tolerancia fue mejor con la reboxetina, que indujo menos abandonos del tratamiento por reacciones adversas; el riesgo acumulativo de sequedad de boca, hipotensión y temblores fue significativamente superior con la administración de imipramina53.
CONCLUSIONES
Desde los clásicos antidepresivos tricíclicos y los IMAO, han ido apareciendo nuevas moléculas que persiguen combinar una mayor eficacia antidepresiva, con una mejor tolerancia. Si bien, en el primer aspecto las expectativas no se han cumplido, se ha conseguido una mayor tolerancia, aunque los estudios que en que se comparan estos efectos colaterales son escasos, y algunos adolecen de imprecisiones y fallos metodológicos. No es sencilla la construcción de una tabla resumen simplificada comparativa entre los diferentes grupos de antidepresivos.
Los antidepresivos tricíclicos constituyen el patrón tanto para evaluar la eficacia antidepresiva como para la tolerancia. Los efectos anticolinérgicos de los antidepresivos tricíclicos en dosis terapéuticas pueden causar alteraciones cardiovasculares (hipotensión ortostática, arritmias, alteraciones electrocardiográficas), alteraciones de la motilidad intestinal (estreñimiento, íleo paralítico), retención urinaria, dilatación pupilar, sequedad de boca y temblor. Los efectos anticolinérgicos centrales pueden producir trastornos de memoria, sedación y confusión (sobre todo en sobredosis).
Los IMAO clásicos prácticamente se encuentran fuera del mercado. La moclobemida, como RIMA, es el único de interés, ya que presenta menos efectos secundarios anticolinérgicos que los antidepresivos tricíclicos y no tiene acción excitatoria sobre el SNC.
Los efectos adversos más frecuentes de los ISRS son los gastrointestinales (náuseas, vómitos, diarreas), aunque también pueden producir un cuadro de excitación del SNC (insomnio, ansiedad, intraquilidad, temblor, vértigos, cefaleas); los principales efectos vegetativos son la sequedad de boca y la sudación. Entre los diferentes antidepresivos del grupo, el perfil de efectos secundarios parece más desfavorable para la fluvoxamina y más favorable para el citalopram.
La mirtazapina puede provocar sedación, aumento de peso y, excepcionalmente, se han descrito discrasias sanguíneas, pero en general no presenta efectos secundarios serotoninérgicos, y los anticolinérgicos son menores que los de los antidepresivos tricíclicos.
La nefazodona puede producir efectos adversos, como somnolencia, vértigo, sequedad de boca, náuseas, estreñimiento, cefaleas, hipotensión y ambliopía. Pero en menor intensidad que los ISRS y los antidepresivos tricíclicos.
La venlafaxina puede provocar nerviosismo, insomnio, sudación, náuseas, sequedad de boca, disfunción sexual e hipertensión. Efectos secundarios inferiores a los antidepresivos tricíclicos y similares a los ISRS, con un porcentaje ligeramente mayor de efectos gastrointestinales.