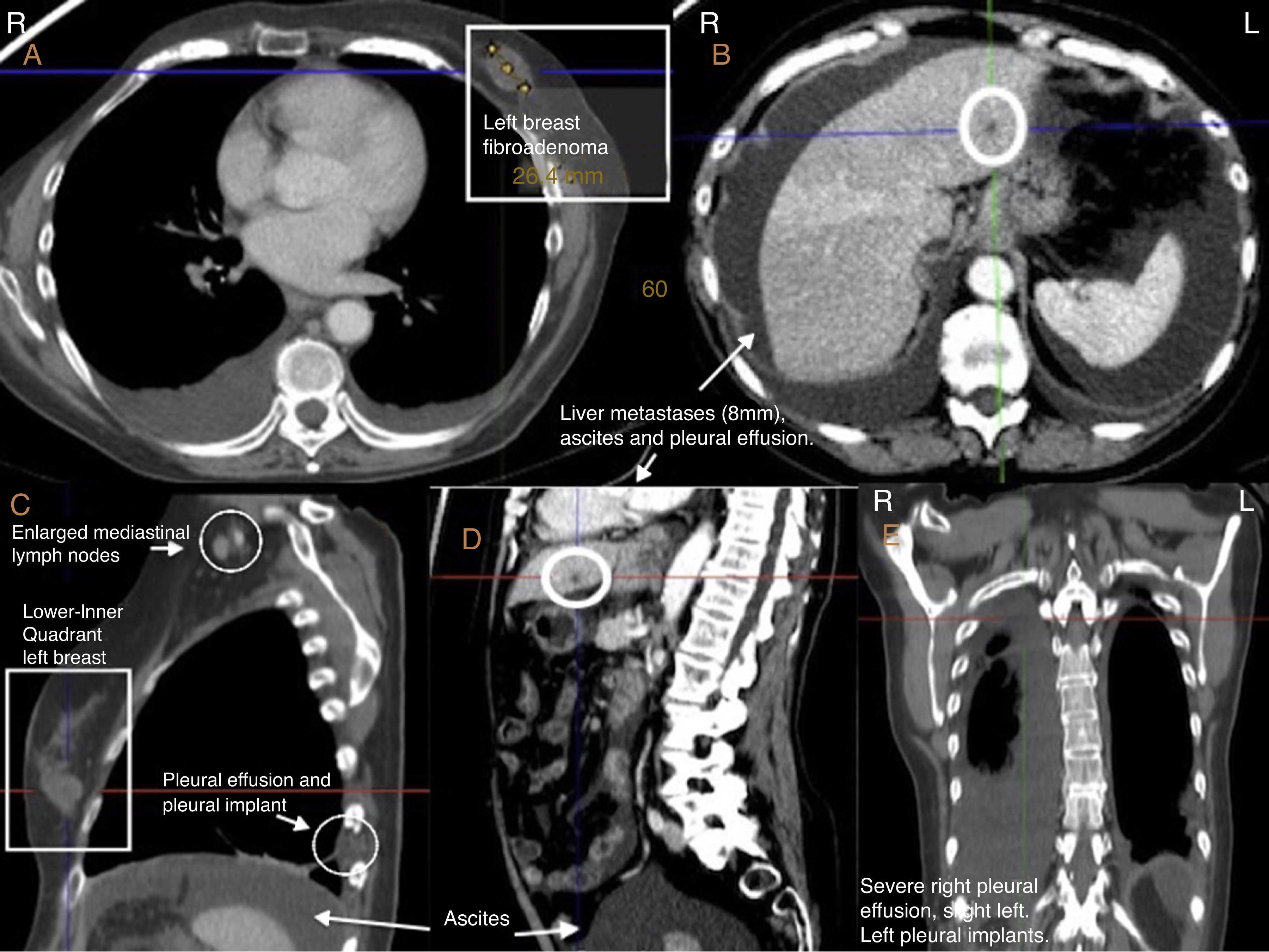
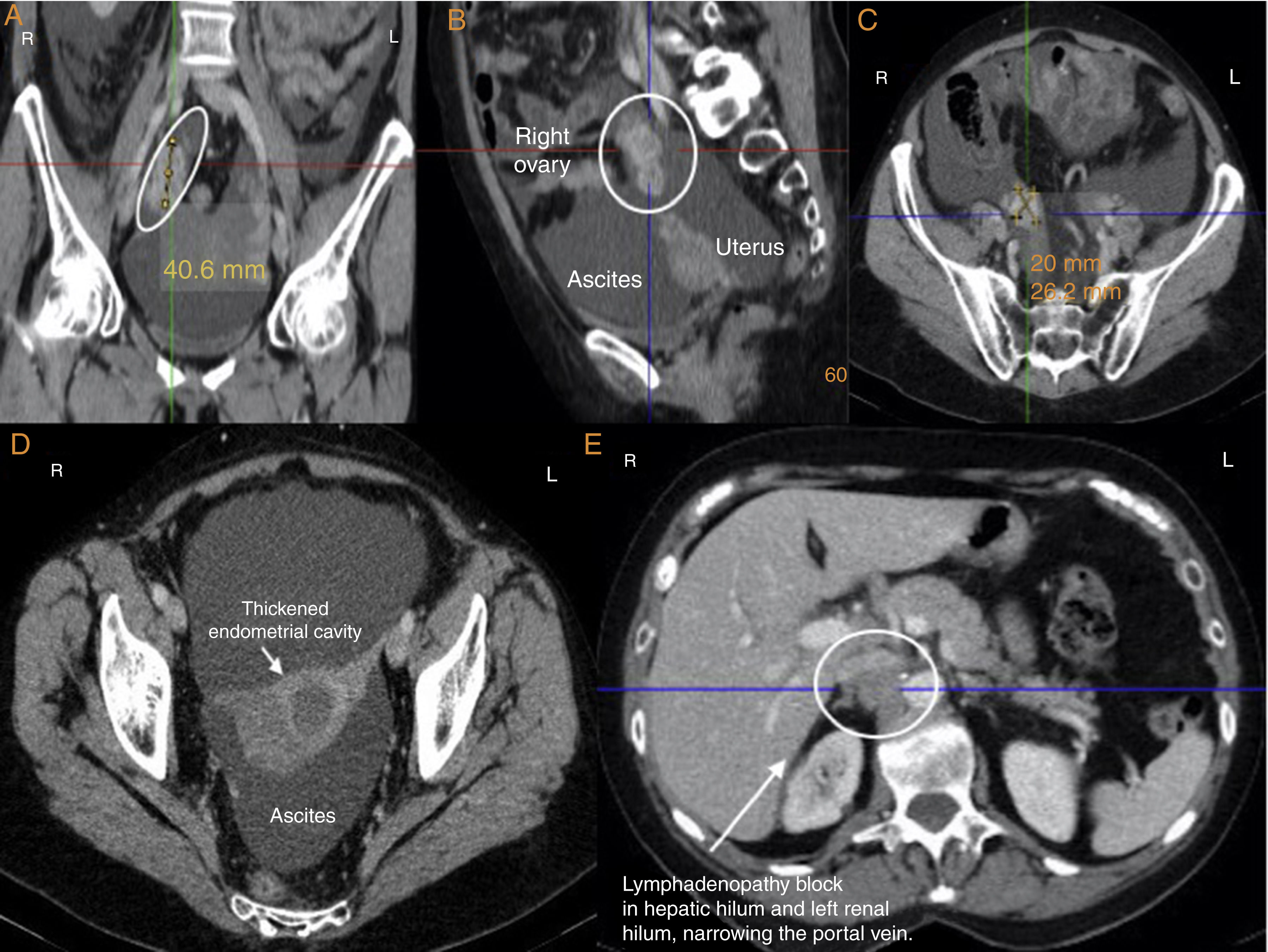
La ascitis quilosa (AQ) o quiloperitoneo es una condición rara (1/20.000 ingresos hospitalarios)1. Se produce por la infiltración, obstrucción o rotura de los vasos linfáticos retroperitoneales con formación de fistulas a la cavidad peritoneal2. Presentamos el caso de una paciente con AQ secundaria a carcinomatosis peritoneal por neoplasia de mama diseminada. Se realizó mastectomía radical y linfadenectomía axilar derechas a los 46 años (año 1997) por carcinoma ductal infiltrante G2 pT2N3M0, posterior poliquimioterapia con antraciclinas (CMF iv 6 ciclos), radioterapia sobre lecho de mastectomía y cadenas ganglionares (50Gy con fraccionamiento convencional) y tamoxifeno 5 años sin incidencias. En diciembre del 2012, recaída ganglionar supra e infradiafragmática tratada con letrozol obteniendo respuesta completa radiológica. En noviembre del 2015, a los 65 años de edad, progresión ganglionar supradiafragmática, micronódulos hepáticos e implantes pleurales. Inicia tratamiento en ensayo clínico con fulvestrant por vía oral, obteniendo respuesta parcial3,4. En control tras 8 semanas de tratamiento, se objetiva progresión de adenopatías supra e infradiafragmáticas, signos de carcinomatosis peritoneal, implantes en ovario derecho, crecimiento de nódulos hepáticos, derrame pleural bilateral y moderada ascitis (figs. 1 y 2). Los marcadores tumorales, hasta ahora negativos, se encontraban elevados (CA125 1051, CEA 8,4, CA15,3 65,3). Dado el deterioro clínico y la distensión abdominal, se decide ingreso para conducta diagnóstico-terapéutica. Se realiza paracentesis evacuadora, obteniendo líquido compatible con linfa, negativo para células tumorales; se deja catéter pig-tail para drenaje intermitente. Es valorada por nutrición ante un estado de desnutrición progresiva (a pesar de IMC 25kg/m2), se solicita valoración por la Unidad de Nutrición y Dietética Hospitalaria, iniciando dieta específica baja en grasas, soporte nutricional basado en triglicéridos de cadena media (MCT) y batidos hiperproteico-calóricos sin lípidos. A pesar de ello, la paciente sigue manteniendo volúmenes altos (2-3 l/día) de drenaje linfático. Se instaura soporte nutricional parenteral con disminución del débito drenado y mejoría clínica. Dada la alta probabilidad de enfermedad abdominal diseminada por cáncer de mama y ante la fragilidad de la paciente, se desaconseja la realización de laparoscopia diagnóstica con toma de biopsia. Inicia taxol semanal iv 80mg/m2. Reintroducción progresiva de nutrición enteral bien tolerada, alta médica con medidas dietéticas y soporte nutricional, aceite MCT y batidos proteicos. Actualmente, la enfermedad está controlada tras 12 ciclos.
La mayoría de AQ son de aparición precoz tras un procedimiento quirúrgico retroperitoneal, en el contexto de un cáncer ginecológico; con una incidencia del 9% en la primera semana tras la cirugía y asociada al número de ganglios para-aórticos resecado (> 14)2. En un 10% la AQ es secundaria a neoplasias avanzadas, cáncer ginecológico, linfomas y adenocarcinomas de origen digestivo o renal5,6. Otras causas no malignas son traumatismos abdominales, cirugía vascular reciente, cambios posradioterapia, cirrosis, tuberculosis abdominal o filariasis7.
La linfa está compuesta por agua, ácidos grasos de cadena larga, linfocitos, minerales y proteínas. Su acumulación no produce síntomas, salvo progresiva distensión abdominal y desnutrición. Su composición genera inflamación e irritación en la cavidad abdominal con el desarrollo de cuadros adherenciales, sintomatología digestiva inespecífica (náuseas, vómitos, dolor abdominal) y un mayor riesgo de peritonitis. El análisis bioquímico del líquido ascítico confirmará la sospecha: quilomicrones y triglicéridos elevados (> 330mg/dl o 3 veces superior al nivel plasmático)5.
Su abordaje es complejo debido al mal estado nutricional e inmunológico derivado de la pérdida de proteínas y linfocitos en la linfa8. El tratamiento de elección es el manejo conservador nutricional junto con drenaje percutáneo de baja presión9. La paracentesis evacuadora intermitente es poco efectiva más allá de la utilidad diagnóstica. El manejo conservador inicial incluye dieta hipercalórica-hiperproteica e hiposódica baja en grasas con soporte de triglicéridos de cadena media6.
La introducción de diuréticos (furosemida, espironolactona), análogos de la somatostatina (octreótido 100mg/ml, una ampolla subcutánea/8 h hasta la resolución) y alimentación parenteral se reserva en casos refractarios o de alto débito9. Más de 2/3 de los casos se resuelven con medidas conservadoras en las primeras 2 semanas10. Para Han et al.11 todos los casos se resolvieron con medidas conservadoras y drenaje peritoneal en una media de 2 semanas, sin ninguna recurrencia. En casos graves puede ser necesario el manejo quirúrgico, mediante embolización percutánea transabdominal de la cisterna magna, ligadura de vasos linfáticos o shunts peritoneovenosos, con poca experiencia al respecto y no exentos de morbilidad7,10. Según Tulunay et al.12, el 71% respondió al manejo conservador y el 29% restante requirió de corrección quirúrgica.
En conclusión, la infiltración tumoral de los conductos linfáticos principales, en el contexto de una carcinomatosis peritoneal es la primera causa de AQ no quirúrgica. El manejo conservador, mediante drenaje continuo o intermitente de baja presión y soporte nutricional, ha de considerarse una primera elección suficientemente efectiva.
Responsabilidades éticasConfidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
A los servicios de Oncología Médica y Nutrición (Dra. Pelegrina Cortés) del Hospital Universitario La Paz, por su dedicación y esfuerzo con la paciente.