Investigar la seguridad de la reintroducción de lamotrigina después de un episodio de rash inicial en pacientes con trastorno bipolar
MétodoEstudio prospectivo de casos abiertos de pacientes que desarrollaron rash inicial al ser tratados con lamotrigina y que fueron refractarios a otros tratamientos, a los cuales se les ofreció reintroducción de lamotrigina usando distintas estrategias de escaladas de dosis. Además, se efectuó una revisión de reportes previos de estrategias de manejo de rash y reintroducción de lamotrigina
ResultadosDe 10 pacientes retratados con lamotrigina 3 requirieron discontinuación de la droga debido a rash persistente. Uno de estos fue potencialmente serio y se resolvió con la discontinuación de lamotrigina. La revisión de la literatura identificó varios estudios de retratamiento con lamotrigina con tasas variables de resultados satisfactorios, entre 70 y 87% según los estudios. Ningún paciente desarrolló síndrome de Stevens-Johnson o necrólisis epidérmica tóxica después de la reintroducción. La tasa de rash fue elevada cuando el retratamiento comenzó dentro de las 4 semanas del rash inicial (19 vs 7%, p=0,001) y se redujo cuando el rash inicial no tuvo signos de seriedad potencial (0 v.19%, p=0,01)
ConclusionesRetratamiento es una opción viable después de rash benigno por lamotrigina y se puede retratar con más precauciones después del rash con uno o 2 signos de seriedad potencial. Para los casos de rash con mas signos de gravedad no hay datos fiables sobre al seguridad del retratamiento y puede conllevar un riesgo significativo. En estos casos el retratamiento debería evitarse dentro de las 4 semanas del rash inicial.
To determine the safety of lamotrigine rechallenge after a first episode of skin rash in bipolar patients.
MethodAn open cases prospective study was conducted with patients who, developed a skin rash when first treated with lamotrigine, were refractory to other treatments, and were offered lamotrigine rechallenge using a different dose titration. Additionally a review was performed on previous skin rash management strategies and lamotrigine rechallenge reports.
ResultsEvery 3 out of 10 lamotrigine rechallenge patients required drug interruption due to persistent rash. One of them was potentially serious and resolved by stopping the lamotrigine. The review of available literature identified several lamotrigine rechallenge studies with rates of positive results varying between 70% and 87% depending on the study. No patient developed Stevens-Johnson syndrome or toxic epidermal necrolysis after rechallenge. The rate of rash was higher when rechallenge began between 4 weeks from initial rash (19% vs. 7%, P=.001) and decreased when first rash showed no potentially serious signs (0% vs.19%, P=.01).
ConclusionsRechallenge is a viable option after a benign lamotrigine-induced rash, and can even be rechallenged after rash with greater precautions when there exists one or two potentially serious signs. In cases of more serious rash there are no reliable data available on rechallenge safety and it may pose a significant risk. In those cases rechallenge should better be avoided between 4 weeks from first rash.
Lamotrigina representa una opción validada en el tratamiento del trastorno bipolar1. Los pacientes con trastorno bipolar pasan cerca del 40% de su vida en fase depresiva y los efectos más importantes de lamotrigina se verifican en la prevención de la depresión bipolar2. Otras ventajas de lamotrigina incluyen su buena tolerancia, perfil cognitivo favorable y adhesión del paciente3. Este perfil es particularmente útil en el paciente bipolar dada su baja tasa de adherencia al tratamiento4. Sin embargo, su uso ha estado limitado por el riesgo de reacciones dermatológicas potencialmente serias, principalmente síndrome de Stevens-Johnson y necrólisis epidérmica tóxica5. Los factores de riesgo conocidos para este tipo de reacciones incluyen el aumento rápido de la dosis, uso concurrente de ácido valproico, historia previa de rash asociado a anticonvulsivantes, género femenino, edad menor de 13 años6,7. Desde la introducción de la normativa acerca de un aumento gradual de dosis, la tasa de reacciones severas cutáneas con lamotrigina ha ido disminuyendo de 1 a 0,1–0,01%8. Sin embargo, la tasa de reacciones cutáneas benignas no ha cambiado permaneciendo entre 8 y 11%9. La aparición de un rash benigno implica un dilema para el clínico que dispone de pocas alternativas terapéuticas eficaces para la depresión bipolar. Para evitar esta reacción adversa se han identificado una serie de precauciones para los pacientes que inician su tratamiento con lamotrigina10 sin que hayan sido capaces de reducir la tasa de aparición como se desprende de un reciente estudio randomizado11. Una estrategia usada habitualmente ante la aparición de un rash es recomenzar el tratamiento con lamotrigina usando una titulación de la dosis más lenta, comenzando habitualmente con 5mg/día, cuando su uso está justificado clínicamente, sin embargo, no se cuenta con estudios a gran escala que hayan identificado marcadores precisos y fiables que permitan predecir con antelación el fracaso o éxito de esta estrategia. En la presente investigación se detallan algunos marcadores que predicen eventos adversos durante la reinstalación del tratamiento con lamotrigina luego de la aparición de rash a través de un estudio de casos abiertos y una revisión de la literatura existente.
MétodoSerie de casosDespués de un período de washout de 5 vidas medias de cualquier medicación psicotrópica previa consumida por el participante, se trataron con lamotrigina para evaluar su eficacia y tolerabilidad para el tratamiento del trastorno bipolar i y ii. Los participantes tenían edades comprendidas entre 18 y 57 años y cumplían con los criterios del DSM-IV para trastorno bipolar i y ii y estaban en fase depresiva o mixta de su trastorno. El trastorno fue confirmado mediante la entrevista clínica del DSM-IV. Los pacientes tenían un valor ≥ 20 en la escala de depresión de Hamilton de 17 ítems12 y un valor ≤ 12 en la escala de manía de Young13. Los criterios de exclusión fueron tener otro diagnóstico del eje i, episodio depresivo actual mayor de 12 meses de duración, trastorno por uso o dependencia de sustancias (DSM-IV) (excepto nicotina) u otra enfermedad médica clínicamente significativa. El estudio fue aprobado por el comité local de ética y conducido de acuerdo a las normas de buenas prácticas clínicas. Se obtuvo consentimiento informado de cada sujeto antes de su inclusión en el estudio.
No se permitió la ingesta de benzodiacepinas durante el período de washout. Se identificaron de manera prospectiva los pacientes con trastorno bipolar que desarrollaron un rash dentro de los 4 meses luego del inicio de tratamiento con lamotrigina durante el año 2010 en un servicio de psiquiatría de pacientes ambulatorios. Para evaluar la intensidad del rash se utilizó una escala de 5 puntos basada en la intensidad y la localización de la erupción (tabla 1)14.
Clasificación de las lesiones eruptivas
| Grado | Características clínicas rash/erupción |
| Grado 1 | Erupción macular o papular o eritema sin síntomas asociados |
| Grado 2 | Erupción macular o papular o eritema con prurito u otros síntomas asociados. Descamación localizada u otras lesiones que cubren < 50% del área de superficie corporal (ASC) |
| Grado 3 | Eritroderma generalizada o erupción macular o papular o vesicular Descamación cubre ≥ 50% ASC |
| Grado 4 | Dermatitis generalizada exfoliativa, ulcerativa o bullosa |
| Grado 5 | Síndrome de Stevens-Johnson grave con riesgo de vida |
En la figura 1 se observan algunos ejemplos de las lesiones eruptivas de acuerdo a su gravedad. En cada caso se contrastó la severidad de la erupción con el beneficio potencial de lamotrigina y se obtuvo el consentimiento informado para cada uno de los pacientes que se consideraron apropiados para reinstituir lamotrigina, excepto en aquellos casos de lesiones grado 3 a 5 debido a la posibilidad de evolución a síndrome de Stevens-Johnson o necrólisis epidérmica. En caso de lesiones benignas (grado 1), se intentó mejorar el rash reduciendo la dosis de lamotrigina, y en caso de que no hubiera mejoría se suspendió la droga y se sugirió la posibilidad de reinstalar el tratamiento posteriormente. Se dejaron pasar 2 semanas como mínimo después de la mejoría del rash antes de intentar la reinstalación del tratamiento. Este se inició con una dosis de lamotrigina de 5mg diarios, o 5mg día por medio para los pacientes con tratamiento concomitante con ácido valproico. La dosis diaria se incrementó 5mg cada 2 semanas hasta alcanzar una dosis de 25mg/día momento en el cual se continuó la titulación de acuerdo con las instrucciones del fabricante15. Un paciente no siguió el esquema de reinstalación del tratamiento correctamente (titulando más rápidamente de lo indicado); sin embargo se incluyó en el análisis. Para el análisis de la mejoría con lamotrigina se empleó la Clinical Global Impression - Improvement scale (CGI-I)16.
Revisión de literatura sobre investigaciones o ensayos de retratamiento con lamotriginaSe realizó una búsqueda por Medline usando palabras claves «lamotrigina» y «rash» (número=240). Se revisaron los abstracts para identificar aquellos donde la lamotrigina se reinstauró después de un episodio de rash titulando más lentamente que el esquema inicial (número=8); además se revisaron las referencias de los estudios indicados (número=4). Se evaluaron los datos extraídos de las publicaciones mencionadas y se clasificaron las erupciones de acuerdo con la escala de la tabla 1. Los datos obtenidos de la revisión de la literatura se combinaron con la serie de casos actual para formar un metaanálisis. Se llevó a cabo un análisis post-hoc para evaluar si el riesgo de rash durante la reinstalación del tratamiento con lamotrigina luego de una erupción se asociaba con la severidad de este último o con el tiempo transcurrido entre la erupción inicial y el retratamiento.
ResultadosSerie de casosDe 80 pacientes medicados con lamotrigina para trastorno bipolar i o ii, 15 (18,75%) desarrollaron una erupción cutánea dentro de los 2 meses siguientes, de los cuales fueron retratados con lamotrigina 10. El retratamiento dio resultados adversos en 2 pacientes: uno desarrolló rash severo grado 4, otro desarrolló erupción escamosa grado 3. Ninguno de los pacientes desarrolló síndrome de Stevens-Johnson o necrólisis epidérmica durante el tratamiento inicial o el retratamiento con lamotrigina (tabla 2).
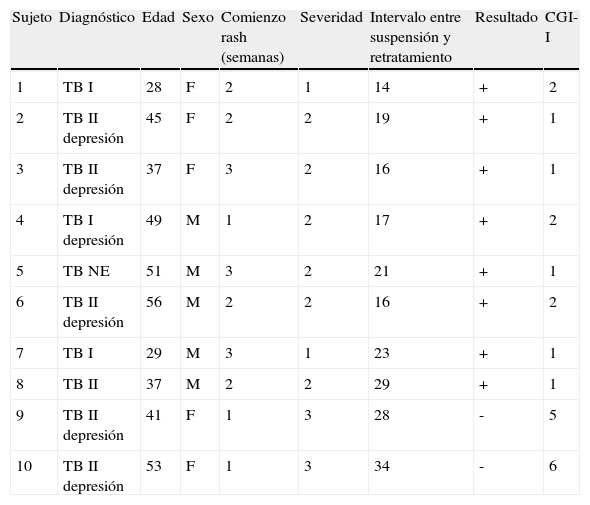
Características de los pacientes retratados con lamotrigina
| Sujeto | Diagnóstico | Edad | Sexo | Comienzo rash (semanas) | Severidad | Intervalo entre suspensión y retratamiento | Resultado | CGI-I |
| 1 | TB I | 28 | F | 2 | 1 | 14 | + | 2 |
| 2 | TB II depresión | 45 | F | 2 | 2 | 19 | + | 1 |
| 3 | TB II depresión | 37 | F | 3 | 2 | 16 | + | 1 |
| 4 | TB I depresión | 49 | M | 1 | 2 | 17 | + | 2 |
| 5 | TB NE | 51 | M | 3 | 2 | 21 | + | 1 |
| 6 | TB II depresión | 56 | M | 2 | 2 | 16 | + | 2 |
| 7 | TB I | 29 | M | 3 | 1 | 23 | + | 1 |
| 8 | TB II | 37 | M | 2 | 2 | 29 | + | 1 |
| 9 | TB II depresión | 41 | F | 1 | 3 | 28 | - | 5 |
| 10 | TB II depresión | 53 | F | 1 | 3 | 34 | - | 6 |
Los 5 pacientes no retratados con lamotrigina resolvieron el rash espontáneamente con la reducción de la dosis de lamotrigina (n=1), fueron cambiados a otra droga (n=2) o rechazaron continuar el tratamiento (n=1). La severidad del rash en los pacientes retratados osciló entre 1 y 2 (media=1,75). Los 2 pacientes retratados con resultados adversos tuvieron severidad de rash de 3 y luego del retratamiento volvieron a presentar lesiones cutáneas potencialmente graves ampollares en dorso y rostro, además de fiebre, esoinofilia y vesículas mucosas en la cavidad bucal, las que remitieron luego de tratamiento con corticoides y suspensión de lamotrigina. El 37,5% de los pacientes refirieron mejoría luego del retratamiento y obtuvieron resultados 1 y 2 (mejoría y mucha mejoría) con relación a la línea basal luego de retratamiento con lamotrigina metaanálisis.
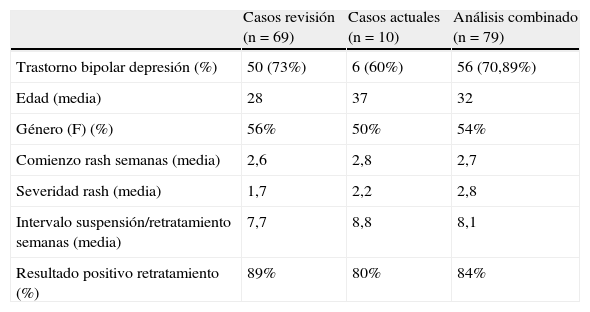
Fueron recuperados 69 casos extraídos de 12 publicaciones en las cuales se llevó a cabo el retratamiento con lamotrigina después de un rash (tabla 3)17–22.
Análisis de casos actuales y de revisión de retratamiento con lamotrigina luego de rash inicial
| Casos revisión (n = 69) | Casos actuales (n = 10) | Análisis combinado (n = 79) | |
| Trastorno bipolar depresión (%) | 50 (73%) | 6 (60%) | 56 (70,89%) |
| Edad (media) | 28 | 37 | 32 |
| Género (F) (%) | 56% | 50% | 54% |
| Comienzo rash semanas (media) | 2,6 | 2,8 | 2,7 |
| Severidad rash (media) | 1,7 | 2,2 | 2,8 |
| Intervalo suspensión/retratamiento semanas (media) | 7,7 | 8,8 | 8,1 |
| Resultado positivo retratamiento (%) | 89% | 80% | 84% |
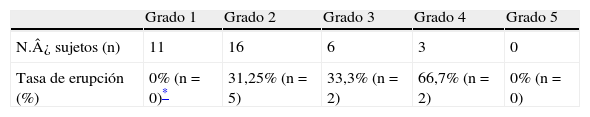
En el 18% de los casos apareció una reacción cutánea durante la reinstauración del tratamiento y resolvió mediante la discontinuación del mismo pero no se reportaron reacciones severas de grado 4 o 5 sugerentes de Síndrome de Stevens-Johnson o necrólisis epidérmica tóxica. La mayoría fueron casos retrospectivos o prospectivos mientras que 4 fueron estudios de caso único19,21,23,24. En 30% de los casos lamotrigina fue reiniciada a una dosis superior a 5mg/día, debido a valores iniciales altos en las dosis de comienzo superiores a 200mg/día en la primera semana. La tasa de resultados positivos en estos casos no difirió de la hallada en los retratamientos con 5mg/día (83 vs 89% respectivamente). El riesgo de rash durante el retratamiento asociado con el intervalo de espera y la severidad del rash inicial se estudiaron con un análisis post-hoc incluyendo los casos adecuados para el análisis publicados anteriormente obtenidos de la revisión (n=26 para severidad, n= 48 para intervalo). La tasa de resultados positivos para el retratamiento después de rash benigno (grado 1) fue del 100%, para rash grado 2 y 3 las tasas de recaída fueron similares (31,25 y 33,3% respectivamente), con rash inicial grado 3 la tasa de recaída fue 66,7% (tabla 4).
Tasa de rash en retratamiento según severidad inicial (análisis combinado)
| Grado 1 | Grado 2 | Grado 3 | Grado 4 | Grado 5 | |
| N.¿ sujetos (n) | 11 | 16 | 6 | 3 | 0 |
| Tasa de erupción (%) | 0% (n = 0)* | 31,25% (n = 5) | 33,3% (n = 2) | 66,7% (n = 2) | 0% (n = 0) |
Los 2 casos actuales que fueron retratados a partir de rash grado 3 no tuvieron evolución favorable, reinstalaron un rash más severo con ampollas en dorso, cara y cavidad bucal y remitieron con la discontinuación del tratamiento.
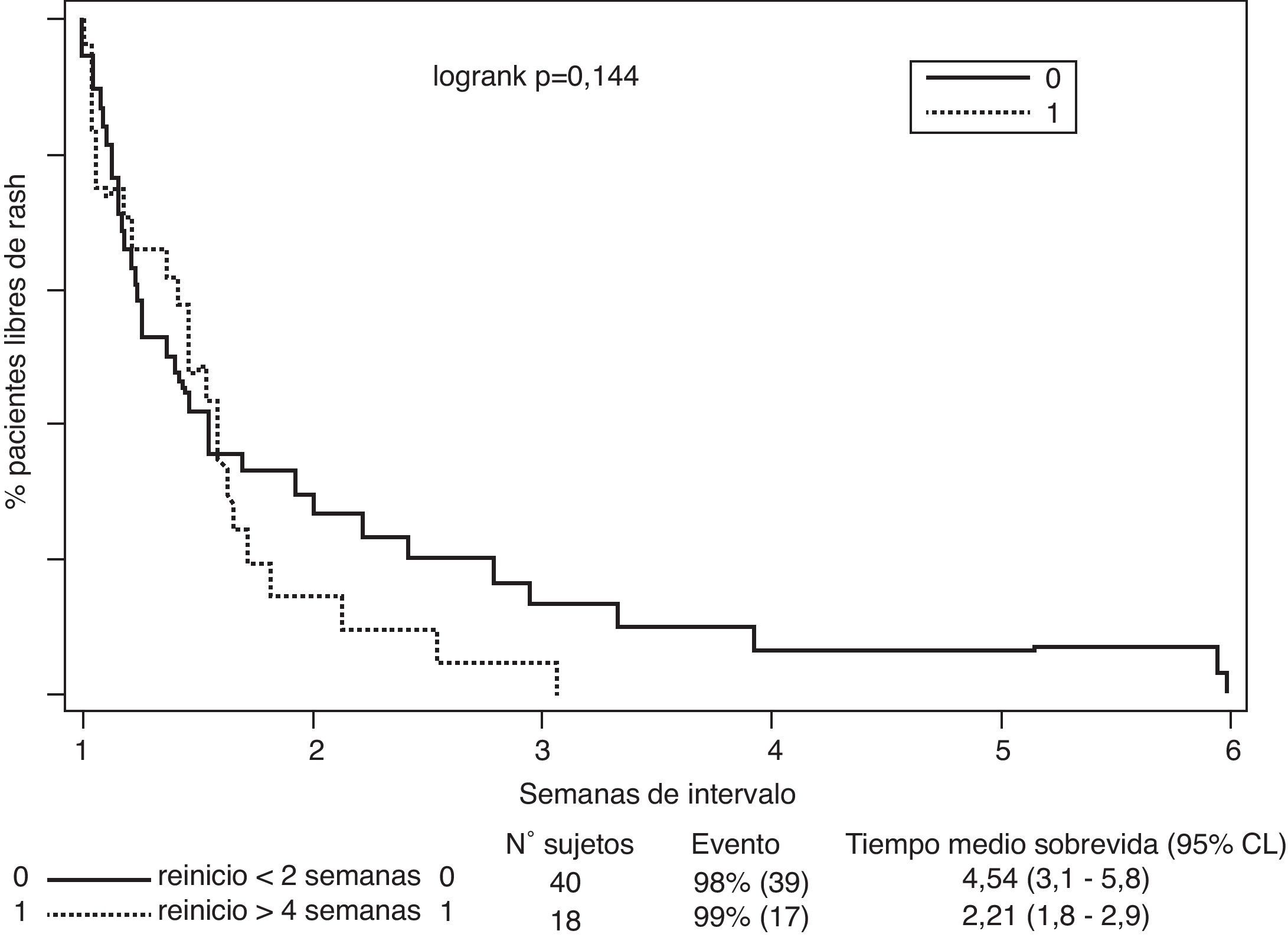
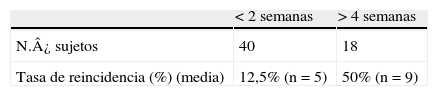
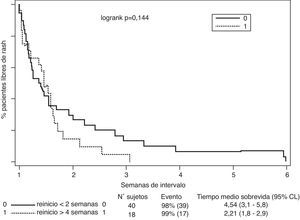
Con respecto a la asociación entre recaída de rash durante el retratamiento e intervalo de tiempo entre terminación de tratamiento inicial y reinstauración del nuevo tratamiento con lamotrigina, los resultados indican que a menor intervalo de tiempo entre terminación de tratamiento y reinstauración del tratamiento con lamotrigina la tasa de recaída es mayor (fig. 2). Este efecto resulta especialmente significativo cuando lamotrigina se reinicia antes de las 2 semanas comparado con el inicio después de las 4 semanas (46% versus 2%, p=0,001) (tabla 5).
DiscusiónLos resultados del presente estudio apoyan la idea de titular el retratamiento con lamotrigina luego de rash con dosis menores. En caso de reacciones cutáneas grado 1 se puede reducir la última dosis en 25 a 50mg, con vigilancia hasta que resuelva el rash, después de lo cual se puede continuar la titulación en dosis ascendentes hasta alcanzar la estabilización clínica. Si el rash no resuelve con la reducción de dosis se puede suspender la lamotrigina y retitular a un paso más lento luego de una espera de 4 a 6 semanas de intervalo sin aparición de reacciones cutáneas. En caso de lesiones cutáneas grado 2 se puede seguir el esquema anterior con mayores precauciones ante la persistencia de la reacción cutánea. Para lesiones superiores a grado 2, como 3 o 4, no se recomienda de rutina el retratamiento con lamotrigina como queda evidenciado en el caso de los 2 pacientes con mala evolución del presente estudio. Análisis post-hoc sugieren que un margen de seguridad de espera de 4 a 6 semanas luego de la mejoría del rash antes de reiniciar el tratamiento con lamotrigina es una opción que ofrece más seguridad con respecto a otros reportes menos conservadores10. En caso de ser necesario la continuación del tratamiento con lamotrigina a pesar de la persistencia del rash, se puede optar por la combinación de lamotrigina con riluzole23 o con valproato19,25. Riluzole y lamotrigina inhiben el glutamato mediante el bloqueo de canales de sodio. Se ha estudiado en depresión resistente y como sustituto de lamotrigina después de rash severo. En tanto que la combinación de lamotrigina con un inhibidor enzimático permite reducir los niveles de la primera mientras se conserva su eficacia terapéutica. Otra alternativa antes de suspender lamotrigina en caso de rash es consultar a un dermatólogo con experiencia en este tipo de erupciones con un intervalo razonable de 48 a 72 horas, pero en caso de que la demora en la interconsulta sea mayor se corre el riesgo de que se agraven las lesiones de rash en cuyo caso puede ser conveniente recurrir a las otras alternativas como reiniciar a una dosis mas baja o suspender la medicación y reiniciar de 2 a 4 semanas más tarde. Con respecto al tratamiento del rash con corticoides, estos pueden agravar el estado depresivo o mixto del trastorno bipolar por lo cual puede resultar conveniente evitarlos en la medida de lo posible26.
Responsabilidades éticasProtección de personas y animales. Los autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.