Introducción: En células de cáncer de mama se encuentran sobreexpresadas las integrinas α(ν)β(3) y/o α(ν)β(5)1-4. Los péptidos marcados con base en la secuencia Arg-Gly-Asp (RGD) han mostrado ser radiofármacos con alta afinidad y selectividad por estas integrinas5,6. El objetivo de este estudio fue establecer un modelo biocinético para el radiofármaco 99mTcEDDA/HYNIC-E-[c(RGDfK)]2 y evaluar su dosimetría en 7 mujeres sanas y 3 pacientes con cáncer de mama.
Materiales y métodos: El marcado con 99mTc se realizó por la adición de una solución de pertecneciato de sodio y una solución buffer de 0.2 M y pH 7.0 a la formulación liofilizada que contiene E-[c(RGDfK)]2, EDDA, tricina, manitol y cloruro estanoso. La pureza radioquímica fue evaluada por Cromatografía Líquida de Alta Resolución en fase reversa y por Cromatografía Instantánea en Capa Fina sobre Silica Gel. Se adquirieron imágenes a cuerpo entero de las 7 mujeres sanas a 0.5, 1, 3, 6 y 24 horas después de la administración del 9mTcEDDA/HYNIC-E-[c(RGDfK)]2 obtenido con una pureza radioquímica > 94%. Se dibujaron regiones de interés (ROIs) alrededor de los órganos de interés en cada periodo de tiempo. Se convirtió cada ROI a actividad usando el método de vistas conjugadas. Se utilizó la secuencia de imágenes para extrapolar curvas de actividad-tiempo del 99mTc-EDDA/ HYNIC-E-[c(RGDfK)]2 en cada órgano para ajustar a un modelo biocinético y calcular el número total de desintegraciones (N) que ocurrieron en las regiones fuente. Se introdujeron los datos de N en el código OLINDA EXM para estimar la dosis de radiación interna. Se obtuvieron imágenes estáticas a una hora, en posición supina con las manos detrás de la cabeza, de 3 pacientes con cáncer de mama confirmado histológicamente.
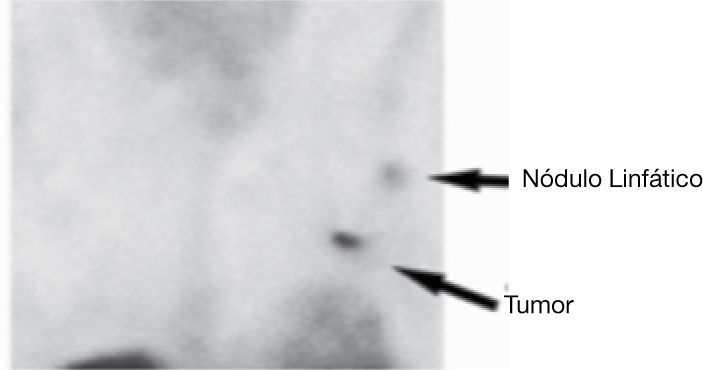
Resultados: El mostró alta estabilidad en suero humano y captación específica por las integrinas. En las voluntarias sanas el radiofármaco tuvo una vida media sanguínea de 1.60 minuto para el componente rápido, de 1.0 hora y 4.03 horas para el primer y segundo componente lento, respectivamente. Las imágenes de pacientes con cáncer de mama mostraron una relación tumor/sangre promedio de 3.61±0.62 a una hora (fig. 1). Las dosis equivalentes promedio calculadas para estas pacientes usando 740 MBq fueron de 6.2, 20.7, 34.5, 4.9, y 57.0 mSv para intestino, bazo, riñones, hígado y tiroides respectivamente y la dosis efectiva fue de 6.1 mSv.
Conclusiones: El 99mTc-EDDA/HYNIC-E-[c(RGDfK)]2 obtenido a partir del kit formulado presenta una alta captación en pacientes con lesiones malignas, por lo que es un radiofármaco prometedor para imagen de blancos específicos de cáncer de mama. Los resultados obtenidos justifican un estudio clínico posterior para determinar la especificidad/sensibilidad de 99mTc-EDDA/HYNIC-E-[c(RGDfK)]2.
Al Consejo Nacional de ciencia y Tecnología por soportar el proyecto (CONACYT-SEP-CB-2010-01-150942).