Se presenta un reporte de caso clínico de un niño con síndrome de cimitarra y revisión de la literatura existente con el fin de describir las principales implicaciones quirúrgicas y anestésicas de estos pacientes. Niño de 4meses de edad, peso de 4700g. Ingresó por cuadro de neumonía con enfisema lobar izquierdo que requirió intubación mecánica y manejo en la unidad de cuidados intensivos. Los diagnósticos asociados son extubación fallida, hipertensión pulmonar severa y síndrome de cimitarra confirmado por ecocardiografía. Es programado para lobectomía pulmonar izquierda. La madre firmó consentimiento informado para la anestesia y para la cirugía. Ingresa a cirugía; se realiza inducción anestésica intravenosa y se coloca catéter venoso central, línea arterial, sonda vesical y pulsioxímetros pre y posductal. Requirió soporte vasopresor con dopamina y transfusión de glóbulos rojos. Sin eventos adversos durante la cirugía. Se lleva de nuevo a la unidad de cuidados intensivos pediátrica intubado, con tubo a tórax, y se logra extubar 2días después, con evolución favorable. El Síndrome de cimitarra se caracteriza por un drenaje venoso pulmonar anómalo derecho asociado a cardiopatías congénitas y malformaciones pulmonares. Tiene una prevalencia baja dentro de la población pero una morbimortalidad perioperatoria muy alta, sobre todo en niños. Con este reporte se presentan unas pautas concretas y prácticas para el manejo anestésico, la monitorización y las metas hemodinámicas de estos pacientes.
We present a clinical case report of a child with scimitar syndrome and a review of the literature in order to describe the main surgical and anesthetic implications of these patients. Child, 4months old, weight 4700g, diagnosed with pneumonia and left lobar emphysema requiring mechanical intubation and ICU care. The associated diagnoses are failed extubation, severe pulmonary hypertension and scimitar syndrome confirmed with echocardiography. He was scheduled for pulmonary lobectomy. His mother signed an informed consent authorization for anesthesia and surgery. The child entered surgery, intravenous anesthetic induction was performed and a central venous catheter, an arterial line, urinary catheter and pre-and post-ductal pulse oximeters were inserted. He required vasopressor support with dopamine and transfusion of red blood cells. No adverse events during surgery. At the end of the surgery he was carried back to pediatric ICU and intubated with a chest tube. Extubation was successfully performed two days later with favorable progress. Scimitar syndrome is characterized by an anomalous right pulmonary venous return associated with congenital heart disease and pulmonary malformations. It has a low prevalence in the population but a very high perioperative morbidity and mortality, especially in children. With this report we present the main standards and practices for anesthetic management, monitoring and hemodynamic goals with these patients.
El Síndrome de cimitarra pertenece a los síndromes venolobares, asociado a secuestro pulmonar y anomalías cardiacas congénitas1. Tiene una incidencia baja, de 1 a 5 por 100 000 nacimientos2. Se caracteriza por un drenaje venoso pulmonar anómalo derecho y alteraciones cardiovasculares3. La presentación en la infancia requiere intervenciones quirúrgicas tempranas para corregir la enfermedad. El objetivo de este reporte de caso es revisar la literatura sobre este tipo de anomalías para describir las principales metas en el manejo anestésico y lograr un buen resultado perioperatorio.
Reporte de casoNiño de 4meses de edad y peso de 4700g con diagnóstico de neumonía y enfisema lobar congénito izquierdo que colapsa el pulmón derecho.
El paciente se encuentra en ventilación mecánica, con antecedente de extubación fallida, hipertensión pulmonar severa (PSP52mmHg) y diagnóstico de síndrome de cimitarra por ecocardiografía. Los resultados paraclínicos se describen en la tabla 1.
Resultados de los exámenes paraclínicos
| Examen | Resultado |
|---|---|
| Ecocardiograma | Arco aórtico derecho, ductus arteriovenoso persistente con repercusión hemodinámica, fracción de eyección del 70%, hipertensión pulmonar con presión arterial sistólica pulmonar de 52mmHg, dextroposición cardiaca y drenaje venoso pulmonar anómalo |
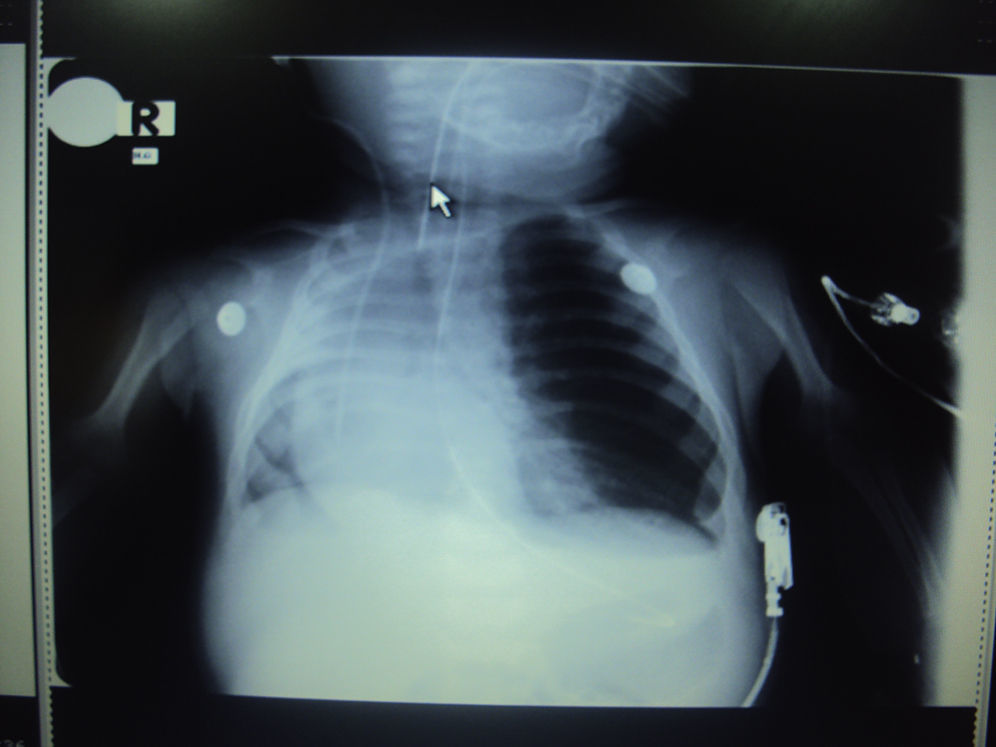
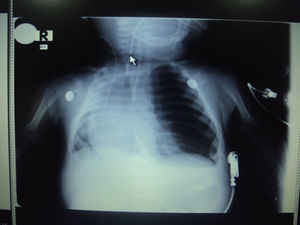
| Radiografía de tórax | Sobreexpansión del pulmón izquierdo asociada a dextroposición y atelectasia completa del pulmón derecho |
Fuente: autores.
El paciente es programado para lobectomía superior izquierda para resección del área pulmonar con enfisema. La madre firmó el consentimiento informado para la anestesia y la cirugía (fig. 1).
La monitorización se hizo con catéter venoso yugular externo izquierdo, línea arterial tibial posterior, electrocardiograma, pulsioxímetro preductal y posductal, capnografía, sonda vesical y temperatura esofágica.
La inducción se realizó con fentanil 50μg y propofol 20mg; el mantenimiento se hizo con remifentanil 0,3μg/kg/min y sevofluorano 1MAC.
La ventilación mecánica estaba controlada por presión, con volúmenes y presiones bajas, con FIO2 del 80% para mantener capnografía (30-36mmHg) y oximetría (90-93%) en rangos normales.
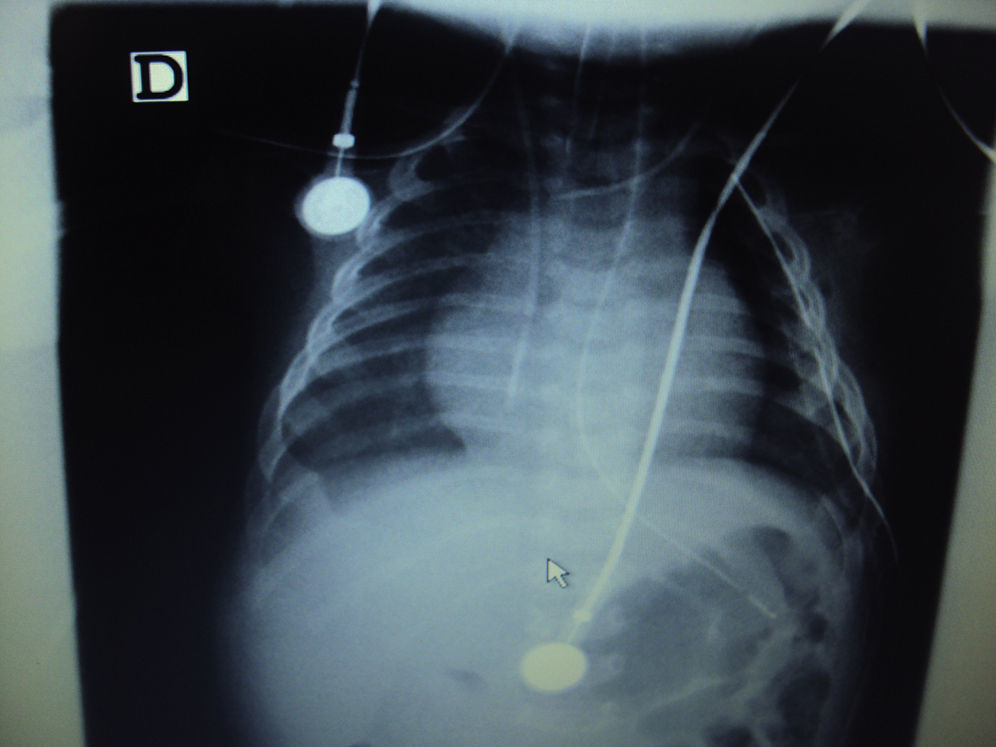
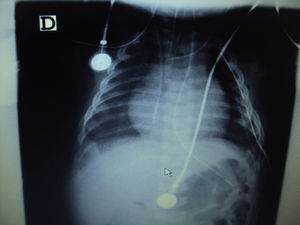
Durante la cirugía presentó hipotensión que requirió dopamina a 5μg/kg/min. La hemoglobina intraoperatoria fue de 8,7mg/dl, por lo que se transfundieron 70cc de glóbulos rojos. No se presentaron eventos adversos durante la cirugía. La radiografía de tórax postoperatoria muestra mejoría en la expansión del pulmón derecho (fig. 2).
El paciente es trasladado a la unidad de cuidados intensivos con soporte ventilatorio y vasopresor, bajo sedoanalgesia con fentanil. Se extubó 2días después, con evolución satisfactoria.
DiscusiónEl síndrome de cimitarra es una enfermedad congénita rara. La serie de casos más grande reportada hasta ahora describe 44 casos en pacientes adultos3 y 16 casos en niños4. La prevalencia en la población general es baja, lo que refleja el reto perioperatorio que tienen estos pacientes y la importancia de conocer las implicaciones anestésicas por su alta mortalidad perioperatoria1,2.
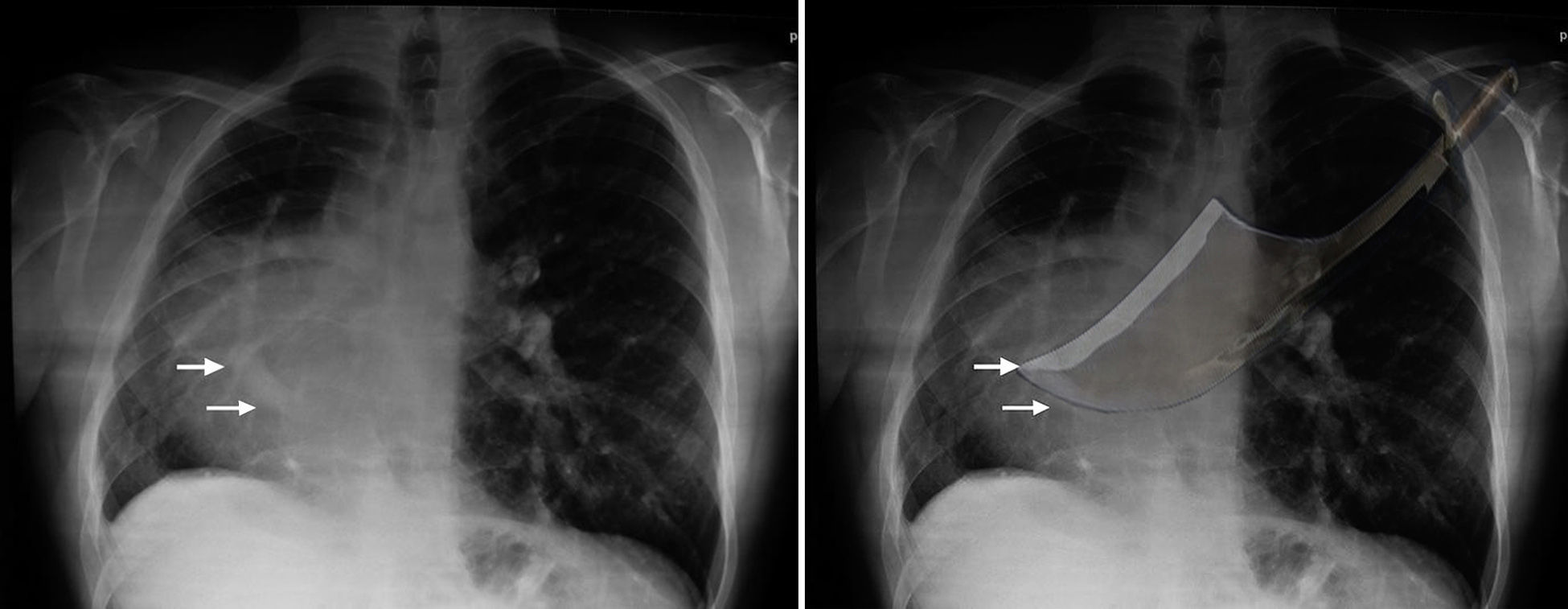
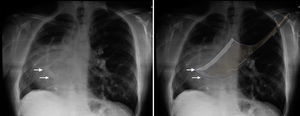
El primer caso fue reportado en 1836 por el doctor Cooper, quien le dio su nombre por la imagen en la placa de tórax: curvilínea y alargada en el borde derecho del corazón, que corresponde al drenaje venoso anómalo del pulmón derecho en la aurícula derecha o en la vena cava, similar a la espada de cimitarra originaria de Persia2,5,6 (fig. 3).
Este síndrome constituye el 4% de los drenajes venosos pulmonares anómalos. Se asocia a alteraciones en la irrigación arterial pulmonar, hipoplasia pulmonar derecha, hipoplasia del bronquio derecho y de la arteria pulmonar derecha4,5,7. Las alteraciones cardiacas más frecuentes son la dextroposición del corazón con desplazamiento del mediastino, ausencia del pericardio y otras malformaciones como la comunicación interauricular (60-70%) o interventricular, coartación de la aorta y tetralogía de Fallot en un 25% de los casos3,6,7.
Se han descrito 2 formas de presentación: adulta y pediátrica. En los adultos el cortocircuito generalmente es bajo, sin hipertensión pulmonar en el 77% de los casos o con hipertensión leve en el 23%. Usualmente no requiere tratamiento. Por el contrario, cuando el síndrome se manifiesta en el periodo neonatal se presenta como una falla cardiaca o respiratoria secundaria a la hipertensión pulmonar y generalmente requieren cirugía. El pronóstico depende de la severidad de las anomalías asociadas, del manejo de la hipertensión pulmonar y de la condición clínica del niño8.
Los pacientes pueden presentar infecciones respiratorias recurrentes y falla respiratoria según el grado de hipoplasia pulmonar; también se puede manifestar con hemoptisis o ser un hallazgo incidental, como ocurre en los adultos5,9. Los niños que tienen síntomas de falla cardiaca por hipertensión pulmonar tienen un mal pronóstico1.
La hipertensión pulmonar se produce por un cortocircuito de izquierda a derecha a través de la circulación anómala del pulmón derecho, lo que, asociado a la hipoplasia pulmonar y al drenaje venoso pulmonar anómalo, aumenta la presión en las cavidades derechas. La hipoplasia pulmonar aumenta el cortocircuito intrapulmonar, que, asociado con la estenosis de la vena pulmonar y otras malformaciones congénitas, produce hipertensión pulmonar persistente10,11. En el examen físico se encuentra desplazamiento de los ruidos cardiacos hacia la derecha, soplos cardiacos, y la auscultación pulmonar puede ser normal o estar disminuida.
El diagnóstico se realiza con el ecocardiograma, que muestra la vena cimitarra en el 70% de los casos, tiene mayor sensibilidad en presentaciones severas y muestra las alteraciones cardiacas asociadas3. La tomografía tridimensional o la resonancia magnética cardiaca son fundamentales para visualizar la vena pulmonar anómala y esclarecer la anatomía del paciente12. El cateterismo cardiaco y la angiografía confirman el diagnóstico; dan información detallada de la anatomía y la severidad de la hipertensión pulmonar. Son útiles para el planeamiento quirúrgico11-13.
El tratamiento depende de la edad y de la sintomatología. En los recién nacidos se inicia manejo para la hipertensión pulmonar. La cirugía está indicada en los pacientes con falla cardiaca persistente, enfermedades infecciosas recurrentes o hipertensión pulmonar refractaria2.
Los casos que se presentan con secuestro pulmonar requieren lobectomías e interrupción del flujo sistémico anómalo mediante embolización o ligadura directa del mismo, así como el cierre de los defectos septales1.
El pronóstico es bueno cuando la hipertensión pulmonar es leve o desaparece. La irrigación arterial anómala, la obstrucción severa de las venas pulmonares y las cardiopatías congénitas complejas se asocian a mal pronóstico3-5.
Implicaciones anestésicasSe debe realizar una valoración integral del paciente, con énfasis en la función cardiaca y la función respiratoria. Como exámenes prequirúrgicos se requieren: hemograma, gases arteriales, hemoclasificación, radiografía de tórax y ecocardiograma.
Es necesario tener reserva de glóbulos rojos y unidad de cuidados intensivos postoperatorios. Las implicaciones anestésicas más importantes están relacionadas con la presencia de cortocircuitos intracardiacos y la hipertensión pulmonar, por lo cual se deben optimizar las condiciones del paciente antes de la cirugía.
La monitorización quirúrgica se realiza con electrocardiograma, presión arterial invasiva, saturación de oxígeno preductal y posductal, sonda vesical, capnografía, temperatura y catéter venoso central.
La vía aérea debe asegurarse con tubo traqueal. No es necesario realizar intubación pulmonar selectiva, dado que cursan con hipoplasia pulmonar y presentan ventilación predominante en el pulmón sano, lo que mejora el campo quirúrgico. Se recomienda la ventilación mecánica controlada por presión para evitar el barotrauma o el volutrauma14. Se recomiendan volúmenes bajos (<8ml/kg) y presiones meseta <30cmH2O.
El riesgo de paro cardiaco, muerte y crisis de hipertensión pulmonar es mayor en pacientes que tienen falla cardiaca. Se deben corregir las causas de la crisis de hipertensión pulmonar, como hipoxia, hipercapnia, acidosis metabólica, hipotermia, dolor y cualquier estímulo del sistema nervioso simpático15.
Las metas anestésicas incluyen mantener un adecuado plano anestésico, garantizar adecuada analgesia, evitar el aumento de la presión en la arteria pulmonar y optimizar la función cardiaca con una presión arterial sistémica normal para la edad.
La inducción anestésica debe garantizar un adecuado plano para la intubación y estabilidad hemodinámica; se puede utilizar un inductor intravenoso (midazolam, ketamina, propofol) más un opiáceo (fentanil o remifentanil) y un relajante muscular no despolarizante. La meta es evitar la hipotensión con la administración de los bolos. La inducción inhalatoria es menos efectiva por la hipoplasia pulmonar y puede producir mayor depresión miocárdica. El mantenimiento anestésico puede realizarse con agentes inhalados más perfusión continua de opiáceos15.
En caso de crisis de hipertensión pulmonar se debe disminuir la resistencia vascular pulmonar, mantener un adecuado gasto cardiaco y retirar el estímulo desencadenante de la crisis16,17. El manejo de la hipertensión pulmonar se realiza con hiperventilación leve con oxígeno al 100%, corrección de la acidosis metabólica y respiratoria, utilización de vasodilatadores pulmonares selectivos como el óxido nítrico inhalado, corrección de la hipotensión y el bajo gasto (norepinefrina, dopamina o epinefrina) y utilización de inodilatadores, como dobutamina o milrinone15-18.
Se recomienda la analgesia intravenosa a base de opiáceos o técnicas analgésicas regionales que no comprometan las condiciones hemodinámicas.
ConclusiónEl síndrome de cimitarra es una alteración rara que se asocia a diversas anomalías congénitas cardiacas y pulmonares. El manejo de los pacientes debe ser individualizado y definido por un equipo multidisciplinario. Las consideraciones anestésicas se deben enfocar en el manejo de la hipertensión pulmonar, las metas hemodinámicas y la analgesia posoperatoria.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciamientoLos autores no recibieron patrocinio para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.