Estudio observacional sobre la diferencia entre el número de casos diagnosticados en situación clínica habitual de acidosis con hiperlactacidemia sospechosa de ser causada por metformina y su incidencia según la ficha técnica. Adicionalmente se exploró la relación con la función renal de la acidosis hiperlactacidémica por metformina.
PacientesSe identificaron los casos de acidosis entre los años 2013 y 2014 mediante el análisis del CMBD y las peticiones al laboratorio. Se seleccionó a los pacientes que presentaban lactato venoso > 2,7 mmol/L en el momento de ser atendidos y para los que constaba el uso ambulatorio de metformina. La relación causal con la metformina fue evaluada independientemente por varios investigadores. Los casos incidentes se calcularon con base en el número de pacientes a los que se les había dispensado un medicamento que contuviera metformina durante el mismo periodo en el área estudiada.
ResultadosSe identificaron 476 casos de acidosis, de los que en 20 se consideró que la metformina era sospechosa de causar el cuadro de acidosis con hiperlactacidemia, lo que supone una incidencia de 6,57/10.000 pacientes. El 85% de los casos presentaban insuficiencia renal aguda.
ConclusionesLa incidencia aparente de acidosis con hiperlactacidemia en pacientes tratados con metformina es mayor que la establecida en la ficha técnica (inferior a 1/10.000). El desarrollo de acidosis con hiperlactacidemia por metformina está relacionado con el deterioro agudo de la función renal.
Observational study on the difference between the number of cases of acidosis with hyperlactacidaemia suspected of being caused by metformin diagnosed in standard clinical practice and the incidence of this condition according to the datasheet. The study also explored the relationship between renal function and metformin-associated hyperlactacidaemia acidosis.
PatientsWe identified cases of acidosis between 2013 and 2014 by analysing the minimum basic data set and laboratory requests. We selected patients who presented venous lactate levels >2.7 mmol/L at the time they were treated and for whom the use of outpatient metformin was confirmed. The causal relationship with metformin was independently evaluated by several researchers. The incident cases were calculated based on the number of patients who had been dispensed a drug containing metformin during the same period in the study area.
ResultsWe identified 476 cases of acidosis. Metformin was suspected of causing the condition of acidosis with hyperlactacidaemia in 20 of these cases, which represents an incidence rate of 6.57/10,000 patients. Eighty-five percent of the cases presented acute renal failure.
ConclusionsThe apparent incidence of acidosis with hyperlactacidaemia in patients treated with metformin is greater than that established in the datasheet (<1/10,000). The onset of metformin-associated hyperlactacidaemia acidosis is related to acute renal impairment.
La metformina es un fármaco hipoglucemiante de amplio uso, incluso en situaciones en las que estaría contraindicado, lo que podría aumentar la incidencia de reacciones adversas1.
Una de estas reacciones adversas poco frecuente pero grave es la acidosis con hiperlactacidemia. Según la ficha técnica de las especialidades que contienen metformina, es una reacción adversa muy rara (frecuencia < 1/10.000)2. Otros estudios epidemiológicos estiman su incidencia en un rango que va de 3 a 16,7 casos cada 100.000 pacientes año3-5.
La acidosis con hiperlactacidemia presenta una mortalidad muy elevada, que se sitúa entre el 27 y el 45% de los casos en función de la serie estudiada6.
La metformina puede causar la hiperlactacidemia debido a la inhibición de la neoglucogénesis, proceso del que el lactato es uno de sus sustratos2,7, sin descartar un posible efecto en el metabolismo mitocondrial8. Dado que la metformina se elimina por vía renal sin metabolizar1,8, un deterioro de la función renal podría aumentar su concentración plasmática y favorecer la aparición de esta reacción adversa. Sin embargo, los estudios disponibles sobre la relación entre la función renal y la acidosis con hiperlactacidemia en consumidores de metformina no son concluyentes4,5,9.
Es de destacar que no existe una definición universalmente aceptada de lo que es una acidosis con hiperlactacidemia, los términos de lactato y ácido láctico se intercambian aleatoriamente10 y no existen unos criterios firmemente establecidos para distinguir entre las elevaciones del ácido láctico y la hiperlactacidemia. Muchos estudios han usado puntos de corte entre 2 y 2,5 mmol/L para definir el lactato sérico elevado10, aunque hasta 2,7 mmol/L podrían considerarse normales en pacientes que consumen metformina11. En otros estudios se considera un lactato sérico alto a partir de 4 mmol/L10 mientras que se asume que la acidosis láctica requiere además la presencia de acidosis metabólica y unos niveles de lactato superiores a 5 mmol/L1,10,12 o incluso de solo un pH ≤ 7,35 y un lactato > 5 mmol/L13. Por el contrario, en la práctica clínica habitual se considera que un pH ≤ 7,35 con un lactato sérico > 2 mmol/L y una PaCO2 ≤ 42mmHg define la acidosis láctica14.
Muchas de estas definiciones no tienen en cuenta si el origen de la muestra en la que se realiza la determinación es arterial o venoso, asunto capital a la hora de definir un umbral de pH para la acidosis.
Por otro lado, la atribución de la acidosis con hiperlactacidemia a la metformina solo es inequívoca si se comprueban unos niveles tóxicos de esta1. No obstante, la determinación del nivel de metformina no suele estar disponible de forma rutinaria en la práctica clínica y, por ello, el diagnóstico de esta entidad tiene que basarse en la valoración clínica.
Ante esta situación, llevamos a cabo un estudio con el objetivo de conocer la incidencia de la acidosis con hiperlactacidemia atribuible a metformina en nuestro medio, definiéndola como acidosis (entendida como un pH venoso < 7,32 o arterial < 7,35) metabólica (PCO2 que no superara el límite de normalidad; esto es: 45mmHg si era arterial y 51 mmHG si venoso) con hiperlactacidemia en consumidores de metformina (lactato venoso > 2,7 mmol/L) en la que clínicamente se sospechara de la metformina como causa.
Otro objetivo del presente estudio ha sido conocer si el deterioro de la función renal puede considerarse un factor contribuyente para la aparición de esta reacción adversa.
Material y métodosSe realizó un estudio de los casos incidentes de acidosis con hiperlactacidemia entre los usuarios de metformina en una cohorte histórica (años 2013 y 2014) de la población del área norte de Tenerife (población de referencia del Hospital Universitario de Canarias) a partir de la valoración de la información de la historia clínica electrónica de atención especializada y primaria y de valores de laboratorio. Este hospital es un centro público, de tercer nivel, con una población de referencia de 373.054 habitantes15. Dado el carácter exploratorio-descriptivo de este estudio, no se hizo predeterminación del tamaño muestral.
El estudio fue evaluado favorablemente por el Comité de Ética de Investigación Clínica del Hospital Universitario de Canarias y clasificado por la Agencia Española de Medicamentos y productos sanitarios con código SFC-MET-2015-01.
Cohorte de estudioSujetos que al ingreso presentaban acidosis con hiperlactacidemia expuestos ambulatoriamente a metformina.
Para localizar a los pacientes con acidosis e hiperlactacidemia se obtuvieron 2listados de pacientes:
- •
Uno a partir del CMBD (registro que almacena los diagnósticos que recibe el paciente codificados mediante el CIE) con pacientes diabéticos con acidosis (códigos CIE 9:250 y 272.2, casos en los que podría existir la reacción adversa).
- •
Otro listado a partir de las solicitudes al laboratorio en las que se había pedido el lactato.
Para conocer el total de pacientes expuestos al fármaco sospechoso durante el periodo de estudio se recurrió a los datos de dispensaciones de metformina como monofármaco o en combinación (códigos ATC A10BA02, A10BD02, A10BD03, A10BD05 y A10BD07) realizadas entre la población de referencia del Hospital Universitario de Canarias durante los años 2013 y 2014, a partir del programa de facturación del Servicio Canario de la Salud, Farmacanarias.
Criterios de selecciónPara ser incluidos los pacientes debían presentar uso actual ambulatorio de metformina sola o en combinación con otros hipoglucemiantes en la indicación autorizada como tratamiento de la diabetes tipo II en el momento de desarrollar la acidosis y una determinacion dentro de las primeras 24 h de asistencia en el Hospital Universitario de Canarias con: acidosis (pH < 7,35 si la determinación era arterial y < 7,32 si era venosa) metabólica (PaCO2 < 45mmHg si la muestra era arterial; < 51mmHg si era venosa) e hiperlactacidemia (lactato > 2,7 mmol/L11 en sangre venosa).
No fueron incluidos aquellos pacientes en los que no había datos suficientes para establecer que existiera acidosis e hiperlactacidemia o que estas fuesen previas al ingreso o para confirmar la exposición a metformina en el momento de desarrollar la acidosis. Solo se incluyó a pacientes diabéticos en tratamiento con metformina, de manera que no hubo necesidad de excluir a pacientes con metformina fuera de indicación. También se excluyó a los pacientes con acidosis de otras causas (respiratoria y cetoacidosis) o con sobredosis intencionada con metformina.
Análisis de la relación causal entre la metformina y la hiperlactacidemiaMediante la historia clínica se evaluaron los motivos de ingreso, datos y pruebas analíticas, antecedentes personales, medicación concomitante, posibles causas alternativas y factores contribuyentes, aplicando el algoritmo de Karch y Lasagna modificado que utiliza el Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano16 para la evaluación de la causalidad. Cada uno de esos ítems fue evaluado de forma independiente y ciega por 2médicos de la Unidad de Medicina Intensiva de este hospital y se puntuaba permitiendo distribuir a los sujetos del estudio en 2grupos: uno en el que la metformina era sospechosa de haber causado la acidosis con hiperlactacidemia (grupo de sospechosos: categorías del algoritmo de posible, probable y definida) y otro en el que era poco probable que la metformina hubiera podido tener algún papel en la aparición del cuadro clínico (grupo de no sospechosos: categorías del algoritmo de condicional e improbable). Los casos en los que hubo discrepancia entre estos 2evaluadores fueron sometidos al estudio de otros 3especialistas relacionados con el ámbito de la farmacovigilancia en la comunidad autónoma.
Insuficiencia renalLa existencia de insuficiencia renal aguda fue valorada usando una variable subrogada (nivel de creatinina plasmática superior a 0,9 mg/dL) y los diagnósticos clínicos, dado que la estimación del filtrado glomerular no estaba disponible para la mayoría de los pacientes.
La existencia de insuficiencia renal crónica se basó exclusivamente en los diagnósticos clínicos.
Dosis de metforminaLa dosis de metformina para cada paciente en el momento del ingreso se obtuvo de las historias clínicas y del módulo de prescripción del Servicio Canario de la Salud.
MortalidadLa mortalidad en los casos de acidosis con hiperlactacidemia es mayor cuando existen factores causales diferentes a la acumulación de metformina1,8. Por ello, la mortalidad y sus causas, valoradas partiendo de la información disponible en la historia clínica, fue comparada entre los grupos de sospechosa y no sospechosa.
Comparación con otros estudiosGran parte de otros estudios que han analizado la acidosis láctica por metformina consideran que la acidosis se acompaña de hiperlactacidemia cuando el nivel de lactato supera los 5 mmol/L, valor superior al utilizado en este estudio. Por tanto, se calculó la incidencia con los casos identificados con base en dicho valor del parámetro analítico.
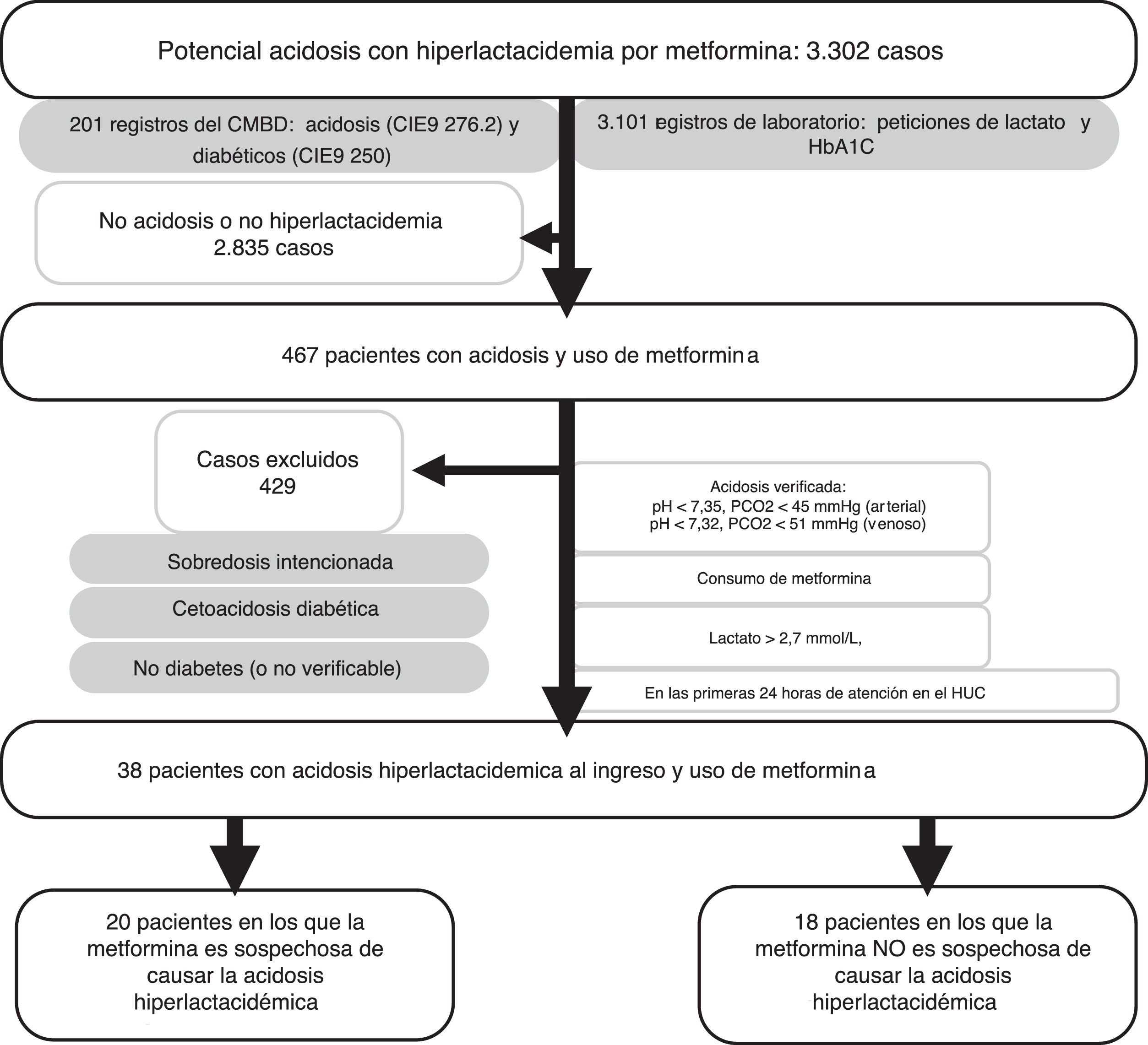
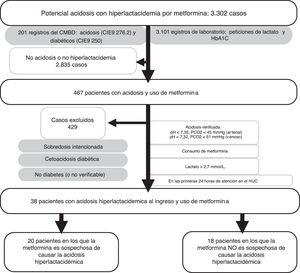
ResultadosDurante los años revisados y a partir del listado del CMBD y el del laboratorio, se identificaron 467 pacientes que podrían cumplir los criterios de inclusión, de los que en 38 se verificaron todos (fig. 1).
En ninguno de los casos incluidos existía un uso de la metformina diferente al establecido por la ficha técnica. En los casos en los que la información sobre la dosis estaba disponible, esta no excedía de lo dispuesto por la ficha técnica (tabla 1).
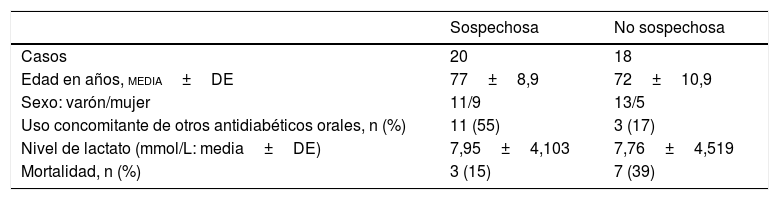
Características de los casos estudiados
| Sospechosa | No sospechosa | |
|---|---|---|
| Casos | 20 | 18 |
| Edad en años, media±DE | 77±8,9 | 72±10,9 |
| Sexo: varón/mujer | 11/9 | 13/5 |
| Uso concomitante de otros antidiabéticos orales, n (%) | 11 (55) | 3 (17) |
| Nivel de lactato (mmol/L: media±DE) | 7,95±4,103 | 7,76±4,519 |
| Mortalidad, n (%) | 3 (15) | 7 (39) |
Realizado el análisis de la relación causal, en 20 de los 38 casos identificados se consideró que la metformina era sospechosa de causar la acidosis con hiperlactacidemia al haberse obtenido una categoría del algoritmo de Karch y Lasagna de posible, probable o definida.
Conforme a los datos de consumo obtenidos del programa de facturación de recetas del SCS, Farmacanarias, hubo 30.399 pacientes expuestos a metformina en ese periodo, lo que permitió calcular una incidencia de 6,57 casos por cada 10.000 pacientes.
Todos estos casos, con sospecha de reacción adversa, identificados y documentados por el Centro Autonómico de Farmacovigilancia de Canarias no deben ser notificados al Sistema Español de Farmacovigilancia según la orden SAS 1344/2017, al tratarse de un estudio clasificado como EPA OD por la AEMPS17.
MortalidadEn los casos en los que se había considerado sospechosa la metformina, el desenlace fue mortal en el 15%. En el otro grupo, en el que la metformina no se consideró sospechosa, hubo 7 muertes de 18 casos (39%).
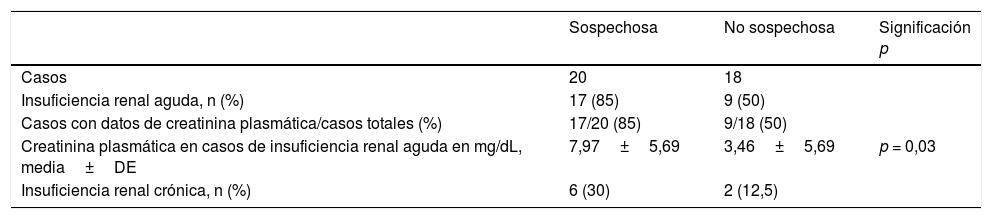
Relación con la insuficiencia renalDe los 20 casos sospechosos, 17 (85%) presentaban un nivel de creatinina elevado en el momento del ingreso, sugestivo de insuficiencia renal aguda, mientras que de los 18 casos no sospechosos, solo 9 presentaban nivel de creatinina plasmática elevado (50%).
La diferencia entre la media del nivel plasmático de creatinina al ingreso en los casos con insuficiencia renal aguda e hiperlactacidemia entre los grupos de sospechosos y los no sospechosos fue significativa (7,9 vs. 3,45 mg/dL; p = 0,03) (tabla 2).
Función renal de los casos estudiados
| Sospechosa | No sospechosa | Significación p | |
|---|---|---|---|
| Casos | 20 | 18 | |
| Insuficiencia renal aguda, n (%) | 17 (85) | 9 (50) | |
| Casos con datos de creatinina plasmática/casos totales (%) | 17/20 (85) | 9/18 (50) | |
| Creatinina plasmática en casos de insuficiencia renal aguda en mg/dL, media±DE | 7,97±5,69 | 3,46±5,69 | p = 0,03 |
| Insuficiencia renal crónica, n (%) | 6 (30) | 2 (12,5) |
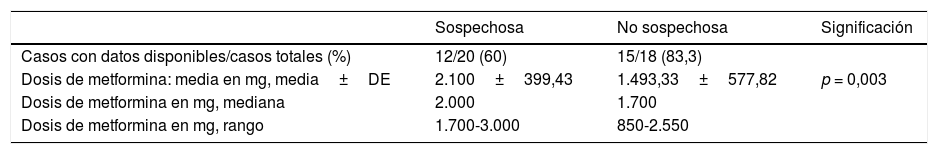
Solo se se pudieron obtener datos fiables acerca de la dosis de metformina en una parte de los pacientes (71%), pero se advertía una diferencia significativa entre los grupos de sospechosos y los no sospechosos (tabla 3).
Dosis de metformina
| Sospechosa | No sospechosa | Significación | |
|---|---|---|---|
| Casos con datos disponibles/casos totales (%) | 12/20 (60) | 15/18 (83,3) | |
| Dosis de metformina: media en mg, media±DE | 2.100±399,43 | 1.493,33±577,82 | p = 0,003 |
| Dosis de metformina en mg, mediana | 2.000 | 1.700 | |
| Dosis de metformina en mg, rango | 1.700-3.000 | 850-2.550 |
Siguiendo el criterio habitualmente empleado en otros estudios (lactato venoso > 5 mml/L) se identificaron 30 casos de hiperlactacidemia, de los cuales 16 eran sospechosos de ser causados por metformina. Por tanto, la incidencia era de 5,27 casos por 10.000.
DiscusiónLos resultados obtenidos muestran que hay una gran diferencia entre la tasa de incidencia estimada de acidosis con hiperlactacidemia asociada a metformina en este estudio y la descrita en la ficha técnica de este medicamento, que recoge una incidencia de < 1:10.000 expuestos, mientras nuestros datos indican una incidencia de 6,57 casos por cada 10.000 pacientes expuestos, es decir, un caso por cada 1.522 pacientes expuestos. Este hallazgo es congruente con algunos estudios que también señalan una incidencia muy superior a la esperable según lo recogido en la ficha técnica8. Cuando se aplicaron criterios más restrictivos, que exigían unos niveles de lactato > 5 mmol/L, la incidencia también fue superior a la esperada (5,27 casos/10.000).
El enfoque clínico adoptado en el estudio para la identificación de los casos, teniendo en cuenta no solo parámetros analíticos, y para la valoración de la causalidad podría ser un factor que explicase la mayor incidencia obtenida. Habría, por ello, una discrepancia entre lo que se considera un caso de acidosis con hiperlactacidemia por metformina en la ficha técnica del producto y lo que se considera un caso tras una valoración basada en la clínica.
Otro hallazgo de relevancia que corrobora el de estudios previos1 es que el nivel medio de lactato fue igual en ambos grupos, lo que indica que no es posible distinguir los casos de hiperlactacidemia debida a la metformina de otras causas de hiperlactacidemia basándose solo en valores de lactacidemia.
El estudio de la mortalidad sirvió para confirmar que el análisis de causalidad era correcto: en el grupo en el que la metformina era sospechosa, cabía esperar que la retirada del medicamento condujera a una recuperación del cuadro de acidosis, mientras que en el grupo no sospechoso no hay por qué esperar una mejoría en esta situación clínica después de la retirada del fármaco1,8.
De igual forma, los datos sobre la dosis de metformina fueron diferentes entre ambos grupos, con una dosis mayor en aquel en que la metformina se juzgó sospechosa de haber causado el cuadro, lo que también apoyaba el análisis de causalidad.
Debe tenerse en cuenta que habitualmente la acidosis con hiperlactacidemia no suele ser debida a un único factor etiológico, sino a varios, entre los que se encontraría la metformina, las comorbilidades del paciente, fenómenos de hipoxia tisular, etc.8. Por ello, es muy posible que exista una infraestimación de los casos en los que la metformina causa o contribuye a la hiperlactacidemia, ya que suelen estar enmascarados por otros cuadros clínicos8. Además, al haberse excluido los casos en los que la acidosis era de origen respiratorio, se puede haber infraestimado la contribución de la metformina en otros cuadros de acidosis.
En cuanto a la influencia de la insuficiencia renal aguda en la aparición de los casos en el grupo en que la metformina es sospechosa, efectivamente se aprecia una mayor proporción de pacientes con insuficiencia renal aguda (85%), pero la diferencia no alcanza significación estadística. Aunque es posible que ello se debiera a la inexistencia de diferencias reales, tampoco puede descartarse que el número de casos fuera insuficente para dotar de significación a esta diferencia. Es destacable la avanzada edad de los pacientes, lo que hace más frecuente que la función renal presente un deterioro subclínico y resulte sencillo desarrollar un fracaso agudo4,18.
Todas las situaciones descritas, incluida la existencia de unos niveles de creatinina significativamente más elevados en el grupo con insuficiencia renal aguda en el que la metformina era sospechosa (de casi el doble que cuando la metformina no era sospechosa), permiten sustentar la hipótesis de que existe una relación directa entre el desarrollo de acidosis con hiperlactacidemia y un deterioro renal agudo y grave en los pacientes que están tomando metformina.
En el grupo en el que se consideraba a la metformina sospechosa de causar la acidosis con hiperlactacidemia, la dosis media de esta era significativamente mayor que en el otro grupo, por lo que las alteraciones de la función renal en aquel grupo son aún más relevantes.
Todas estas observaciones son congruentes con las recomendaciones actuales: la ficha técnica europea de las especialidades que contienen metformina contraindican su uso si el filtrado glomerular o el aclaramiento de creatinina es inferior a 30 mL/min/1,73 m2 y la nota de seguridad de la FDA19 considera que no es recomendable iniciar un tratamiento con metformina con tasas de filtrado entre 30 y 45 mL/min. Ambos documentos indican que la existencia de cualquier condición clínica que pueda deteriorar la función renal obligaría a replantearse el balance riesgo-beneficio en el uso de metformina.
Un dato que debe investigarse es el papel que juega el uso concomitante de otros antidiabéticos orales en asociación con la metformina, al haberse observado una mayor proporción de pacientes con tratamiento combinado en el grupo en el que la metformina se consideró sospechosa. Si bien la acidosis láctica no es una reacción adversa frecuente con otros antidiabéticos orales, no puede descartarse un efecto no descrito que podría favorecer este cuadro clínico.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.