La larva migrans cutánea (LMC) es la dermatitis tropical más frecuente y corresponde a una zoonosis causada por nemátodos, cuyo hospedero son los gatos y los perros. El hombre actúa como hospedero accidental. Clínicamente se presenta como una placa lineal eritematosa pruriginosa, de crecimiento lento en la planta del pie. El diagnóstico es clínico, basado en la morfología de la lesión, asociado al antecedente de viaje a zonas endémicas.
ObjetivoPresentar un caso de LMC autóctona en Chile.
Caso clínicoNiño de 3 años sano, con lesión lineal en la planta del pie, clínicamente compatible con LMC. Se indica tratamiento con ivermectina, evolucionando con resolución completa de la lesión. El paciente no presentaba antecedentes de viajes fuera de Chile, pero sí de contacto con perros.
ConclusiónLa LMC es descrita clásicamente como una dermatitis del viajero. Se presenta este caso debido a que hasta la fecha no se registran reportes previos de LMC en niños adquirida en Chile.
Cutaneous larva migrans (CLM) is the most common tropical dermatitis. It is caused by nematodes hosted by cats and dogs. Humans act as an accidental reservoir. Clinically, it manifests as a slow-growing, elevated linear, erythematous and pruritic plaque, on the sole of the foot. Diagnosis is clinical, based on the morphology of the lesion associated with recent travel to endemic areas.
ObjectiveTo present an autochthonous case of CLM in Chile.
Clinical caseA 3-year-old boy, presented with a linear lesion on his foot, clinically compatible with CLM. He received a single dose of ivermectin and had complete resolution of the lesion. The patient had no history of travel outside of Chile, but had contact with dogs.
ConclusionCLM is classically described as travellers dermatitis. We present this case, because there are no previous reports of CLM acquired in Chile by children.
La larva migrans cutánea (LMC) es una zoonosis producida por nemátodos de las especies Ancylostoma braziliense, Ancylostoma caninum y Uncinaria stenocephala, cuyos hospederos son los gatos y los perros. El ser humano actúa como hospedero accidental, produciéndose la infección al tener contacto la piel con larvas provenientes de las heces de estos animales. La larva penetra hasta la dermis, produciendo una reacción inflamatoria local al migrar. La infección es autolimitada, pero sin tratamiento esta puede durar desde semanas a meses1.
Clínicamente se caracteriza por la aparición de una lesión única de tipo placa lineal, solevantada, pruriginosa, de crecimiento lento con un avance promedio de 2,7mm al día2,3.
El diagnóstico es fundamentalmente clínico, basado en la morfología de la lesión asociado al antecedente de viaje a zonas endémicas de la infección como Brasil, el Caribe y el Sudeste asiático3–5. Los exámenes de laboratorio suelen ser normales, pudiendo encontrarse en algunos casos eosinofilia.
La biopsia de piel no se realiza de rutina. Sin embargo, esta puede ser útil en caso de que existan dudas diagnósticas. Dentro de los hallazgos a la histología se ha descrito la presencia de espacios redondeados en la epidermis, con espongiosis y exudado fibrinoide, asociado a eosinófilos y queratinocitos necróticos. En la dermis puede observarse edema asociado a un infiltrado inflamatorio con eosinófilos6. Es infrecuente observar el parásito, debido a que este puede encontrarse a centímetros del extremo visible de la lesión.
ObjetivoEl objetivo de este trabajo es reportar un caso pediátrico de LMC adquirida en Chile en una zona urbana, debido a que hasta la fecha solo se han descrito casos en pacientes adultos con antecedentes de viajes a zonas endémicas7.
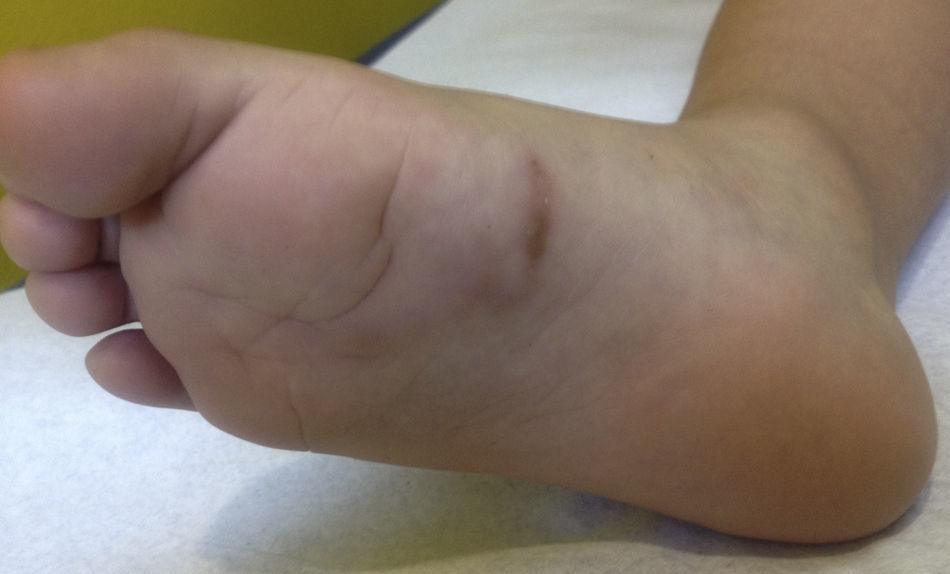
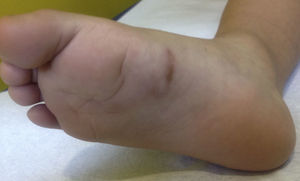
Caso clínicoNiño de 3 años, sano, derivado por su pediatra por una lesión en la planta del pie de semanas de evolución asociada a prurito. Al examen físico se observó en la planta del pie derecho la presencia de una placa palpable, eritematosa lineal solevantada de 3cm de largo. En el resto del examen físico no se observaban otros hallazgos (fig. 1).
Por la morfología y localización de la lesión se planteó el diagnóstico de LMC. Se preguntó a los padres por antecedentes de viajes al extranjero, indicando que el paciente nunca había salido de Chile. Al preguntar por otros factores de riesgo se constató que los abuelos del niño tenían un perro no desparasitado.
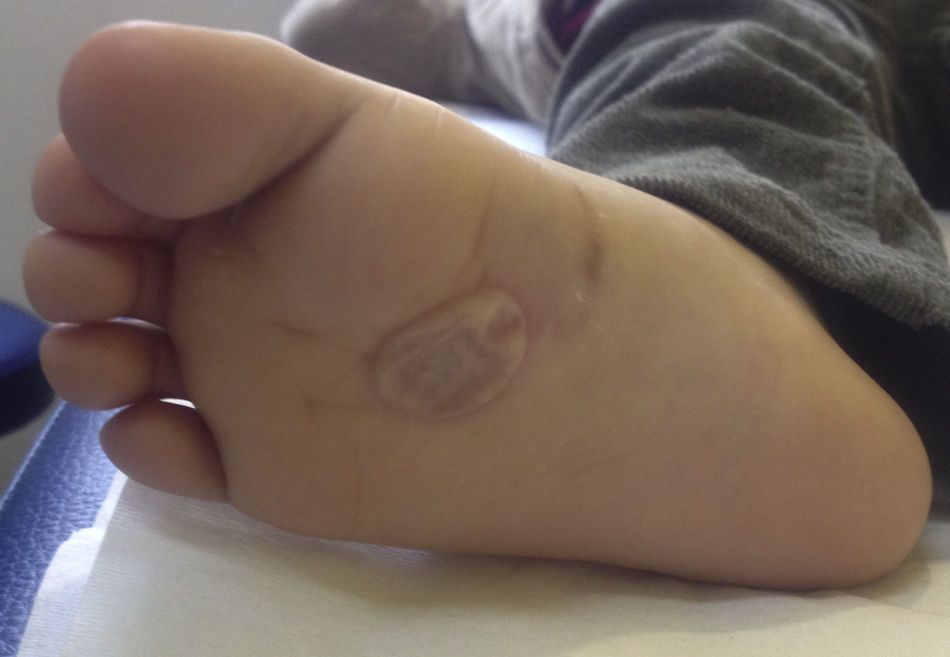
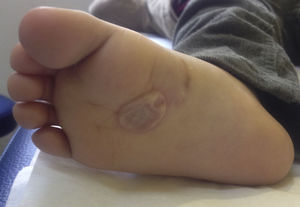
Se indicó tratamiento con ivermectina 200μg/kg en dosis única y control en 7 días. Al momento del control el paciente no presentaba prurito y la lesión se había mantenido estable. Sin embargo, en un extremo distal se desarrolló una bula serosa tensa de 3cm, la cual se puncionó con una aguja estéril para aliviar las molestias del paciente (fig. 2).
El paciente fue citado nuevamente a control, observándose resolución completa del cuadro.
DiscusiónLa LMC corresponde a una zoonosis cuyo hospedero son gatos y perros, quienes albergan la forma adulta de la larva en el intestino. Las heces de estos animales contienen los huevos, los que eclosionan en la tierra en donde maduran las larvas, las que ya pueden infectar a la semana de vida. En un ambiente húmedo y tibio, protegidas de la luz, las larvas pueden sobrevivir y mantener su capacidad de infectar durante meses.
De las dermatitis del viajero la LMC corresponde a la reportada con mayor frecuencia, especialmente en viajes al Caribe5. Lederman et al. revisaron las bases de datos de 31 centros centinelas de medicina tropical, observando que la LMC correspondía al 9,8% de las dermatitis del viajero, siendo especialmente frecuente en pacientes que volvían de Barbados, Jamaica y Malasia4. Caumen et al. analizaron 269 consultas por dermatitis asociadas a viajes en una unidad de medicina tropical, observando que la prevalencia de LMC llegaba al 24,9% de estas8. Otras dermatitis del viajero que le siguen en frecuencia son las infecciones cutáneas con un 7,7% a 17,8% y las picaduras de insecto con 8,2% a 9,7%, respectivamente4,8.
Para controlar el contagio de LMC los perros y los gatos deben ser desparasitados regularmente. Sin embargo, esto resulta difícil, ya que esta infección es endémica de países en vías de desarrollo, lo que generalmente se asocia a déficit de los sistemas sanitarios veterinarios y gran cantidad de animales callejeros.
En su mayoría, los casos descritos de LMC corresponden a viajeros que visitan zonas endémicas. García-Fernández et al. describieron un caso en Perú de un paciente que había viajado al Caribe7. En España Sabat et al. describieron una serie de 8 pacientes con LMC, 7 de los cuales tenían el antecedente de haber viajado a países tropicales como México, Brasil y Tailandia6.
Hasta la fecha el único caso descrito en un paciente chileno ha sido reportado por Kolbach et al. Ellos presentaron el caso de un adulto con LMC quien se contagió en un viaje a Brasil9.
Si bien es infrecuente, se han descrito casos de pacientes sin antecedentes de viajes a zonas endémicas. Klosey et al. publicaron 3 casos de pacientes contagiados en Alemania10, Beattiey et al. presentaron un caso de LMC en Escocia, quien no había salido del país en 3 años11, Patterson et al. describieron el caso de un niño contagiado en Inglaterra, quien tenía perros no desparasitados12, y Tamminga y et al. presentaron un paciente noruego quien adquirió la infección tras un viaje a Francia13.
Entre los factores de riesgo comunes a todos estos casos se encontraban el haber estado en playas o lagos locales, clima caluroso y contacto con perros no desparasitados14.
Hasta la fecha no se han reportado casos de pacientes chilenos infectados en territorio nacional9. Sin embargo, la presencia de larvas de LMC ha sido descrita a lo largo del país. Mercado et al. estudiaron la presencia de larvas en muestras fecales de perros obtenidas en parques públicos de Chile. Se tomaron un total de 600 muestras en 13 ciudades a lo largo del país. Las muestras se procesaron y estudiaron con el método Harada-Mori15, en el que se reproduce parte del ciclo del parásito, para luego observarlo al microscopio. En este estudio se evidenció la presencia de larvas de Ancylostomatidae en 8 ciudades, con una frecuencia que variaba entre el 2% y el 40%, encontrándose la mayor proporción en la ciudad de Temuco16.
En estudios similares realizados en Brasil se encontraron huevos de Ancylostoma en el 56,8% de las muestras obtenidas en parques públicos17. A su vez, en otro estudio se observó que las muestras obtenidas llegaban a ser positivas en hasta el 85% para muestras de tierra y en el 99% para muestras de heces respectivamente18.
De lo anterior se concluye que la presencia de estos parásitos es alta, tanto en países donde la infección es endémica como en países como el nuestro. Sin embargo, es probable que las características propias del clima, así como de los hábitos de las personas (caminar descalzo, utilizar menos cantidad de ropa, etc.) expliquen en parte las diferencias en el número de casos reportados.
La presencia de bulas en pacientes con LMC, tal como ocurrió en nuestro paciente, ha sido descrita previamente. El desarrollo de estas puede observarse hasta en un 15% de los casos, generalmente posterior al tratamiento19. Si bien su patogenia es desconocida, se ha postulado que pudiesen corresponder a una reacción de hipersensibilidad retardada producida por liberación de antígenos de la larva, o que serían secundarias a la liberación de enzimas líticas del parásito. También se ha descrito que podrían ocurrir como manifestación de una dermatitis de contacto irritativa secundaria al uso de tratamientos tópicos20,21. En nuestro paciente no se utilizaron tratamientos tópicos, por lo tanto no se puede descartar que esta bula haya ocurrido por alguna de las otras causas.
Si bien la LMC tiende a la resolución espontánea, generalmente se indica tratamiento debido a las molestias que produce.
Durante mucho tiempo el uso de albendazol oral en sus diferentes esquemas fue considerado como terapia de primera línea, ya que alcanza tasas de curación cercanas al 100%. Este se encuentra disponible en Chile en presentación de jarabes y comprimidos. Sin embargo, en los últimos años diversos estudios han propuesto el uso de ivermectina como terapia de elección para el tratamiento de LMC. Esto es debido a que su uso que se ha asociado con menor número de efectos adversos, y a que puede ser utilizada en niños a partir de los 2 años1,22.
La ivermectina se ha usado en dosis de 200μg/kg por una vez, esquema que alcanza una tasa de curación de entre el 77% al 100%23. En los casos en los cuales no haya habido respuesta el tratamiento se puede repetir a los 10 días. Este fármaco actúa uniéndose a los canales de iones cloruro de las células nerviosas y musculares de la larva, produciendo una hiperpolarización, lo que provoca parálisis y muerte del parásito24. Su uso está aprobado a partir de los 2 años o en niños que pesen más de 15kg, ya que en lactantes menores la barrera hematoencefálica pudiese estar menos desarrollada, permitiendo el paso del fármaco al sistema nervioso central24. Sin embargo, y a pesar de no estar aprobada aún, ha sido utilizada de forma exitosa en lactantes, en quienes no se reportaron efectos adversos23,25,26. No obstante, aún faltan estudios que certifiquen la seguridad de ivermectina en niños pequeños.
El uso de albendazol tópico es una opción para aquellos pacientes quienes no pueden recibir terapias sistémicas o en el caso de lesiones pequeñas27. Sin embargo, este no se encuentra disponible en Chile.
También ha sido descrito el uso de crioterapia con nitrógeno líquido. Sin embargo, no se recomienda su uso en niños debido a que la larva puede encontrarse a centímetros de la lesión visible, asociado al dolor que produce esta técnica y a la posibilidad de dejar cicatrices27.
ConclusiónLa LMC es una zoonosis descrita principalmente en habitantes de países en donde la infección es endémica y en turistas quienes visitan zonas tropicales. Si bien se ha descrito la presencia de huevos y larvas de LMC en diferentes parques a lo largo del país, en nuestro conocimiento y hasta la fecha no se han descrito otros casos de LMC en niños adquirida en Chile.
Esto sugiere que debemos sospechar el diagnóstico de LMC en un paciente con clínica característica, a pesar de no tener antecedentes de viaje a zonas endémicas.
Por lo anterior, es importante educar a la población sobre la tenencia responsable de mascotas, y a partir de esto implementar medidas de prevención tales como la desparasitación de animales y mejoras en el saneamiento ambiental.
Conflicto de interesesEste trabajo cumple con los requisitos sobre consentimiento/asentimiento informado, comité de ética, financiación, estudios animales y sobre la ausencia de conflicto de intereses según corresponda.