Identificar las características de las guías de práctica clínica publicadas para el manejo del cáncer epitelial de ovario que sugieren una buena calidad metodológica.
Materiales y métodosRevisión de la literatura. Se identificaron 25 guías de práctica clínica de cáncer epitelial de ovario en diferentes bases de datos (MEDLINE, Guidelines International Network, National Guidelines Clearinghouse) publicadas entre 2007 a 2014. Se evaluó la calidad de las guías con la herramienta Appraisal of Guidelines Research and Evaluation II. Se realizaron análisis descriptivos y bivariados para evaluar la asociación entre la calidad de las guías y algunas características de las mismas y de sus desarrolladores.
ResultadosEl 48% de las guías fueron calificadas como de baja calidad. Las sociedades científicas o centros independientes, y la financiación privada o la baja notificación en el origen de la financiación, estuvieron estadísticamente asociados con una menor calidad de las guías de práctica clínica (p<0,01). Las guías desarrolladas por programas nacionales de guías tuvieron una mediana de puntuación consistentemente superior en todos los dominios del Appraisal of Guidelines Research and Evaluation II, siendo significativas las diferencias en la definición de alcance y objetivos, la participación de los grupos de interés, el rigor metodológico en la elaboración y la aplicabilidad al contexto.
ConclusionesCaracterísticas como la naturaleza del desarrollador y la financiación de la guía son predictores de calidad que deben ser considerados con antelación al uso de las recomendaciones de un documento de referencia.
To identify the characteristics of the published clinical practice guidelines for the management of epithelial ovarian cancer that suggest a good methodological quality.
Material and methodsA literature review was performed on 25 clinical practice guidelines for epithelial ovarian cancer that were identified in different databases (MEDLINE, Guidelines International Network, National Guidelines Clearing house) published between 2007 and 2014. The quality of the guidelines was evaluated using the Appraisal of Guidelines Research and Evaluation II tool. Descriptive and bivariate analyses were performed to assess the association between the quality of the guidelines and of some of their features and their developers.
ResultsJust under half (48%) of the guidelines were rated as low quality. Scientific societies or independent centres and private funding, or under-reporting the source of funding, were statistically associated with lower quality of clinical practice guidelines (P<.01). The guidelines developed by National Program Guidelines had a median of consistently higher scores in all domains of the Appraisal of Guidelines Research and Evaluation II, with significant differences in the definition of scope and objectives, the participation of stakeholders, the methodological rigour of development, and applicability to the context.
ConclusionsFeatures such as the nature of the developer and funding of the guidelines are predictors of quality that should be taken into account prior to the use of the recommendations of a document.
El cáncer de ovario fue el séptimo cáncer más común en mujeres mundialmente en el año 2012. Aproximadamente 17.921 nuevos casos fueron diagnosticados en Latinoamérica en este periodo, lo cual representó una incidencia en Sudamérica de 5,8 casos por cada 100.000 mujeres1. Según cifras reportadas por el Instituto Nacional de Cancerología en Colombia, se presentaron aproximadamente 1.691 casos anuales de cáncer de ovario durante el periodo 2002-2006, con una tasa de incidencia anual ajustada por edad de 7,9 por 100.000 y una tasa de mortalidad de 3,2 por 100.000 en 20112. De acuerdo a las predicciones elaboradas por el GLOBOCAN project de la Organización Mundial de la Salud respecto al año 2015, se estimaron 1.577 casos nuevos1. El cáncer epitelial de ovario (CEO) predomina en el 90% de los casos de cáncer de ovario y su incidencia aumenta con la edad, ocurriendo la mitad de las veces en mujeres mayores de 65 años3,4.
Desde la década de los años noventa, programas nacionales de guías, sociedades científicas y otras instituciones de salud han realizado esfuerzos importantes para desarrollar guías de práctica clínica (GPC) en aspectos tan variados como la detección temprana, diagnóstico clínico, tratamiento, seguimiento y manejo paliativo del cáncer de ovario. No obstante, dado el esfuerzo de colaboraciones como Appraisal of Guidelines for Research and Evaluation (AGREE) y ADAPTE collaboration por unificar las metodologías para el desarrollo de guías, se ha observado una heterogeneidad considerable en los métodos y calidad de las GPC publicadas5.
Las GPC son instrumentos que favorecen la toma de decisiones clínicas con el fin de mejorar la calidad de la atención en los pacientes, por lo cual deben ser desarrolladas mediante una metodología estructurada, apropiada y explícita para identificar la mejor evidencia disponible, lo cual permita obtener los desenlaces clínicos deseados6. Se ha sugerido que los beneficios potenciales de las GPC se relacionan con su calidad7; cuando las guías carecen de un rigor metodológico adecuado durante su elaboración no es posible garantizar la calidad de la información analizada y de las recomendaciones elaboradas5,8,9, incluso se considera que la calidad influye negativamente en la efectividad final de las recomendaciones y su impacto en el cuidado de los pacientes10. La adopción de guías con validez cuestionable posiblemente lleve a la realización de intervenciones poco efectivas, ineficientes y que pueden afectar la seguridad de los pacientes11,12. En este sentido, la evaluación de la calidad de las guías publicadas adquiere una relevancia especial en la selección de GPC fuente para los procesos de adopción, adaptación e implementación de sus recomendaciones en un contexto determinado11.
Algunas características de los desarrolladores de las GPC y de la metodología empleada para su elaboración influyen en el nivel de calidad final de las guías. Las GPC de buena calidad se caracterizan por unos objetivos y alcance bien definidos, una estrategia estructurada, documentada y reproducible de búsqueda y selección de la evidencia, un proceso explícito de evaluación de calidad y síntesis de la evidencia y unos métodos específicos para la formulación de las recomendaciones que en general involucran las decisiones y preferencias de los usuarios finales6. El desarrollo y financiación por entidades gubernamentales, privadas o programas especializados en guías, son factores que pueden influir en la calidad13. La colaboración AGREE define la calidad de una GPC como la confianza en que los sesgos potenciales de su desarrollo han sido resueltos de forma adecuada y que las recomendaciones son válidas internamente y aplicables a la práctica habitual14. Para evaluar la calidad de las guías publicadas la colaboración AGREE diseñó un instrumento estandarizado aceptado internacionalmente, el cual permite mediante la evaluación de 6 dominios clasificar los documentos analizados y evidenciar las áreas de mayor compromiso de la calidad durante su desarrollo7.
El crecimiento acelerado de información en la actualidad demanda que los profesionales de salud reconozcan características que se relacionan con la calidad de la evidencia que leen, las cuales les permiten anticipar las fuentes de evidencia con buena calidad para sus procesos de adaptación o adopción de las recomendaciones. El presente trabajo resume el análisis de calidad de un grupo de GPC de CEO publicadas, y analiza un grupo de características relacionadas con la buena calidad de la notificación, juzgada mediante los métodos disponibles.
Materiales y métodosSe realizó una revisión estructurada de GPC sobre cáncer epitelial de ovario publicadas en el marco del desarrollo de una GPC con alcance nacional. Se diseñó una estrategia de búsqueda en MEDLINE y búsquedas específicas de GPC en repositorios especializados de guías, como el de la Red internacional de Guías de Práctica Clínica G-I-N y el repositorio de guías del National Guidelines Clearinghouse. Se combinaron los términos Neoplasm Ovarian, Ovary Neoplasms, Ovary Cancer, Ovarian Cancer, Cancer, Ovar*, sin restricción de fecha o idioma de publicación. De forma complementaria se incluyeron otras GPC disponibles a través de Google Académico utilizando como término adicional en español «guía de cáncer de ovario», y aquellas referenciadas en las guías encontradas (estrategia «bola de nieve») o sugeridas por expertos clínicos.
La selección inicial de las guías a partir del título fue realizada por 2 de los autores. Las discrepancias presentadas durante la selección inicial se resolvieron por acuerdo. No se evaluó el grado de concordancia entre los evaluadores. Se incluyeron guías en inglés o español dirigidas al manejo de pacientes con CEO en cualquier etapa de la historia natural de la enfermedad.
La calidad de las guías fue evaluada por 2 investigadores independientes usando el instrumento AGREE en su versión ii (AGREE II). En esta herramienta se valoran 23 ítems organizados en 6 dominios: 1) alcance y objetivo; 2) participación de los implicados; 3) rigor en la elaboración; 4) claridad de la presentación; 5) aplicabilidad; y 6) independencia editorial7. Cada evaluador asignó a cada ítem una puntuación entre 1 y 7, siendo 1 «Totalmente en desacuerdo» y 7 «Completamente de acuerdo» con el planteamiento de cada ítem. La ponderación de las calificaciones de los 2 evaluadores se realizó de acuerdo al manual de la herramienta, obteniendo un porcentaje final agregado para cada uno de los 6 dominios, donde 0% es «mal desempeño» y 100% el mejor desempeño7. Además de la calificación de cada dominio, uno de los autores extrajo de la información publicada en cada guía un grupo de características generales.
Para definir la calidad de las guías evaluadas se empleó un punto de corte basado en el rigor metodológico, acorde con lo sugerido por la guía metodológica para la elaboración de GPC en Colombia15. Se definió una guía de buena calidad como aquella con una puntación igual o superior al 60% en el dominio 3. Se realizaron análisis descriptivos de frecuencias absolutas y relativas para las variables categóricas, y mediana y rango intercuartílico para las variables cuantitativas. Se realizaron análisis bivariados para evaluar la asociación entre la calidad de las notificaciones de las guías y diferentes variables, así como la relación entre el tipo de desarrollador y la puntuación obtenida en los 6 dominios de la herramienta. Para realizar estas comparaciones se usó el test exacto de Fisher para proporciones, y para la comparación de medianas se comprobó previamente la normalidad de la distribución de las variables mediante inspección visual y la prueba de Shapiro Wilk; las variables continuas evaluadas presentaron una distribución no paramétrica, por lo que se emplearon las pruebas U de Mann Whitney y Kruskall-Wallis, según el número de grupos a comparar.
ResultadosFueron analizados 36 documentos identificados como GPC; un total de 25 guías de CEO fueron evaluadas con la herramienta AGREE II3,4,16–38.
Características generales y calidad de las guías de práctica clínicaEn la tabla 1 se describen las características generales de las GPC evaluadas. Solo 2 de las 25 guías evaluadas fueron publicadas en español. Para el caso del cáncer de ovario el 60% de las GPC provenían de programas nacionales de guías, y el 88% fueron desarrolladas para un alcance nacional en el país de origen. Doce guías evaluadas fueron financiadas con recursos públicos.
Características generales y calidad de las guías de práctica clínica en cáncer de ovario
| Características | n=25 | % |
|---|---|---|
| Origen | ||
| Norteamérica | 12 | 48 |
| Europa | 9 | 36 |
| Oceanía | 3 | 12 |
| Latinoamérica | 1 | 4 |
| Tipo de desarrollador | ||
| Programa nacional de guías | 15 | 60 |
| Sociedad científica | 8 | 32 |
| Centro de investigación u hospital | 2 | 8 |
| Alcance | ||
| Nacional | 22 | 88 |
| Internacional | 3 | 12 |
| Métodos para el desarrollo | ||
| De novo | 15 | 60 |
| Adaptación/adopción | 10 | 40 |
| Fuente de financiación | ||
| Pública | 12 | 48 |
| Privada | 3 | 12 |
| No reporta | 10 | 40 |
| Reporta conflicto de interesesa | ||
| No reporta | 12 | 48 |
| No declara la existencia de conflicto de intereses | 7 | 28 |
| Declara la existencia de conflicto de intereses | 6 | 24 |
| Reportan nivel de evidencia en las recomendaciones | ||
| Sí | 12 | 48 |
| No | 13 | 52 |
| Formulación de recomendaciones | ||
| Centradas en evidencia | 12 | 48 |
| Centradas en consenso | 3 | 12 |
| No responde | 10 | 40 |
| Calidad de las guíasb | ||
| Alta calidad | 13 | 52 |
| Baja calidad | 12 | 48 |
| Bases de datos consultadas por las guías | ||
| MEDLINE | 17 | 68 |
| Cochrane | 12 | 48 |
| EMBASE | 9 | 36 |
| National Guidelines Clearinghouse | 6 | 24 |
| CINALH | 4 | 16 |
| Health Technology Assessment Database | 3 | 12 |
| Economic evaluations database | 3 | 12 |
| Dare | 2 | 8 |
| National Library for Health | 2 | 8 |
| PSYINFO | 2 | 8 |
| Lilacs | 1 | 4 |
| Vigencia a la publicación (años)c | ||
| 0 | 3 | 12 |
| 1 | 10 | 40 |
| 2 | 2 | 8 |
| 3 | 2 | 8 |
| No se reporta | 8 | 32 |
Notificación de conflicto de intereses. No reporta (no existe información en el documento), no declara (se reporta en el documento que no existe conflicto de intereses), declara conflicto de intereses (se reporta en el documento la presencia de conflicto de intereses).
En relación con los métodos empleados en su elaboración, el desarrollo de novo guarda una relación 3 a 2 con respecto a la adaptación de guías. Doce de las guías evaluadas fueron calificadas como de baja calidad acorde con el rigor en su elaboración. La notificación de información sobre conflicto de intereses se encontró en 13 de las guías evaluadas, 6 de las cuales reportaron la existencia de algún conflicto en los integrantes del grupo desarrollador.
Las bases de datos consultadas con mayor frecuencia como fuente de evidencia fueron: Medline (17 de 25), Cochrane (12 de 25) y Embase (9 de 25). Ocho guías no notificaron la fecha de última búsqueda. Solo 3 de las 25 GPC evaluadas fueron publicadas en el mismo año de su elaboración, y 10 en el año siguiente.
La financiación pública de las guías fue más frecuente en Europa (5 de 9) y Oceanía (3/3). Las GPC de Canadá e Inglaterra fueron desarrollos en el marco de programas nacionales de guías, con 5 de 6 y 4 de 5 guías respectivamente.
De las guías elaboradas por sociedades científicas 5 de 8 fueron adaptaciones/adopciones, en contraste con el predominio de desarrollos de novo en los programas nacionales de guías (10 de 15).
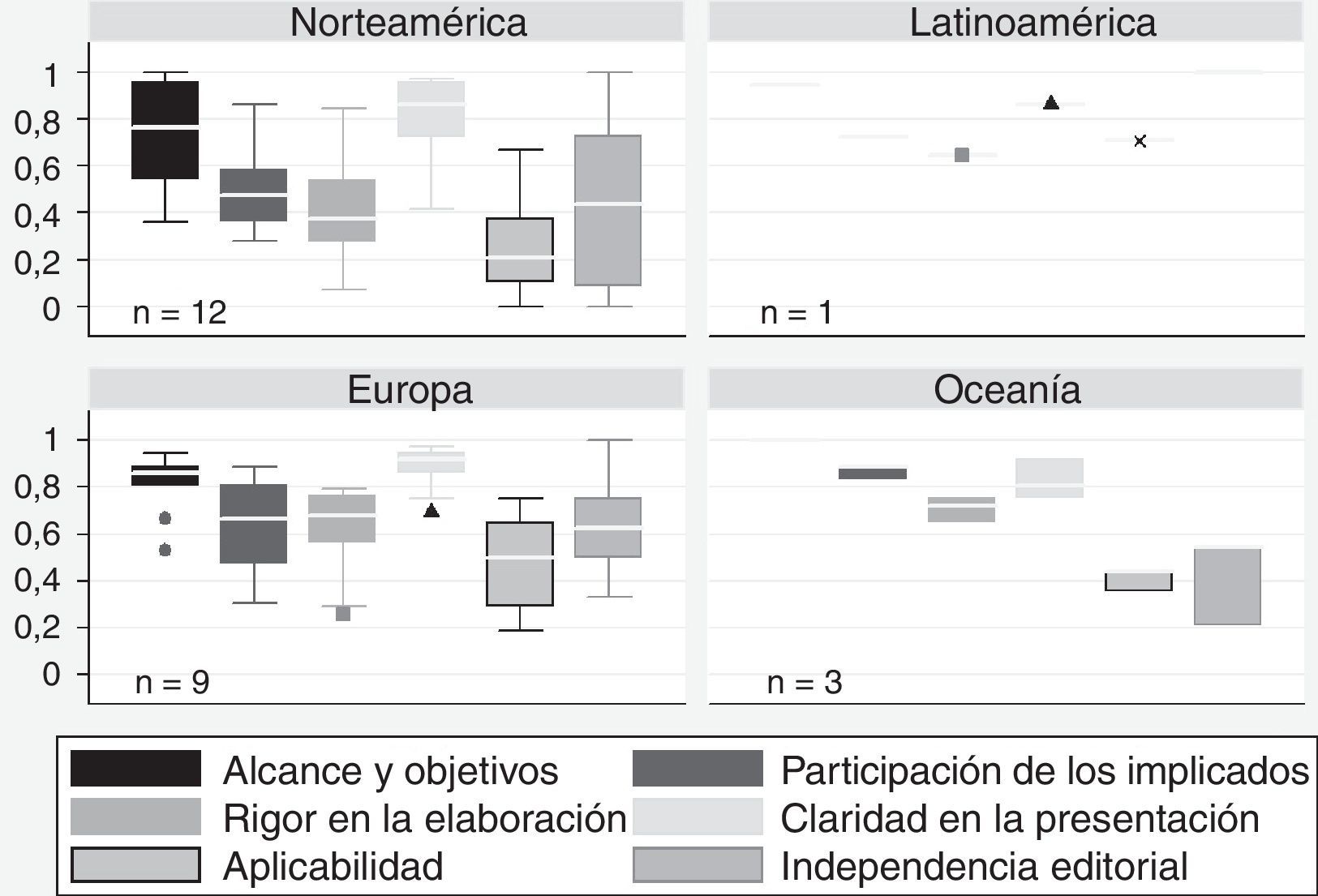
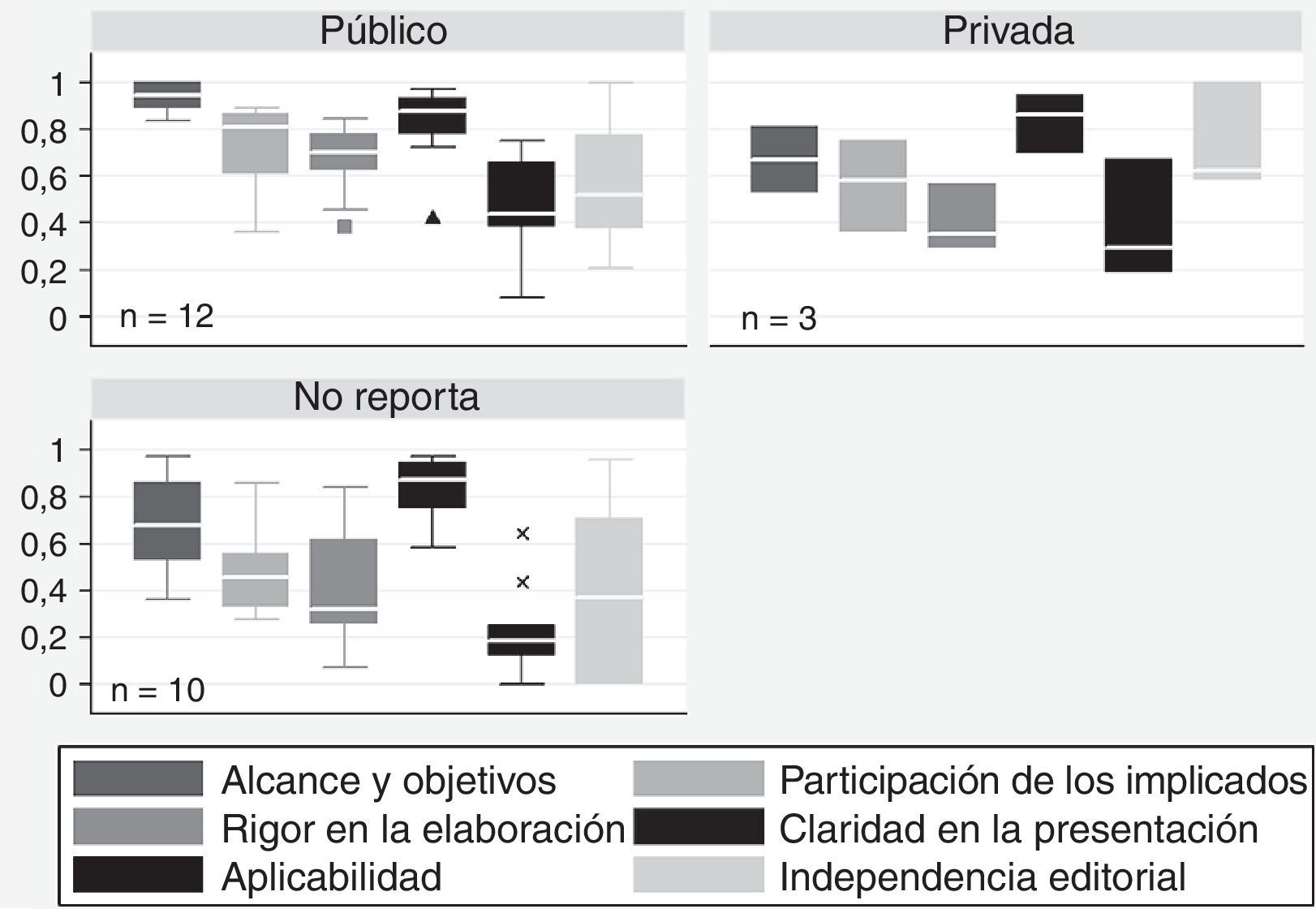
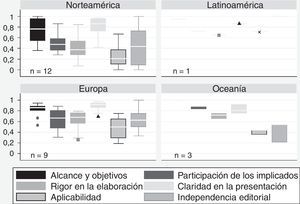
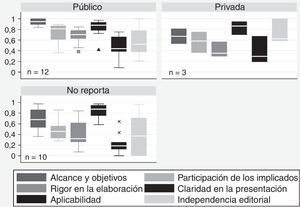
La puntuación obtenida por las GPC en cada dominio de la herramienta AGREE II y la proporción de guías que obtuvieron un alto nivel de calidad se presentan en la tabla 2. Las GPC de origen norteamericano presentaron un menor desempeño en la mayoría de los dominios del AGREE II, en comparación con Europa y Oceanía (fig. 1). Aunque las guías europeas mostraron el mejor desempeño en todos los dominios, las puntuaciones de aplicabilidad al contexto e independencia editorial fueron consistentemente bajas, independientemente del origen de los documentos evaluados. La figura 2 muestra un mejor desempeño en los dominios del AGREE II para las guías financiadas con recursos públicos. El dominio claridad de la presentación no varió según el tipo de financiación de la guía.
Calificación obtenida por las guías en cada dominio de la herramienta AGREE II
| Dominios herramienta AGREE II | GPC alta puntuación n=25 (100%)a | Mediana (rango) puntuación |
|---|---|---|
| Dominio «alcance y objetivo» | 20 (80) | 86,1 (36,1-100) |
| Dominio «participación de los implicados» | 11 (44) | 58,3 (27,8-88,9) |
| Dominio «rigor en la elaboración» | 13 (52) | 60,4 (7,3-84,4) |
| Dominio «claridad de la presentación» | 23 (92) | 86,1 (41,7-97,2) |
| Dominio «aplicabilidad» | 6 (24) | 35,4 (0-75) |
| Dominio «independencia editorial» | 9 (36) | 54,2 (0-100) |
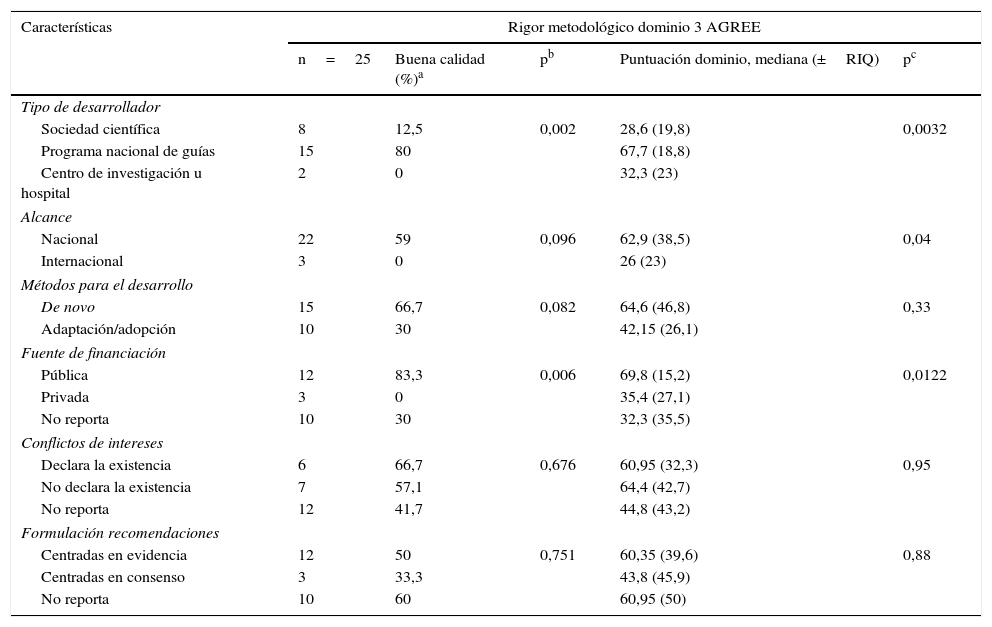
Cuando se analizaron los factores asociados con la baja calidad de 12 de las 25 guías evaluadas se evidenció que el tipo de desarrollador sociedad científica o centro independiente (p<0,01) y la financiación privada o la baja notificación en el origen de la financiación (p<0,01) parecen factores asociados con una menor calidad de las guías (tabla 3). El alcance internacional de las guías también resultó ser un factor asociado a la baja calidad al analizarlo como una variable continua; sin embargo, al evaluarlo como una variable dicotómica, la poca cantidad de guías de alcance nacional influyó en el resultado y este no fue significativo.
Factores asociados con buen rigor metodológico en las guías de práctica clínica en cáncer de ovario
| Características | Rigor metodológico dominio 3 AGREE | ||||
|---|---|---|---|---|---|
| n=25 | Buena calidad (%)a | pb | Puntuación dominio, mediana (±RIQ) | pc | |
| Tipo de desarrollador | |||||
| Sociedad científica | 8 | 12,5 | 0,002 | 28,6 (19,8) | 0,0032 |
| Programa nacional de guías | 15 | 80 | 67,7 (18,8) | ||
| Centro de investigación u hospital | 2 | 0 | 32,3 (23) | ||
| Alcance | |||||
| Nacional | 22 | 59 | 0,096 | 62,9 (38,5) | 0,04 |
| Internacional | 3 | 0 | 26 (23) | ||
| Métodos para el desarrollo | |||||
| De novo | 15 | 66,7 | 0,082 | 64,6 (46,8) | 0,33 |
| Adaptación/adopción | 10 | 30 | 42,15 (26,1) | ||
| Fuente de financiación | |||||
| Pública | 12 | 83,3 | 0,006 | 69,8 (15,2) | 0,0122 |
| Privada | 3 | 0 | 35,4 (27,1) | ||
| No reporta | 10 | 30 | 32,3 (35,5) | ||
| Conflictos de intereses | |||||
| Declara la existencia | 6 | 66,7 | 0,676 | 60,95 (32,3) | 0,95 |
| No declara la existencia | 7 | 57,1 | 64,4 (42,7) | ||
| No reporta | 12 | 41,7 | 44,8 (43,2) | ||
| Formulación recomendaciones | |||||
| Centradas en evidencia | 12 | 50 | 0,751 | 60,35 (39,6) | 0,88 |
| Centradas en consenso | 3 | 33,3 | 43,8 (45,9) | ||
| No reporta | 10 | 60 | 60,95 (50) | ||
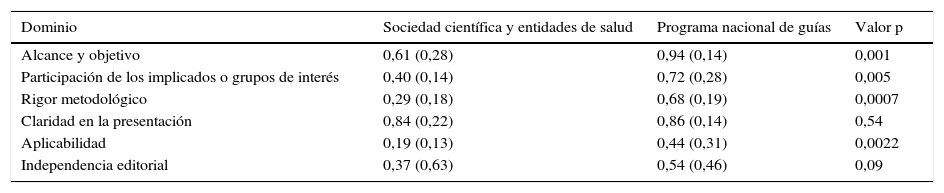
Aquellas guías desarrolladas por un programa nacional de guías organizado tuvieron una mediana de puntuación de calidad consistentemente superior en todos los dominios del AGREE II, siendo estadísticamente significativas las diferencias en la definición de alcance y objetivos, la participación de los grupos de interés, el rigor en la elaboración y la aplicabilidad al contexto local colombiano (tabla 4). La claridad en la presentación no fue un dominio que se afectara por el tipo de desarrollador.
Asociación entre el tipo de desarrollador y el nivel de calidad de las guías de práctica clínica en cáncer de ovario
| Dominio | Sociedad científica y entidades de salud | Programa nacional de guías | Valor p |
|---|---|---|---|
| Alcance y objetivo | 0,61 (0,28) | 0,94 (0,14) | 0,001 |
| Participación de los implicados o grupos de interés | 0,40 (0,14) | 0,72 (0,28) | 0,005 |
| Rigor metodológico | 0,29 (0,18) | 0,68 (0,19) | 0,0007 |
| Claridad en la presentación | 0,84 (0,22) | 0,86 (0,14) | 0,54 |
| Aplicabilidad | 0,19 (0,13) | 0,44 (0,31) | 0,0022 |
| Independencia editorial | 0,37 (0,63) | 0,54 (0,46) | 0,09 |
Comparación de medianas de la puntuación de calidad metodológica mediante la prueba U de Mann Whitney.
El tipo de organización implicada en el desarrollo de las GPC y su fuente de financiación resultaron predictores de la calidad metodológica y de la notificación de información en las guías. Los resultados obtenidos sugieren que los programas nacionales de guías y las organizaciones con financiación pública desarrollan guías de calidad superior.
Los programas especializados en el desarrollo de GPC disponen de un personal capacitado para brindar apoyo a los paneles de expertos clínicos durante el proceso de desarrollo, formulación y redacción de guías; además, suelen contar con amplios presupuestos financiados por el gobierno, lo cual permite la elaboración de guías de buena calidad13. Estas organizaciones orientan el desarrollo de sus guías en función de las directrices definidas en la herramienta AGREE II39. Diferentes estudios han obtenido hallazgos similares: las guías procedentes de sociedades científicas o centros privados suelen presentar puntuaciones significativamente menores en la mayoría de los dominios del AGREE II, principalmente en el rigor metodológico por la falta de adherencia a los métodos para el desarrollo de guías o ausencia de dicha información en la notificación12,13,40. Las guías desarrolladas por paneles de expertos también presentan diferencias estadísticamente significativas respecto a las GPC basadas en evidencia en relación con el rigor de la elaboración41.
Los países con sistemas de salud que disponen de autoridades especiales para el desarrollo o regulación de GPC diseñan guías que cumplen rigurosos estándares metodológicos, por lo que su calidad suele ser superior. Algunos ejemplos de dichas instituciones son NICE y SIGN en Inglaterra y Escocia, y el National Health and Medical Research Council en Australia. Las guías europeas generalmente son desarrolladas por instituciones de carácter público, mientras que en Estados Unidos numerosas guías son elaboradas por las sociedades médicas12.
Actualmente existe incertidumbre sobre si la calidad metodológica y de la notificación de las guías asegura la validez de las recomendaciones clínicas. Es posible que una GPC bien documentada contenga recomendaciones erróneas, y por el contrario, una guía que no sea desarrollada sistemáticamente, o tenga una notificación inadecuada de información, proporcione recomendaciones sólidas, consistentes con la evidencia42. Una calificación alta obtenida por una GPC evaluada con AGREE II no garantiza que sus recomendaciones sean excelentes, ya que esta herramienta evalúa principalmente el proceso metodológico y la exhaustividad en la notificación de información, mas no el contenido o idoneidad de las recomendaciones clínicas43,44. Demostrar el impacto entre el rigor metodológico y la validez de las recomendaciones es de crucial importancia para esfuerzos futuros de generación de GPC, pues los 3 métodos (desarrollo con altos estándares metodológicos, adaptación sistemática y desarrollo no sistemático) difieren considerablemente en el tiempo y recursos requeridos45. Se considera que la descripción de las fortalezas y debilidades del cuerpo de la evidencia de las GPC puede ser un precursor de la validez e idoneidad de las recomendaciones, sin embargo, el consorcio AGREE priorizará este asunto próximamente en la iniciativa de AGREE A343.
Al evaluar la calidad metodológica de las GPC adaptadas se obtienen puntuaciones inferiores respecto a las guías con desarrollo de novo. Esta diferencia puede ser explicada por la falta de ítems específicos del instrumento AGREE II para evaluar la calidad de las GPC creadas por adaptación, proceso cuya metodología es distinta a un desarrollo de novo7. La metodología de adaptación cuenta desde 2010 con el soporte metodológico de la colaboración ADAPTE y el grupo de trabajo de G-I-N, quienes han refinado el proceso y han brindado apoyo y entrenamiento a los grupos interesados en el tema. La adaptación de GPC de alta calidad es recomendable debido a que es un proceso menos costoso, que requiere menor tiempo, reduce la duplicación de esfuerzos y permite mejorar los aspectos de aplicabilidad en el contexto en comparación con un desarrollo de novo46.
Es posible que esta revisión presente un potencial sesgo de publicación al incluir pocas guías realizadas en Latinoamérica, debido a que la búsqueda se realizó en bases de datos y grandes repositorios de GPC en idioma inglés y no en LILACS. Otra posible limitación del estudio se relaciona con la falta de información en el 40% de las guías respecto al tipo de financiación y el número reducido de guías de financiación privada, lo cual impide establecer afirmaciones concluyentes respecto a la asociación entre la financiación pública y la buena calidad de las GPC.
De acuerdo a los resultados obtenidos, las GPC presentan ciertas características que podrían permitir deducir su calidad como el tipo de desarrollador de la guía, su fuente de financiación y la disponibilidad de información respecto a la metodología empleada. Es recomendable que las GPC elaboradas por sociedades científicas o instituciones privadas incluyan en su notificación las estrategias de búsqueda, el proceso de selección de la literatura, tablas de evidencia y el acceso a documentos o anexos electrónicos, con el fin de mejorar su calidad y confiabilidad respecto a las recomendaciones emitidas; sin embargo, también se sugiere que estas organizaciones se adhieran a un programa coordinado y estructurado para el desarrollo de GPC, asegurando la publicación de guías de alta calidad.
Aunque aún no existan estudios concluyentes respecto a la relación de la calidad metodológica de las GPC, la calidad de las recomendaciones finales y su impacto en la práctica, existe un acuerdo general en que la evaluación de calidad de las guías es una herramienta que permite seleccionar mejor las guías a ser utilizadas en la práctica clínica, las cuales permitan mejorar la calidad de la atención y hacer un uso eficiente de los servicios de salud.
Es pertinente diseñar un instrumento que evalúe principalmente la aplicabilidad, la calidad metodológica y la calidad de la notificación de las guías elaboradas por adaptación debido a que el proceso de desarrollo es distinto al empleado durante un desarrollo de novo. Adicionalmente, es importante que los desarrolladores de GPC en Latinoamérica indexen sus guías en bases de datos reconocidas internacionalmente como G-I-N, con el fin de reducir la barrera idiomática y facilitar el acceso de información a los profesionales en salud de esta región.
Declaración de cumplimiento de estándares de publicaciónLa presente investigación, por su naturaleza documental, se categoriza en la normatividad colombiana como investigación sin riesgo. Se espera que la información presentada beneficie a los profesionales de salud que consultan permanentemente las GPC disponibles para la toma de decisiones en pacientes con cáncer de ovario.
Declaración de transparenciaEl manuscrito representa un registro honesto, preciso y transparente de los resultados encontrados; no se han omitido aspectos importantes que puedan cambiar el sentido y significado de las conclusiones.
FinanciaciónEsfuerzo propio de los autores y del Instituto IECAS.
Conflicto de interesesLos autores declaran la no existencia de conflicto de intereses que pueda afectar el presente estudio.
Agradecemos el apoyo de la Asociación Colombiana de Ginecólogos Oncólogos, en especial el de los doctores Heydi Ramírez, Jesús Acosta, Mauricio González, Robinson Fernández, Jaime Fernando Ruiz y Daniel Sanabria, por su participación en el proceso de evaluación de calidad de las guías de práctica clínica.