La espectrometría de masas (EM) (matrix assisted laser desorption ionization-time of flight) MALDI-TOF demostró ser una herramienta robusta para la identificación de numerosos grupos taxonómicos. No obstante, presenta limitaciones. Una ventaja clave de la técnica es la flexibilidad para la incorporación de espectros proteicos de microorganismos ausentes en la base de datos comercial. Dada la prevalencia de Burkholderia contaminans en los pacientes fibroquísticos en Argentina, y a que en ellos es crucial el diagnóstico microbiológico rápido y confiable, la EM MALDI-TOF surge como una herramienta estratégica. El objetivo del trabajo fue desarrollar una base de datos adicional con espectros peptídicos de aislamientos de referencia de B. contaminans. La misma demostró ser exitosa para la identificación del 97% de los aislamientos analizados. Por lo cual la EM MALDI-TOF con la base de datos extendida resultó ser una herramienta útil para la identificación y diferenciación de otras especies relacionadas a B. contaminans.
MALDI-TOF (matrix assisted laser desorption ionization-time of flight) mass spectrometry (MS) proved to be a robust tool for the identification of numerous taxonomic groups. However, it has limitations. A key advantage of this technique is the flexibility for the incorporation of protein profiles of microorganisms not included in the commercial database. Due to the prevalence of Burkholderia contaminans in fibrocystic patients in Argentina and the fact that rapid and reliable microbiological diagnosis is crucial in them, MALDI-TOF MS emerges as a strategic tool. The aim of this work was to develop an additional database with peptide spectra of reference isolates of B. contaminans. This database demonstrated to be successful for the identification of 97% of the isolates analyzed. Therefore, MALDI-TOF MS with the extended database was a useful tool for the identification and differentiation of other related species to B. contaminans.
Las bacterias que conforman el complejo Burkholderia cepacia (CBC) son patógenos oportunistas capaces de causar enfermedad en plantas, humanos y animales5. En el hombre pueden establecer infecciones crónicas y frecuentemente graves, por lo general en pacientes fibroquísticos y en inmunocomprometidos4. Burkholderia contaminans tiene una baja prevalencia en pacientes con fibrosis quística alrededor del mundo, excepto en Argentina, España y Portugal3. Un estudio de 2013, que incluyó un grupo de 66 pacientes fibroquísticos y un total de 120 aislamientos del CBC recuperados de especímenes clínicos, demostró la prevalencia en nuestro país de B. contaminans (57,6%), seguida por Burkholderia cenocepacia (15%)11. Un informe publicado en 2017, que consideró 46 pacientes fibroquísticos y 68 aislamientos del CBC, mostró nuevamente la prevalencia de B. contaminans (49%), seguida de B. cenocepacia (25%), lo cual confirma la permanencia de esta epidemiología particular con alta frecuencia de la especie B. contaminans en la Argentina3.
Dado que no es posible distinguir entre especies dentro del CBC mediante pruebas bioquímicas, es necesario recurrir a métodos de biología molecular para su correcta identificación10. Actualmente la secuenciación del gen recA es el método patrón de oro, pero este es un procedimiento caro y laborioso, por lo que no es factible su aplicación en la rutina de muchos laboratorios clínicos. En los últimos años, los laboratorios de microbiología clínica han incorporado la espectrometría de masas (EM) mediante la plataforma MALDI-TOF para la rápida identificación de bacterias, levaduras y hongos miceliales de importancia clínica7. La ionización MALDI (desorción/ionización mediante láser asistida por matriz), acoplada a un analizador TOF (tiempo de vuelo), es una técnica de ionización suave utilizada en EM, que permite el análisis de biomoléculas que tienden a fragmentarse cuando son ionizadas por un láser.
El sistema EM MALDI-TOF permite la identificación certera de algunas especies dentro del CBC y diferencia correctamente de otros géneros de bacilos gram negativos no fermentadores, pero presenta limitaciones debido a la ausencia de perfiles proteicos en su base de datos comercial de 6 especies del CBC, entre ellos, los de B. contaminans1,2,6,8. La plataforma Microflex LT (Bruker Daltonics®) permite la incorporación de espectros de referencia (main spectrum profiles [MSP]) mediante el uso de softwares específicos9.
El objetivo de este trabajo fue desarrollar una base de datos adicional con espectros peptídicos de aislamientos de referencia de B. contaminans, debido a que dicha especie no está incluida en las bases de datos comercial de la plataforma Microflex LT (Bruker Daltonics®), y evaluar su desempeño para la identificación correcta de esta especie.
Para la generación de los MSP fueron seleccionados 40 aislamientos clínicos de B. contaminans de la Colección de Cultivos del Servicio Bacteriología Especial (CCBE). Dichos aislamientos provenían de materiales respiratorios de pacientes fibroquísticos (n=22) y de otros materiales clínicos (hemocultivo y orina) de pacientes hospitalizados no fibroquísticos (n=18). Todos ellos fueron identificados previamente por secuenciación parcial del gen recA utilizando los cebadores y las condiciones descriptas en al trabajo de Mahenthiralingam et al.10; las secuencias fueron depositadas en la base de datos del GenBank® (material suplementario). Los aislamientos que estaban criopreservados en caldo tripticasa soja-glicerol al 10% a −80°C, fueron descongelados y cultivados en agar tripticasa soja con el 5% de sangre de carnero e incubados en aerobiosis a 35°C durante 24h. La generación de los perfiles proteicos fue realizada por el método de extracción proteica según lo descripto por Khot et al.7. Cada aislamiento fue analizado por octuplicado. La metodología consistió en sembrar cada pocillo de la placa de acero inoxidable (Bruker Daltonics®) con 1μl del extracto obtenido y secar a temperatura ambiente. Luego, los pocillos fueron cubiertos con 1μl de la solución de matriz orgánica HCCA (solución saturada de ácido α-ciano-4-hidroxicianocinámico con el 50% de acetonitrilo y el 2,5% de ácido trifluoroacético). Para la calibración del espectrómetro se utilizó el estándar comercial BTS (Bruker Daltonics®).
Los nuevos espectros fueron generados según el método estándar MALDI BioTyper® MSP Creation en el software FlexControl 3.4. Cada espectro fue obtenido en modo positivo lineal a través de 240 disparos del láser (6 tandas de 40 disparos; frecuencia del láser N2: 60Hz; voltaje de la fuente de iones I: 20kV; voltaje de la fuente de iones II: 16,7kV, y rango de masas del detector: 2000-20000Da). Se realizó una triple lectura de cada pocillo, generando un total de 24 espectros para cada aislamiento. El análisis de los 24 espectros crudos se efectuó con el programa FlexAnalysis 3.4 y se seleccionaron aquellos espectros con picos de alta intensidad y bajo ruido. Se utilizó un número mínimo de 20 espectros por aislamiento para generar un MSP mediante el programa MALDI Biotyper® 3.0. Para la incorporación de los MSP a la base de datos adicional, estos debían cumplir con los siguientes criterios: estar conformados por 20 a 24 espectros y tener al menos 70 picos conservados con una frecuencia mínima del 75% para cada masa. Esta nueva base de datos generada a partir de aislamientos locales de B. contaminans fue denominada RENAEM v2.0.
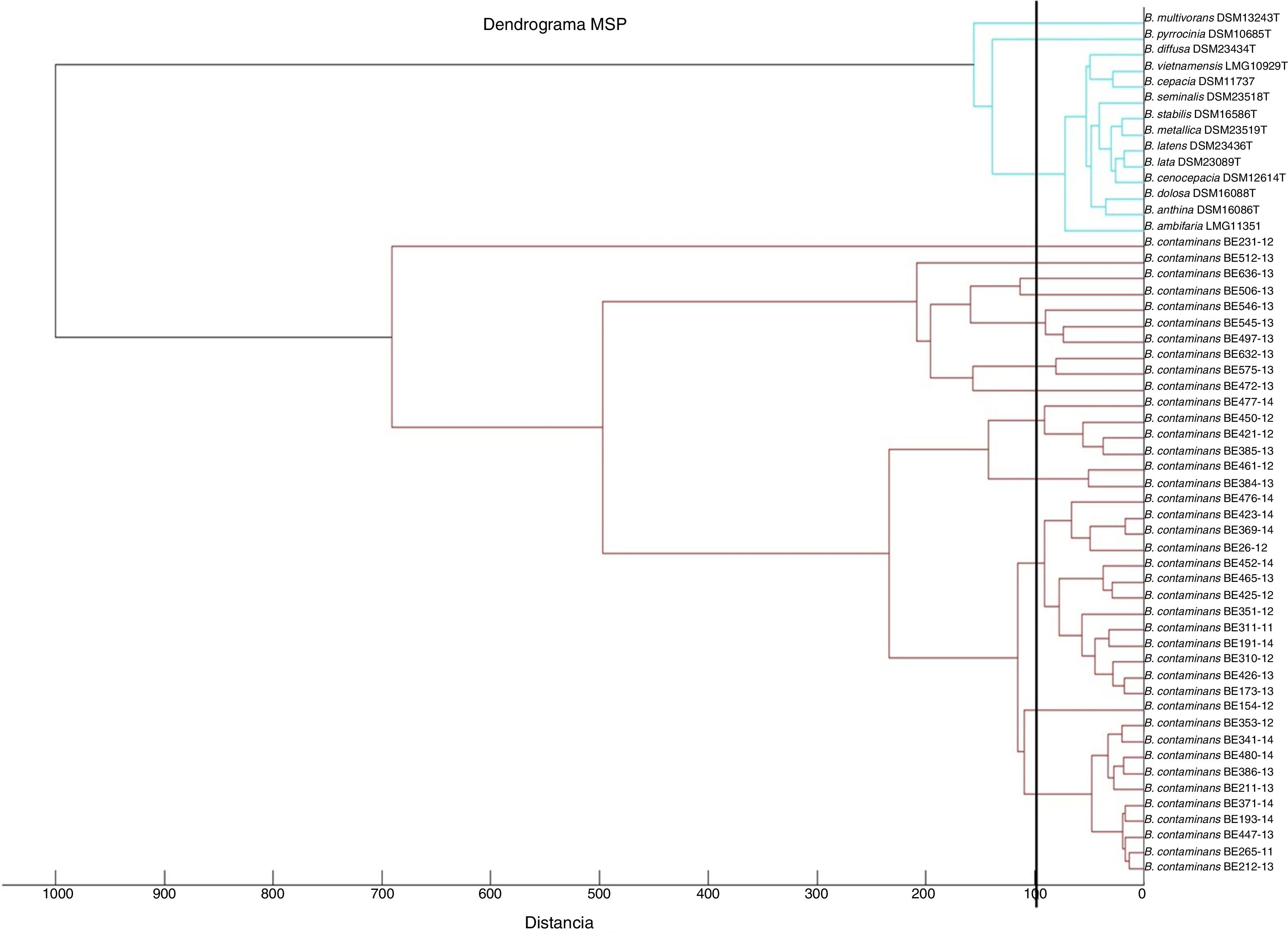
Una vez generados los 40 MSP, se construyó un dendrograma de MSP (fig. 1). Los MSP de B. contaminans no se agruparon con los de otras especies del CBC (base de datos comercial) en el punto de corte del 10% (línea vertical) en el nivel de distancia entre 0 (idéntico) y 1.000 (no relacionado). Este es uno de los criterios para la identificación confiable a nivel de especie.
En el laboratorio de referencia (LR1) fue evaluado el desempeño de EM MALDI-TOF utilizando la base de datos incluida en el MALDI Biotyper® 3.0 junto con la base complementaria RENAEM v2.0. Los aislamientos fueron procesados por el método de extendido directo. Para la identificación confiable a nivel de especie fueron considerados los siguientes criterios: valor de score mayor o igual a 2 y divergencia del 10% entre la primera y la segunda especie con mejor valor de score.
Se usó un panel de 55 aislamientos identificados por el método patrón de oro en el LR1, conformado por 30 aislamientos de B. contaminans, 15 aislamientos de B. cenocepacia, 6 aislamientos de B. cepacia, 2 aislamientos de Burkholderia gladioli, un aislamiento de Burkholderia multivorans y un aislamiento de B. seminalis. Todos los aislamientos de B. contaminans fueron identificados correctamente y cumplieron los 2 criterios de aceptación para la identificación confiable. Los 25 aislamientos de Burkholderia sp. no fueron identificados de manera errónea como B. contaminans. Por lo tanto, la incorporación de la base de datos generada in house permitió identificar de forma apropiada a la especie B. contaminans y no identificó otras especies del CBC como tal.
Luego, la base de datos RENAEM v2.0 fue transferida a un laboratorio de referencia externo (LR2), el cual seleccionó un panel de 37 aislamientos de B. contaminans identificados por secuenciación del gen recA y evaluó el desempeño de la base de datos adicional en su plataforma. Estos aislamientos fueron procesados por el método de extendido directo y se obtuvo un 94% (n=35) de identificación correcta a nivel de especie. El 6% (n=2) de los aislamientos solo pudo ser identificado como CBC debido a que no se observó el 10% de divergencia entre los scores de identificación de B. contaminans, B. cepacia y B. cenocepacia. Los 2 aislamientos no identificados fueron procesados a través del método de extendido directo con el agregado de 1μl de ácido fórmico al 70%. No se observó una mejora en la identificación.
La metodología EM MALDI-TOF presenta grandes ventajas por sobre los sistemas o algoritmos de identificación clásicos o automatizados, ya que reduce de modo sustancial el tiempo de respuesta a costos más bajos. Debido a la alta frecuencia con que B. contaminans es aislada en nuestro país, es necesaria la identificación rápida, precisa y confiable de esta especie. El diagnóstico rápido de los patógenos involucrados en las infecciones de la población fibroquística impacta directamente en el pronóstico del paciente y en el manejo terapéutico para el control de la enfermedad y la prevención de nuevas infecciones.
La base de datos adicional RENAEM v2.0 permitió la identificación confiable y reproducible en el 97% (65/67) de los aislamientos de B. contaminans analizados. Esta mejora permitió obtener resultados comparables con los obtenidos por el método de secuenciación del gen recA, pero con una reducción sustancial en tiempo, insumos, laboriosidad y costo para la obtención de resultados. Esta constituye la primera base de datos creada en Argentina para el mejoramiento de la identificación bacteriana del CBC por EM MALDI-TOF.
Debido a que la expansión de las bases de datos comerciales con espectros de proteínas de aislamientos patógenos locales es importante para mejorar la eficiencia y la utilidad de la tecnología EM MALDI-TOF, la base RENAEM v2.0 fue transferida, a través de la Red Nacional de Espectrometría de Masas (RENAEM), a todos los laboratorios de microbiología clínica del país que cuentan con esta plataforma.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.