Evaluar la seguridad y permeabilidad del tratamiento de la obstrucción del drenaje venoso hepático tras trasplante ortotópico con endoprótesis autoexpandibles. Valorar las diferencias en la respuesta en pacientes con obstrucción precoz y tardía.
Material y métodosAnálisis retrospectivo de 16 pacientes trasplantados con obstrucción del drenaje venoso hepático tratados con endoprótesis (1996-2011). El seguimiento se realizó mediante venografía/manometría, ecografía, TC y pruebas de laboratorio. Se realizó análisis estadístico descriptivo de supervivencia de pacientes e injertos, éxito técnico y clínico, recurrencia y complicaciones del total de la muestra, así como inferencial para comparar las diferencias entre pacientes con obstrucción precoz y tardía.
ResultadosLa media de seguimiento fue de 3,34 años (21-5.331 días). La tasa de éxito técnico fue del 93,7%, y la de éxito clínico, del 81,2%. La tasa de complicaciones fue del 25%. La tasa de supervivencia para pacientes fue de 87,5%, y para injertos, de 92,5%. La tasa de recurrencia fue del 12,5%. La tasa de permeabilidad primaria a los 3, 6, 12 y 60 meses fue de 0,96 (IC 95% 0,91-1), 0,96 (IC 95% 0,91-1), 0,87 (IC 95% 0,73-1) y 0,87 (IC 95% 0,73-1), respectivamente. No hubo diferencias significativas entre los pacientes con obstrucción precoz o tardía, aunque las tasas de permeabilidad primaria mostraron tendencia a ser significativamente superiores en el grupo precoz (p=0,091).
ConclusionesEl tratamiento con endoprótesis autoexpandibles en obstrucciones del drenaje venoso hepático tras trasplante ortotópico es efectivo, duradero y seguro. No hay diferencias significativas entre pacientes con obstrucción precoz y tardía.
To evaluate the safety and patency of self-expanding stents to treat hepatic venous outflow obstruction after orthotopic liver transplantation. To evaluate differences in the response between patients with early obstruction and patients with late obstruction.
Material and methodsThis is a retrospective analysis of 16 patients with hepatic venous outflow obstruction after liver transplantation treated with stents (1996-2011). Follow-up included venography/manometry, ultrasonography, CT, and laboratory tests. We did a descriptive statistical analysis of the survival of patients and stents, technical and clinical success of the procedure, recurrence of obstruction, and complications of the procedure. We also did an inferential statistical analysis of the differences between patients with early and late obstruction.
ResultsThe mean follow-up period was 3.34 years (21-5,331 days). The technical success rate was 93.7%, and the clinical success rate was 81.2%. The rate of complications was 25%. The survival rates were 87.5% for patients and 92.5% for stents. The rate of recurrence was 12.5%. The rate of primary patency was 0.96 (95% CI 0.91-1) at 3 months, 0.96 (95% CI 0.91-1) at 6 months, 0.87 (95% CI 0.73-1) at 12 months, and 0.87 (95% CI 0.73-1) at 60 months. There were no significant differences between patients with early and late obstruction, although there was a trend toward higher rates of primary patency in patients with early obstruction (P=.091).
ConclusionsTreating hepatic venous outflow obstruction after orthotopic transplantation with self-expanding stents is effective, durable, and effective. There are no significant differences between patients with early obstruction and those with late obstruction.
La técnica piggyback para hepatectomía del receptor y trasplante hepático ortotópico (THO), descrita por Calne y Williams en 1968 y Tzakis et al. en 19891,2, se ha convertido en una de las técnicas de referencia. Se caracteriza por preservar la vena cava inferior (VCI) retrohepática del receptor, que será conectada a la VCI del donante mediante una anastomosis terminolateral a través de un manguito vascular creado a partir de las venas suprahepáticas del receptor. Las ventajas potenciales de esta técnica incluyen: a) la ausencia de by-pass venovenoso del receptor y de las complicaciones asociadas; b) reducción del tiempo de isquemia caliente, así como de la duración total del procedimiento, y c) disminución de las complicaciones asociadas a la disección de la VCI retrohepática del receptor. A pesar de sus ventajas, la técnica de piggyback no restaura completamente la situación fisiológica pretrasplante, por lo que el riesgo de obstrucción del drenaje venoso hepático aumenta. En consecuencia, el THO mediante piggyback no elimina el riesgo de complicaciones potencialmente graves.
La incidencia de la obstrucción del drenaje venoso hepático tras THO oscila entre 1-7% considerando todas las variantes de trasplante (donante cadáver, donante vivo, injerto reducido, trasplante pediátrico). La incidencia con la técnica de piggyback en donante cadáver es de 1-2,5%3–6. Las manifestaciones clínicas incluyen ascitis, hepatomegalia e insuficiencia hepática. El tratamiento endovascular mediante angioplastia con balón y/o endoprótesis ha sido ampliamente descrito para el tratamiento de estenosis de VCI y vena porta tras el THO7–9. Sin embargo, pocos estudios han analizado los resultados del tratamiento endovascular de las estenosis de las venas suprahepáticas tras THO10–12. Una primera cuestión que debe valorarse es la elección de la vía de acceso, ya que existen múltiples posibilidades (transyugular, transfemoral, transhepática). La vía de acceso más frecuentemente descrita en la bibliografía es la transyugular. Este acceso permite un cateterismo de las venas suprahepáticas técnicamente más sencillo, especialmente en anastomosis tipo piggyback13. La vía transfemoral puede ser utilizada para colocar endoprótesis en las venas suprahepáticas, aunque en anastomosis tipo piggyback el ángulo entre la VCI y las suprahepáticas es más pronunciado, lo que puede dificultar o imposibilitar el cateterismo. Por su parte, el acceso transhepático mediante control ecográfico permite cateterizar simultáneamente múltiples venas suprahepáticas y ver mejor los orificios de las venas y su relación con la VCI del donante, pero el riesgo de complicaciones inmediatas por la punción de la cápsula hepática es mayor14,15. Un factor relevante a la hora de seleccionar el tipo de acceso va a ser el número y localización de las estenosis. En pacientes con estenosis únicas, la vía de acceso preferida va a ser la transyugular. En aquellos pacientes con múltiples estenosis, el acceso transhepático permite desplegar simultáneamente las endoprótesis, por lo que puede ser una buena alternativa a la vía transyugular. Una segunda cuestión es el tipo de endoprótesis a utilizar. Para las estenosis de las venas suprahepáticas se pueden usar tanto las autoexpandibles como las balón-expandibles16. Varios estudios han evidenciado que la resistencia radial de las endoprótesis balón-expandibles es mayor17, aunque todavía son necesarios estudios que confirmen si este hecho implica una respuesta mejor. A estas cuestiones hay que añadir el hecho de que existe poca información sobre los resultados a largo plazo de seguridad y permeabilidad18,19.
El objetivo de este estudio es evaluar retrospectivamente la seguridad y permeabilidad a largo plazo del tratamiento endovascular con endoprótesis autoexpandibles en pacientes con THO y obstrucción del drenaje venoso hepático. Como objetivo secundario estudiaremos las diferencias en la respuesta terapéutica entre pacientes con obstrucción de instauración precoz y tardía.
Material y métodosPacientesEntre enero de 1996 y febrero de 2011, 16 de los 295 pacientes (5,4%) a los que se realizó un THO en nuestro centro presentaron una obstrucción del drenaje venoso hepático y fueron tratados con endoprótesis autoexpandibles. Los estudiamos retrospectivamente con el aval del comité de ética hospitalario. Todos los procedimientos contaban con consentimiento informado.
El grupo de estudio incluyó a 12 hombres y 4 mujeres (edad media 53,2 años, IC del 95% 31-65 años). La causa más frecuente del trasplante hepático fue la cirrosis alcohólica, con o sin enfermedades concomitantes (n=8), seguida de la cirrosis por virus de la hepatitis C (n=3) y otras causas (n=5). En 15 casos la complicación fue diagnosticada durante el primer trasplante, y solo en un caso en un retrasplante. En todos los casos se trató de un THO con injerto completo de donante cadáver. La técnica de piggyback se aplicó en 15 pacientes (manguito de 3 vasos [n=12]; manguito de 3 vasos+cavocavostomía [n=2]; manguito de 2 vasos [n=1]), y en un paciente se utilizó una cavocavostomía terminoterminal. En 8 casos (50%), la obstrucción se detectó en el periodo postoperatorio precoz (en los primeros 30 días después de la cirugía). En los otros 8 (50%), la obstrucción apareció en el periodo postoperatorio tardío (entre un mes y 4 años después del trasplante).
El diagnóstico se basó inicialmente en los hallazgos clínicos y de laboratorio, y posteriormente se completó mediante ecografía y/o tomografía computarizada (TC) (tabla 1). En 11 pacientes se realizó también una biopsia hepática para descartar un rechazo del injerto u otros procesos que pudieran causar las alteraciones clínicas y de laboratorio. Los parámetros evaluados incluyeron dolor abdominal, aumento de peso, ascitis, edema de las extremidades inferiores, derrame pleural, hepatoesplenomegalia y alteraciones analíticas de la función hepática. La manifestación más frecuente fue la alteración analítica de la función hepática, expresada como elevación de la bilirrubina y los parámetros de coagulación, y disminución de la albúmina sérica. Este hallazgo estuvo presente en todos los pacientes (n=16).
Resumen del diagnóstico
| Tiempo hasta el diagnóstico (n=16) | |
| Precoz | 8 (50%) |
| Tardía | 8 (50%) |
| Hallazgos clínicos y de laboratorio (n=16) | |
| Ascitis | 13 |
| Disfunción hepática | 16 |
| Hallazgos ecográficos (n=16) | |
| Estenosis de la anastomosis del piggyback | 11 |
| Patrón de onda monofásico en las venas hepáticas | 6 |
| Ausencia/baja velocidad de flujo en venas hepáticas | 2 |
| Estenosis entre la anastomosis del piggyback y la VCI del receptor | 1 |
| Hallazgos de la TC (n=4) | |
| Segmentos estenóticos en la anastomosis del piggyback | 3 |
| Ausencia/escasez de realce en venas hepáticas | 2 |
| Biopsia hepática (n=11) | |
| Congestión venosa con dilatación de venas centrales y sinusoides | 4 |
| Rechazo del injerto | 7 |
TC: tomografía computarizada; VCI: vena cava inferior.
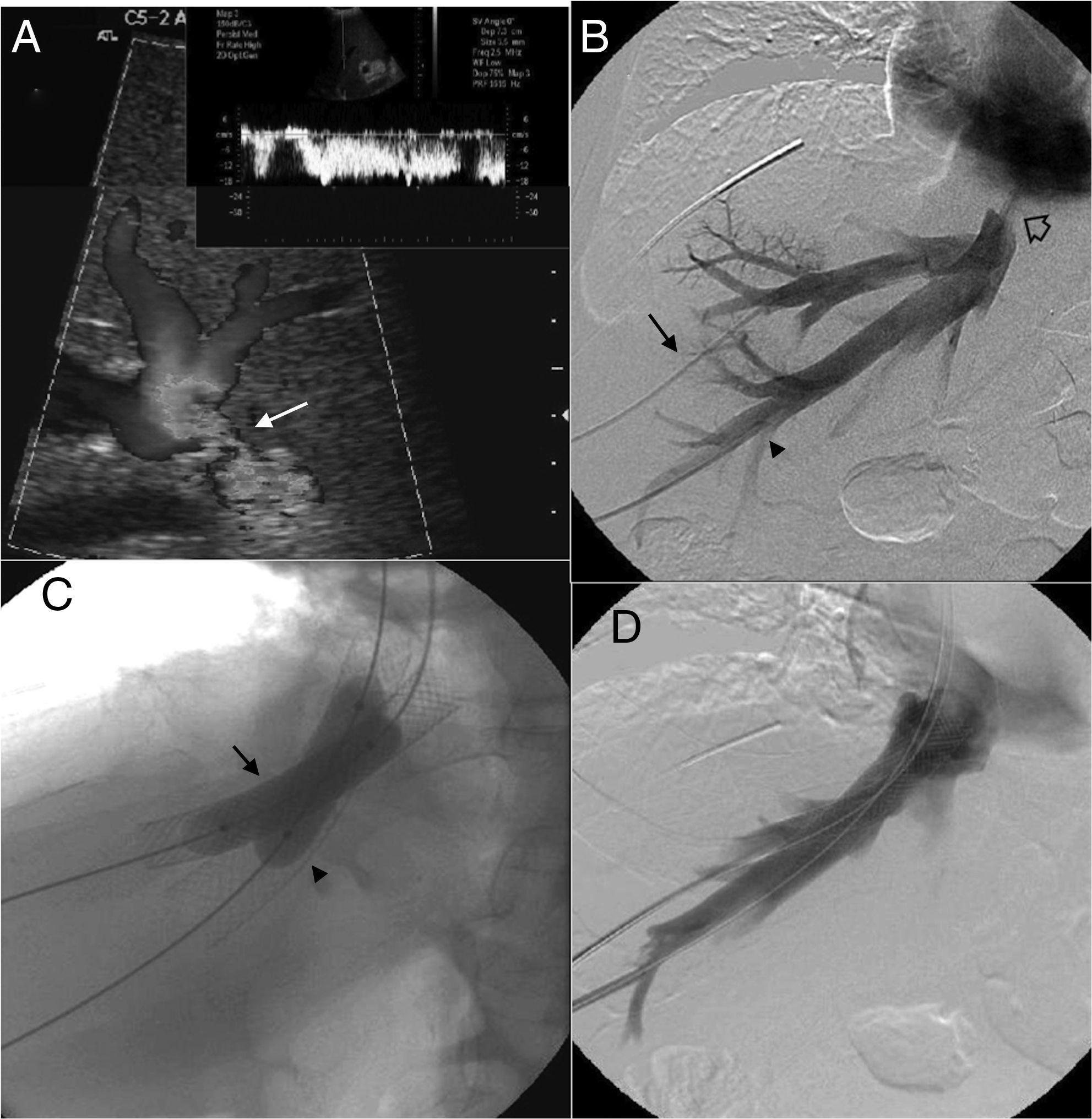
La ecografía fue realizada en todos los pacientes (n=16), e incluyó estudio en modo B y modos doppler color/doppler pulsado (Antares/Acuson S2000™; Siemens Healthcare, Erlangen, Alemania). Los hallazgos indicativos de obstrucción del drenaje venoso hepático20 fueron la estenosis de la anastomosis (fig. 1A), un flujo ausente o de velocidad baja, o un patrón de onda monofásico en las venas suprahepáticas. La exploración mediante TC (TCMD; Somatom Sensation y Definition/Axiom, Siemens Healthcare, Erlangen, Alemania) fue realizada en 4 casos con el fin de caracterizar morfológicamente la estenosis y localizarla con precisión. En todos los casos existía un estudio ecográfico previo indicativo de obstrucción del drenaje venoso hepático. Los hallazgos de TC compatibles con una obstrucción del drenaje venoso hepático incluyeron la estenosis de la anastomosis venosa y realce ausente o escaso de las venas suprahepáticas con alteración asociada de la perfusión del parénquima.
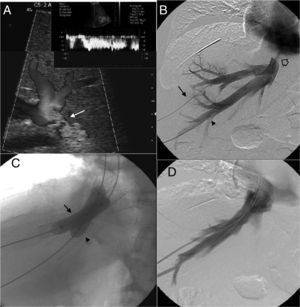
Paciente con trasplante hepático ortotópico con técnica de piggyback que presenta ascitis y alteración de las pruebas de función hepática. A) Ecografía. Las imágenes doppler color muestran una estenosis de la anastomosis del piggyback (flecha). La forma de la onda de la vena hepática en el estudio doppler pulsado muestra un aplanamiento sin cambios con la respiración. B) Estudio venográfico. Cateterismo selectivo de las venas hepáticas derecha y media por vía transhepática con control ecográfico (flecha y cabeza de flecha). El medio de contraste confirma la estenosis de la anastomosis del piggyback (flecha hueca). C) Estudio venográfico. Dilatación con balón de 2 endoprótesis autoexpandibles colocadas consecutivamente en las venas hepáticas derecha y media (flecha y cabeza de flecha). D) Estudio venográfico. Se identifican 2 endoprótesis autoexpandibles colocadas en las venas hepáticas derecha y media atravesando la estenosis de la anastomosis. La inyección del medio de contraste no muestra estenosis o reflujo de contraste hacia las venas hepáticas.
La biopsia hepática se realizó en 11 pacientes para descartar otros procesos que pudieran justificar la situación clínica y analítica. La vía de acceso fue transhepática o transyugular. En 7 pacientes (63,3%) se encontraron diversos grados de rechazo del injerto.
Tras establecerse el diagnóstico inicial de obstrucción del drenaje venoso hepático y comenzar con un tratamiento anticoagulante, los 16 pacientes fueron sometidos a venografía y manometría. El objetivo de estas pruebas era confirmar y localizar con exactitud la obstrucción (fig. 1B), así como cuantificar el gradiente de presión portal y entre las venas suprahepáticas y la aurícula derecha, que se consideró significativo cuando era superior a 3mmHg21. La visión directa de la obstrucción se consiguió en 11 pacientes. En los otros 5 se detectó por signos indirectos (colaterales, flujo inverso). El gradiente de presión fue significativo en los 16 pacientes. Respecto al patrón de obstrucción, 3 pacientes presentaron una estenosis única de las venas suprahepáticas, 10 pacientes, múltiples estenosis de las venas suprahepáticas, y 3 pacientes, estenosis en las venas suprahepáticas y la VCI (tabla 2).
ProcedimientoEl tratamiento endovascular se realizó inmediatamente después de la confirmación venográfica o diferidamente, según la necesidad de pruebas adicionales para planificar el tratamiento. El procedimiento se realizó bajo anestesia general en 15 pacientes. Se prefirió realizar el procedimiento bajo anestesia general con el fin de garantizar la inmovilidad del paciente durante el mismo para maximizar la calidad de la venografía y aumentar la precisión durante la cateterización selectiva y el despliegue de las endoprótesis22. En un paciente se utilizó sedación profunda por recomendación del anestesista. El acceso a las venas suprahepáticas se realizó por vía transhepática con guía ecográfica en 15 pacientes, y por vía transyugular en un paciente. La vía transyugular fue la preferida cuando había una estenosis de una sola vena suprahepática, mientras que la vía transhepática se eligió si la estenosis afectaba a más de una vena o cuando el cateterismo de estenosis únicas por vía transyugular resultaba técnicamente difícil. En los 3 casos en los que coexistía una estenosis de la VCI del receptor, esta se trató con una endoprótesis mediante acceso transfemoral. En todos los casos se colocaron guías de seguridad en la VCS a partir de un acceso transfemoral o transyugular. En aquellos casos en los que se usó la vía transhepática, las venas suprahepáticas fueron inicialmente puncionadas con una aguja de calibre 21G para introducir una guía de 0,035” (Terumo, Tokio, Japón) mediante un kit AccuStick™ II (Boston Scientific, Spencer, IN, EE. UU.). A continuación se colocó un introductor vascular (4-11F) (Cordis Co., Miami, FL, EE. UU.) dentro de la luz de cada vena suprahepática y se atravesó cada estenosis mediante guías rígidas Amplatz™ (Boston Scientific), dejando el extremo distal de las guías en la vena cava superior. El despliegue de las endoprótesis autoexpandibles (Wallstent®, Boston Scientific, Natick, MA, EE. UU.) a través de las estenosis desde las venas suprahepáticas y/o VCI del receptor fue siempre seguido de dilatación de las prótesis con balones de angioplastia con el tamaño apropiado (Wanda™, Boston Scientific, Galway, Irlanda) (fig. 1C). El diámetro de las endoprótesis osciló entre 10-20mm, y su longitud, entre 60-100mm. En todos los casos se realizó un control después del procedimiento con venografía (fig. 1D) y gradiente de presión para determinar la respuesta técnica al procedimiento. Los tractos transhepáticos fueron embolizados mediante espirales de 0,035”. El seguimiento inmediato tras el procedimiento consistió en una valoración clínica, tests de laboratorio y un estudio de ecografía doppler durante las 24-72h después de la colocación de la endoprótesis. El seguimiento a largo plazo consistió en una valoración clínica y tests de laboratorio cada 1-3 meses, así como un estudio de ecografía doppler a los 1, 3, 6, 9 y 12 meses, y, posteriormente, cada 3 meses. Los estudios de TC y/o venografía se reservaron para aquellas situaciones en las que existía sospecha clínica de complicaciones o recurrencia de la obstrucción.
Consideramos como éxito técnico la resolución angiográfica de la estenosis con mejora del flujo sanguíneo tras inyectar contraste y una reducción significativa del gradiente de presión. El éxito clínico fue considerado como la mejora inmediata y significativa del estado clínico del paciente, evaluada mediante signos y síntomas como dolor abdominal, ascitis, edema de las extremidades inferiores y derrame pleural.
Consideramos como complicaciones mayores relacionadas con el procedimiento las que pudieran implicar un nivel superior de cuidados del paciente, intervención quirúrgica, prolongación de la estancia hospitalaria, secuelas permanentes o muerte. Incluyeron no solo aquellas directamente relacionadas con la colocación de la endoprótesis (sangrado, neumotórax, hemotórax o lesión visceral), sino también las complicaciones que pudieran manifestarse mucho tiempo después de la intervención (malposición, migración u oclusión).
La recurrencia se definió como la reaparición de hallazgos clínicos, ecográficos, tomográficos o angiográficos indicativos de una nueva obstrucción del drenaje venoso hepático. Entre estos hallazgos destacan la ascitis (tras haber presentado una mejoría significativa tras la intervención), la recurrencia de los gradientes de presión significativos en las venas suprahepáticas o VCI, y la aparición de nuevas estenosis. Consideramos como supervivencia de los pacientes y de los injertos la tasa de pacientes e injertos vivos al finalizar el seguimiento.
La permeabilidad primaria se definió como el intervalo de tiempo entre la colocación de la endoprótesis y la primera vez que aparecieron signos de obstrucción del drenaje venoso hepático que requirieron un estudio angiográfico percutáneo. La permeabilidad primaria asistida se definió como el período de tiempo transcurrió desde que se realizó el primer procedimiento endovascular para asegurar el flujo en una endoprótesis comprometida, hasta que fue necesario realizar un nuevo procedimiento endovascular para mantener su permeabilidad.
Análisis estadísticoPara comparar la supervivencia de los pacientes e injertos, el éxito técnico, el éxito clínico, la recurrencia y las complicaciones entre los pacientes con obstrucción precoz y tardía se utilizó el test de Chi-cuadrado de Pearson. Para calcular la tasa de permeabilidad de las endoprótesis se utilizó el test de Kaplan-Meier. El test log-rank se utilizó para comparar las tasas de permeabilidad entre los pacientes con obstrucción precoz y tardía del flujo venoso. Todos los análisis estadísticos se realizaron con el paquete estadístico SPSS® (versión 15.0, SPSS, Chicago, IL, EE. UU.). La significación estadística se estableció en un valor de p<0,05.
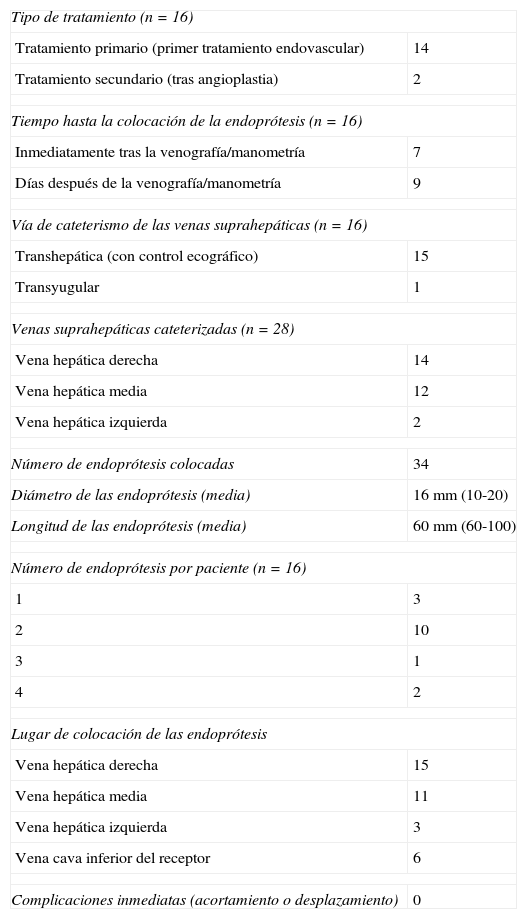
ResultadosEl número de venas suprahepáticas cateterizadas por paciente osciló entre 1 y 3 (mediana 2). La vena suprahepática derecha fue cateterizada en 14 pacientes, la vena suprahepática media en 12 pacientes y la vena suprahepática izquierda en 2 pacientes. El número total de endoprótesis autoexpandibles colocadas fue 34. El número de prótesis colocadas por paciente osciló entre 1 y 4. Las endoprótesis se colocaron en la vena suprahepática derecha, la vena suprahepática media, la vena suprahepática izquierda o la VCI del receptor en función de la ubicación y extensión de la estenosis en la anastomosis vascular. Trece de 16 (81,25%) pacientes requirieron más de una endoprótesis. En todos los casos las endoprótesis se desplegaron en el área de estenosis sin complicaciones inmediatas como acortamiento o malposición. La información sobre la colocación de las endoprótesis se encuentra resumida en la tabla 3.
Información sobre la colocación de las endoprótesis
| Tipo de tratamiento (n=16) | |
| Tratamiento primario (primer tratamiento endovascular) | 14 |
| Tratamiento secundario (tras angioplastia) | 2 |
| Tiempo hasta la colocación de la endoprótesis (n=16) | |
| Inmediatamente tras la venografía/manometría | 7 |
| Días después de la venografía/manometría | 9 |
| Vía de cateterismo de las venas suprahepáticas (n=16) | |
| Transhepática (con control ecográfico) | 15 |
| Transyugular | 1 |
| Venas suprahepáticas cateterizadas (n=28) | |
| Vena hepática derecha | 14 |
| Vena hepática media | 12 |
| Vena hepática izquierda | 2 |
| Número de endoprótesis colocadas | 34 |
| Diámetro de las endoprótesis (media) | 16mm (10-20) |
| Longitud de las endoprótesis (media) | 60mm (60-100) |
| Número de endoprótesis por paciente (n=16) | |
| 1 | 3 |
| 2 | 10 |
| 3 | 1 |
| 4 | 2 |
| Lugar de colocación de las endoprótesis | |
| Vena hepática derecha | 15 |
| Vena hepática media | 11 |
| Vena hepática izquierda | 3 |
| Vena cava inferior del receptor | 6 |
| Complicaciones inmediatas (acortamiento o desplazamiento) | 0 |
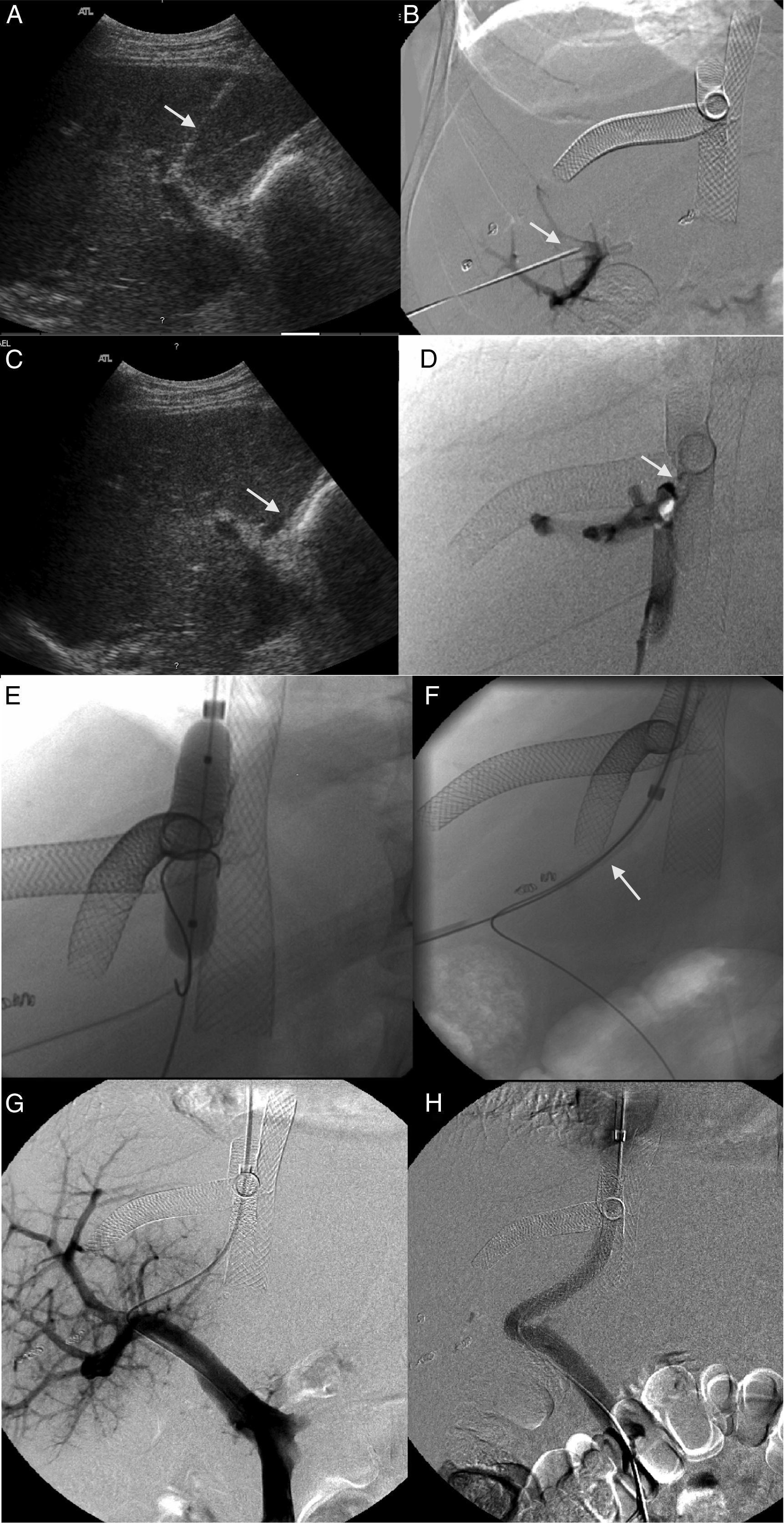
Durante el seguimiento, 2 pacientes requirieron un shunt portosistémico percutáneo (TIPS) después del tratamiento endovascular (223 y 256 días tras el procedimiento) por persistencia de una hipertensión portal significativa (fig. 2). En el primer caso, el paciente presentó una mejoría clínica significativa, pero murió 20 días después por un cuadro de coagulación intravascular diseminada. En el segundo caso, el paciente presentó una mejoría clínica significativa y seguía vivo y sin recurrencia 2 años y 4 meses después de colocar el TIPS.
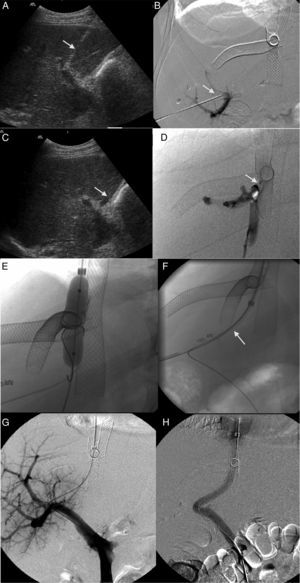
Paciente con obstrucción del flujo venoso hepático tratado con endoprótesis en la vena hepática media (VHM), vena hepática izquierda (VHI) y vena cava inferior (VCI). El paciente presentaba un cuadro de hipertensión portal grave de instauración brusca por oclusión de la endoprótesis colocada en la VHM. A) Ecografía. Cateterismo selectivo de la vena porta derecha (VPD) por vía transhepática con control ecográfico (flecha). B) Estudio venográfico. La inyección del medio de contraste a través del acceso transhepático confirma el cateterismo de la VPD (flecha). Se identifican las endoprótesis autoexpandibles desplegadas en la VHM, VHI y VCI. C) Ecografía. Cateterismo selectivo de la VCI del donante por vía transhepática con control ecográfico (flecha). D) Estudio venográfico. La inyección del medio de contraste en la VCI del donante muestra una estenosis de la anastomosis del piggyback (flecha). No existe paso de contraste a la VCI del receptor y existe reflujo del medio de contraste hacia la vena hepática derecha. No hay reflujo a la VHM. E) Estudio venográfico. Dilatación de la estenosis de la anastomosis desde el acceso en la VCI del donante. F) Estudio venográfico. Creación de un shunt entre la VCI del receptor y la VPD pasando a través de la VCI del donante (flecha) con una aguja de Colapinto mediante un acceso transyugular derecho. G) Estudio venográfico. La inyección de medio de contraste desde el acceso transyugular derecha opacifica el árbol portal confirmando la creación de un shunt portosistémico. H) Estudio venográfico. Despliegue de endoprótesis Viator® y Wallstent® a través del shunt entre la VCI del receptor y la VPD. Una inyección del medio de contraste confirma la permeabilidad del shunt.
La tasa de éxito técnico fue del 93,7% (15 de 16 casos). En un caso se registró una disminución no significativa del gradiente de presión, aunque sí que hubo una mejoría clínica significativa. La tasa de éxito clínico fue del 81,25% (13 de 16 pacientes). Dos de los casos fallidos correspondieron a pacientes con una obstrucción del drenaje venoso hepático aguda poco tiempo después del trasplante, que no respondió clínicamente al tratamiento endovascular. Uno de los casos requirió retrasplante a los 15 días del procedimiento y el otro caso finalizó con el fallecimiento del paciente a los 6 días. El tercer paciente presentó una hipertensión portal significativa, que no mejoró después de un tratamiento endovascular repetido, y necesitó finalmente la colocación de un TIPS.
La tasa global de complicaciones mayores fue de un 25% (4 de 16 casos). La tasa de complicaciones mayores inmediatas fue de 12,5% (50% de las complicaciones). El primer caso consistió en un derrame pleural que requirió drenaje percutáneo, y el segundo, en un hematoma intrahepático que necesitó transfusiones. La tasa de complicaciones mayores a largo plazo fue también del 12,5% (50% de las complicaciones). El primer caso correspondió a la trombosis de una endoprótesis asociada a hipertensión portal sintomática (ascitis refractaria), que requirió colocar un TIPS. El segundo caso correspondió a la migración de una endoprótesis hacia la VCI del receptor. El paciente presentó posteriormente un cuadro brusco de disnea y un soplo sistólico de nueva aparición. El estudio ecocardiográfico reveló una fístula aortoauricular derecha y un defecto del septo auricular con sobrecarga derecha causados por la migración de la endoprótesis desde la VCI hasta la aurícula derecha. El tratamiento quirúrgico para extraer la endoprótesis migrada y cerrar el defecto del septo auricular y la fístula aortoauricular transcurrió sin complicaciones. El paciente estaba vivo y sin secuelas al finalizar el estudio.
El período de seguimiento osciló entre 21 y 5.331 días (media 3,34 años). La tasa de supervivencia fue del 87,5% para los pacientes (14 de 16) y del 92,5% para los injertos (15 de 16). La tasa de recurrencia de la obstrucción del drenaje venoso hepático con manifestaciones clínicas que requirió reintervención fue del 12,5% (2 de 16).
La permeabilidad global calculada en función del número de endoprótesis fue del 97% (33 de 34). La tasa de permeabilidad primaria global fue del 91,7% (31 de 34), y la tasa de permeabilidad primaria asistida global de un 5,8% (2 de 34). Las tasas de permeabilidad primaria a los 3, 6, 12 y 60 meses tras colocar las endoprótesis fueron de 0,96 (IC 95% 0,89-1), 0,96 (IC 95% 0,91-1), 0,86 (IC 95% 0,70-1) y 0,86 (IC 95% 0,70-1). La tasa de permeabilidad primaria asistida fue de 1 a los 3, 6 y 12 meses.
Al comparar los resultados entre los pacientes con obstrucción precoz (n=8) y tardía (n=8) no se encontraron diferencias estadísticamente significativas (tabla 4). No obstante, había una tendencia a presentar tasas de permeabilidad primaria más altas en el grupo de pacientes con obstrucción precoz.
Comparación de los resultados entre los pacientes con obstrucción precoz y tardía del flujo venoso hepático
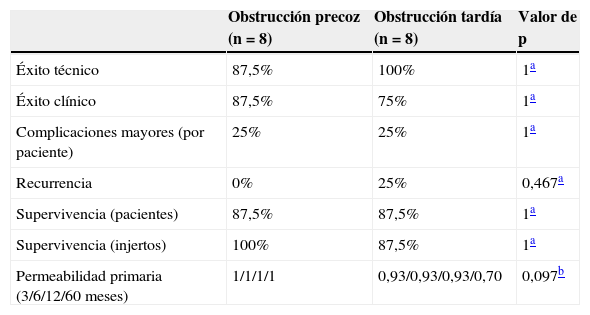
| Obstrucción precoz (n=8) | Obstrucción tardía (n=8) | Valor de p | |
|---|---|---|---|
| Éxito técnico | 87,5% | 100% | 1a |
| Éxito clínico | 87,5% | 75% | 1a |
| Complicaciones mayores (por paciente) | 25% | 25% | 1a |
| Recurrencia | 0% | 25% | 0,467a |
| Supervivencia (pacientes) | 87,5% | 87,5% | 1a |
| Supervivencia (injertos) | 100% | 87,5% | 1a |
| Permeabilidad primaria (3/6/12/60 meses) | 1/1/1/1 | 0,93/0,93/0,93/0,70 | 0,097b |
Nuestros resultados apoyan la hipótesis de que el tratamiento de la obstrucción del drenaje venoso hepático tras THO con endoprótesis autoexpandibles es eficaz y seguro. Los parámetros de eficacia arrojan unos excelentes resultados de éxito técnico y clínico (>81,25%), con una baja tasa de recurrencias (12,5%). Por otro lado, las tasas de supervivencia para pacientes e injertos son elevadas (>87,5%), con una aceptable tasa de complicaciones mayores (12,5%) atendiendo a la bibliografía. Los resultados en los pacientes con obstrucción precoz y tardía del drenaje no son significativamente diferentes, aunque existe una tendencia a presentar permeabilidades primarias mayores en casos de obstrucción precoz.
La obstrucción del drenaje venoso hepático es una complicación poco frecuente y potencialmente grave del THO, con una tasa de mortalidad de hasta el 24%3. Además afecta de manera importante a la supervivencia del injerto. La incidencia se ha establecido clásicamente entre el 1 y el 7%3–5 de los pacientes con THO, aunque varios estudios han demostrado que existen variaciones según el tipo de técnica utilizada (donante cadáver, donante vivo, injerto reducido, pacientes pediátricos, etc.). En nuestra serie, la incidencia es del 5,4%, similar a las tasas de incidencia publicadas para el THO de donante cadáver.
A lo largo de los años se han propuesto múltiples causas que podrían estar relacionadas con esta complicación. La obstrucción precoz de la anastomosis venosa (8 casos en nuestra serie) puede estar relacionada con una compresión directa de la anastomosis por un injerto demasiado grande o muy congestionado, la torsión de la anastomosis venosa cuando el injerto es demasiado pequeño, o cuando las suturas están excesivamente apretadas3,4. Las obstrucciones tardías (8 casos en nuestra serie) se han relacionado con la hiperplasia de la íntima y/o cambios fibrosos en la anastomosis11. Un factor que puede contribuir a la obstrucción del drenaje venoso hepático en los pacientes con THO piggyback es el tipo de manguito vascular. Parrilla et al.4 estudiaron retrospectivamente una cohorte de 1.112 casos, y la tasa de complicaciones difería según el tipo de manguito vascular utilizado. La incidencia de complicaciones (7,3 frente a 0,9%) y el riesgo de obstrucción precoz del flujo (1,6 frente a 0,28%) fueron mayores en los pacientes con manguito de 2 vasos que en los de 3 vasos. Esta mayor incidencia pudiera relacionarse con la disminución del diámetro de la anastomosis (por lo menos 1cm menor) y la mayor longitud del segmento venoso entre el injerto y la VCI del receptor. En consecuencia, el riesgo de morbilidad puede ser mayor para el injerto cuando se utiliza un manguito vascular de 2 vasos21–23. En nuestra serie, 14 de los 15 casos con técnica de piggyback tenían un manguito de 3 vasos.
El diagnóstico de la obstrucción del drenaje venoso hepático tras el THO se basa en la detección de alteraciones clínicas, de laboratorio y pruebas de imagen como ecografía, TC o estudios de venografía/manometría8,24,25. Los gradientes de presión tienen un papel clave en el diagnóstico, pero no hay consenso acerca de qué valores de gradiente corresponden a una estenosis significativa. Se acepta generalmente un gradiente superior a 5-6mmHg como el umbral para inducir síntomas, aunque gradientes de presión superiores a 3mmHg pueden ser hemodinámicamente significativos21. Ko et al.18 han defendido que, si hay síntomas, se debe colocar una endoprótesis incluso con gradientes bajos, con el fin de mejorar el cuadro clínico y prevenir la obstrucción.
La angioplastia con balón y las endoprótesis han sido frecuentemente descritas en pacientes con THO para tratar estenosis venosas portales y de VCI del receptor7–9. Sin embargo, no lo han sido tanto para las venas suprahepáticas. A pesar de que se han publicado algunos casos10,14 y series cortas11,12,18,19,26, todavía hay poca información sobre los resultados a largo plazo del tratamiento endovascular. La angioplastia con balón ha demostrado ser un tratamiento eficaz para la obstrucción del drenaje venoso hepático, esté relacionada o no con el THO6,26. Sin embargo, la incidencia de recurrencia de la obstrucción es alta, con permeabilidades primarias en torno a 80% a los 3 meses, 60% a los 12 meses y 60% a los 60 meses tras el procedimiento26, lo que implica una tasa de reintervenciones alta. Para garantizar la permeabilidad primaria a largo plazo y evitar reintervenciones, la colocación de endoprótesis es una estrategia que debe considerarse tanto en pacientes con obstrucción precoz como tardía21,24.
Los accesos vasculares más descritos para colocar endoprótesis en las venas suprahepáticas son el transyugular y el transfemoral10. El acceso transhepático se utiliza raramente, aunque ofrece ventajas10,27,28 como ver mejor el orificio de las venas suprahepáticas y su relación con la VCI del receptor, lo que, en nuestra opinión, permite ser más precisos al desplegar las endoprótesis. Este hecho puede ser particularmente importante cuando se utilizan endoprótesis autoexpandibles por el acortamiento que sufren al liberarse. Por lo tanto, el acceso transhepático puede reducir el riesgo de colocar mal la prótesis o que protruya en la VCI18. Otras ventajas son la posibilidad de cateterizar simultáneamente varias venas suprahepáticas, o un menor riesgo de perforación cardiaca o rotura de la VCI durante el procedimiento28. Las desventajas están relacionadas con la perforación de la cápsula hepática, y un riesgo teóricamente mayor de complicaciones inmediatas (hemorragia intraperitoneal y laceración hepática)15. La mayoría de estas complicaciones se pueden prevenir controlando ecográficamente la punción de entrada. Al final del procedimiento, el tracto transhepático debe ser embolizado con espirales u otros materiales27.
Respecto a la elección del tipo de endoprótesis, tanto las autoexpandibles como las balón-expandibles son opciones aceptadas. Las endoprótesis balón-expandibles parecen ofrecer una mayor resistencia radial, lo cual puede ser mejor para tratar las estenosis de origen fibroso17. Además, tienen un acortamiento intrínseco menor al liberarse. Sin embargo, las endoprótesis autoexpadibles se adaptan a la forma de la vena en la que se colocan, lo que permite maniobrar mejor para desplegarlas dentro de la anastomosis del piggyback, aunque haya que tener cuidado con el acortamiento al liberarlas. Por tanto, la elección debe basarse sobre todo en los conocimientos y la experiencia del radiólogo intervencionista con cada tipo de endoprótesis.
Después de un periodo de seguimiento de hasta 5.331 días (media de 3,34 años) los resultados mostraron unas tasas de supervivencia del 87,5% para los pacientes y del 93,7% para los injertos. Estos resultados son similares a otros publicados, que oscilan entre un 72 y un 100%11,19. Las causas de muerte en nuestra serie correspondieron a complicaciones infecciosas relacionadas con el trasplante y la terapia inmunosupresora. La tasa de éxito técnico (93,7%) fue similar a las encontradas por otras series, que van desde el 94 al 100%11,18,19. Nuestra tasa de éxito clínico (81,25%) fue consistente con los resultados presentados por Ko et al.18 (82,2%), pero ligeramente por debajo de las encontradas por otros grupos (92,3 a 100%)11,19. La tasa de recurrencia de la obstrucción fue del 12,5%, inferior a la descrita para la angioplastia con balón y similar a las tasas publicadas por Ko et al. (12,94%) y Carnevale et al. (11,11%)18,19. La tasa de permeabilidad global fue del 97%, con una tasa de permeabilidad primaria del 91,7% (de 6 a 5.331 días) y del 5,8% de permeabilidad primaria asistida. En las endoprótesis con una permeabilidad primaria limitada, la obstrucción reapareció a los 62, 301 y 512 días, y necesitó ser reintervenida. Al evaluar la eficacia del tratamiento en los pacientes con obstrucción precoz y tardía del flujo venoso hepático, no se encontraron diferencias significativas, aunque sí se encontró una tendencia a una mayor permeabilidad primaria en pacientes con obstrucción precoz. En cuanto a la seguridad del procedimiento, la tasa global de complicaciones fue del 25%. La incidencia de complicaciones inmediatas (2 casos, 12,5%) es ligeramente mayor que la encontrada en otras series (0-5,5%)7,12, sin embargo, en ambos casos hubo una mejoría rápida y sin secuelas. La tasa de complicaciones tardías (12,5%) no difiere significativamente de las obtenidas por otras series, que van desde 4,6 a 7,6%11,18,19.
La principal limitación del estudio es su diseño retrospectivo con un solo brazo de estudio y una muestra pequeña. Sin embargo, en la mayoría de los pacientes el período de seguimiento fue largo, y puesto que el análisis se limita principalmente a la estadística descriptiva, los resultados no están muy influidos por las limitaciones. Solo las comparaciones entre los grupos precoz y tardío están limitadas por el pequeño número de sujetos, por lo que cualquier hallazgo deberá ser refrendado por estudios dirigidos.
En resumen, el tratamiento endovascular con endoprótesis autoexpandibles es una técnica no exenta de riesgos, pero eficaz para tratar la obstrucción del drenaje venoso hepático tras THO. Cuando se comparan los resultados del tratamiento en pacientes con una obstrucción precoz y tardía tras el THO, no hay diferencias significativas, aunque existe una tendencia a que la permeabilidad primaria sea mayor en pacientes con obstrucción precoz.
Autoría- 1.
Responsable de la integridad del estudio: JIB.
- 2.
Concepción del estudio: JIB, FR, JIH.
- 3.
Diseño del estudio: JIB.
- 4.
Obtención de los datos: GVR, AAB, ISY.
- 5.
Análisis e interpretación de los datos: GVR, ISY.
- 6.
Tratamiento estadístico: GVR, AAB.
- 7.
Búsqueda bibliográfica: GVR, AAB, ISY.
- 8.
Redacción del trabajo: GVR, ISY.
- 9.
Revisión crítica del manuscrito con aportaciones intelectualmente relevantes: JIB, FR, JIH, AAB.
- 10.
Aprobación de la versión final: GVR, AAB, ISY, FR, JIH, JIB.
Los autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.