Con el desarrollo de los programas de detección precoz de cáncer de mama basados en la mamografía se han ido desarrollando de forma paralela técnicas de biopsia percutánea guiadas por la imagen para el diagnóstico de las lesiones detectadas sospechosas de cáncer de mama.
Aunque la técnica tradicional de punción con aguja fina sigue teniendo indicaciones, se ha ido sustituyendo por las mas modernas técnicas de biopsia con aguja gruesa o sistemas de biopsia asistidos por vacío, con guía ecográfica, estereotáxica o por resonancia magnética (RM). Los resultados de esta técnica son de una alta fiabilidad, por lo que se ha reducido al mínimo la biopsia quirúrgica.
El papel del radiólogo es determinante para el diagnóstico histológico del cáncer de mama en sus fases iniciales, la valoración de su extensión local y regional mediante la utilización de la RM y realización de la técnica del ganglio centinela.
Imaging-guided percutaneous biopsy techniques have been developed to diagnose the lesions detected in breast cancer screening programs based on mammography.
Although traditional fine-needle aspiration cytology continues to be indicated in some cases, in many others it has been supplanted by more modern techniques like core biopsy or vacuum-assisted biopsy guided by ultrasonography, stereotaxy, or magnetic resonance imaging. These highly reliable techniques have minimized the need for surgical biopsy.
Radiologists play a key role in the histological diagnosis of breast cancer in the early stages of disease and in the evaluation of its local and regional extension through magnetic resonance imaging and sentinel node biopsy.
Con el uso de la mamografía, la ecografía y la resonancia magnética (RM), se ha demostrado una gran eficacia en la detección precoz, diagnóstico y valoración de la extensión del cáncer de mama, lo que ha influido de una forma determinante en la reducción de la mortalidad a causa de esta enfermedad1.
Actualmente, el radiólogo especialista en este campo ha adquirido nuevas responsabilidades, que incluyen la detección precoz del cáncer de mama, el diagnóstico preciso mediante procedimientos de biopsia pecutánea, la valoración de la extensión local mediante la RM y la introducción del radiotrazador para la correcta realización de la técnica del ganglio centinela.
La biopsia quirúrgica escisional ha sido tradicionalmente la técnica de confirmación diagnóstica. Sin embargo, con la difusión de los programas poblacionales de detección precoz de cáncer de mama, y la definitiva inclusión de la ecografía y la RM como técnicas de imagen complementarias, se han desarrollado procedimientos intervencionistas guiados por estas técnicas de imagen con el objetivo de conseguir un diagnóstico histológico preciso sin recurrir a la cirugía2.
Localización prequirúrgica de lesiones no palpablesEs la técnica tradicional y la que más frecuentemente se utiliza actualmente. Para conseguir la extirpación quirúrgica de una lesión no palpable se requiere previamente la localización de la misma, lo que habitualmente se hace mediante la introducción de guías metálicas o marcando el lecho de biopsia inyectando una solución de carbón estable o un radiotrazador3.
Técnica y resultadosAunque inicialmente la técnica de localización se basó en la colocación de agujas en la zona de la lesión, a partir de las coordenadas de situación que proporciona la mamografía, con el tiempo se fue imponiendo la utilización de guías metálicas que conseguían un mejor anclaje en la mama.
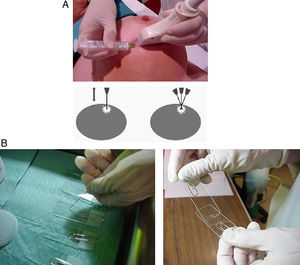
Guías metálicas («arpones»)Son radioopacas, con la punta diseñada para evitar su desplazamiento una vez insertada en la mama. Para su colocación pueden usarse la guía mamográfica o la ecográfica, según en cuál de estas técnicas se vea mejor la lesión.
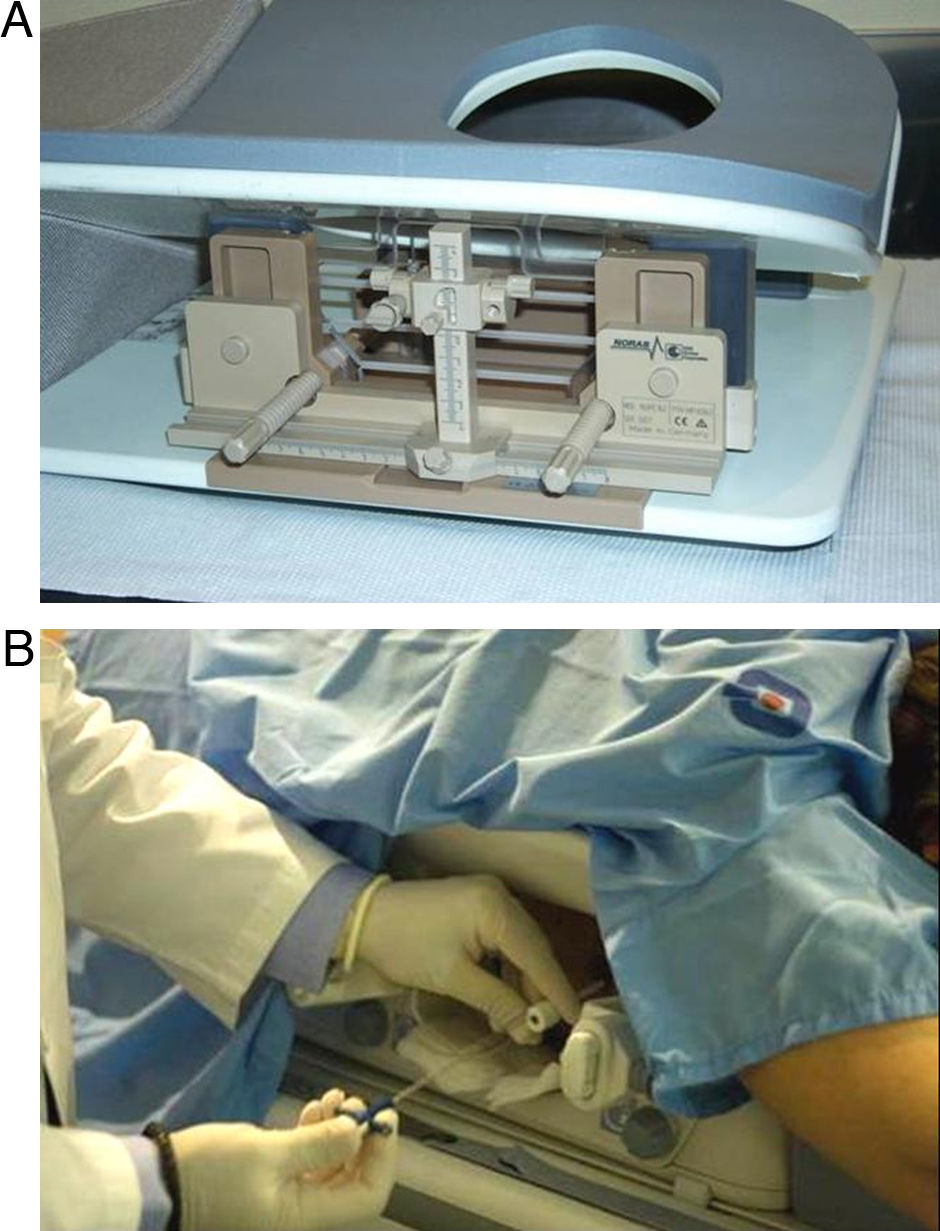
Cuando se utiliza la guía mamográfica, habitualmente se emplean compresores fenestrados con demarcación alfanumérica radiopaca (fig. 1). Algunos radiólogos prefieren utilizar el dispositivo de estereotaxia, aunque hay que tener en cuanta que se pueden producir desplazamientos no deseables a causa del «efecto acordeón» tras la descompresión de la mama.
Siempre que sea posible, es más eficaz utilizar la guía ecográfica ya que la paciente se encuentra acostada, no precisa de compresión, no utiliza radiaciones ionizantes, no hay ocupación de la sala de mamografía y se controla el procedimiento en tiempo real.
Obviamente, en aquellos casos en los que la lesión es solo visible por RM, será necesaria la localización utilizando esta técnica. En estos casos, se puede intentar la colocación de un marcador no ferromagnético en la lesión para facilitar la posterior localización mamográfica o ecográfica de la misma.
Independientemente del sistema de guía que se utilice, siempre hay que procurar elegir el abordaje que permita el camino más corto para el cirujano y en todos los casos se debe confirmar la localización final del arpón mediante dos proyecciones, lateral y craneocaudal, que deben mostrarse al cirujano antes de la intervención, para que éste conozca la relación espacial entre la guía y la lesión, la profundidad y la vía de abordaje más adecuada. En lesiones extensas puede ser necesaria la inserción de dos o más arpones.
Inyección de solución de carbónEs un método menos utilizado, aunque según los autores que lo utilizan es de gran precisión. El método consiste en la realización de un «tatuaje» del lecho de biopsia mediante la inyección en el mismo de una solución de carbón estable. Aunque la técnica es segura, más barata que la anterior y puede practicarse días antes de la intervención, no carece de efectos indeseables como es la posible alteración histológica del lecho de biopsia4.
Técnica de ROLL (Radioguided occult lesion localisation)Consiste en la inyección guiada con técnicas de imagen de un radiotrazador en el lecho de biopsia. El objetivo es localizar preoperatoria e intraoperatoriamente la lesión con sondas gammagráficas. Una gran ventaja de esta técnica es que en localizaciones para la guía de intervenciones terapéuticas, puede asociarse la realización de la técnica del ganglio centinela. Además, hay evidencias de que la obtención de bordes libres de tumor en la pieza quirúrgica es más probable con esta técnica5.
Independientemente de la técnica que se realice y del sistema de guía utilizado, es imprescindible la realización de una radiografía de la pieza quirúrgica para confirmar la extirpación de la lesión. En ocasiones, será incluso necesario realizar una ecografía de la misma y marcar el lugar de la lesión mediante la colocación de una o más agujas para facilitar su localización por el patólogo.
La seguridad de la localización de lesiones no palpables mediante estas técnicas es variable, con un porcentaje de fallos entre el 2 y el 18%, siendo deseable que este porcentaje fuese inferior al 5%. Las causas más frecuentes de fallo en la extirpación de la lesión son la colocación incorrecta del dispositivo de localización, el desplazamiento del mismo o la falta de comunicación entre el radiólogo y el cirujano.
Si no se identifica la lesión en la radiografía de la pieza quirúrgica, es necesario comprobar mediante nueva mamografía que la lesión se encuentra aún en la mama.
IndicacionesLa técnica de localización preoperatoria de lesiones no palpables para una biopsia quirúrgica ha sido la técnica tradicional de biopsia utilizada en las pacientes con lesiones de carácter sospechoso de las categorías 4 y 5 de BI-RADS6 y las que tienen un resultado no concluyente o de alto riesgo tras una biopsia percutánea previa.
Debido precisamente al auge que han ido tomando las técnicas percutáneas de biopsia, actualmente la localización preoperatoria de estas lesiones se realiza habitualmente con un fin terapéutico más que diagnóstico, cuyo objetivo es localizar lesiones no palpables de carácter maligno a las que se desea tratar mediante cirugía conservadora.
Punción aspiración con aguja finaLa punción aspiración con aguja fina (PAAF), es una técnica diagnóstica ampliamente utilizada desde hace décadas, que permite la obtención de una muestra de células para análisis citológico. Aunque se aplicó al estudio de las lesiones no palpables mediante la utilización de la guía ecográfica y la mamográfica (estereotaxia), con la difusión de las técnicas de biopsia con aguja gruesa (BAG) actualmente ha ido quedando relegada, utilizándose en la actualidad para algunas situaciones especiales que mencionamos en el apartado de indicaciones7.
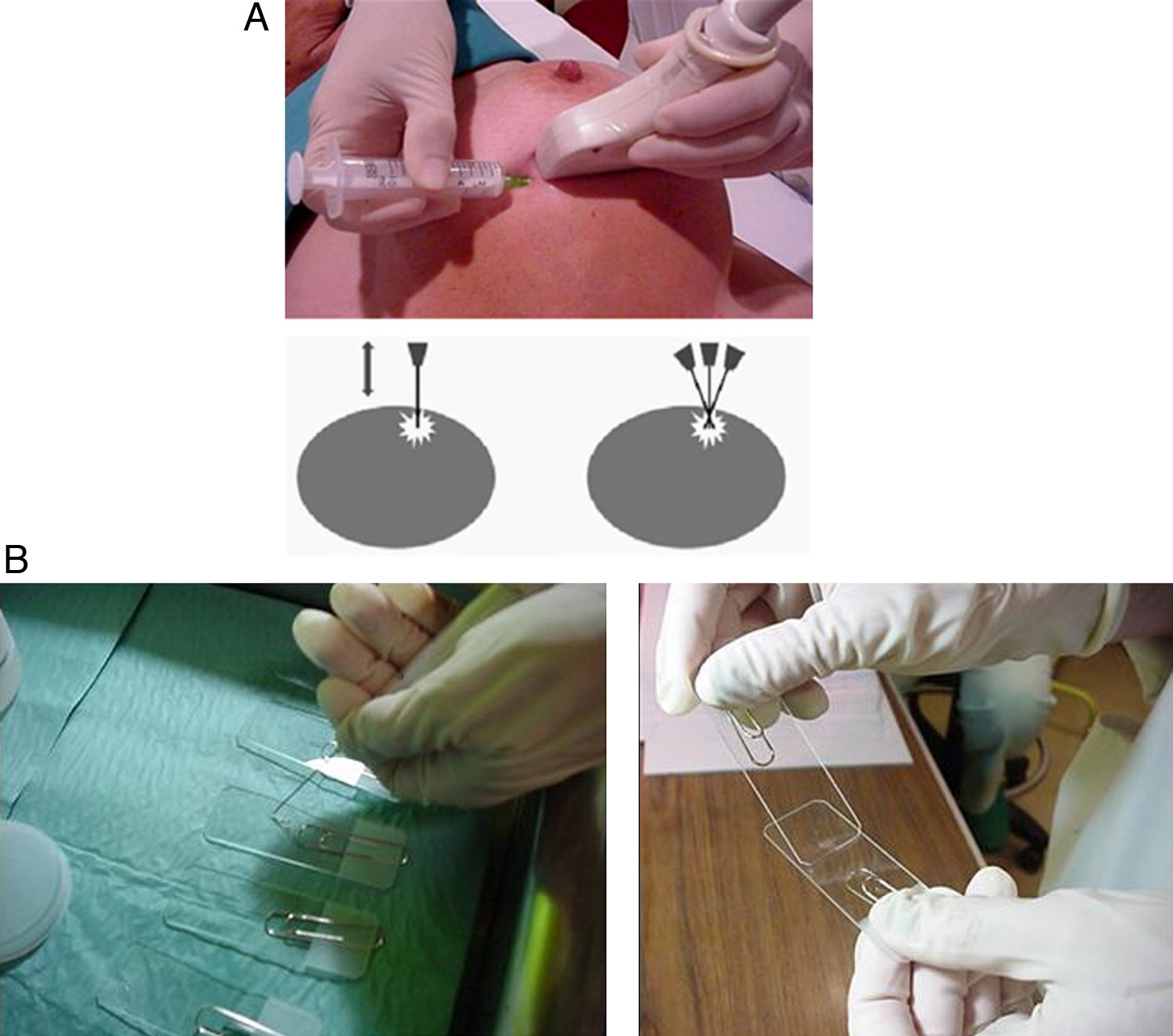
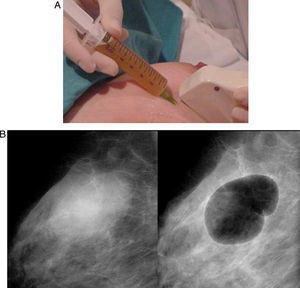
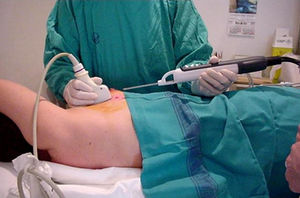
Técnica y resultadosLa PAAF puede realizarse utilizando la guía ecográfica, independientemente de que la lesión sea o no palpable, ya que este tipo de guía aumenta el rendimiento diagnóstico de la punción. Generalmente se emplea la técnica de aspiración, al aplicar vacío mediante una jeringa unida a una aguja de 20G-25G. Para facilitar la aspiración con una sola mano, se puede encajar el protector de la aguja entre el émbolo y la jeringa o utilizar dispositivos especiales de soporte de la jeringa.
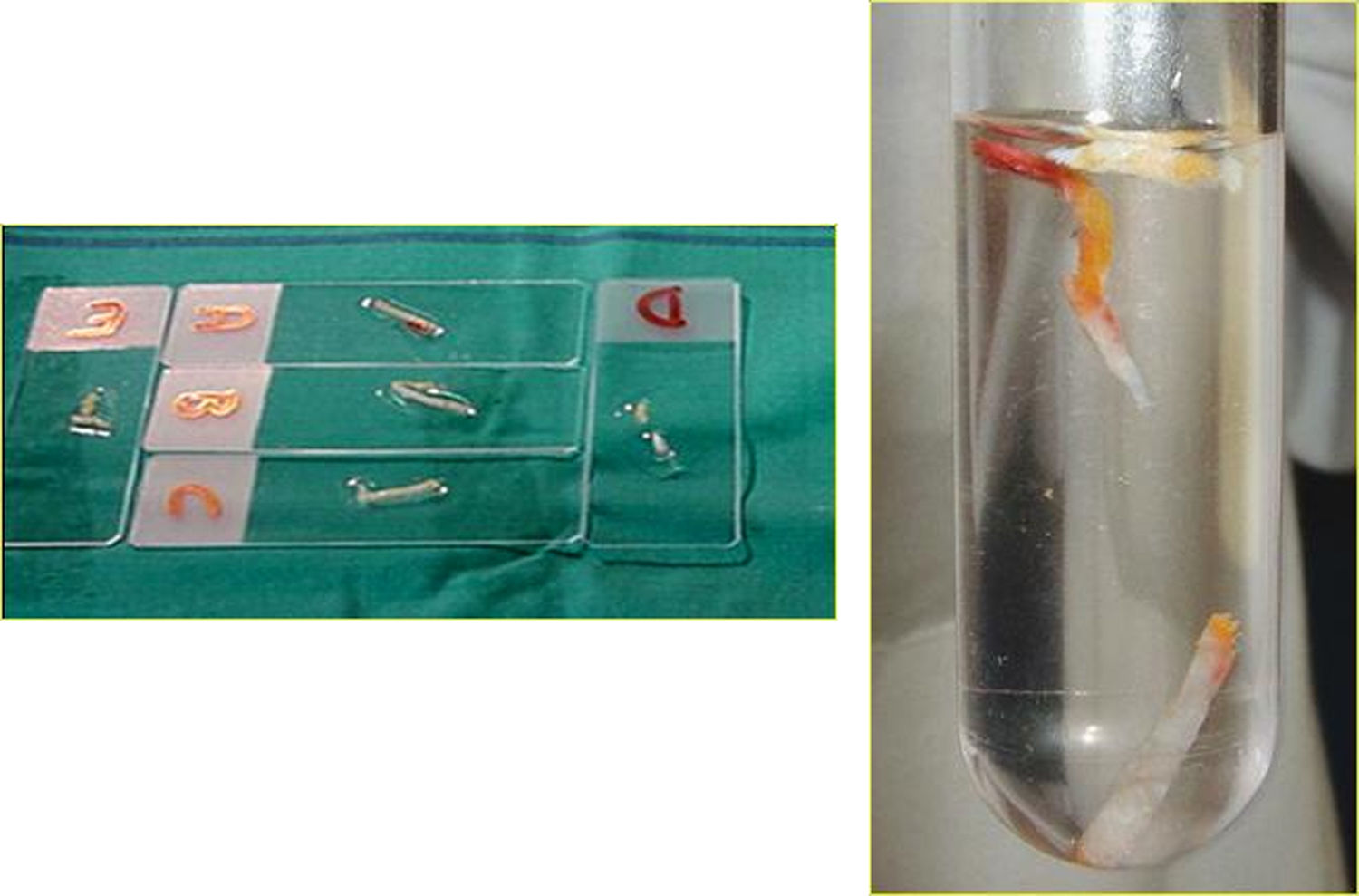
Tras la asepsia de la piel con alcohol, se realiza la punción sin necesidad de anestesia local. Tras comprobar que la punta de la aguja está en el interior de la lesión, se realizan maniobras de entrada y salida en la misma manteniendo la aguja en aspiración en todos los planos, con el fin de conseguir una mayor representación celular de la lesión. Es importante suspender la aspiración antes de extraer la aguja, con el fin de evitar la contaminación con material aspirado del trayecto de la aguja y que el material obtenido se aspire hacia la jeringa. Una vez retirada la aguja, el material es expulsado sobre portaobjetos, extendido y fijado de acuerdo con las recomendaciones del laboratorio de Anatomía Patológica (fig. 2).
Aunque la técnica prácticamente carece de complicaciones, es recomendable comprimir el punto de punción durante unos minutos, para evitar la aparición de hematomas. Solo en raras ocasiones puede producirse un hematoma de tamaño significativo. La posibilidad de complicaciones más graves como un neumotórax es casi inexistente si se realiza una técnica de punción adecuada con control estricto del avance de la aguja.
Para la obtención de buenos resultados es imprescindible contar con un citopatólogo experto, el cual habitualmente informa de los resultados utilizando las siguientes categorías: normal, benigno, atípico, sospechoso, maligno e insuficiente.
La sensibilidad de la técnica es muy variable (70-90%), porque los falsos negativos no son infrecuentes. Ante un resultado atípico o sospechoso de malignidad, siempre es necesario realizar un diagnóstico histológico mediante una biopsia percutánea o quirúrgica8. Aunque la especificidad es alta, la técnica no carece de falsos positivos (1-2%), por lo que la mayor parte de los cirujanos/ginecólogos no toman decisiones quirúrgicas basadas en un resultado de malignidad sin una biopsia introperatoria ya que, además, la PAAF no permite la diferenciación entre carcinoma in situ e infiltrante. Un resultado de benignidad solo es aceptable en pacientes con lesiones de la categoría BI-RADS 3.
IndicacionesLa PAAF se realiza actualmente tanto en lesiones palpables como no palpables, siendo las indicaciones más frecuentes las siguientes:
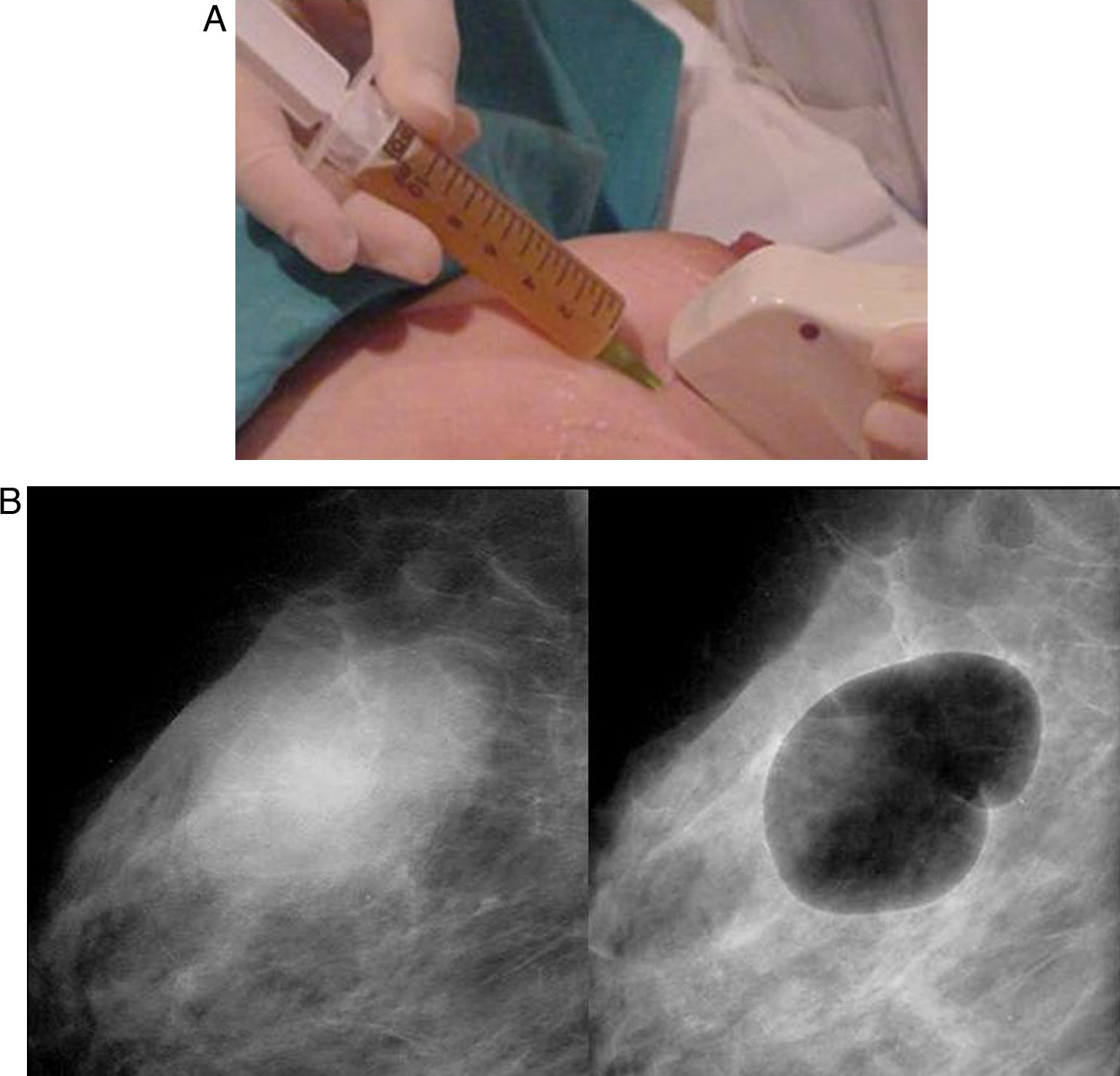
Evacuación de quistes palpablesSituación clínica muy frecuente que suele generar gran ansiedad y en la que la utilización de la PAAF resulta muy eficaz. El drenaje del quiste se realiza con control ecográfico y ocasionalmente se continúa con la realización de mamografía tras la inyección de una cantidad de aire equivalente a los dos tercios del líquido extraído (neumoquistografía). Esta maniobra tiene ya poca utilidad diagnóstica gracias a la calidad actual de la imagen ecográfica y es discutible si tiene utilidad terapéutica, reduciendo la frecuencia de quistes recidivantes (fig. 3). La neumoquistografía no debe realizarse en los quistes con lesiones sólidas intraquísticas, por la posibilidad de que la lesión sólida no pueda ser identificada posteriormente para su biopsia. Tampoco es necesario el análisis citológico del líquido extraído. Sin embargo, esto último puede ser útil si una lesión palpable es aún apreciable en la mama después del drenaje del quiste.
Diferenciación entre lesión sólida y quísticaPueden presentarse casos dudosos como ocurre con cierta frecuencia en los quistes complejos, los cuales tienen un contenido ecogénico debido a un líquido de carácter generalmente inflamatorio, que puede simular una lesión sólida en la ecografía.
Estudio citológico de áreas palpablesEspecialmente frecuente en el caso de las lesiones de aspecto probablemente benigno (categoría 3 de BI-RADS), situación muy frecuente en mujeres jóvenes con un posible fibroadenoma.
Puede ser útil también en pacientes con áreas palpables indefinidas, sin clara correlación radiológica o en mamas densas.
Punción de adenopatías axilaresSituación frecuente en las pacientes con un cáncer de mama con el fin de valorar el estado de la axila. La positividad de la PAAF evita la realización de la técnica del ganglio centinela. También es posible realizar la punción de adenopatías supraclaviculares, infraclaviculares y de la región laterocervical, todas ellas fácilmente accesibles al estudio ecográfico.
Otras indicaciones de esta técnica son la punción de nódulos de probable naturaleza inflamatoria o infecciosa, nódulos múltiples de categoría BI-RADS 3 y otras situaciones especiales.
Punción biopsia con aguja gruesaLa punción biopsia con aguja gruesa (BAG) se ha ido imponiendo como la técnica de elección para el diagnóstico histológico de las lesiones mamarias, palpables y no palpables, especialmente en aquellos casos en los que la lesión es visible por ecografía. La BAG es una técnica de un alto rendimiento diagnóstico ante cualquier lesión mamaria que precise de un diagnóstico histológico debido a su seguridad, rapidez, ausencia de complicaciones y bajo coste9.
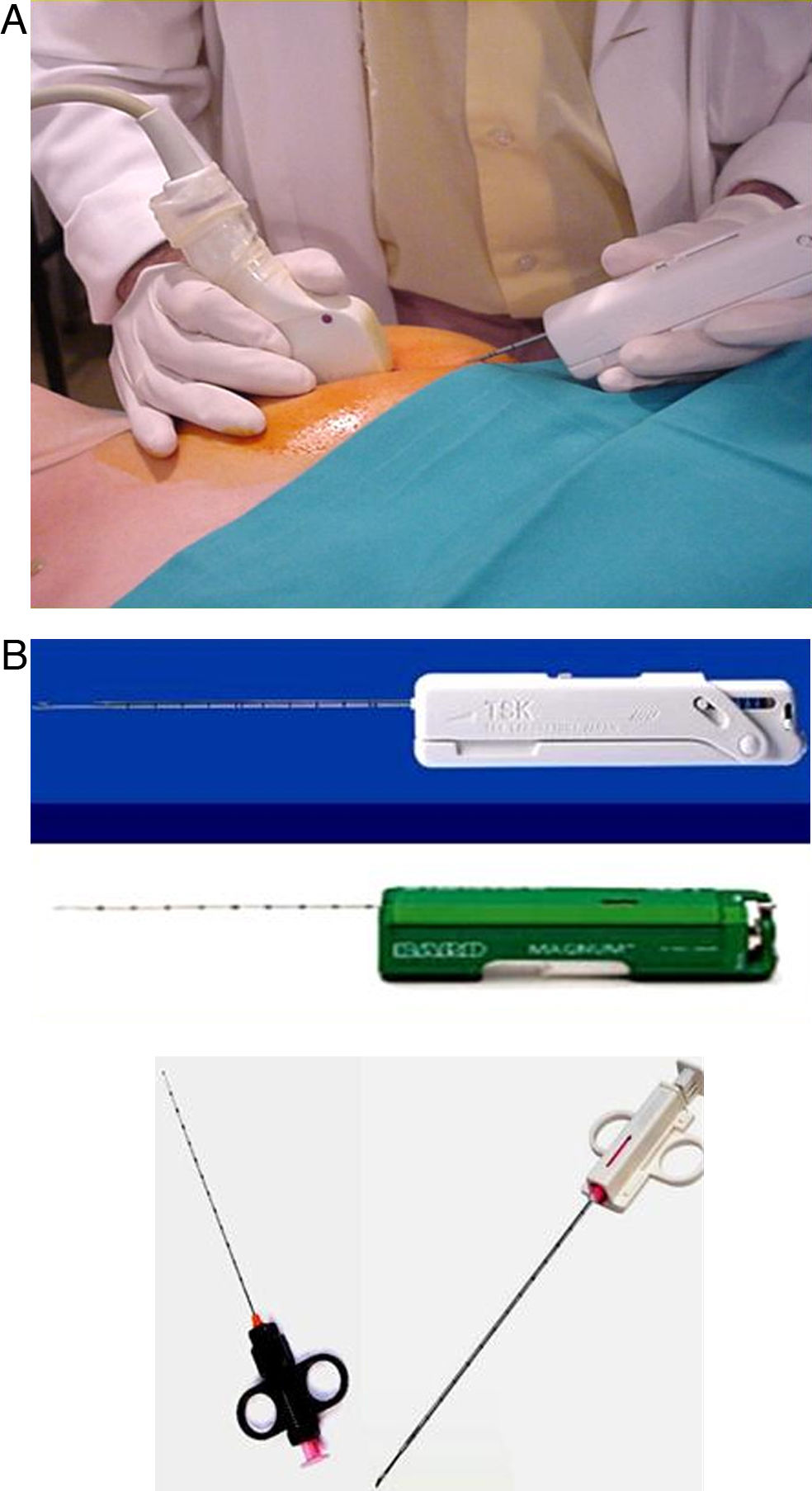
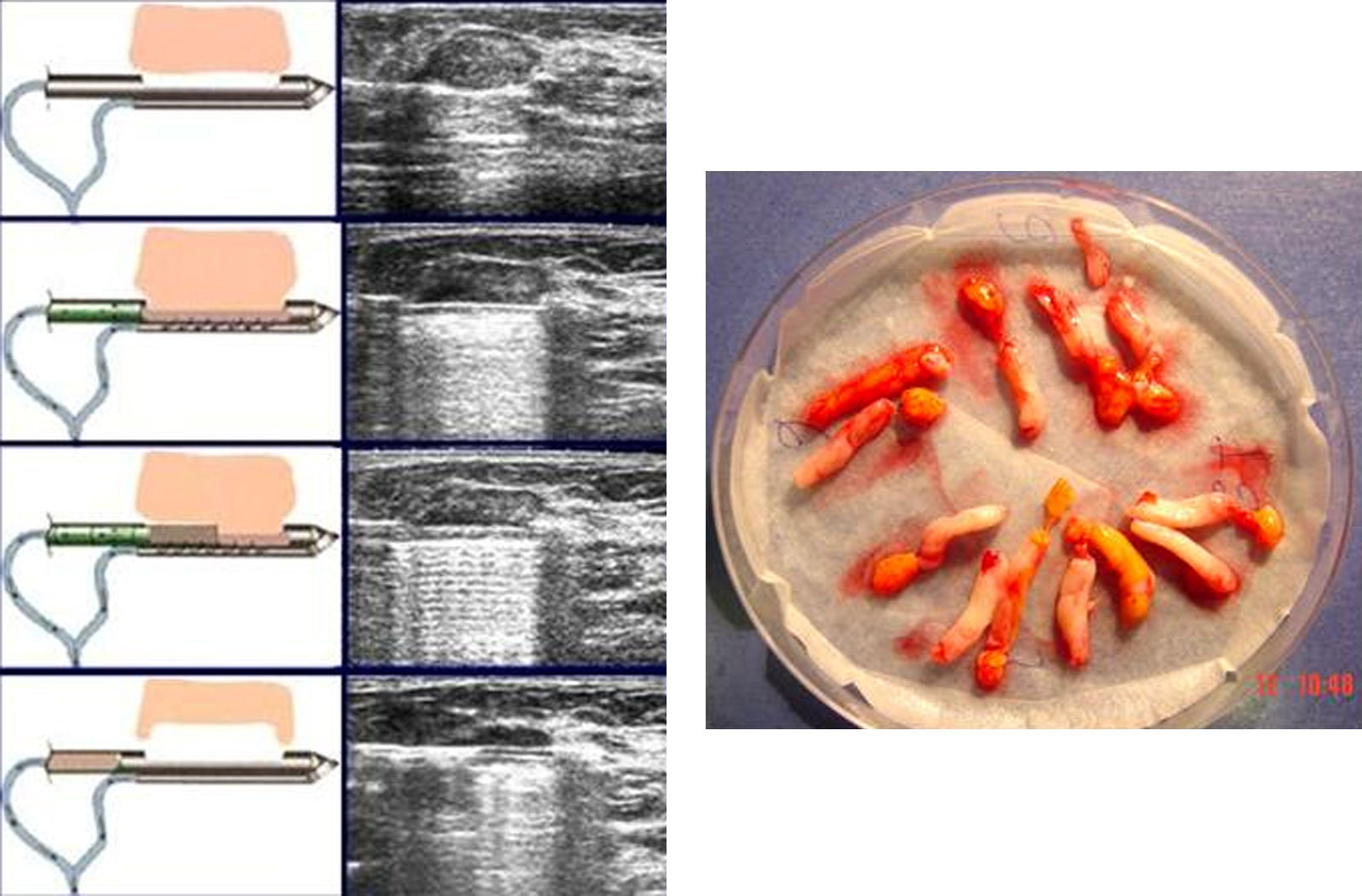
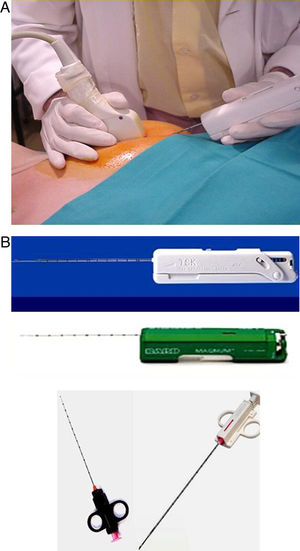
Técnica y resultadosPara la realización de la BAG se utilizan dispositivos automáticos o semiautomáticos, con agujas de corte de tipo trucut de calibre 14 G (2,1mm de sección), con las que se extrae una pequeña muestra de tejido procedente de la lesión (fig. 4). La BAG se realiza con anestesia local y, en general, se extraen de tres a 5 muestras, aunque en el caso de la biopsia de un grupo de microcalcificaciones es muy recomendable la obtención de un número superior.
Las técnicas de imagen que generalmente se utilizan como guía son la estereotaxia y especialmente la ecografía:
Guía estereotáxicaEsta técnica se basa en el cálculo de las coordenadas de situación de la lesión, a partir de la evaluación de los aparentes desplazamientos de la misma en dos imágenes mamográficas obtenidas con angulación a±15°-20° sobre la lesión. En los equipos de estereotaxia digital en mesa con la paciente en decúbito prono, el tiempo de exploración es más corto y la menor probabilidad de movimientos de la paciente mejora los resultados.
La seguridad de la biopsia mediante estereotaxia es alta, aunque existe la posibilidad de falsos negativos y en los casos de calcificaciones es posible una infravaloración de la lesión cuando el resultado de la punción es de hiperplasia atípica o carcinoma intraductal (en aproximadamente 50 y 30% de casos respectivamente puede tratarse de un carcinoma intraductal o infiltrante en la cirugía)10.
Guía ecográficaEs la técnica ideal en las lesiones que son visibles por ultrasonidos. Es muy similar a la técnica referida para la PAAF, aunque el mayor calibre de la aguja obliga a utilizar anestesia local.
La guía por ecografía es más deseable que la estereotáxica ya que no utiliza radiaciones ionizantes, es más eficaz en el abordaje de lesiones en cualquier localización, permite el control en tiempo real de la aguja y es más cómoda para la paciente. Además, los costes son menores.
Como la PAAF, es una técnica que prácticamente carece de complicaciones, siendo posible incluso realizarla en pacientes en tratamiento con anticoagulantes. La complicación más habitual es la producción de hematomas, generalmente de pequeño tamaño, y que no requieren de tratamiento.
La siembra de células malignas en el trayecto de la aguja no es exclusivo de la BAG, ya que puede ocurrir en cualquier procedimiento intervencionista, incluida la biopsia quirúrgica, y se considera prácticamente irrelevante11.
El neumotórax es extraordinariamente raro si se realiza una técnica de punción adecuada.
VentajasLa principal ventaja es que con la BAG se obtiene un diagnóstico histológico de todo tipo de lesiones, con una probabilidad de obtener muestras insuficientes muy inferior a la citología. La seguridad diagnóstica de la técnica con guía ecográfica es muy alta, superior al 95%12,13.
Otra ventaja de esta técnica es que permite diferenciar el carcinoma intraductal del infiltrante en la mayor parte de los casos, por lo que se facilita la toma de decisiones quirúrgicas en un solo tiempo. Además, reduce los costes del proceso de biopsia al disminuir muy significativamente la cirugía diagnóstica.
InconvenientesLos inconvenientes más importantes de esta técnica están generalmente ligados a la biopsia de calcificaciones:
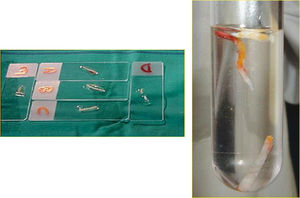
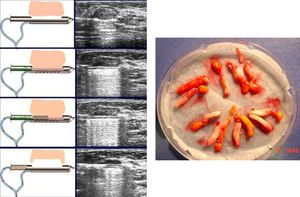
Error en la toma de muestrasLa BAG extirpa unas pequeñas muestras de tejido de la lesión, lo que puede resultar no representativo de la misma. En lesiones de alta sospecha, un resultado de malignidad se asume como correcto. Sin embargo, si el resultado es benigno puede haber duda sobre la validez de la muestra (especialmente en microcalcificaciones), por lo que está indicada una nueva BAG o una biopsia quirúrgica. Una muestra se considera adecuada cuando los hallazgos histológicos son concordantes con la imagen y la exploración clínica.
Un signo de utilidad es la valoración de la flotabilidad de los cilindros extraídos (los que se hunden en formol suelen ser representativos de la lesión biopsiada) (fig. 5).
Infravaloración histológicaUn resultado en la BAG de hiperplasia atípica o carcinoma intraductal puede subestimar en porcentajes significativos la existencia de un carcinoma intraductal o infiltrante. Es más frecuente en microcalcificaciones, y obliga a la confirmación del diagnóstico con una nueva punción o una biopsia quirúrgica14.
Por otra parte, hay un conjunto de lesiones consideradas también de riesgo, que pueden igualmente ser mal valoradas o infravaloradas por la BAG: en los casos con resultado de tumor papilar benigno, cicatriz radial, tumor fillodes benigno o carcinoma lobulillar in situ será necesario recurrir a la cirugía, o a la técnica de la biopsia asistida por vacío (BAV) (ver apartado siguiente), para conseguir un diagnóstico más concluyente.
IndicacionesLa BAG está indicada en todas las lesiones palpables y no palpables de sospecha intermedia o alta (categorías 4 y 5 de BI-RADS) y en casos seleccionados en los que esté indicado el diagnóstico histológico de lesiones probablemente benignas (categoría 3 de BI-RADS) en lugar del seguimiento radiológico.
Al igual que en la PAAF, algunos autores prefieren utilizar la BAG en los casos de adenopatías axilares u en otras localizaciones accesibles debido a que aporta un diagnóstico mas preciso.
Biopsia asistida por vacíoLas técnicas de BAV nacen con el fin de conseguir una muestra más abundante de la lesión y con ello reducir los casos de falsos negativos y los errores de infravaloración que se producen con la BAG.
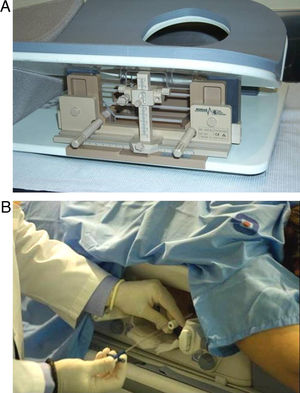
Técnica y resultadosLos sistemas BAV aprovechan el efecto de aspiración, gracias a una potente bomba de vacío conectada al dispositivo, con el efecto de corte que proporciona un bisturí giratorio interno que discurre por el alma de la aguja. Las muestras se obtienen tras ser la lesión atraída por el vacío hacia la cámara de extracción de la aguja (una abertura en su parte distal), y una vez allí ser cortadas por el bisturí interno. Las agujas que se emplean con esta técnica son de calibres entre 8G-14G. Al cortar las muestras de forma continua y contigua, la cantidad y calidad de las mismas es mayor que la que se obtiene con la BAG (fig. 6).
Para la realización de la BAV se puede utilizar cualquiera de los tres posibles sistemas de guía: estereotáxica, ecográfica y por RM.
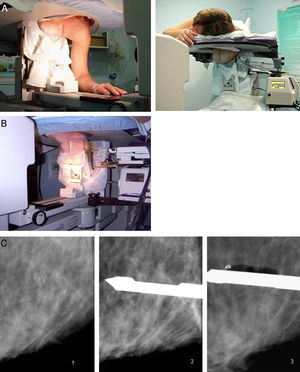
La guía estereotáxica es la más frecuentemente utilizada y hoy se considera la técnica más adecuada en la biopsia percutánea de las calcificaciones mamarias sospechosas, a causa de los falsos negativos y de la infravaloración histológica que se producen con la BAG (fig. 7).
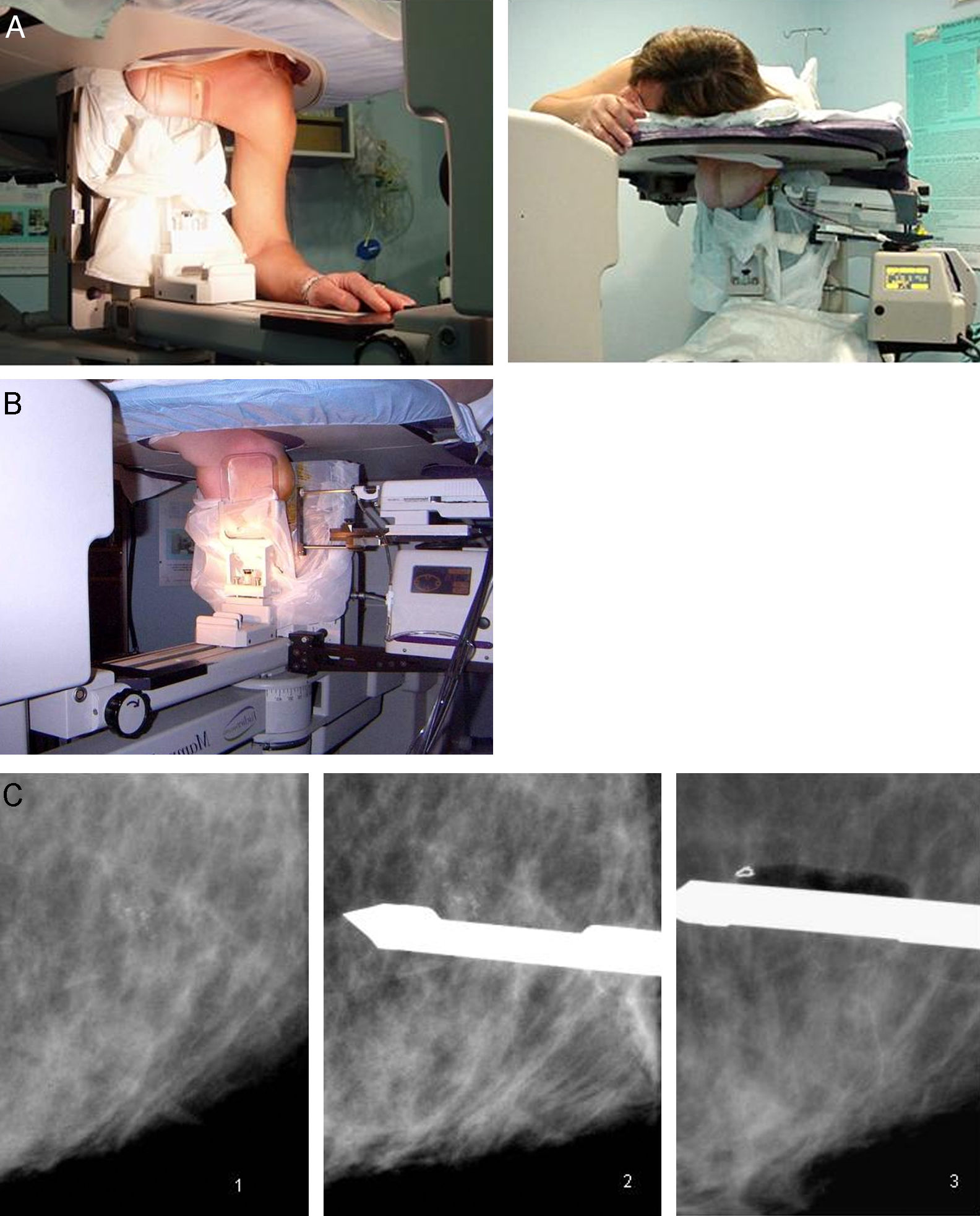
Técnica de estereotaxia mediante utilización de sistema de biopsia asistido por vacío (BAV). A) Colocación de la paciente en la mesa prona. Para acceso a la cola mamaria es útil la colocación del brazo en la abertura; B) Punción con sistema de BAV con cánula de calibre 11G (acceso lateral); C) Biopsia con cánula de sistema asistido por vacío 11G de calcificaciones. Tras su extirpación se coloca un clip de marcado del lecho de biopsia.
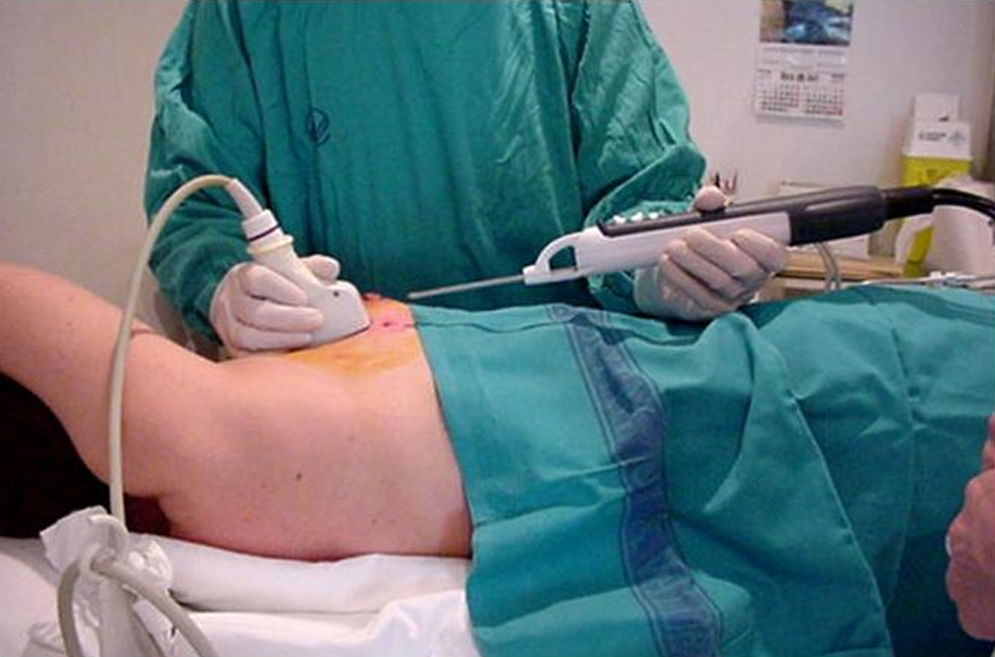
La guía ecográfica no difiere significativamente de la BAG (fig. 8) y no aporta un mayor rendimiento diagnóstico en los casos de biopsia de las masas visibles por ultrasonidos, por lo que no se debe de emplear como alternativa a la BAG al resultar más agresiva y de mayor coste. Sin embargo, debido a la potencial capacidad de extirpación completa de la lesión que existe con la BAV, esta técnica puede ser muy eficaz como alternativa terapéutica en lesiones de categoría BI-RADS 315.
La guía por RM es poco utilizada debido a su complejidad, poca disponibilidad y alto coste (fig. 9). Indudablemente, es la técnica idónea cuando los hallazgos solamente son visibles por RM, tras la comprobación de que la mamografía y la ecografía no pueden ser utilizadas como sistemas de guía.
Debido a que con estas técnicas de BAV es posible la extirpación completa de la lesión, en algunas situaciones es necesaria la utilización de marcadores metálicos no ferromagnéticos para identificar el lecho de la misma en previsión de que sea necesaria su extirpación quirúrgica posterior (pacientes con un resultado de carcinoma, lesión de alto riego o sospecha de infravaloración). La colocación de estos marcadores está especialmente indicada tras la extirpación completa de lesiones de las categorías 4 y 5 de pequeño tamaño, ya que existe una alta probabilidad de que sea necesaria la extirpación quirúrgica posterior del lecho de biopsia. La colocación de estos marcadores se puede realizar inmediatamente después del procedimiento (a través de la aguja de punción), o de forma diferida utilizando como guía el hematoma en el lecho de la biopsia (con guía ecográfica).
La seguridad de la BAV es muy alta, equivalente a la de la cirugía. Sin embargo no se debe olvidar que existe la posibilidad de un falso negativo y aunque estos dispositivos reducen significativamente las infravaloraciones histológicas (casos con resultado de hiperplasia epitelial atípica y carcinoma intraductal), no las eliminan de forma definitiva, ya que en aproximadamente 20% de los casos de hiperplasia atípica y un 10% de los carcinoma intraductales en la BAV son carcinomas intraductales o infiltrantes en la cirugía respectivamente16. La infravaloración histológica también es posible en casos con resultado de tumor papilar, incluso con extirpaciones completa de la lesión.
Entre las complicaciones, hay que resaltar que la producción de hematomas es mayor que con la BAG, especialmente cuando se utiliza la guía ecográfica o por RM, al haber un menor grado de compresión de la mama durante el procedimiento. Sin embargo, estos hematomas en general se resuelven sin necesidad de tratamiento. Por otra parte, con la BAV el procedimiento puede ser más doloroso, por lo que habitualmente es preciso administrar dosis mayores de anestésico local.
IndicacionesExisten diversos tipos de indicaciones en función del tipo de guía que se vaya a utilizar. Para la mayor parte de los radiólogos, la guía de utilización más frecuente es la estereotáxica, cuya indicación fundamental es la biopsia de microcalcificaciones sospechosas y distorsiones de la arquitectura. Al obtener mayor cantidad de muestras, se reduce la posibilidad de casos de infravaloración.
Para la guía ecográfica las indicaciones más relevantes son la repetición de la biopsia tras un resultado histológico de alto riesgo o incongruente con la BAG, la extirpación de nódulos de naturaleza probablemente benigna como alternativa a la cirugía y la extirpación de lesiones papilares intraquísticas e intraductales.
Para la guía con RM la única indicación es la biopsia de las lesiones sospechosas solamente visibles con esta técnica de imagen.
GalactografíaLa secreción mamaria es un síntoma común en patología mamaria y frecuentemente responde a un origen medicamentoso o un proceso que no depende de una patología local de la mama. Solamente en el caso de una secreción unilateral, por un solo orificio y de forma espontánea, es decir, sin expresión de la mama, estaremos probablemente ante una secreción patológica, la cual suele ser serosa, serosanguínea o sanguinolenta siendo su causa más frecuente el papiloma intraductal. El cáncer de mama es una causa relativamente infrecuente, oscilando entre el 1 y el 15% de los casos publicados17.
El manejo de la secreción mamaria ha sido un tema controvertido. Aunque hay cirujanos que realizan la extirpación del tejido retroareolar con el fin de incluir el conducto secretante sin un estudio de imagen previo, generalmente se acepta que la realización de una galactografía antes de la toma de decisiones quirúrgicas es una medida adecuada, ya que proporciona la certeza de la existencia o no de una lesión intraductal y su localización precisa en el conducto patológico18.
Técnica y resultadosLa galactografía se realiza generalmente con la paciente en decúbito supino. La canalización del conducto galactofórico en el que se produce la secreción se realiza mediante catéteres apropiados o sondas de sialogafía, tras expresión suave de la mama para identificarlo.
Tras desinfectar el pezón, se introduce el catéter unos 5-10mm, previamente purgado de burbujas. A continuación, se inyecta una pequeña cantidad de contraste yodado hidrosoluble (0,5-1ml) hasta que la paciente nota escozor o dolor. Tras la inyección, el catéter se puede extraer o dejarlo introducido para posibles reinyecciones y se realizan dos proyecciones mamográficas ortogonales (craneocaudal y mediolateral), preferentemente magnificadas.
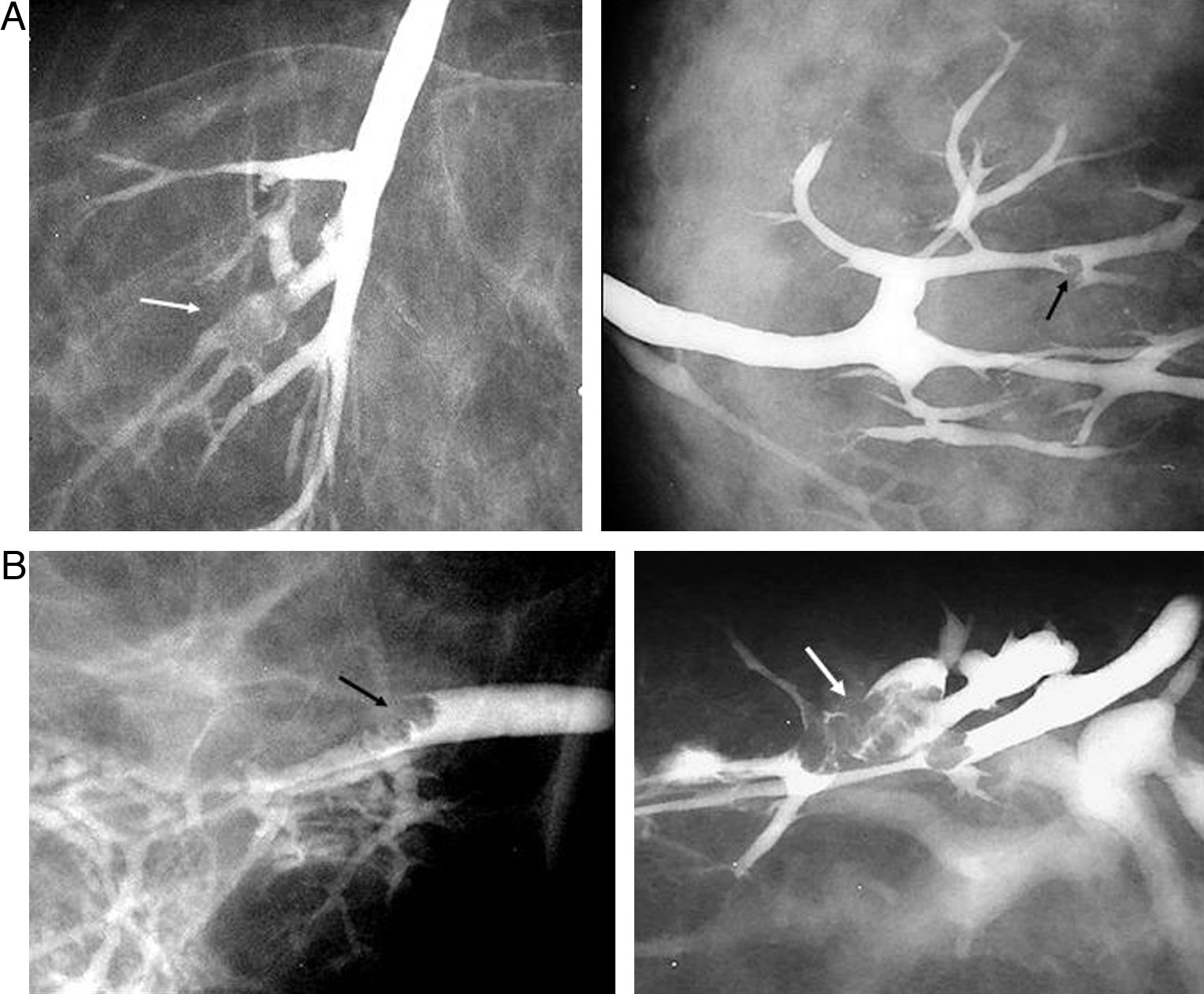
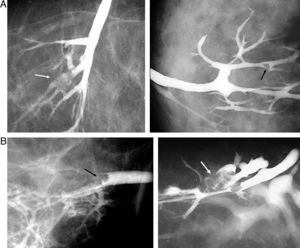
Las lesiones intraductales se identifican como imágenes de defecto de repleción o stop de la columna de contraste (fig. 10). La mayor parte de las lesiones responsables de la secreción son benignas, fundamentalmente papilomas.
Galactografía: hallazgos patológicos. A) Imagenes de galactografía que muestra un defecto de repleción en el ductus característico de una lesión papilar intraductal (flecha); B) Defectos de repleción característico de papiloma intraductal (flecha). No es posible descartar carcinoma papilar.
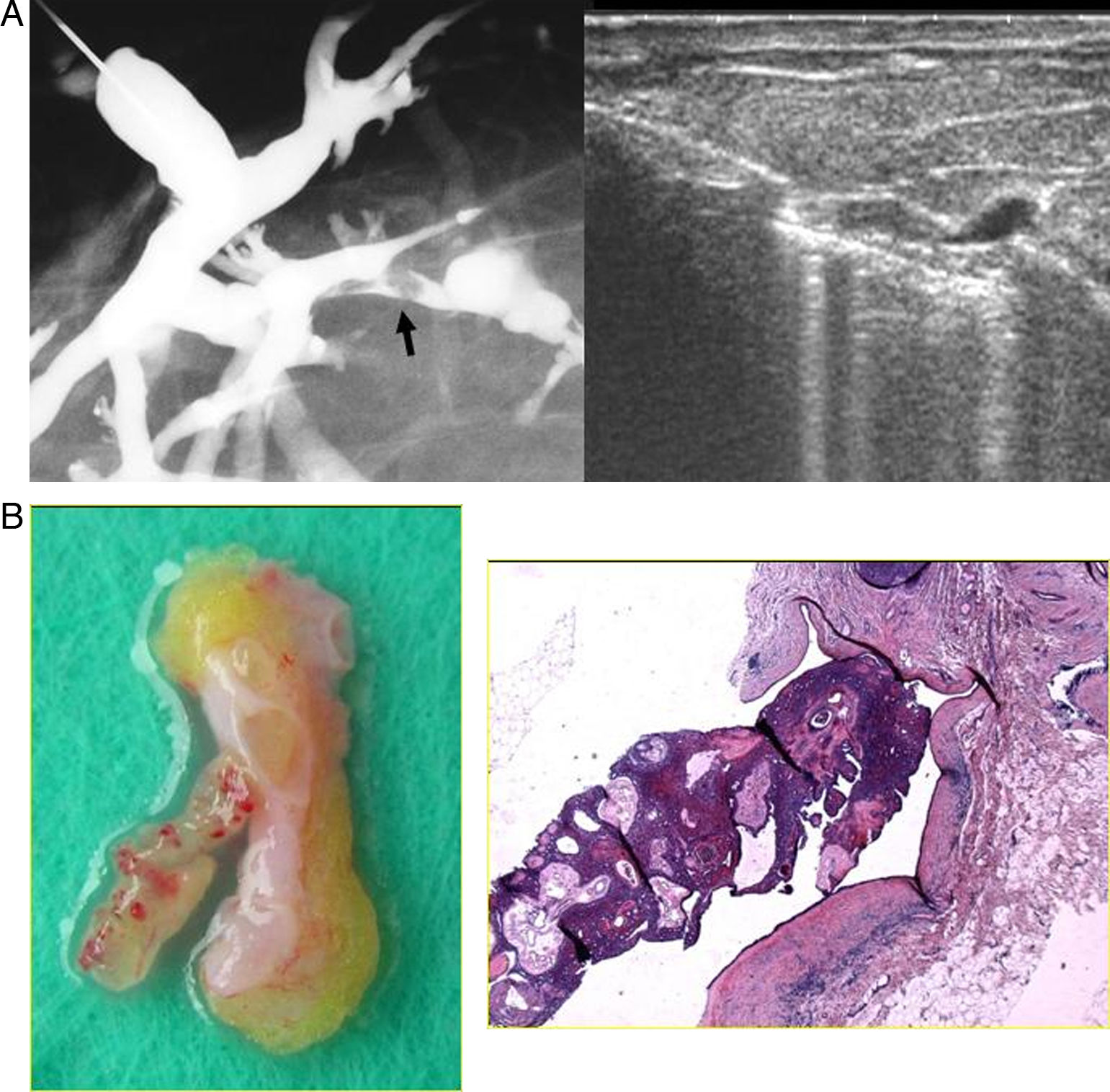
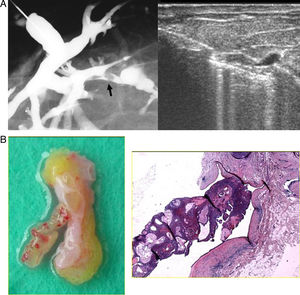
La extirpación de la lesión intraductal detectada por galactografía puede realizarse mediante procedimientos percutáneos de BAV, guiados generalmente por ecografía19, en centros que disponen de esta técnica (fig. 11).
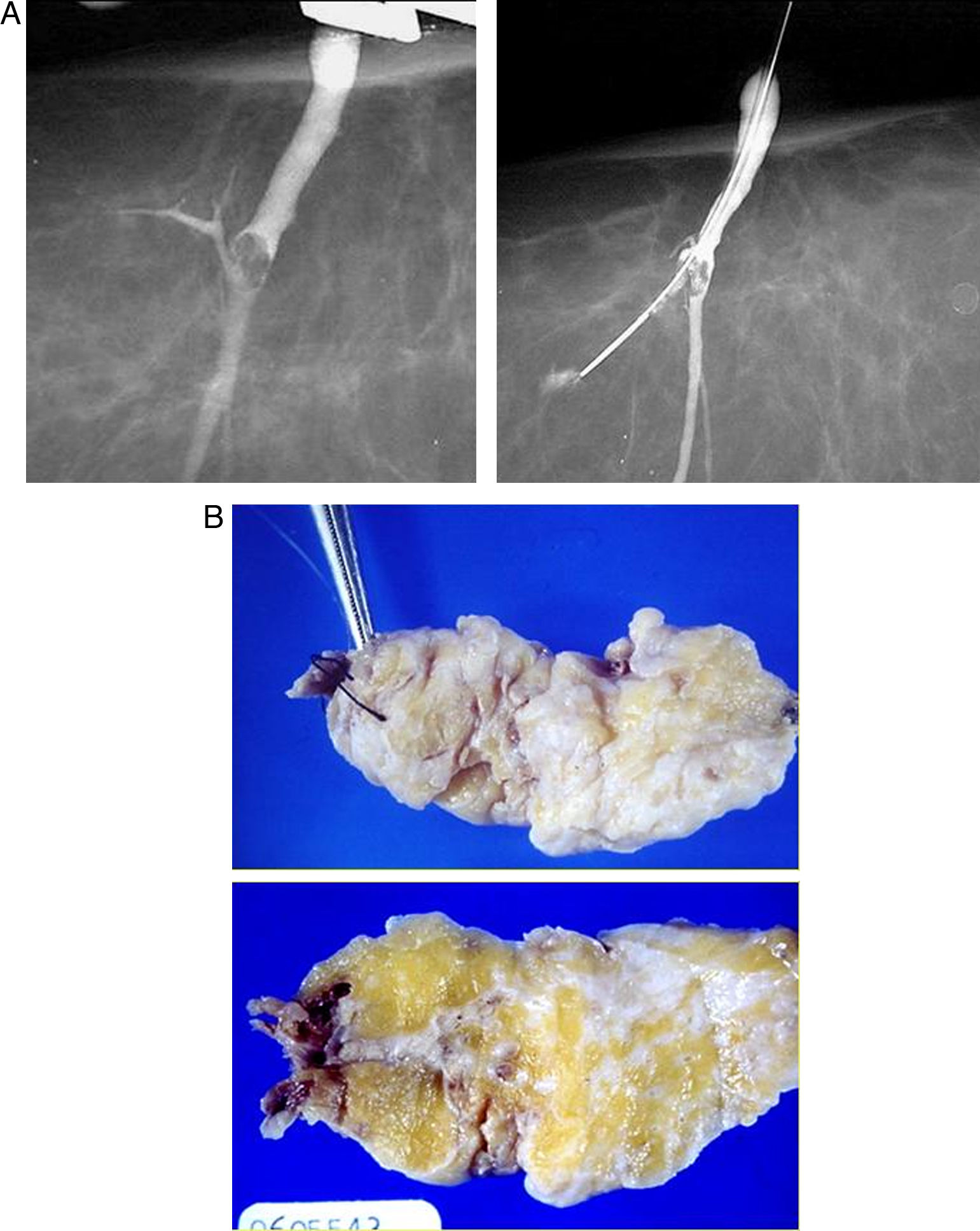
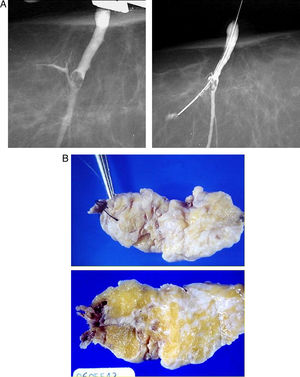
La localización para biopsia quirúrgica de estas lesiones galactográficas se realiza gracias a las coordenadas que nos proporciona la propia galactografía («galactoarpón»), o bien pueden utilizarse otras técnicas de identificación del conducto patológico mediante la inyección de azul de metileno o la introducción de guías metálicas (fig. 12). La localización preoperatoria del conducto patológico es importante, ya que en caso contrario hay altas posibilidades de no identificar la lesión en la pieza quirúrgica20.
IndicacionesLa galactografía está indicada en casos de secreción patológica por el pezón por su alta probabilidad de asociación con lesión intraductal, generalmente papilomas.
No está indicada en secreciones bilaterales o multiorificiales, ya que con la excepción de la ectasia ductal, habitualmente no representan patología mamaria.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
AgradecimientosAl Dr. Vicente Martinez de Vega y la Dra. Mercedes Torres Tabanera por las imágenes de las figuras 9 y 11, respectivamente.