La hemorragia digestiva (HD) supone un problema diagnóstico tanto en su forma de presentación aguda, que requiere una rápida localización del punto de sangrado, como en la crónica, que precisa de exploraciones repetidas para determinar su etiología. El diagnóstico y tratamiento se basa en estudios endoscópicos, aunque los estudios radiológicos mediante angiografía por tomografía computarizada (TC) en la hemorragia aguda y mediante TC enterografía en la crónica son cada día más utilizados en la práctica clínica, a pesar de no estar incluidos todavía en las guías clínicas de la HD. La TC puede ser una exploración diagnóstica de primera elección en la hemorragia aguda masiva, sustituyendo a la angiografía, y una exploración diagnóstica complementaria a la cápsula endoscópica y la gammagrafía en la hemorragia crónica o recurrente cuando se sospecha un origen en el intestino delgado. La angiografía es actualmente un método terapéutico complementario a la endoscopia en el manejo de esta afección.
Gastrointestinal bleeding represents a diagnostic challenge both in its acute presentation, which requires the point of bleeding to be located quickly, and in its chronic presentation, which requires repeated examinations to determine its etiology. Although the diagnosis and treatment of gastrointestinal bleeding is based on endoscopic examinations, radiological studies like computed tomography (CT) angiography for acute bleeding or CT enterography for chronic bleeding are becoming more and more common in clinical practice, even though they have not yet been included in the clinical guidelines for gastrointestinal bleeding. CT can replace angiography as the diagnostic test of choice in acute massive gastrointestinal bleeding, and CT can complement the endoscopic capsule and scintigraphy in chronic or recurrent bleeding suspected to originate in the small bowel. Angiography is currently used to complement endoscopy for the treatment of gastrointestinal bleeding.
La hemorragia digestiva (HD) constituye un problema clínico importante, siendo una causa frecuente de hospitalización, con una mortalidad en su presentación aguda entre el 6 y el 10% en la hemorragia digestiva alta (HDA) y del 4% en la hemorragia digestiva baja (HDB). Su estudio y tratamiento requiere un abordaje multidisciplinario en el que se encuentran implicados digestólogos, endoscopistas, cirujanos y radiólogos. Las hemorragias digestivas son autolimitadas en el 80% de casos, requiriendo únicamente tratamiento médico de soporte, aunque la persistencia de la misma supone un reto diagnóstico para localizar el lugar del sangrado (especialmente en sangrados importantes) y determinar si es posible su causa. Esto permitirá seleccionar el manejo terapéutico más adecuado, con el fin de disminuir la morbimortalidad, acortar el tiempo de hospitalización y disminuir los requerimientos transfusionales.
Tipos de hemorragia digestivaDebemos distinguir entre diferentes escenarios clínicos en la HD, según su lugar de origen y forma de presentación.
Hemorragia digestiva según su origenHemorragia digestiva altaEs la hemorragia proximal al ángulo de Treitz, corresponde al 75% de las HD y se presenta en forma de hematemesis o melenas, sin embargo si la hemorragia es muy abundante puede manifestarse en forma de sangre roja rectal. La colocación de una sonda nasogástrica puede orientar hacia un origen en el tracto digestivo superior, aunque debe evitarse en pacientes hepatópatas para no causar lesiones en posibles varices esofágicas. La causa más frecuente de HDA es la enfermedad ulcerosa péptica y las varices esofágicas en pacientes con hipertensión portal, aunque su etiología puede ser muy variada (tabla 1).
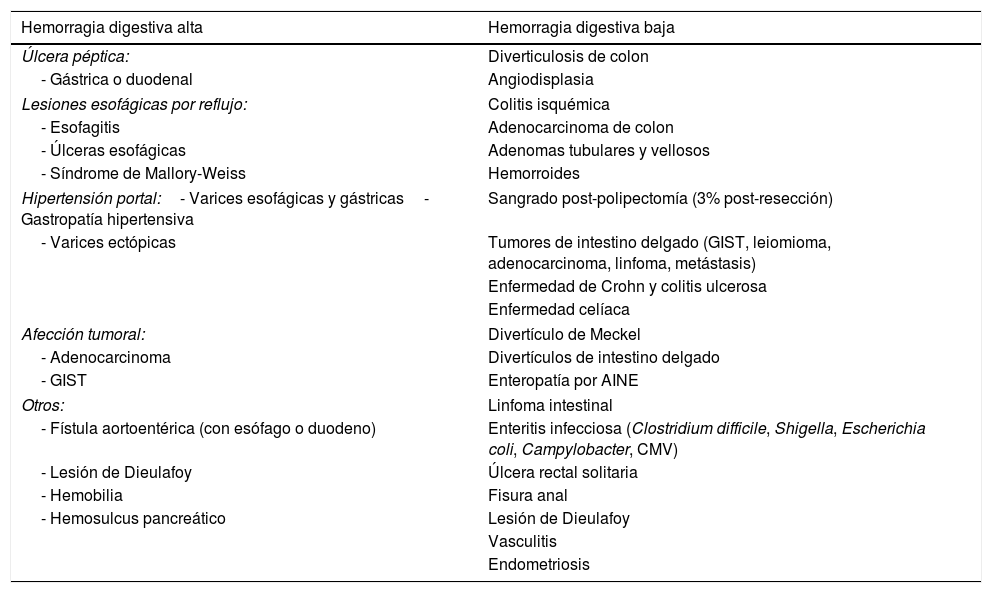
Principales causas de hemorragia digestiva
| Hemorragia digestiva alta | Hemorragia digestiva baja |
|---|---|
| Úlcera péptica: | Diverticulosis de colon |
| - Gástrica o duodenal | Angiodisplasia |
| Lesiones esofágicas por reflujo: | Colitis isquémica |
| - Esofagitis | Adenocarcinoma de colon |
| - Úlceras esofágicas | Adenomas tubulares y vellosos |
| - Síndrome de Mallory-Weiss | Hemorroides |
| Hipertensión portal:- Varices esofágicas y gástricas- Gastropatía hipertensiva | Sangrado post-polipectomía (3% post-resección) |
| - Varices ectópicas | Tumores de intestino delgado (GIST, leiomioma, adenocarcinoma, linfoma, metástasis) |
| Enfermedad de Crohn y colitis ulcerosa | |
| Enfermedad celíaca | |
| Afección tumoral: | Divertículo de Meckel |
| - Adenocarcinoma | Divertículos de intestino delgado |
| - GIST | Enteropatía por AINE |
| Otros: | Linfoma intestinal |
| - Fístula aortoentérica (con esófago o duodeno) | Enteritis infecciosa (Clostridium difficile, Shigella, Escherichia coli, Campylobacter, CMV) |
| - Lesión de Dieulafoy | Úlcera rectal solitaria |
| - Hemobilia | Fisura anal |
| - Hemosulcus pancreático | Lesión de Dieulafoy |
| Vasculitis | |
| Endometriosis | |
La HDB se origina entre el ángulo de Treitz y el recto, supone alrededor de un 25% de las HD y se presenta clínicamente en forma de rectorragia, hematoquecia o melenas, según la cuantía y localización del sangrado. Hasta en un 12% de casos con diagnóstico inicial de HDB, su origen es alto, especialmente en sangrados importantes. Las causas más comunes de HDB incluyen la angiodisplasia y la diverticulosis (tabla 1), aumentando su incidencia con la edad debido a la mayor frecuencia de estas afecciones1. En pacientes jóvenes, las causas más comunes son inflamatorias e infecciosas.
Recientemente se ha propuesto una nueva clasificación basada en el acceso endoscópico a las diferentes partes del tracto gastrointestinal, introduciendo el concepto de HD media, con origen entre la papila de Vater y el íleon terminal, poco accesible a los estudios endoscópicos convencionales y cuyo estudio precisa la enteroscopia con doble balón o la cápsula endoscópica2–4.
Hemorragia digestiva según su forma de presentación:Hemorragia visibleSangrado digestivo que se manifiesta por la presencia de sangre en los vómitos (hematemesis si corresponde a sangre fresca, o vómito «en poso de café» si corresponde a sangre negra) o las heces (melenas si corresponde a heces negras o hematoquecia/rectorragia si corresponde a sangre roja).
Hemorragia ocultaPacientes con sangre oculta en heces medida con método inmunológico (fecatest) y/o anemia ferropénica sin sangrado clínico evidente.
Hemorragia agudaLa hemorragia aguda se clasifica según su volumen y rapidez del sangrado, considerándose masiva aquella que precisa trasfundir al menos 4 unidades de sangre en 24 horas, en la que el paciente muestra una franca inestabilidad hemodinámica con tensiones sistólicas inferiores a 100mmHg, un descenso del hematocrito superior al 20%, una frecuencia cardiaca superior a 100 latidos/min o hemoglobina < 100g/l1. Los valores de hematocrito y hemoglobina tienen escaso valor en la evaluación inicial ya que no se alteran hasta que no se administra suero o expansores del plasma para reponer la volemia, produciéndose entonces una hemodilución. La hemorragia se considera moderada cuando no condiciona una inestabilidad hemodinámica ni precisa transfusión sanguínea. La hemorragia aguda continúa siendo una afección urgente, con un alto índice de mortalidad, que puede llegar incluso al 21-40% en hemorragias masivas5, siendo la mortalidad superior en pacientes de edad avanzada, con comorbilidad severa o resangrado1,6.
Hemorragia crónica o recurrente de origen indeterminadoCorresponde al sangrado intestinal persistente o recurrente después de estudios baritados convencionales y endoscópicos negativos3, aunque debido al escaso papel de los estudios radiológicos convencionales en esta afección, habitualmente se considera como tal aquella que persiste o recurre tras una endoscopia alta y una colonoscopia negativas7. A su vez este sangrado puede ser visible, en forma de melenas o hematoquecia (la hematemesis es una forma rara de presentación) u oculta, con fecatest positivo persistente, anemia ferropénica o ambas8. La presencia de fecatest positivo únicamente indica hemorragia crónica si se asocia a anemia ferropénica. Sus causas más frecuentes aparecen en la tabla 2.
Causas de hemorragia digestiva de origen indeterminado según su origen
| HD alta | HD baja |
|---|---|
| Lesión de Dieulafoy | Angiectasia |
| Ectasia vascular antral gástrica | Tumores de intestino delgado (adenocarcinoma, GIST, linfoma, tumor carcinoide) |
| Ectasias vasculares | Enteropatía por AINE |
| Varices gástricas o duodenales | Enfermedad de Crohn |
| Erosiones de Cameron (hernia de hiato) | Varices ectópicas |
| Gastropatía hipertensiva portal | Enfermedad celíaca |
| Úlcera péptica | Divertículo de Meckel |
| Hemobilia | Diverticulosis |
| Hemosulcus pancreáticoFístula aortoentérica | Tumores de colon (adenocarcinoma) |
HD: hemorragia digestive.
Se considera la técnica de elección en el estudio de la HDA, ya que permite localizar y tratar la lesión sangrante (coagulación térmica, inyección de epinefrina, clips, bandas o fulguración con argon-beam). Esa técnica ofrece una sensibilidad (92-98%) y una especificidad variables (30-100%)9, si bien otros estudios afirman que en un 24% de casos de HDA aguda no se llega a un diagnóstico10.
ColonoscopiaIndicada en el sangrado de colon e íleon distal. Precisa la preparación previa del colon, lo que puede retrasar la exploración unas 3-4 horas; en estos casos, además, existe un porcentaje no despreciable de colonoscopias incompletas (5-15%) y una baja sensibilidad en la detección de sangrado en algunas series, en que solo identifican el lugar de sangrado en un 13% de casos en situación de urgencia11. La propia hemorragia puede dificultar el examen adecuado de la mucosa y la visualización del punto de sangrado, de manera que el sangrado masivo (>1ml/min) o la ausencia de preparación condicionan la existencia de resultados negativos. En caso de identificar el punto de sangrado, ya sea visualizando la hemorragia activa o identificando un vaso visible, el tratamiento endoscópico ofrece una opción eficaz, con una baja morbilidad. La excepción a esta indicación es el paciente con HDB masiva12.
Cápsula endoscópicaLa cápsula endoscópica (CE) permite explorar la totalidad del intestino delgado y visualizar la afección gástrica o colónica que haya pasado desapercibida en un estudio inicial3. Su principal indicación es la hemorragia de origen indeterminado en la que diversos estudios muestran una mayor eficacia que otras técnicas de imagen, con una sensibilidad entre el 42 y el 80% según las series7,13. Las limitaciones de la técnica incluyen una baja resolución de la imagen, el peligro de retención de la cápsula en áreas de estenosis o divertículos, su elevado precio y la existencia de discrepancias inter-observador14. La CE está contraindicada en pacientes con marcapasos, desfibrilador, cirugía digestiva previa o sospecha de estenosis/obstrucción intestinal8. La duración de la exploración y la revisión de las imágenes hace que esta técnica tenga poca utilidad en la hemorragia aguda, especialmente si es masiva; y en la HD de origen indeterminado las mejores sensibilidades se obtienen cuando existe un sangrado activo (92,3 versus 44,2% en la HD oculta)8,15.
Endoscopia asistida con balónEsta técnica, descrita recientemente16, permite teóricamente explorar la totalidad del intestino delgado de forma anterógrada, retrógrada o una combinación de ambas, mediante la insuflación de dos balones y el pliegue del intestino sobre sí mismo, permitiendo además la realización de biopsia y/o tratamiento8,17. La tasa de enteroscopias completas mediante esta técnica es muy variable según las series, entre un 16 y un 86%17 y su rendimiento diagnóstico se sitúa entre el 55-80%7,17. Por otro lado, tiene una tasa de éxito de tratamiento del 43-81%18. La disponibilidad de esta técnica es muy variable, y precisa preparación al igual que los estudios endoscópicos convencionales7.
Medicina nuclearLos estudios gammagráficos utilizan hematíes marcados con tecnecio (Tc99m) para localizar el punto de sangrado. Detecta sangrados a débitos entre 0,1 y 0,4ml/min, con una sensibilidad del 93% y una especificidad del 95%19. Los criterios diagnósticos son el acúmulo intraluminal del trazador, el aumento progresivo de intensidad y movimiento del radiotrazador a lo largo del tiempo (por el tránsito intestinal)7. Se utilizan fundamentalmente en la HDB, donde la endoscopia tiene un papel limitado, siendo útil en la HD visible de origen indeterminado a bajo débito, en sangrados venosos y sangrados intermitentes ya que el trazador permanece en el torrente sanguíneo durante 24 horas7,8,20,21. Como contrapartida presenta problemas para localizar adecuadamente el punto de sangrado (movimiento del radiotrazador) con un 22% de falsas localizaciones22 y no permiten caracterizar su etiología19. El uso de la imagen híbrida (SPECT-TC) permite mejorar la localización del punto de sangrado23. La visualización de un sangrado precoz en el estudio gammagráfico ha sido utilizada como dato para indicar la realización de una arteriografía aumentando el rendimiento de esta exploración24, aunque otros estudios lo desmienten25. La gammagrafía tiene escaso valor en la hemorragia oculta de origen indeterminado7.
En pacientes jóvenes con HDB y sospecha de divertículo de Meckel, la gammagrafía con pertecnetato de tecnecio permite su diagnóstico ya que se acumula en la mucosa gástrica ectópica del divertículo (presente en el 50% de casos) así como en la existente en duplicaciones intestinales. La sensibilidad para detectar el divertículo de Meckel se sitúa sobre el 60-75%26, aunque el uso actual de los inhibidores de la bomba de protones como pretratamiento la aumenta hasta el 87%27.
Estudios baritadosLos estudios baritados convencionales no tienen en la actualidad ninguna indicación en el estudio de la HD debido a su baja sensibilidad7.
El papel de la enteroclisis en la hemorragia digestiva oculta fue descrito por Maglinte en 198528 y confirmado en diversos estudios29,30, aunque su eficacia diagnóstica es del 10-25%, siendo inferior a los estudios de enteroclisis o enterografía realizados con TC o RM y a los estudios de CE, por lo que es de escasa utilidad.
EcografíaLa ecografía con contraste permite detectar hemorragia activa al visualizar la extravasación del mismo, especialmente en órganos sólidos. Se ha descrito su utilidad en la valoración de lesiones traumáticas, terapia anticoagulante y rotura de aneurismas aórticos31. Un artículo reciente32 estudia su capacidad para detectar el sangrado intestinal, comparando los resultados con la endoscopia y obteniendo una sensibilidad del 73,7% y una especificidad del 97,1%, sin embargo se trata de un solo estudio, no valora el intestino delgado y, como los propios autores apuntan, se precisan más estudios prospectivos para determinar su eficacia.
TC multidetectorLa tomografía computarizada multidetector (TCMD) se usa cada vez con mayor frecuencia, ya que es un método diagnóstico ampliamente disponible, no invasivo, rápido, que permite visualizar la totalidad del tracto digestivo, detectar lesiones del mismo, identificar su vascularización, posibles anomalías vasculares, y no precisa una preparación especial en casos de sangrado agudo5,33–35. La utilidad de la TC angiografía para detectar la extravasación intraluminal de contraste en el estudio de la hemorragia oculta recurrente fue descrita en 1997 por Ettorre36, aunque el estudio de TC se realizaba tras la colocación de un catéter en la aorta abdominal para la administración de contraste, lo que suponía un procedimiento invasivo. Posteriores artículos demostraron la utilidad de la TC helicoidal en la HDB aguda mediante la inyección de contraste intravenoso37–40, y con la aparición de aparatos de TCMD, más rápidos y con colimaciones submilimétricas, numerosos estudios han demostrado su eficacia34,41.
En 2006 aparece el primer trabajo prospectivo con TCMD de 4 filas de detectores5 para la detección y localización de la hemorragia aguda masiva, mostrando una sensibilidad del 90,9% y especificidad del 99% comparado con la angiografía convencional. Otros artículos confirman la utilidad de esta técnica en la detección de HD aguda20,35,42,43, tanto alta como baja, especialmente en el sangrado masivo, pudiendo visualizar la causa del mismo en el 78% de los casos (figs. 1–7)35,43.
Sangrado digestivo en un paciente durante el postoperatorio de un bypass en la extremidad inferior. A) Corte axial de TC que muestra una ulceración en un asa de yeyuno con sangrado activo en el nicho ulceroso (flecha) e intraluminal. B) La reconstrucción coronal en MIP demuestra el sangrado a nivel de la úlcera (flecha). C) La reconstrucción en fase venosa, más tardía, evidencia una mayor acúmulo de contraste extravasado y mejor delimitación del patrón mucoso del yeyuno (flechas). El ulcus fue tratado mediante enteroscopia con colocación de hemoclip y argón. La biopsia mostró una infección por citomegalovirus.
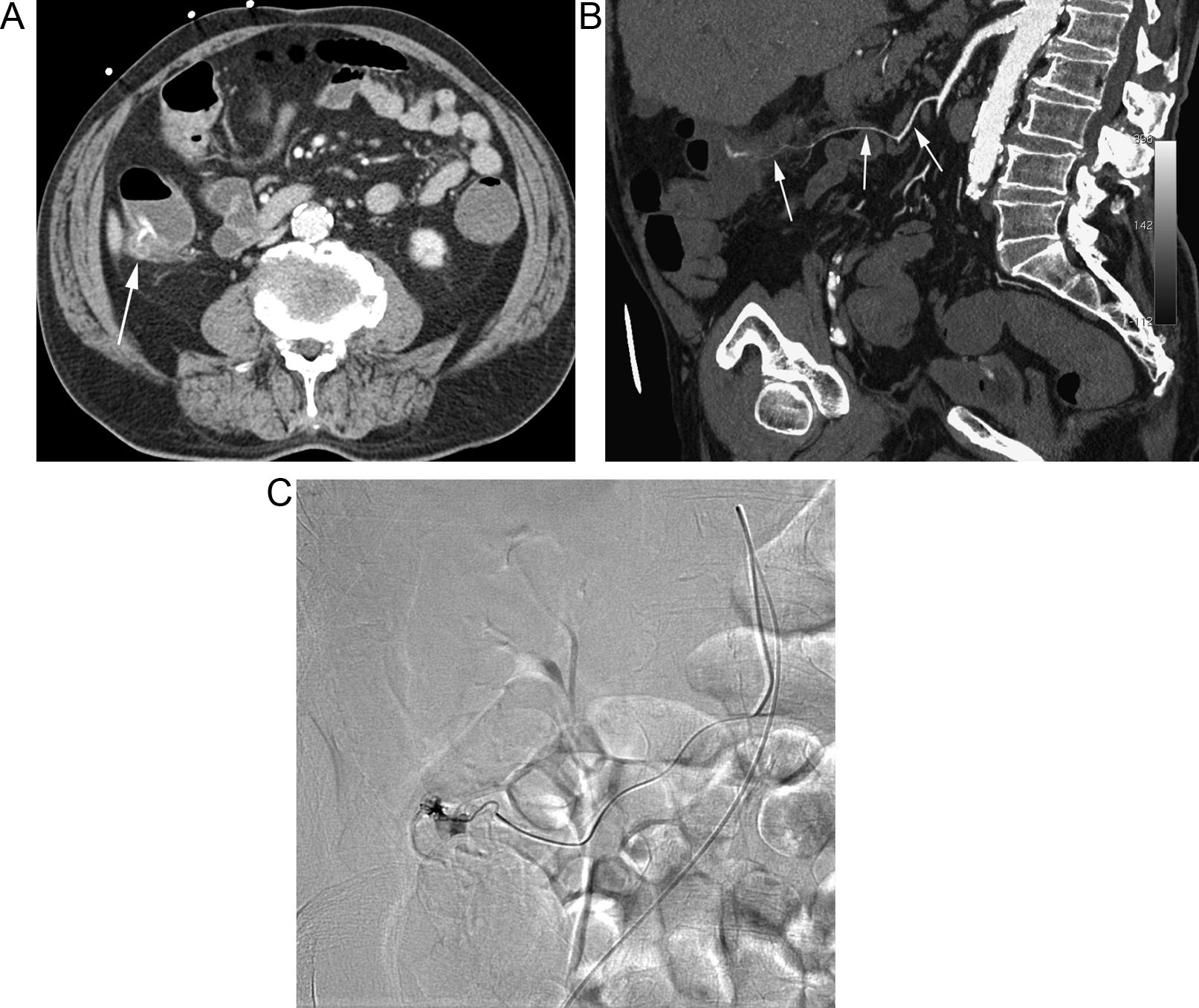
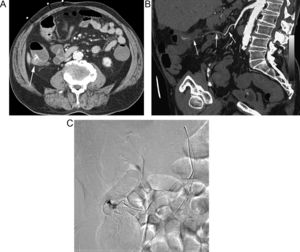
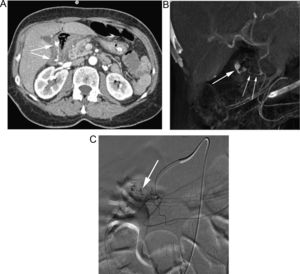
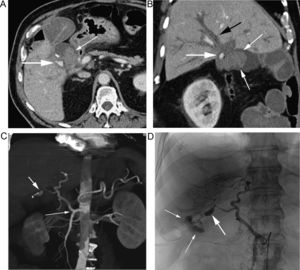
Paciente con HDB aguda masiva. A) La TC muestra una hemorragia activa de un divertículo del ángulo hepático del colon (flecha). B) La reconstrucción vascular permite demostrar el aporte vascular al divertículo sangrante (flechas) a través de una rama de la arteria cólica media. C) Arteriografía selectiva guiada por los hallazgos de la TC con embolización del vaso causante de la hemorragia.
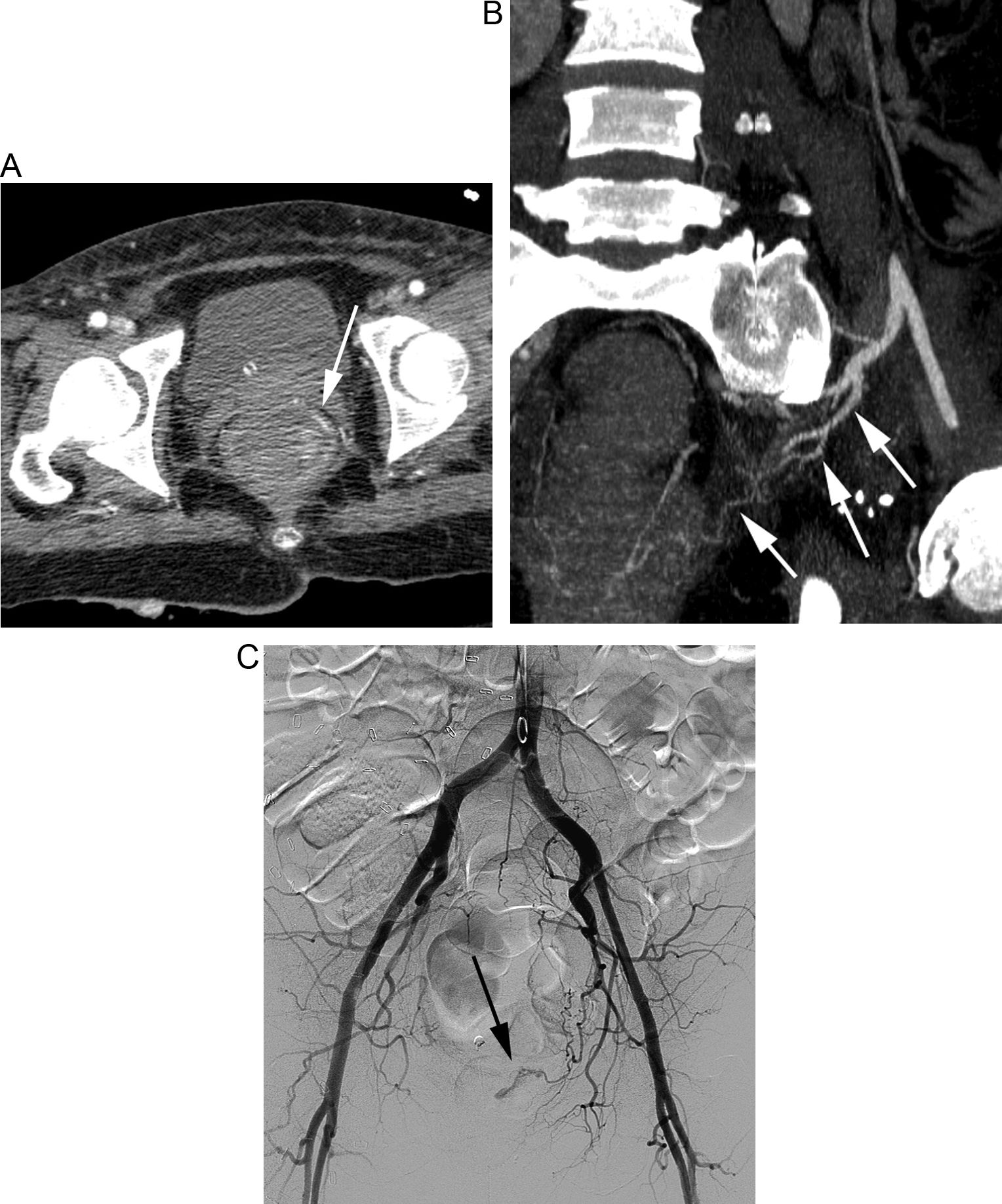
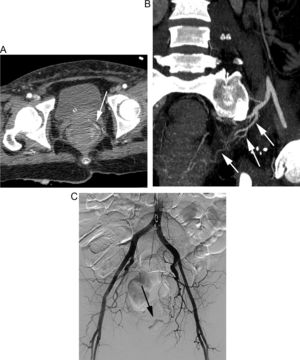
A) TC en paciente con HDB masiva que muestra la extravasación de contraste en la cara ánterolateral izquierda del recto (flecha). B) La reconstrucción curva demuestra el origen de la hemorragia, procedente de la rama hipogástrica homolateral (flechas). C) La arteriografía se realizó de forma dirigida y centrada en el sector ilíaco, evitando el estudio inicial de la arteria mesentérica inferior y confirmando el origen, así como el sangrado activo (flecha); posteriormente se realizó la embolización selectiva (no mostrada).
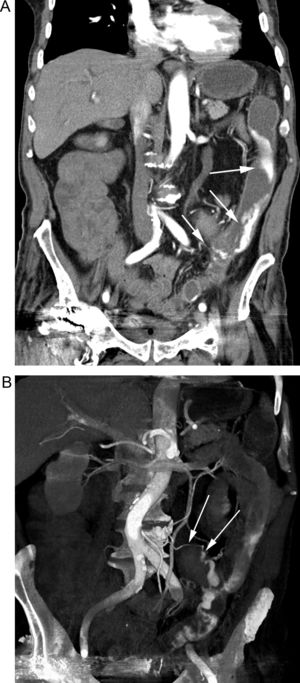
Paciente con HBD masiva en el postoperatorio de una reconstrucción de Hartmann. A) Reconstrucción coronal de TC en fase arterial tardía que muestra una extensa extravasación de contraste en el colon izquierdo (flechas). B) La reconstrucción «volume rendering» delimita el origen vascular del sangrado en una rama de la arteria mesentérica inferior (flechas).
Paciente con sospecha de HDB masiva. A) El estudio de angioTC muestra un sangrado activo en el bulbo (flechas). B) La reconstrucción MIP delimita el origen del sangrado (flecha gruesa) a través de ramas de la arteria gastroduodenal (flechas finas). C) La arteriografía guiada por TC confirma la extravasación de contraste (flecha), con posterior embolización selectiva.
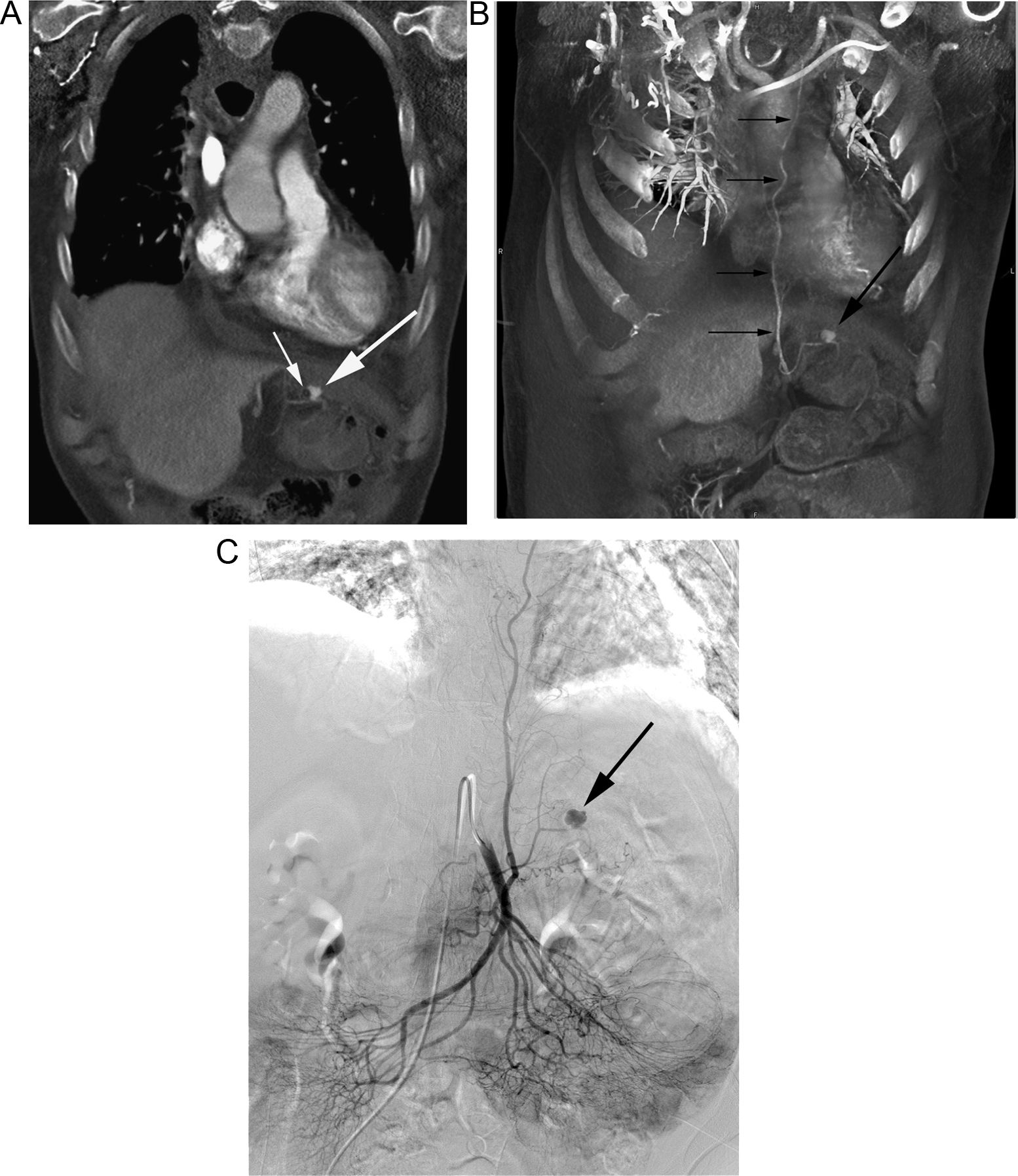
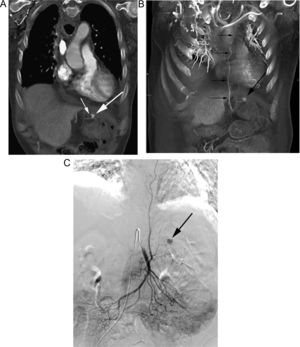
Paciente intervenido de neoplasia esofágica y reconstrucción mediante coloplastia, que presenta hematemesis. A) Reconstrucción coronal de TC que muestra un pseudoaneurisma (flecha gruesa) adyacente a la sonda de alimentación (flecha fina). B) La reconstrucción «volume rendering» demuestra el pseudoaneurisma (flecha gruesa) dependiente de una rama de la arteria cólica media (flechas finas). C) La arteriografía guiada por los hallazgos de la TC confirma la existencia del pseudoaneurisma (flecha), con posterior embolización del mismo.
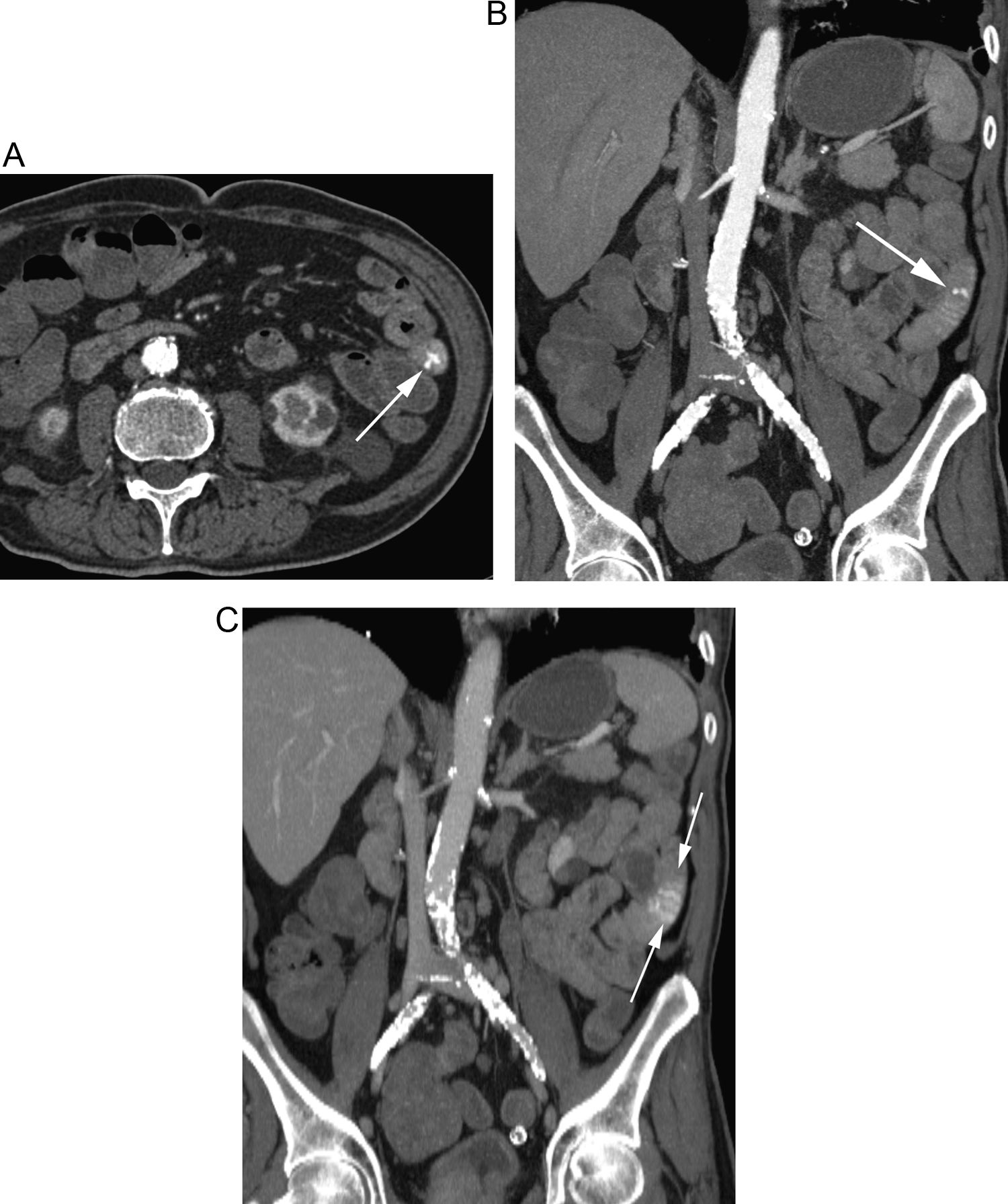
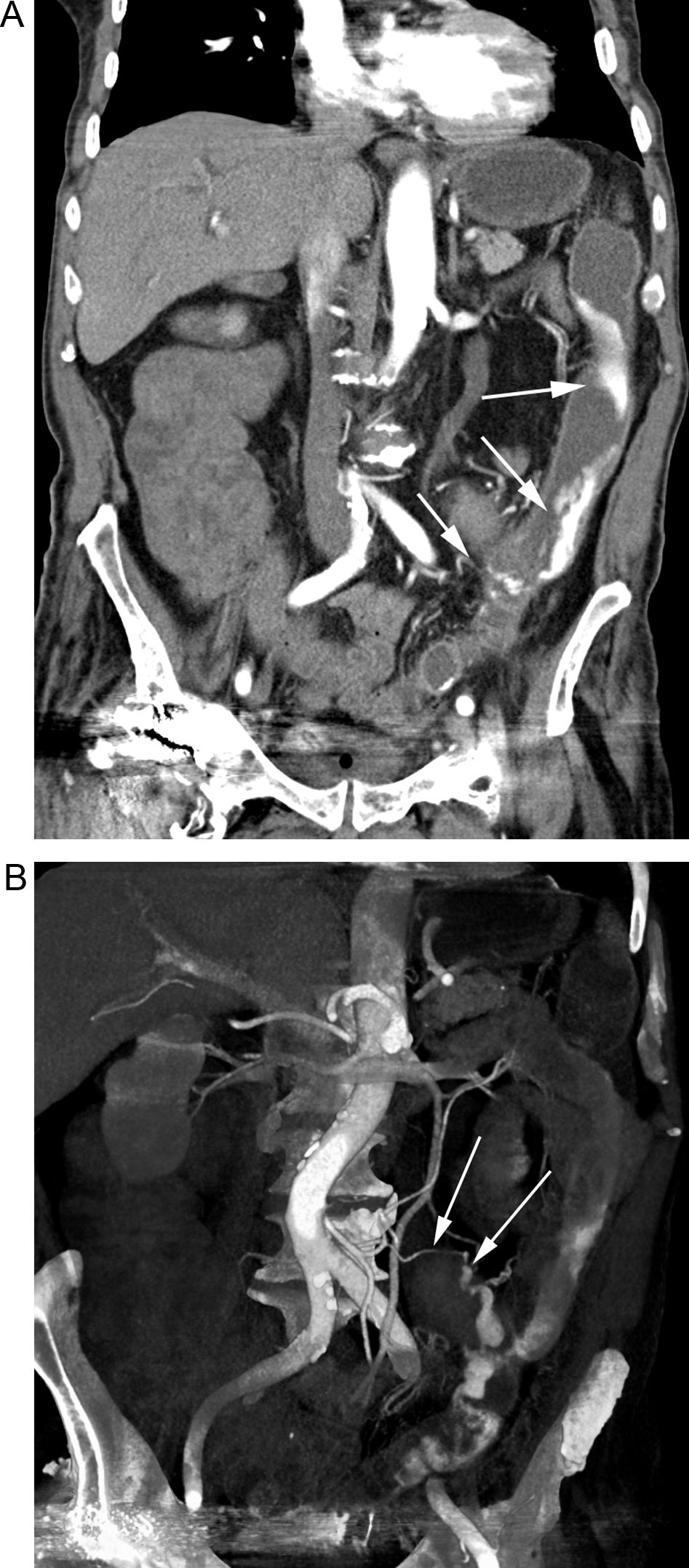
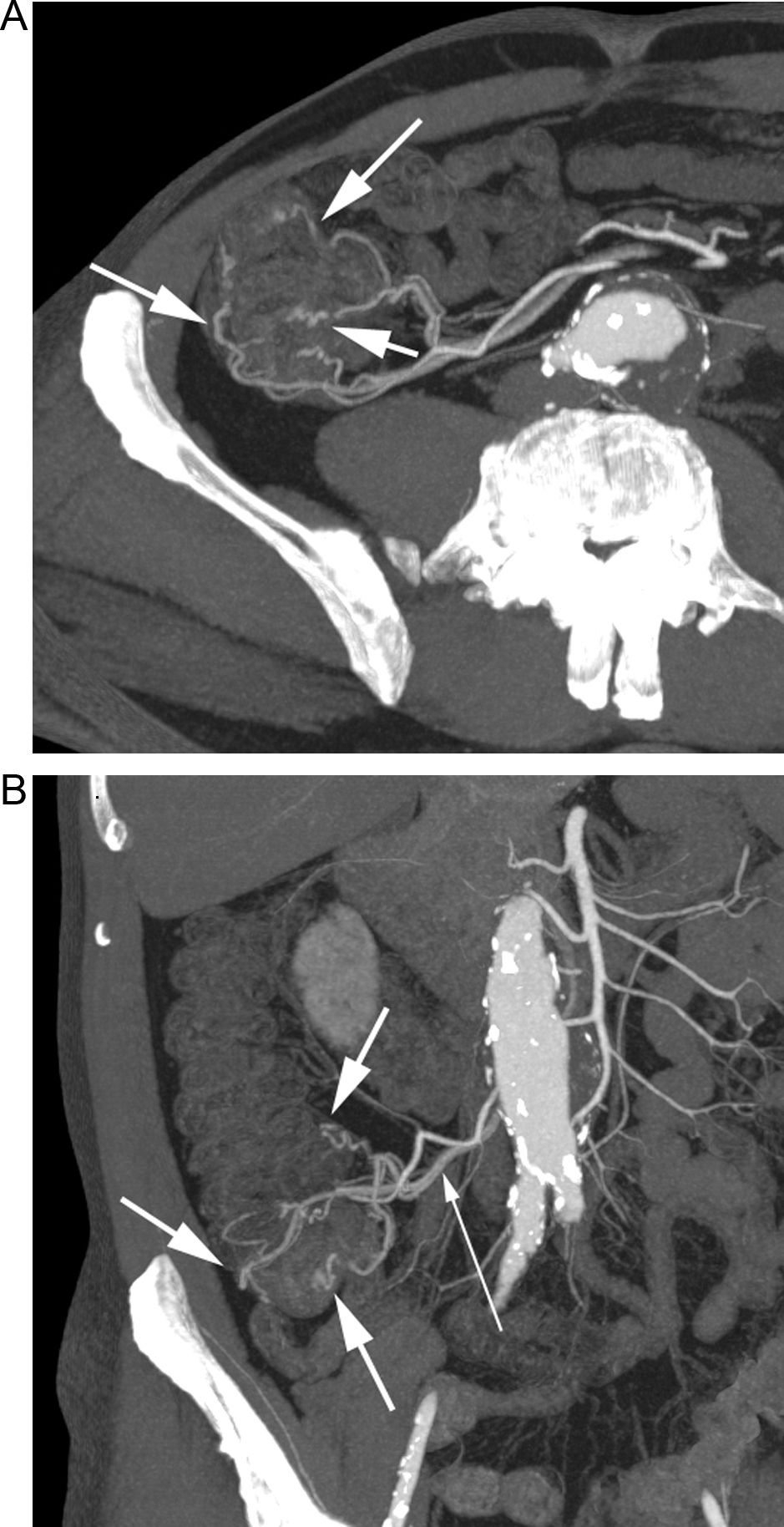
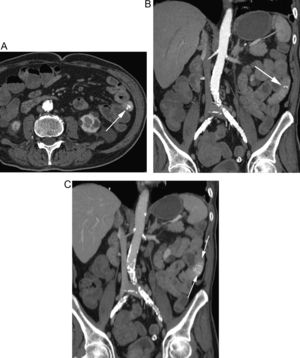
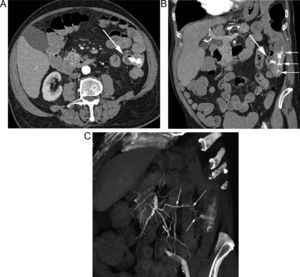
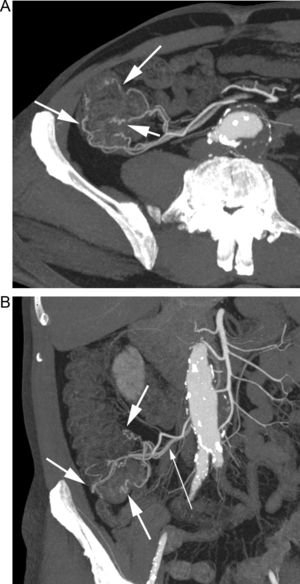
Paciente con anemia ferropénica y estudios endoscópicos previos negativos, que acude por HDB visible. A) La TC muestra extravasación de contraste en un divertículo de yeyuno (flecha). B) Reconstrucción coronal que muestra el divertículo sangrante (flecha gruesa), con extravasación de contraste a la luz intestinal (flechas finas). C) Reconstrucción «volume rendering» que muestra el aporte vascular al divertículo a través de una rama yeyunal (flechas) de la arteria mesentérica superior.
Kuhle y Sheiman demostraron en un estudio experimental animal que la TC helicoidal podía detectar sangrados a débitos tan bajos como 0,3ml/min, inferior al que necesita la angiografía si no se realiza de forma selectiva, y semejante a los requeridos por la gammagrafía44. Estos hallazgos han sido corroborados en estudios experimentales recientes45,46, sugiriéndose su utilidad para evitar angiografías negativas y como guía para la angiografía terapéutica en los casos positivos.
En el estudio de la hemorragia aguda, no es precisa una preparación específica, la administración de contraste oral positivo podría impedir visualizar el punto de sangrado e incluso la administración de contraste neutro podría dificultar la visualización del sangrado por dilución del contraste intravenoso extravasado en la luz intestinal5,33–35, aunque otros autores afirman que facilita su detección al distender las asas7,13,40. Es necesario realizar una TC basal, previa a la administración de contraste intravenoso para visualizar el posible contenido hiperdenso intraluminal o mural (pastillas, cuerpos extraños, restos fecales, clips, suturas quirúrgicas, restos de contraste en divertículos…) y evitar falsos positivos tras la administración del contraste5,19,20,33,35,37,39,41,42. En este estudio basal, la visualización de contenido hemático intraluminal (40-60 UH), que puede observarse hasta en el 50% de los casos (fig. 8)35, puede orientarnos sobre la localización del sangrado. A continuación debe realizarse una adquisición en fase arterial tardía (bolus tracking en la aorta más 15-25s de retraso según el equipo de TC utilizado) que nos permitirá visualizar el sistema vascular arterial y dará tiempo para que el contraste llegue a la lesión sangrante y se extravase a la luz intestinal, hallazgo que no sería detectado en una fase arterial pura. En general, los estudios publicados realizan una segunda fase, venosa, que permitiría ver sangrados más tardíos o a bajo débito, aumento del extravasado respecto al estudio arterial, mejor delimitación del patrón mucoso (fig. 1) y visualización de lesiones vasculares como angiodisplasias, así como realizar una estadificación si la causa es tumoral13,34,35,42,43; sin embargo su valor añadido respecto a la fase arterial tardía para ver el sangrado es discutida, por lo que hay estudios que solo realizan la fase arterial5,7,19,20,34. En la HD aguda es muy importante intentar realizar la exploración en el momento en que existe sospecha de hemorragia activa, ya que aumenta notablemente la sensibilidad en la detección de contraste extravasado, con un 100% en casos de sangrado masivo, frente a un 14% en pacientes con sangrado moderado35. Aún en el caso de no observar extravasación de contraste, la TC puede ser útil para orientar hacia el probable origen y causa del sangrado (diverticulosis, angiodisplasia, pseudoaneurismas, lesiones tumorales como GIST, pólipos, neoplasia de colon, enfermedad inflamatoria intestinal) y planificar el tratamiento más adecuado (figs. 1 y 6).
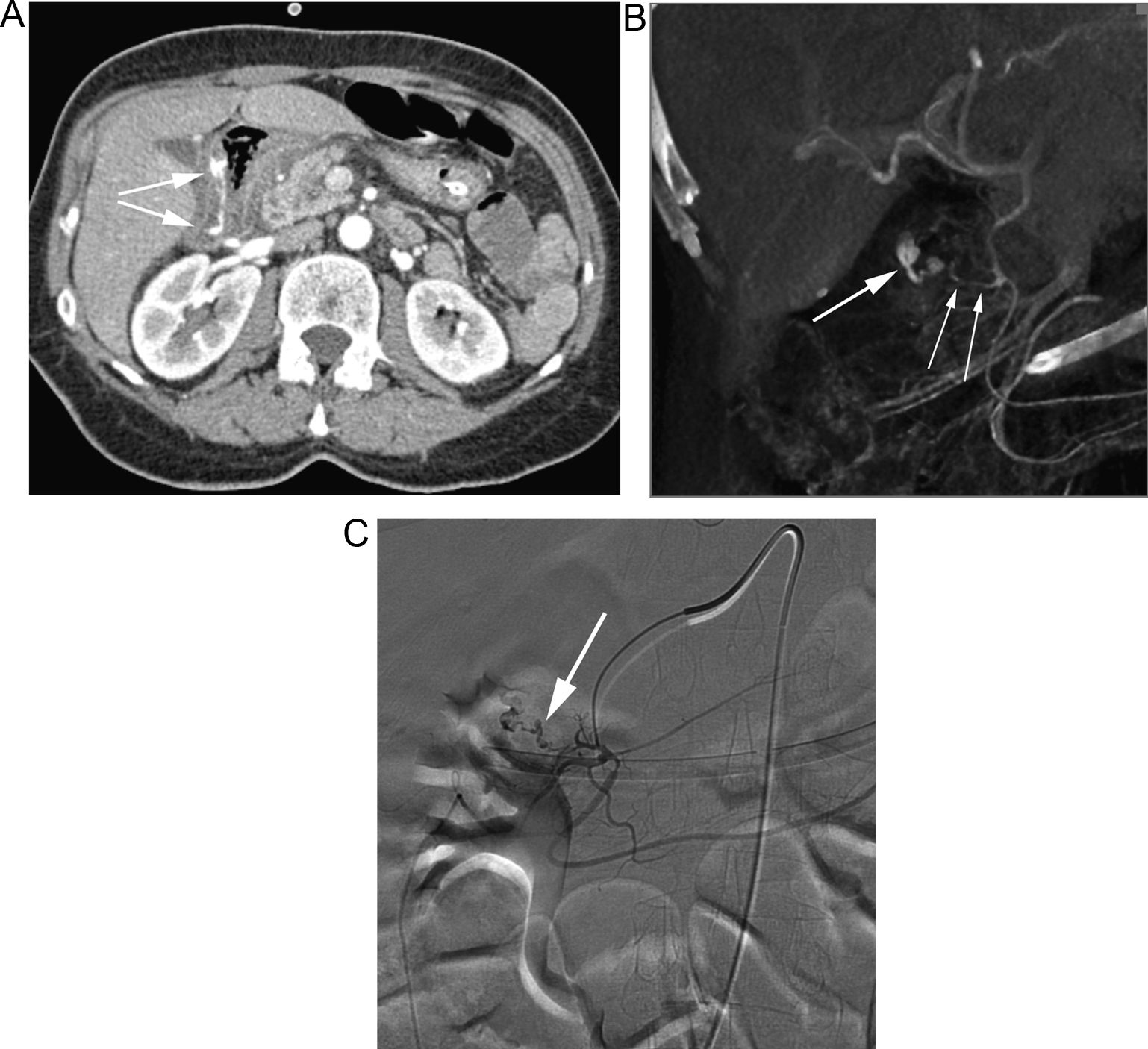
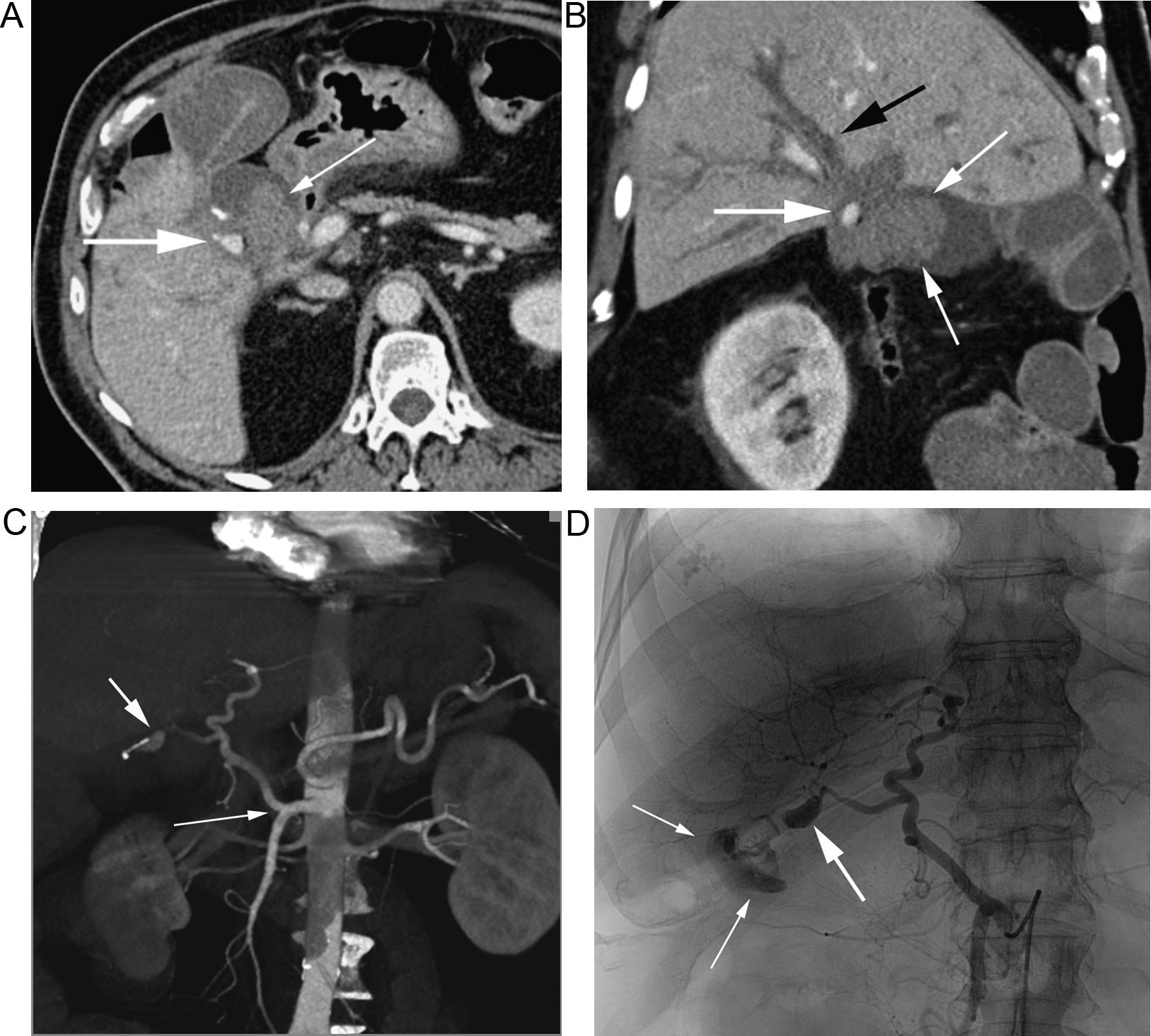
Sangrado digestivo en un paciente portador de una derivación bilioentérica. A) Corte axial de TC que muestra la presencia de coágulos en el asa yeyunal de la derivación (flecha fina) y una imagen de pseudoaneurisma en la anastomosis (flecha gruesa). B) Reconstrucción curva que permite ver la zona de la anastomosis, coágulos intraluminales (flechas finas blancas), el pseudoaneurisma (flecha gruesa blanca) y la dilatación de la vía biliar proximal (flecha negra). C) Reconstrucción «volume rendering» que muestra el origen de la arteria hepática en la mesentérica superior (flecha fina) y el pseudoaneurisma dependiente de la arteria hepática derecha (flecha gruesa). D) La arteriografía confirma estos hallazgos (pseudoaneurisma, flecha gruesa) y visualiza el sangrado activo al asa yeyunal durante la exploración (flechas finas). Se realizó la embolización del pseudoaneurisma con espirales, con preservación de la vascularización hepática y cese del sangrado.
En el estudio de la HD de origen indeterminado, especialmente si es oculta o visible de bajo débito, la exploración de elección es la TC-enterografía (TC-E) o TC-enteroclisis, siendo la primera más utilizada ya que no existen datos que demuestren mejores resultados para una de las dos técnicas7 y es mejor tolerada por el paciente, más fácil de realizar y no requiere una sala especial ni radiación adicional para la colocación de una sonda nasoyeyunal. Debe utilizarse contraste oral neutro (densidad semejante al agua) y no reabsorbible (PEG, manitol, sorbitol) para conseguir una adecuada distensión de las asas intestinales, y contraste intravenoso para delimitar el árbol vascular abdominal y la pared intestinal, con adquisiciones en fases arterial, entérica y retardada13 o bien una sola fase47, dependiendo de los autores. Aunque se ha demostrado la utilidad de la TC en la detección de las causas vasculares de sangrado (fig. 9), la mayoría corresponde a casos aislados o series cortas y con diferentes técnicas48–50, por lo que se asume una menor sensibilidad para estas lesiones frente a la CE. Los estudios realizados sugieren que la TC-E puede ser complementaria a la cápsula endoscópica13, que permite una visión directa de la mucosa intestinal, con una sensibilidad superior para visualizar lesiones planas.
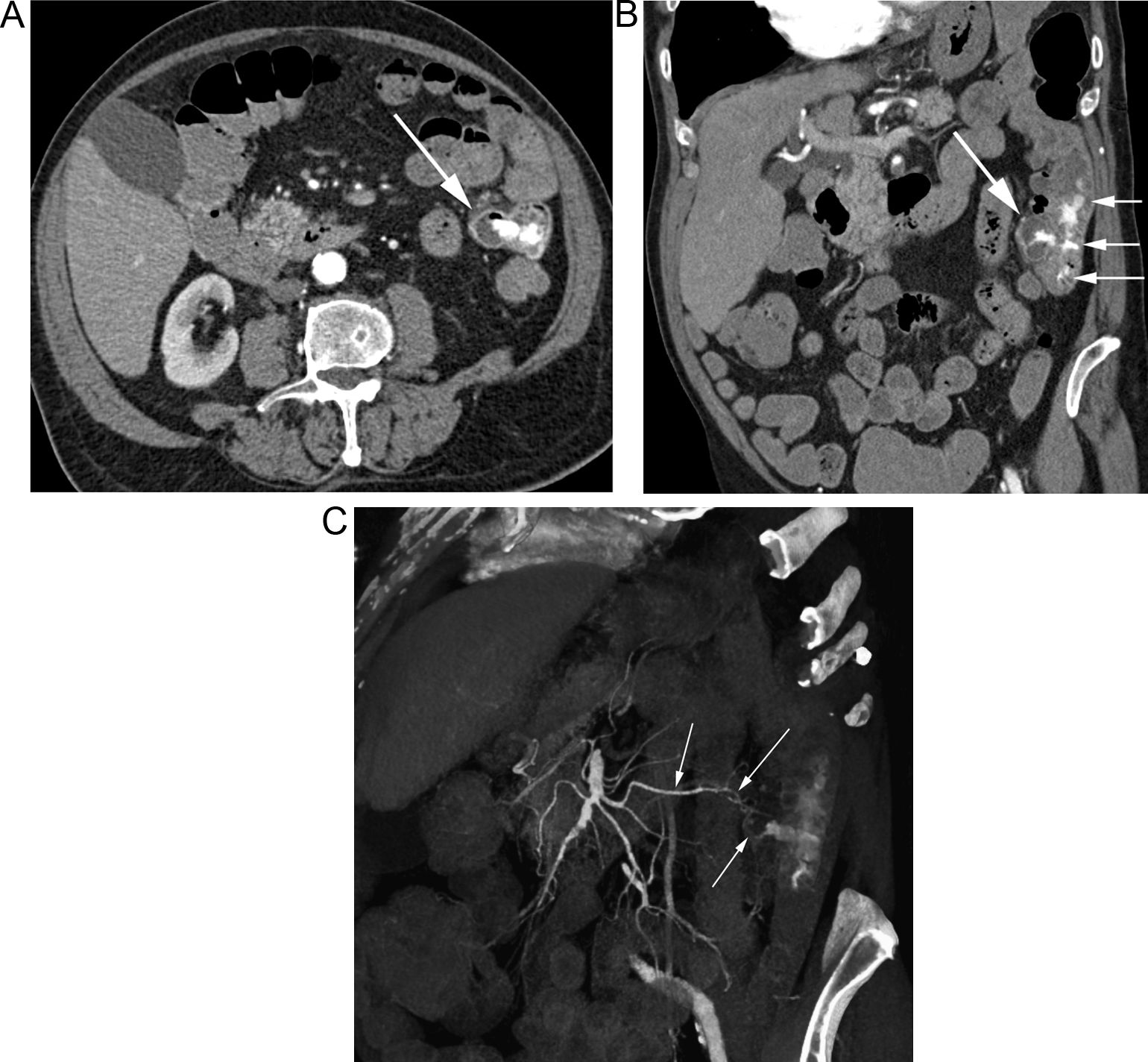
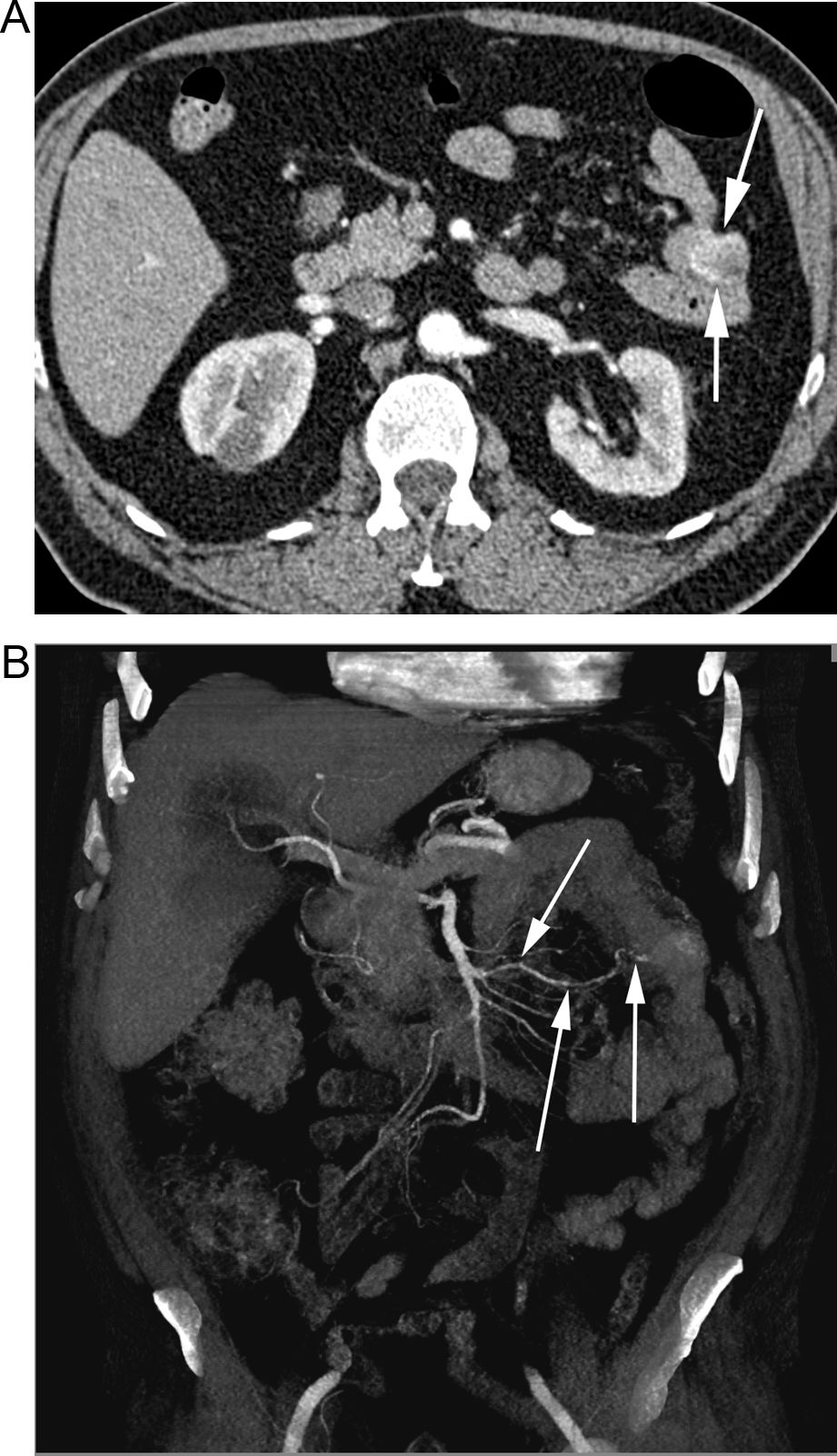
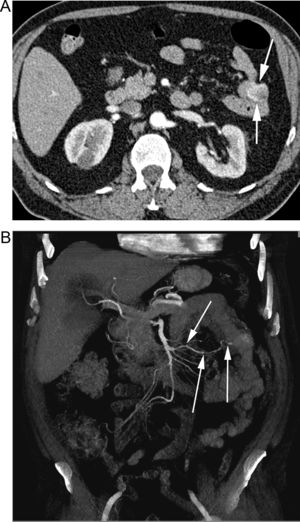
TC en paciente de 75 años con HD crónica de origen indeterminado. A) Reconstrucción MIP axial que muestra múltiples ectasias vasculares en el ciego (flechas) correspondientes a angiodisplasia. B) La reconstrucción MIP coronal muestra las dilataciones vasculares (flechas gruesas) y el retorno venoso precoz de la vena ileocecocólica (flecha fina).
La utilidad de la resonancia magnética (RM) para la detección de sangrado intestinal activo ha sido descrita de forma experimental51, con resultados incluso superiores a la gammagrafía52, y un artículo demuestra la utilidad de esta técnica en su uso clínico, aunque corresponde a un caso aislado53, lo que unido a su menor disponibilidad en comparación con la TCMD, hace que su papel en la hemorragia aguda sea actualmente anecdótico.
Existen pocos artículos sobre el uso de la RM-enterografía o RM-enteroclisis en el estudio de la hemorragia de origen indeterminado, la mayoría en forma de casos únicos53,54. La RM podría tener un papel en pacientes jóvenes en los que los tumores de intestino delgado son una causa frecuente de hemorragia de origen indeterminado y en cuyo diagnóstico la RM ha demostrado utilidad55.
AngiografíaLa angiografía ha sido durante muchos años la técnica diagnóstica complementaria a la endoscopia y la medicina nuclear en la HD aguda, permitiendo detectar extravasaciones de contraste intraluminal con sangrados a débitos de 0,5ml/min o superiores y, en ocasiones, determinar la causa del mismo. La angiografía tiene una sensibilidad entre el 63-90% en la HDA y del 58-86% en la HDB. El único signo directo de sangrado es la extravasación intraluminal de contraste, y son signos indirectos la visualización de un ovillo vascular y una vena de drenaje precoz (angiodisplasia), pseudoaneurismas, fístulas arteriovenosas, hiperplasia vascular (enfermedad), neovascularización (tumores) y relleno de contraste extraluminal (divertículos). Actualmente su papel diagnóstico ha sido sustituido por el de la TCMD19,42.
El gran avance en catéteres y microcatéteres y, fundamentalmente, los avances en los materiales de embolización (partículas, microcoils, materiales líquidos de polimerización rápida, etc.) han convertido la arteriografía en una herramienta terapéutica de primer orden en el manejo de estos pacientes, mediante la embolización supraselectiva, especialmente en la HDB aguda, y en casos de HDA no controlada mediante endoscopia o cirugía. Consigue controlar la hemorragia en el 70-90% de casos sin complicaciones isquémicas mayores y con bajas tasas de resangrado3,21,56, especialmente en la HDB19. Las complicaciones postembolización como la estenosis intestinal son raras y asintomáticas57,58.
Diagnóstico de la hemorragia digestivaHemorragia digestiva agudaEn la HD aguda, antes de proceder al diagnóstico deben establecerse medidas para estabilizar al paciente: maniobras de resucitación, estabilización de la presión sanguínea y reposición de la volemia.
En la HDA aguda la exploración inicial es la endoscopia, por su elevada eficacia diagnóstica y terapéutica. La angiografía por TCMD debe realizarse únicamente en aquellos casos en que la endoscopia no sea capaz de delimitar el punto de sangrado, fundamentalmente en casos de hemorragia masiva (fig. 5), para localizar el punto de sangrado42 y, eventualmente, su causa, lo que facilitará la elección del tratamiento más adecuado en cada caso, sirviendo de guía para la embolización cuando sea precisa. La arteriografía se considera el método terapéutico de elección para el control de la HDA tras dos endoscopias fallidas59, e incluso se plantea como tratamiento en pacientes con resangrado tras el tratamiento endoscópico, aunque no se visualice sangrado activo, guiándose por la ubicación de los clips metálicos colocados por endoscopia60.
En la HDB aguda, la colonoscopia es la exploración inicial3,61, pero en el 25-32% de las colonoscopias no se localiza el punto de sangrado, y la cifras de exactitud de la colonoscopia varían entre un 48 y 90% según las series1,22,62,63. Su uso, aceptado cuando el sangrado ha cesado y tras preparación del colon, es más cuestionado en la HD aguda masiva y sin preparación5,42,64, ya que la detección de lesiones es baja12,64. Tampoco existe un consenso en cuanto al momento de realizar la endoscopia, de forma urgente sin preparación o tras preparación del colon1,65. Ante una colonoscopia negativa, en la que se sospecha un sangrado de intestino delgado, o bien no concluyente debido a presencia de heces, coágulos o sangrado masivo, el estudio mediante angiografía por TC puede ser de utilidad para visualizar el punto de sangrado y su causa, siendo de especial utilidad en la hemorragia masiva, debido a la alta sensibilidad de la TC en esta situación (figs. 1–4, fig. 7)66.
La angiografía por TC permite obviar la realización de una angiografía si es negativa, con el consiguiente descenso de arteriografías negativas34,35,37,39, o bien localizar el punto de sangrado, orientar el tratamiento (endoscopia, angiografía o cirugía), y determinar su etiología, con el consiguiente valor pronóstico7. En caso de precisar una embolización posterior, la TC nos servirá como guía para la vía de acceso (estado de las arterias femorales e ilíacas), visualizar posibles variantes anatómicas vasculares, localizar el punto de sangrado y su origen vascular. Con ello facilitará una angiografía dirigida, disminuyendo la duración de la prueba, la cantidad de contraste utilizado y la dosis de radiación para el paciente y el radiólogo intervencionista (figs. 2, 3, 6 y 8)5,19,37,41. También permite orientar los procedimientos quirúrgicos, limitando la extensión de la resección quirúrgica si se localiza el punto de sangrado, evitando resecciones segmentarias «ciegas» o colectomías, asociadas a una elevada morbimortalidad39. Así mismo, puede evitar endoscopias innecesarias si el sangrado es de intestino delgado. Por ello, algunos autores defienden el uso de la TC como primer método diagnóstico en la HDB aguda para orientar el manejo del paciente19,38,46, en especial en casos de estabilidad hemodinámica, pudiendo realizar tratamiento conservador si el estudio por TC es negativo, con la posibilidad de repetir los exámenes en caso de resangrado. La TC también debe tenerse en cuenta como estudio inicial en casos de hemorragia digestiva postquirúrgica ya que son pacientes difíciles de estudiar y tratar mediante endoscopia, especialmente si se han realizado técnicas quirúrgicas como la duodenopancreatectomía cefálica o resecciones de intestino delgado, con el foco del sangrado posiblemente fuera del alcance de la endoscopia convencional (figs. 4, 6 y 8).
Si la colonoscopia y la TC son negativas y el paciente está estable, probablemente el sangrado haya cesado y únicamente se precise un tratamiento de soporte. Si pese a la negatividad de las pruebas, el paciente está hemodinámicamente inestable, deberá realizarse una arteriografía. Otros procedimientos diagnósticos como la cápsula endoscópica o la gammagrafía podrían ser usados si el paciente se mantiene hemodinámicamente estable y no se ha llegado a un diagnóstico.
La angiografía tiene un papel importante en el tratamiento de este tipo de HD, con un porcentaje de éxito en la HDB masiva del 81-93% y una mortalidad del 0-7%, por lo que varios autores defienden la embolización supraselectiva urgente como terapia de elección para los pacientes con HDB severa tras la localización del punto de sangrado mediante TCMD65,67.
La cirugía debe limitarse a aquellos casos de HD en que la localización del sangrado haya sido identificada y los métodos endoscópicos y angiográfícos no consigan controlar la hemorragia, realizando una resección segmentaria dirigida65,67.
Hemorragia crónica o recurrente de origen indeterminadoEn la mayoría de ocasiones en este tipo de HD, la causa se localiza en el esófago, el estómago o el colon, siendo los estudios iniciales negativos bien porque las lesiones hayan dejado de sangrar, por hipovolemia o anemia importante que hacen que pasen desapercibidas, por presentar un sangrado intermitente y lento o por presencia de coágulos o mala preparación del colon17. Por ello, tras un estudio endoscópico inicial negativo, debe repetirse la endoscopia alta ya que hasta en un 50% de casos se podrán localizar lesiones inadvertidas en la primera endoscopia (erosiones de Cameron, varices en el fundus gástrico, enfermedad ulcerosa péptica, angioectasias, lesión de Deulafoy o ectasia vascular antral gástrica). Algunos autores prefieren realizar una enteroscopia que permitirá, además, visualizar el intestino delgado proximal35 y tratar lesiones en esta localización. En el caso de la colonoscopia únicamente se verán lesiones en la segunda endoscopia en el 6% de casos, aunque pueden existir neoplasias o angiectasias inadvertidas en el primer estudio68.
Ante estudios endoscópicos repetidos y negativos, se asume que el sangrado se origina en el intestino delgado (5-27% de casos)3,69 y en este caso dispondremos de varias herramientas diagnósticas: CE, enteroscopia, gammagrafía con hematíes marcados, angiografía por TC, TC enterografía y angiografía.
Si la hemorragia es visible y se sospecha de un alto débito, deberemos proceder de la misma forma que en la hemorragia aguda. Si es visible de bajo débito u oculta, la CE es la exploración recomendada para su diagnóstico. La CE permite visualizar todo el intestino delgado, localizar la lesión y guiar el tratamiento3, con un rendimiento del 42-80% en la HD de origen indeterminado70.
La TCMD enterografía puede localizar el punto de sangrado, aunque con una sensibilidad mucho menor que en el sangrado agudo o, con mayor frecuencia, detectar alteraciones intestinales causantes potenciales del mismo, como tumores de intestino delgado que representan entre el 6-9% de las causas de HD crónica de origen indeterminado, siendo una causa frecuente en pacientes menores de 50 años (fig. 10)17,47. Su uso frente a otras técnicas como la CE o la gammagrafía dependerá de la disponibilidad y experiencia de cada centro, teniendo en cuenta que son métodos frecuentemente complementarios13,47,71,72. La CE permite un mejor diagnóstico de lesiones planas como angiodisplasia y ulceraciones, mientras que la TC-E presenta mejores resultados en la detección de tumores (fig. 10)47,71,72, siendo el rendimiento de ambas exploraciones similar47,73.
Algunos autores utilizan la TC-E como método inicial de diagnóstico en la HD no filiada oculta, previo a la CE4,7,71, ya que permite descartar la existencia de estenosis o diverticulosis que pudiesen ser causa de retención de la CE, otros sin embargo, sugieren iniciar el estudio con CE ya que las angiodisplasias son la causa más común de sangrado4.
En la HD visible de origen indeterminado, también puede iniciarse el estudio con gammagrafía con hematíes marcados si el paciente está estable, mientras que en caso de inestabilidad o gammagrafía negativa realizaremos un estudio mediante TC y angiografía si es preciso7.
ConclusiónLa HD frecuentemente supone un problema diagnóstico que precisa de exploraciones repetidas, sin llegar, en ocasiones, a un diagnóstico. Aunque el diagnóstico y el tratamiento se basan en estudios endoscópicos, los estudios por TC han demostrado su utilidad en esta afección. La sensibilidad de la TC-angiografía es cercana al 100% en la HD aguda masiva por lo que puede ser de utilidad como método inicial de estudio o tras un estudio endoscópico no diagnóstico y, aunque la sensibilidad de la TC disminuye notablemente en sangrados moderados, en un porcentaje elevado de casos permite ver signos indirectos que sugieren el origen y la causa del sangrado. En la HD de origen indeterminado la TC-enterografía es una herramienta complementaria a la CE y la gammagrafía, especialmente en pacientes jóvenes para descartar tumores intestinales como causa de sangrado. Aunque su lugar exacto en el algoritmo diagnóstico de la HD aún no está bien definido, probablemente por falta de estudios prospectivos comparativos con las técnicas endoscópicas, sin duda ocupa un lugar complementario con las técnicas endoscópicas, sustituyendo a la angiografía como método diagnóstico.
La angiografía tiene un papel terapéutico importante y complementario a la endoscopia en el manejo de estos pacientes, mediante el estudio dirigido y la embolización supraselectiva, guiada por los hallazgos de la endoscopia o la TC.
Autorías- 1.
Responsable de la integridad del estudio: S. Quiroga Gómez y M. Pérez Lafuente.
- 2.
Concepción del estudio: S. Quiroga Gómez y M. Pérez Lafuente.
- 3.
Diseño del estudio: S. Quiroga Gómez y M. Pérez Lafuente.
- 4.
Obtención de datos: S. Quiroga Gómez, M. Pérez Lafuente, M. Abu-Suboh Abadia y J. Castell Conesa.
- 5.
Análisis e interpretación de los datos: S. Quiroga Gómez, M. Pérez Lafuente, M. Abu-Suboh Abadia y J. Castell Conesa.
- 6.
Tratamiento estadístico: Artículo de revisión, sin tratamiento estadístico.
- 7.
Búsqueda bibliográfica: Sergi Quiroga Gómez, Mercedes Pérez Lafuente, M. Abu-Suboh Abadia y J. Castell Conesa.
- 8.
Redacción del trabajo: S. Quiroga Gómez, M. Pérez Lafuente, M. Abu-Suboh Abadia y J. Castell Conesa.
- 9.
Revisión crítica del manuscrito con aportaciones intelectualmente relevantes: S. Quiroga Gómez, M. Pérez Lafuente, M. Abu-Suboh Abadia y J. Castell Conesa.
- 10.
Aprobación de la versión final: S. Quiroga Gómez, M. Pérez Lafuente, M. Abu-Suboh Abadia y J. Castell Conesa.
Los autores declaran no tener ningún conflicto de intereses.