Sin medidas de prevención, entre el 1 y el 2% de los recién nacidos (RN) de madres colonizadas por estreptococo grupo B (EGB) desarrollan infección neonatal precoz, que cursa como septicemia, neumonía o meningitis. Aproximadamente el 25% de los casos ocurren en prematuros y en su gran mayoría en las primeras 24h de vida. Las consecuencias de la infección pueden extenderse más allá del periodo neonatal, con pérdidas de audición o visión y retraso mental.
Además del requisito de colonización materna, la prematuridad, la rotura prolongada de membranas, la fiebre intraparto (que puede reflejar corioamnionitis) y el haber tenido un RN previo afectado aumentan el riesgo de infección.
En el parto por cesárea el riesgo de infección por EGB es muy bajo si la cesárea se efectuó con la bolsa íntegra y antes del inicio del parto.
En los últimos 25años se ha demostrado que la administración intravenosa (i.v.) de profilaxis antibiótica intraparto (PAI) con penicilina o ampicilina a las madres colonizadas es muy efectiva para proteger al RN, siendo la cefazolina una alternativa útil en pacientes con hipersensibilidad moderada a los betalactámicos. La eficacia de otros antibióticos no ha sido probada, y la recomendación es administrar PAI durante 4 o más horas. Actualmente el uso de eritromicina no se recomienda.
El estado de portadora de EGB puede ser variable en el tiempo y los cultivos realizados con menos de 5 semanas antes del parto predicen adecuadamente el estado de portadora en el momento del parto. Sin embargo, los realizados con anterioridad a 5 semanas deben ser repetidos. Aunque se han desarrollado pruebas rápidas para detectar EGB basadas en la PCR, por ahora no se recomienda su uso rutinario.
La administración de penicilina al RN asintomático puede protegerlo frente a la infección cuando, existiendo indicación de PAI, esta no se realizó. Por ello se ha recomendado administrar al RN en estos casos una dosis de penicilina G intramuscular durante la primera hora de vida.
La aplicación sistemática de PAI incrementa el número de embarazadas que reciben antibióticos en el parto y puede aumentar el riesgo de infección por bacterias resistentes, pero este hecho no se ha podido confirmar. Pero dado que la sepsis por bacilos gramnegativos reviste especial gravedad, se debe evitar el uso innecesario o prolongado de antibióticos.
La administración de PAI a las madres colonizadas por EGB ha reducido la incidencia de la infección en España de 1,3 por 1.000 RN vivos en 1996-1997 a 0,36 en 2010. Hoy la mayoría de casos de infección en RN no prematuros se deben a resultados falsamente negativos en la detección de EGB, a falta de comunicación entre laboratorios y unidades obstétricas o a fallos en el cumplimiento del protocolo de prevención.
En 2010 los Centers for Disease Control (CDC) publicaron nuevas recomendaciones para la prevención de la infección neonatal precoz por EGB, y este hecho, junto con los nuevos conocimientos disponibles, ha llevado a las sociedades españolas de Obstetricia y Ginecología, Neonatología, Enfermedades Infecciosas y Microbiología Clínica, Quimioterapia y Medicina Familiar y Comunitaria a actualizar sus recomendaciones.
En España, en los RN de menos de 1.500g la incidencia de sepsis neonatal no ha disminuido. Por ello se hace especial referencia a la conducta ante la amenaza de parto y/o rotura de membranas antes de la 37 semana de gestación. También se ha evaluado la mejor estrategia para manejar los RN asintomáticos de madres portadoras de EGB, pues fácilmente puede llegarse a sobreactuaciones médicas frente a estos RN.
Las principales novedades introducidas en estas recomendaciones son:
- •
Detallada explicación y algoritmo sobre los métodos microbiológicos para identificar las embarazadas portadoras de EGB, incluyendo la realización de pruebas de sensibilidad antibiótica.
- •
Clarificación de los criterios sobre la presencia de EGB en orina de la embarazada.
- •
Actualización y algoritmos sobre el uso de PAI en la embarazada en diversas circunstancias.
- •
Manejo respecto a la PAI ante la amenaza de parto pretérmino y/o rotura prematura de membranas pretérmino.
- •
Recomendaciones y algoritmo para el manejo del RN en relación con el estado de portadora de la madre.
Las sociedades participantes recomiendan el cribado universal de las embarazadas para detectar el estado de portadora de EGB y la aplicación de PAI a todas las embarazadas portadoras.
Estas recomendaciones son, con modificaciones, similares a las realizadas por estas sociedades en 2003 y por los CDC en 2010. Asimismo, siempre que ha sido posible se ha incluido el nivel de evidencia utilizado por los CDC (tabla 1).
Nivel de evidencia utilizado por los CDC
| Sistema utilizado para determinar la fuerza de las recomendaciones | ||
| Categoría | Definición | Recomendación |
| Fuerza de la recomendación | ||
| A | Importante evidencia de eficacia y beneficio clínico | Muy recomendado |
| B | Importante o moderada evidencia de eficacia pero limitada evidencia de beneficio clínico | Generalmente recomendado |
| C | Evidencia de eficacia insuficiente o eficacia que no supera posibles efectos adversos | Opcional |
| D | Evidencia moderada de falta de eficacia o de efectos adversos | Generalmente no recomendado |
| E | Importante evidencia de falta de eficacia o de efectos adversos | No recomendado |
| Calidad de la evidencia que apoya la recomendación | ||
| I | Evidencia derivada de al menos un ensayo aleatorizado bien realizado y controlado o de un ensayo experimental de laboratorio rigurosamente diseñado y que ha sido reproducido por un investigador independiente | |
| II | Evidencia derivada de al menos un ensayo bien diseñado, no aleatorizado en cohortes o estudios analíticos caso-control (preferentemente realizado en más de un centro), múltiples estudios de series temporales, resultados que no admitan duda de estudios no controlados o evidencias de experimentos de laboratorio | |
| III | Evidencia obtenida de opiniones de expertos basadas en su experiencia clínica o de laboratorio, estudios descriptivos o informes de comités de expertos | |
Fuente: CDC 2010.
Dado que la profilaxis antibiótica no es eficaz en la prevención de la infección neonatal tardía por EGB, estas recomendaciones carecen de eficacia en su prevención.
Recomendaciones: detección de portadoras de estreptococo grupo BToma y transporte de muestrasLa detección de embarazadas portadoras de EGB debe efectuarse por cultivo, utilizando un único escobillón vaginorrectal, obteniendo primero el exudado vaginal y luego introduciéndolo en el esfínter anal. Si es necesario puede utilizarse un escobillón vaginal y otro rectal. Las muestras cervicales no son aceptables. La muestra ha de obtenerse antes de cualquier manipulación vaginal, no deben haberse utilizado productos de higiene femenina antes de la toma ni la embarazada debe estar recibiendo tratamiento antibiótico.
La muestra debe obtenerse con escobillón del tercio externo de la vagina (sin usar espéculo) y de la zona anorrectal (introduciendo el escobillón a través del ano). Los escobillones se introducen en un medio de transporte adecuado y se envían al laboratorio el mismo día. Si ello no es posible, pueden conservarse hasta 24h en frigorífico antes de su envío al laboratorio. La petición debe indicar claramente que la muestra es para cribado (screening) de EGB y si existe sospecha de alergia a betalactámicos.
Resumen de la obtención de muestra para detección de portadoras de EGBA quién. A todas las embarazadas.
Cuándo. En el periodo que va de la 35 a la 37 semana de gestación.
Dónde. Tercio externo de la vagina y el recto.
Con qué. Uno o dos escobillones que después de la toma se introducirán en medio de transporte.
Transporte. Enviar al laboratorio el mismo día de la obtención y, si no es posible, al día siguiente. Si la muestra no puede ser enviada al laboratorio el día de su obtención, debe conservarse en frigorífico hasta su envío.
Conservación de la muestra en el laboratorio hasta el procesamiento. 24h en frigorífico. Un tiempo de conservación mayor puede disminuir el inóculo de EGB presente en la muestra, hecho que, en pacientes con bajos inóculos, puede dar lugar a resultados falsos negativos del cultivo.
Petición. Indicar claramente «Cribado de EGB». Indicar posible alergia a penicilinas.
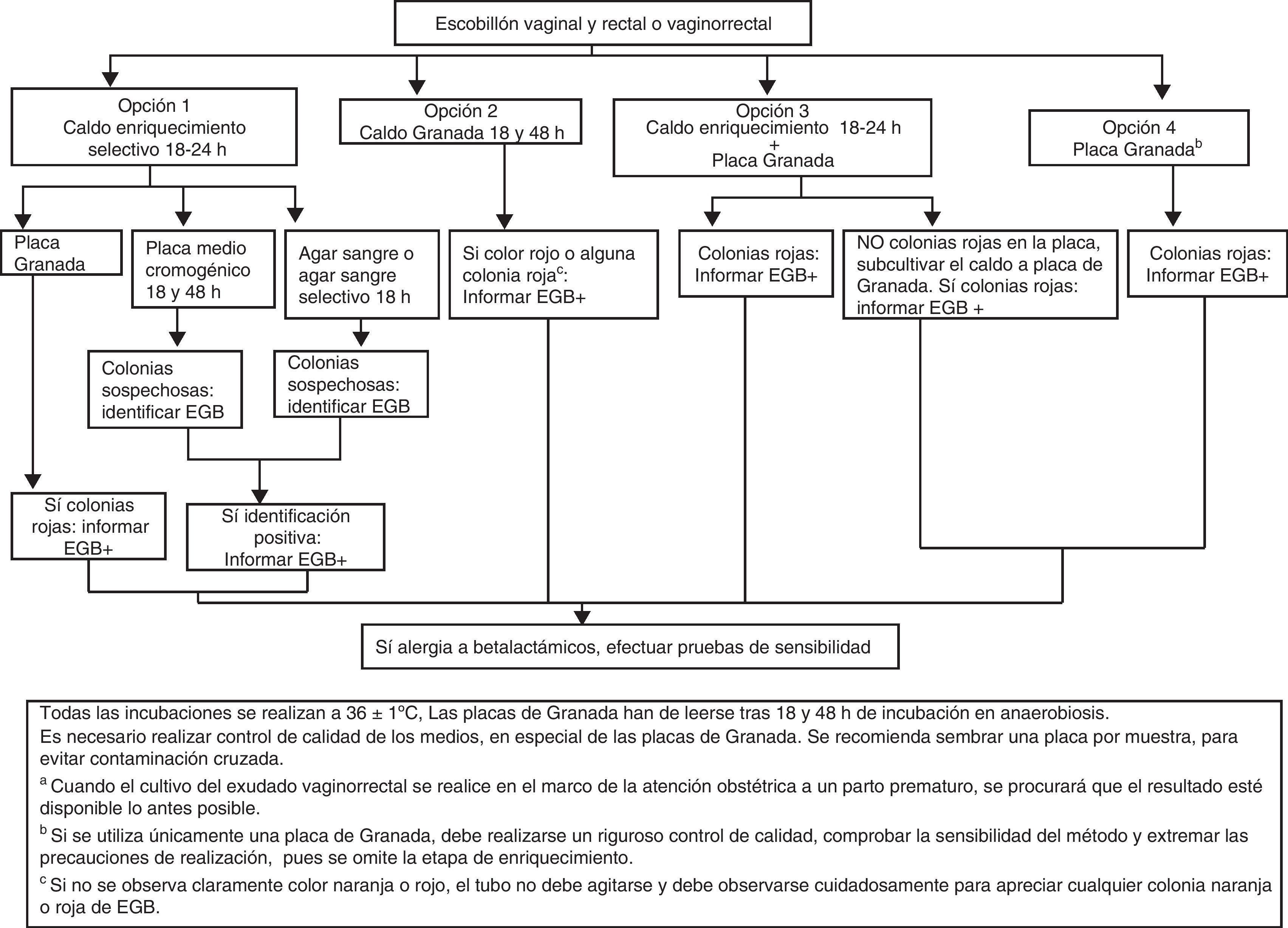
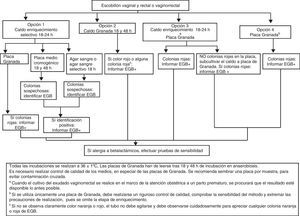
Procesamiento de las muestrasEscobillones vaginales, rectales o vaginorrectales: el procedimiento a emplear se resume en la figura 1.
Opción 1. Sembrar en medio líquido de enriquecimiento selectivo para EGB (Todd Hewitt con colistina y nalidíxico o con gentamicina y nalidíxico) y tras 18-24h de incubación subcultivar a una placa de medio Granada, a una placa de agar sangre, o a una placa de agar sangre selectivo (p.ej., con nalidíxico) o a una placa de medio cromogénico para EGB.
Opción 2. Sembrar en caldo Granada e incubar en aerobiosis 18h. Los tubos negativos se reincubarán como mínimo un día más antes de descartarlos.
Opción 3. Sembrar en medio líquido de enriquecimiento selectivo y en una placa de agar Granada. Si la placa de Granada es negativa a las 18h, subcultivar el tubo a una placa de medio adecuada como en la opción 1.
Opción 4. Sembrar en una placa de medio Granada e incubar en anaerobiosis durante 48h antes de considerarla negativa. Esta opción requiere un riguroso control de calidad para comprobar su sensibilidad.
Las colonias anaranjadas o rojas en medio Granada se identifican directamente como EGB. Las colonias betahemolíticas en agar sangre y las colonias que den la coloración indicada en medio cromogénico (diferente según el fabricante) se identifican mediante aglutinación con látex, por la prueba del hipurato, prueba de CAMP o MALDI-TOF.
No es necesario realizar antibiograma, salvo en pacientes alérgicas a la penicilina.
Los resultados de los cultivos han de estar disponibles en el momento del parto, por lo que es fundamental asegurar una adecuada comunicación entre el laboratorio y los centros asistenciales.
Cuando el cultivo del exudado vaginorrectal se realice en el marco de la atención obstétrica a una amenaza de parto prematuro y/o a una rotura prematura de membranas inferior a 37semanas, se procurará que el resultado esté disponible lo antes posible.
Comentario. Cada laboratorio debe controlar que su técnica de detección de EGB tiene la sensibilidad adecuada, lo cual puede inferirse de la frecuencia de portadoras de EGB detectada, que no debe ser inferior al 15%.
Es importante adquirir medios de cultivo de alta calidad y realizar controles de calidad. Esto es fundamental con las placas de medio Granada, pues se observan resultados no satisfactorios en algunos lotes de medio.
Como alternativa menos satisfactoria a la incubación en anaerobiosis, las placas de agar Granada pueden incubarse en aerobiosis y colocar un cubreobjetos sobre el inóculo para facilitar la producción de pigmento por las colonias de EGB.
Se debe ser cuidadoso respecto a la siembra de múltiples escobillones de diferentes pacientes en una única placa de medio, pues puede producirse contaminación cruzada.
La siembra de los medios cromogénicos ha de efectuarse de forma que se obtengan colonias bien aisladas, pues en cultivos polimicrobianos con escasa cantidad de EGB las colonias de EGB pueden ser difíciles de detectar.
Un escaso número de cepas de EGB son no hemolíticas y no pigmentadas y se consideran menos virulentas. Estas cepas crecen perfectamente en medio Granada, como colonias blancas no pigmentadas y en agar sangre como colonias no hemolíticas. Si se desea detectar estas cepas, debe recurrirse a otras técnicas microbiológicas.
Antibiograma. No es necesario, salvo en caso de alergia a betalactámicos, donde se ha de probar la sensibilidad a la clindamicina. En caso de cepas aparentemente resistentes a la eritromicina y sensibles a la clindamicina, se debe efectuar una prueba de resistencia inducible.
Recomendaciones: aspectos obstétricosIndicaciones del cribado vaginorrectal de EGBEn todas las gestantes entre la semana 35 y 37 (AII), preferentemente en la semana 36, incluso a las que se prevea cesárea programada (por si se ponen espontáneamente de parto antes de realizar la cesárea).
Dada la naturaleza intermitente de la colonización, los cultivos realizados 5 semanas o más antes del parto no predicen adecuadamente la colonización en el parto y se deben repetir si han transcurrido más de 5 semanas y el parto aún no se ha producido. Por ello debe indicarse a la embaraza que si el parto no se ha producido en 4 semanas desde la obtención de la muestra, debe acudir a la consulta para repetir el cultivo.
No es necesario efectuar la determinación de EGB si existe un hijo anterior con infección neonatal por EGB o si se ha detectado la presencia de EGB en orina durante la gestación (AIII). En estos casos debe administrase PAI.
Cuando se haya realizado más de un cultivo, la actuación para la prevención de la infección por EGB debe ser consecuente con el resultado del último cultivo.
Identificación de embarazadas candidatas a recibir PAIPAI indicada- 1.
Todas las mujeres identificadas por cultivo como portadoras vaginales o rectales de EGB en un cultivo al final del embarazo. El momento óptimo para la toma del cultivo es en la semana 35-37 de gestación (AII).
- 2.
Todas las mujeres en que se detecta EGB en orina durante la gestación, independientemente del resultado del cultivo vaginorrectal si este se ha realizado (AII). No es necesario realizar cultivo vaginorrectal en la semana 35-37.
- 3.
Todas las gestantes que previamente han tenido un hijo con infección neonatal por EGB, con independencia del resultado del cultivo vaginorrectal si este se ha realizado.
- 4.
Todos los partos con menos de 37 semanas de gestación en los que no se disponga del resultado del cultivo.
- 5.
Todos los partos en que exista rotura de membranas superior a 18h cuando no se disponga del resultado del cultivo.
- 6.
Todos los partos en que exista fiebre intraparto (38°C o más) cuando no se disponga del resultado del cultivo. En este caso debe considerarse la posible existencia de corioamnionitis u otra infección maternal.
- 7.
Mujeres a las que se les ha realizado una prueba molecular (PCR) intraparto de detección de colonización por EGB y el resultado es positivo (AII). Estas pruebas se realizan solo en algunos hospitales y habitualmente no están disponibles.
Comentario. Si al comienzo del parto una prueba rápida de PCR es negativa pero existe algún factor de los indicados en los puntos 4, 5 y 6, está indicada PAI.
PAI no indicada- 1.
Cultivo vaginorrectal negativo a EGB en la presente gestación (en un cultivo practicado durante las 5 semanas previas al parto) aunque hayan sido positivas en un embarazo anterior.
- 2.
Cesárea programada sin comienzo del parto y membranas íntegras, aunque el cultivo a EGB haya sido positivo (CIII).
- 3.
Partos en embarazo de más de 37 semanas de duración con estado de colonización por EGB desconocido y sin factores de riesgo. En estos casos (no realización de cultivo, pérdida de resultados, etc.) que son no deseables y deben ser excepcionales, no se utilizará PAI y el RN se someterá a observación.
El uso, en su caso, de profilaxis antibiótica para prevenir complicaciones infecciosas en cesáreas no debe ser alterado por la presencia o no de EGB.
La observación del RN no requiere necesariamente su ingreso separado de la madre. El alta hospitalaria del RN puede hacerse siempre que se cumplan todos los criterios de alta y no tiene que estar condicionada por la posible infección por EGB.
PAI y amenaza de parto pretérmino con o sin rotura prematura de membranas (menos 37 semanas)- •
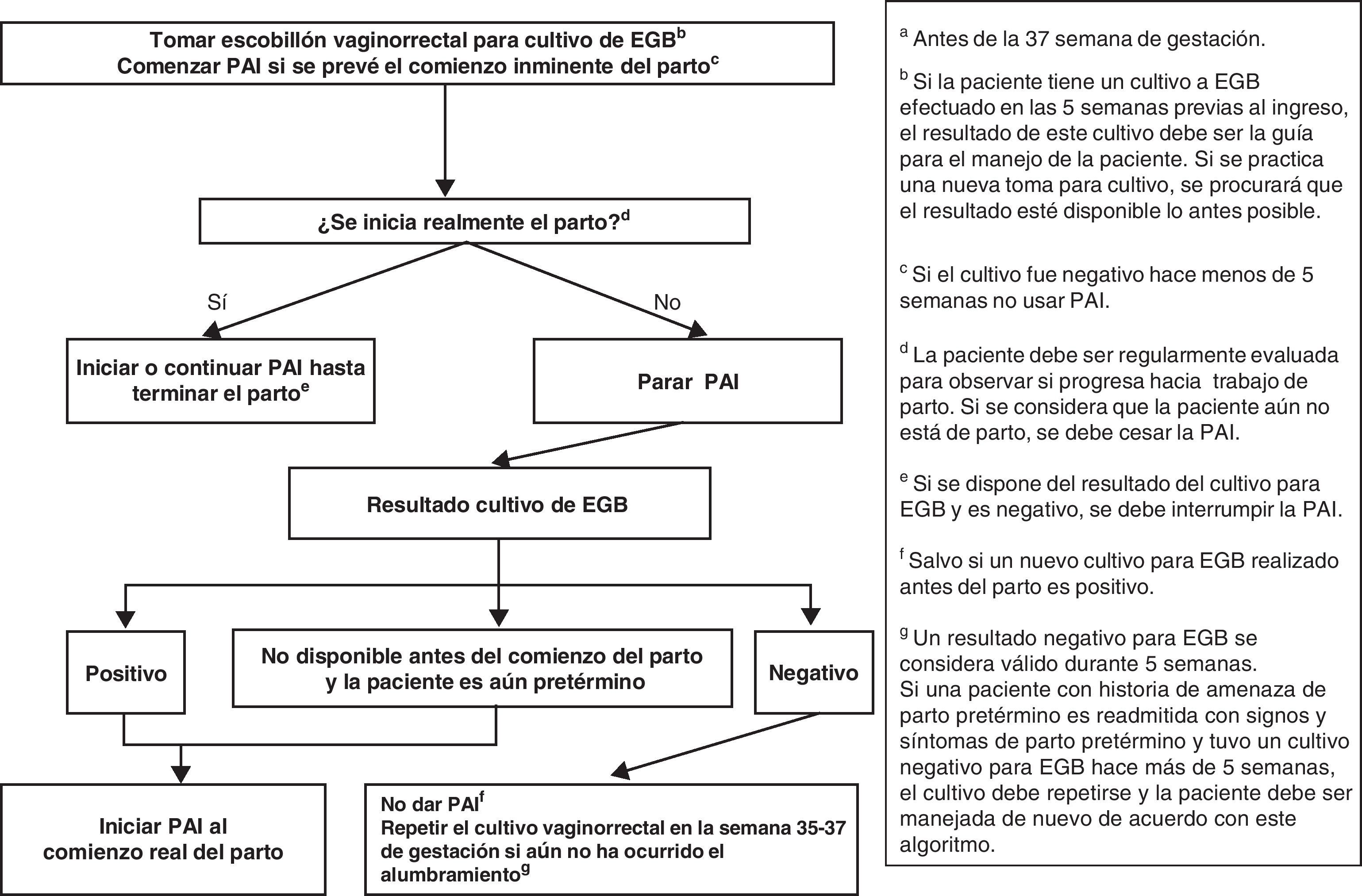
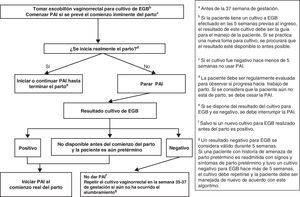
La mujer admitida con amenaza de parto pretérmino, SIN rotura prematura de membranas, debe ser manejada de acuerdo con la figura 2.
- •
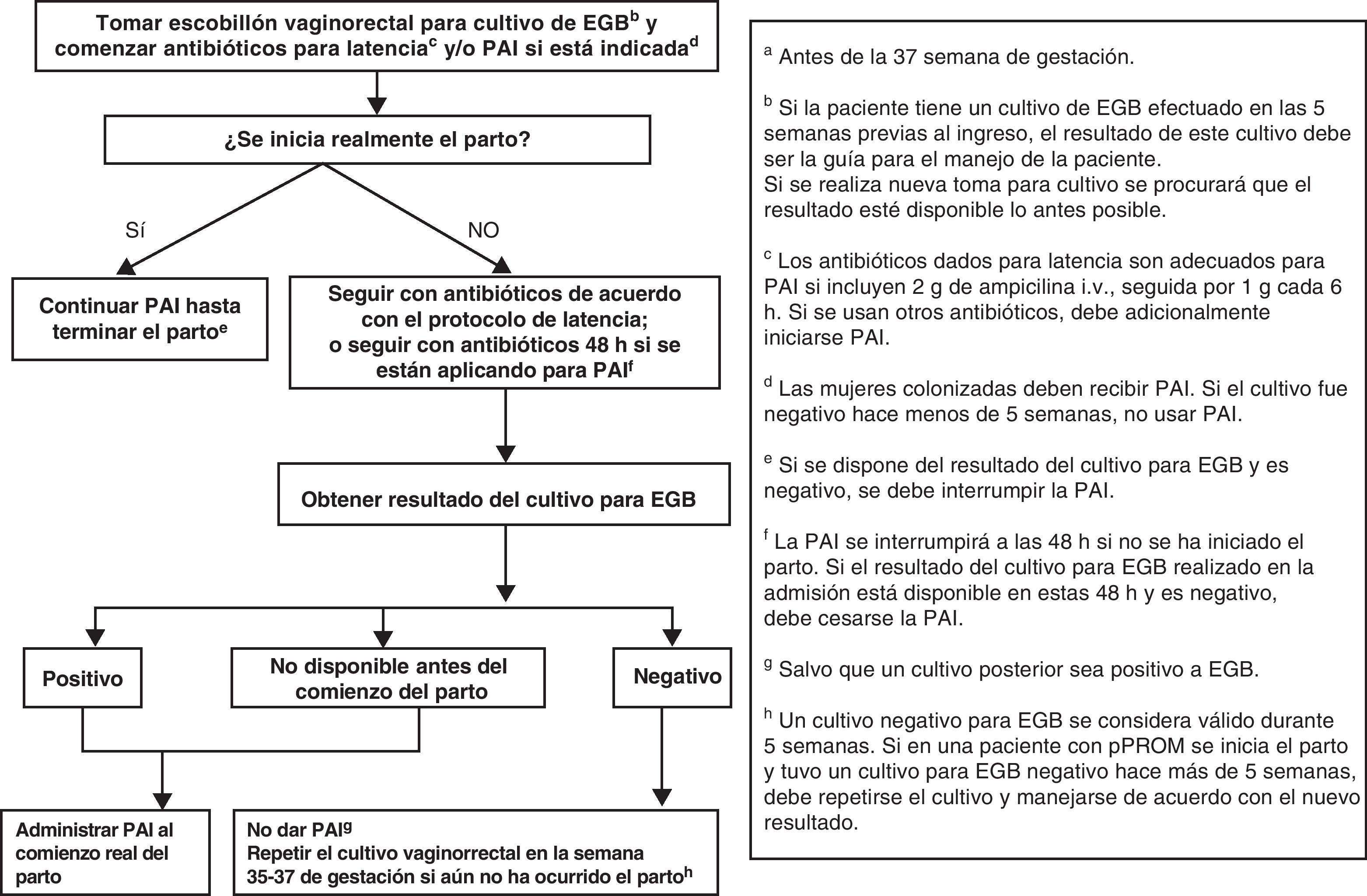
Las mujeres admitidas con amenaza de parto pretérmino CON rotura prematura de membranas (pPRM) deben ser manejadas de acuerdo con la figura 3.
- •
Al ingreso se le tomará un cultivo para EGB, si no se ha realizado en las últimas 5 semanas (AII). Es también recomendable que al ingreso se obtenga asimismo una muestra vaginal para investigación de otros microorganismos potencialmente patógenos (p.ej., E. coli).
- •
El cultivo para EGB se repetirá si no ha ocurrido el parto y han transcurrido más de 5 semanas desde el cultivo anterior.
- •
Si la mujer tiene un cultivo de EGB negativo en las 5 semanas anteriores, no se usará PAI.
En casos de amenaza de parto pretérmino:
- •
Si la gestante tiene un cultivo positivo en las últimas 5 semanas, o si el resultado del cultivo es desconocido, se iniciará la PAI cuando se prevea el comienzo inminente del parto.
- •
Si el parto no progresa, se interrumpirá la PAI (AI).
En casos de rotura prematura de membranas:
- •
La PAI se debe iniciar desde el momento del ingreso.
- •
Si el parto no progresa, se interrumpirá la PAI tras 48h de tratamiento (AI).
- •
Si el resultado del cultivo de EGB realizado en admisión es negativo, debe interrumpirse la PAI (AII).
- •
En la mujer con cultivo EGB positivo en que se interrumpió la PAI porque el parto no progresaba, esta se reanudará cuando comience de nuevo el parto (AII).
Comentarios
- •
La mujer con pPRM que no está de parto y SÍ está recibiendo antibióticos para prolongar la latencia y que incluyen cobertura adecuada de EGB debe ser manejada según la condición de su pPRM, sin tener en cuenta los cultivos de EGB (BIII).
- •
La mujer con pPRM que no está de parto y NO está recibiendo antibióticos para prolongar la latencia, o estos antibióticos NO incluyen cobertura adecuada de EGB, debe recibir PAI durante 48h, salvo que tenga un cultivo de EGB negativo en las 5 semanas anteriores. En estas 48h deberán recibirse los resultados del cultivo para detección de EGB y del cultivo vaginal.
- •
Si se indican antibióticos para prolongar la latencia, estos se consideran también adecuados para la PAI de EGB (mientras la paciente está recibiendo este tratamiento) (CIII) si incluyen 2g de ampicilina i.v. seguida de 1g cada 6h. Si se usan otros antibióticos para prolongar la latencia y se requiere utilizar PAI, deben añadirse además antibióticos adecuados para la PAI (BIII).
- •
Un resultado negativo del cultivo de EGB no debe influir en la administración de antibióticos indicados por cualquier otro motivo (AIII) (p.ej., sospecha de corioamnionitis).
- •
La administración oral de antibióticos no es adecuada para PAI (DII).
En caso de existir algún signo clínico o biológico que haga sospechar corioamnionitis (infección intraamniótica) u otro tipo de infección bacteriana materna, la administración de antibióticos a la madre adquiere carácter terapéutico y se deben utilizar los recursos diagnósticos apropiados (p.ej., hemocultivo, cultivo de líquido amniótico) y un tratamiento antibiótico que, además de EGB, cubra otros probables patógenos, principalmente bacilos gramnegativos como E. coli (p.ej., gentamicina, cefalosporinas de amplio espectro, amoxicilina-clavulánico).
Los signos clínicos de corioamnionitis pueden estar ausentes en el momento de la evaluación inicial, sobre todo en amenaza de parto prematuro con membranas intactas.
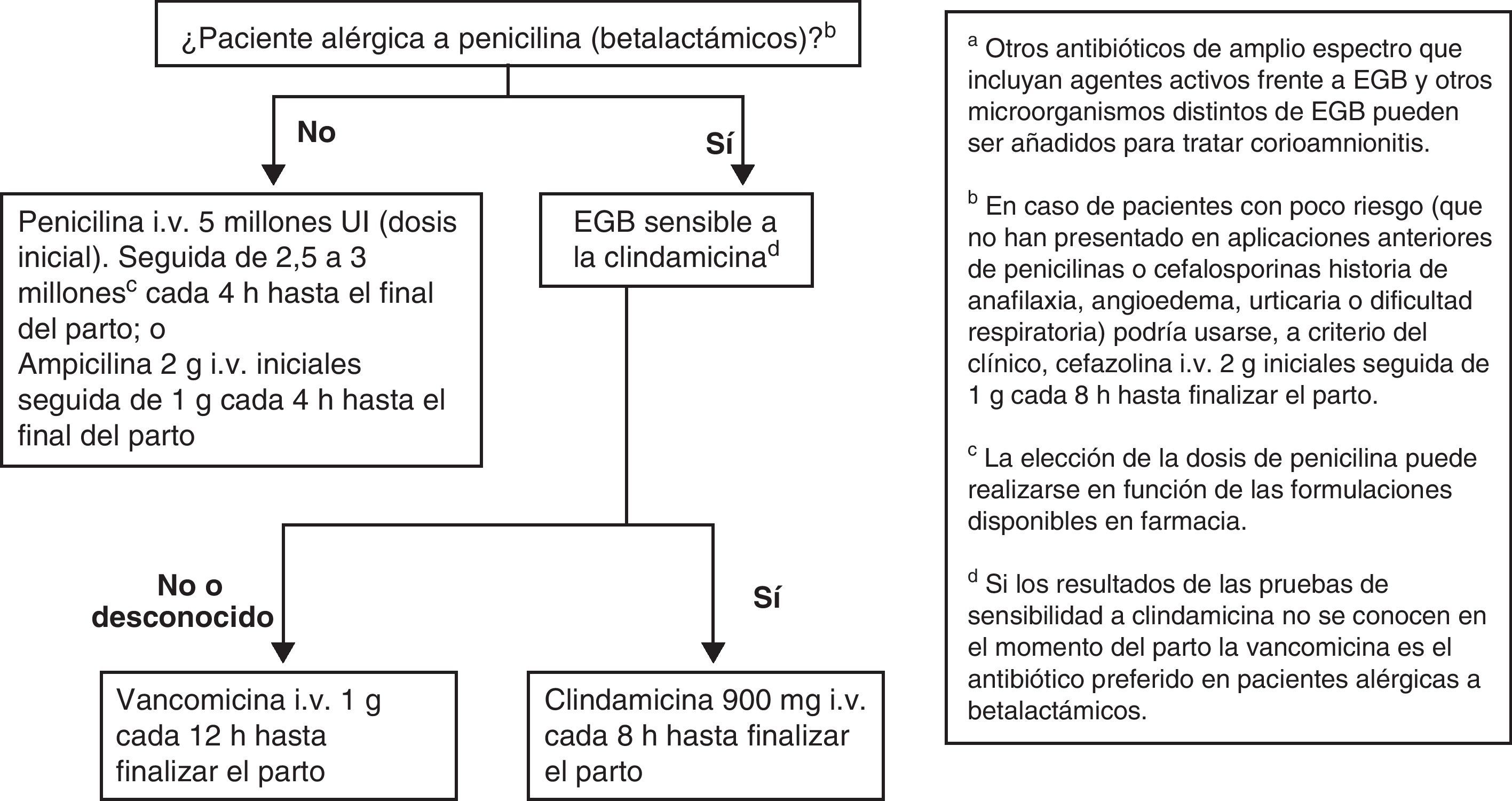
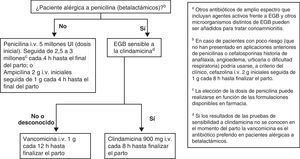
Recomendaciones antibióticas para PAI de la infección neonatal precoz por EGBLas recomendaciones se muestran en la figura 4.
La PAI para EGB debe administrase de acuerdo con la siguiente pauta:
– Penicilina i.v., 5 millones de UI (dosis inicial), seguida de 2,5 a 3 millones de UI i.v. cada 4h hasta el final del parto.
o
– Ampicilina i.v., 2g iniciales seguidos de 1g cada 4h hasta el final del parto.
- •
La penicilina sigue siendo el agente de elección por su menor espectro antimicrobiano, aunque la ampicilina es aceptable (AI).
- •
En la petición de cultivo para cribado de EGB se debe informar si hay sospecha de alergia a la penicilina o a las cefalosporinas (AIII).
En pacientes alérgicas, si a juicio del clínico no hay riesgo de anafilaxis, la alternativa a la penicilina o a la ampicilina puede ser la cefazolina (BII), 2g i.v. como dosis inicial, seguida de 1g i.v. cada 8h hasta el final del parto.
Los puntos fundamentales son los siguientes:
- •
En pacientes alérgicas a la penicilina debe realizarse el estudio de sensibilidad del EGB a la eritromicina y a la clindamicina (incluyendo, si la cepa es resistente a la eritromicina y sensible a la clindamicina, una prueba de resistencia inducible) (AII). Si esta prueba no se ha realizado o no se conoce el resultado, el EGB debe ser considerado resistente a la clindamicina y el antibiótico a usar es la vancomicina (CIII).
- •
Si la paciente es alérgica a la penicilina y el EGB es sensible a la clindamicina, este es el antibiótico que debe usarse (CIII).
- •
La eritromicina no es alternativa aceptable para usar en la PAI para prevención de infección neonatal precoz por EGB.
- •
Si existen signos clínicos y/o biológicos de posible infección materna y/o fetal, la administración de antibióticos adquiere carácter terapéutico y debe cubrir un espectro de etiologías más amplio (p.ej., ampicilina-gentamicina u otros antibióticos, de acuerdo con la política antibiótica del centro).
- •
Desde el punto de vista del manejo del RN, solo se considera profilaxis adecuada la realizada con penicilina, ampicilina o cefazolina con la pauta indicada.
Los datos disponibles no son suficientes para sugerir que el estado de portadora de EGB deba influir sobre los procedimientos obstétricos de monitorización, maduración cervical o inducción del parto. Estos procedimientos se reservarán para sus indicaciones y no se modificarán en las mujeres colonizadas por EGB (CIII).
Los datos disponibles no son suficientes para hacer recomendaciones respecto al momento de aplicación de los procedimientos destinados a facilitar la progresión del parto, tales como la amniotomía en las mujeres colonizadas por EGB.
Dado que la PAI se considera óptima si comienza al menos 4h antes del final del parto, la aplicación de estos procedimientos debe adaptarse en lo posible a este tiempo (CIII).
Presencia de EGB en la orina de la gestanteSi en el cribado de la bacteriuria asintomática de la gestante se detecta la presencia de EGB en orina en cualquier número de unidades formadoras de colonias (ufc)/ml, debe informarse, pero no se deben usar antibióticos para intentar erradicar el estado de portadora vaginorrectal de EGB en la gestante.
Sin embargo, cuando en el cribado de infección urinaria durante el embarazo se detecte bacteriuria asintomática por EGB (recuentos iguales o superiores a 100.000 ufc/ml en una muestra) o en el transcurso del embarazo se detecta una infección urinaria por EGB (igual o más de 10.000 ufc/ml con piuria y/o clínica compatible de infección del tracto urinario), debe instaurarse tratamiento y realizar seguimiento con urocultivos mensuales.
Todas las gestantes con presencia de EGB en orina durante el embarazo requieren la administración de PAI sin que sea necesario realizar cultivo vaginorrectal en la semana 35-37.
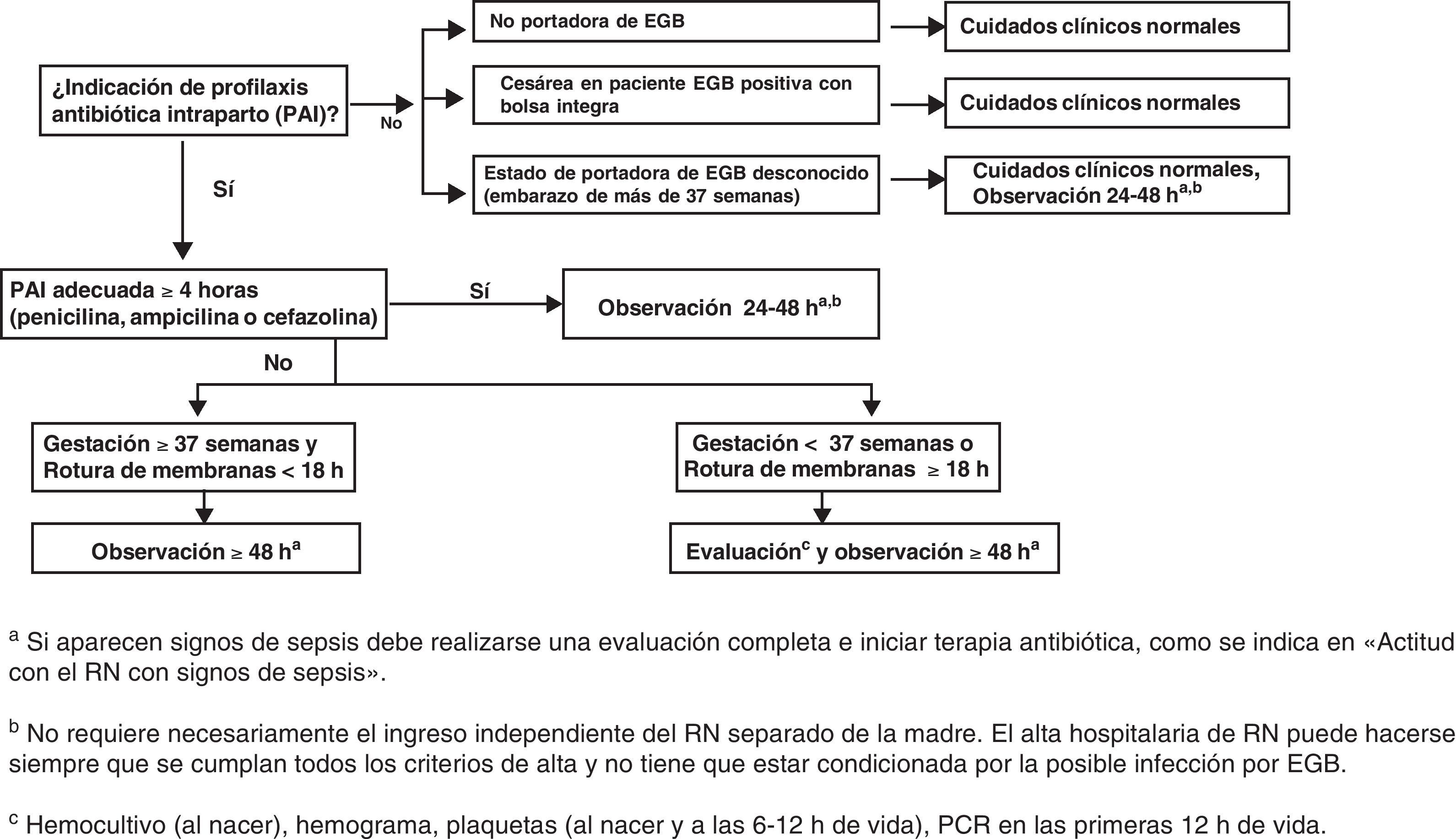
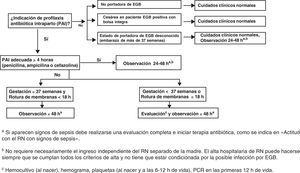
Recomendaciones: actitud con el recién nacidoActitud con el RN asintomático sin sospecha de corioamnionitis maternaLos puntos fundamentales del manejo de estos RN se muestran en la figura 5.
Las estrategias actuales de prevención de la infección neonatal precoz por EGB no son capaces de prevenir todos los casos. Por ello, la detección rápida de la infección es fundamental para minimizar la morbilidad y la mortalidad en los casos de infección neonatal precoz por EGB que aún se producen.
Punto fundamental. Solo se considera profilaxis completa la realizada con penicilina, ampicilina o cefazolina a las dosis indicadas.
Esto significa un mínimo de 2 dosis de penicilina o ampicilina en todos los partos y un mínimo de 2 dosis de cefazolina si el parto se prolonga más de 8h.
Los demás antibióticos y dosificaciones se consideran PAI incompleta respecto al manejo del RN (AII).
Madre sin indicación de PAI no portadora de EGBManejar de acuerdo con los cuidados neonatales habituales (CIII).
Madre sin indicación de PAI. Gestación de más de 37 semanas sin ningún factor de riesgo y EGB desconocidoNo se requieren pruebas diagnósticas adicionales (BIII).
En el caso (no deseable y que debe ser excepcional) de que se desconozca si la madre es portadora de EGB (no realización de cultivo, pérdida de resultados, etc.), el RN se someterá a observación que se prolongará 48h. La observación del RN no requiere necesariamente su ingreso separado de la madre. El alta hospitalaria del RN puede hacerse siempre que se cumplan todos los criterios de alta y no tiene que estar condicionada por la posible infección por EGB.
Madre portadora de EGB, PAI correctaNo se requieren pruebas diagnósticas adicionales (BIII).
El RN se someterá a observación. Esta observación no requiere necesariamente el ingreso del RN separado e la madre. El alta hospitalaria del RN puede hacerse siempre que se cumplan todos los criterios de alta y no tiene que estar condicionada por la posible infección por EGB.
Esta recomendación está basada en:
- •
La efectividad demostrada de la PAI para prevenir la infección neonatal por EGB y disminuir la transmisión vertical.
- •
Que la administración intraparto de antibióticos no parece alterar el curso clínico ni retrasar la aparición de síntomas en el RN infectado intraútero.
- •
Que la gran mayoría de las manifestaciones clínicas de las infecciones neonatales precoces por EGB se inician durante las primeras 24h de vida posnatal.
El RN será sometido a observación clínica durante 48h. No son necesarias pruebas diagnósticas adicionales (BIII).
Pero si aparece sospecha clínica de sepsis, se recogen cultivos, se inicia tratamiento antibiótico y se realiza chequeo de sepsis, recuento y fórmula leucocitarios, plaquetas y proteína C reactiva en las primeras 12 y 24h de vida.
Se recomienda, en el caso de que el RN no haya recibido ningún tipo de PAI, administrar al RN (independientemente del estado clínico o del resultado de las pruebas realizadas) una sola dosis de penicilina G intramuscular durante la primera hora de vida (50.000UI si el peso al nacer es mayor de 2.000g o 25.000UI si el peso es menor).
Madre que debió recibir PAI pero no la recibió o no fue adecuada, con gestación de menos de 37 semanas o con rotura de membranas de 18 o más horasEl RN se someterá a observación durante al menos 48h (BIII) y se le practicará hemocultivo, recuento y fórmula leucocitarios, plaquetas y proteína C reactiva en las primeras 12 y 24h de vida.
Estos RN serán manejados de acuerdo con sus características de inmadurez y edad gestacional.
Se recomienda, en el caso de que el RN no haya recibido ningún tipo de PAI, administrar al RN (independientemente del estado clínico o del resultado de las pruebas realizadas) una sola dosis de penicilina G intramuscular durante la primera hora de vida (50.000U si el peso al nacer es mayor de 2.000g o 25.000U si el peso es menor).
Actitud con el RN asintomático con sospecha de corioamnionitis maternaSi durante el parto se han presentado signos o síntomas maternos o fetales que sugieran corioamnionitis, independientemente del tratamiento que se haya administrado intraparto (tratamiento que además de frente al EGB debe ser activo frente a otros posibles patógenos), de la edad gestacional y del estado del niño al nacer, se iniciará evaluación diagnóstica incluyendo hemocultivo, recuento y fórmula leucocitaria, plaquetas al nacer y proteína C reactiva a las 12 y 24h de vida.
Inmediatamente después se instaurará tratamiento antibiótico empírico activo frente a EGB y otros microorganismos capaces de causar infección neonatal.
El tratamiento se prolongará hasta tener los resultados analíticos y los cultivos.
Es necesario mantener consulta con el obstetra para evaluar la sospecha de corioamnionitis materna.
Actitud con el RN con signos de sepsisCualquier RN con signos o síntomas de sepsis (independientemente de si la madre es o no portadora de EGB), con PAI o sin ella, será sometido a evaluación diagnóstica completa: hemocultivo, recuento y fórmula leucocitaria, plaquetas, proteína C reactiva y estudio de líquido cefalorraquídeo (después de estabilizar al RN) y radiografía de tórax si hay anormalidades respiratorias.
Se iniciará tratamiento inmediato con antibióticos activos frente a EGB y otros microorganismos (p.ej., E. coli) capaces de causar infección neonatal (AII).
Consideraciones sobre el manejo posterior del RN- •
En caso de RN en que la madre hubiese recibido alguna dosis de antibióticos intraparto y posteriormente presenten clínica o marcadores de infección positivos, se recomienda repetir el hemocultivo y, si se dispone de la técnica, efectuar una prueba de amplificación de ácidos nucleicos (PCR) para detección de otros microorganismos.
- •
Si a las 48h de vida el hemocultivo es negativo, la situación clínica es normal y los marcadores de infección (hemograma, PCR) son negativos, se recomienda suspender la administración de antibióticos (si se habían iniciado) y el caso se considera falsa sospecha de sepsis neonatal.
- •
Si a las 48h el hemocultivo es negativo, pero existe clínica de infección y/o los marcadores de infección fueron o son positivos, se realiza el diagnóstico de sepsis clínica del RN y se continúa o se inicia la administración de antibióticos.
- •
Si a las 48h el hemocultivo es positivo y los marcadores de infección fueron o son positivos, se inicia o continúa la administración de antibióticos y se realiza el diagnóstico de sepsis del RN.
- •
Si a las 48h el hemocultivo es positivo pero no hubo ni hay clínica de sepsis y los marcadores de infección fueron negativos, se establece el diagnóstico de bacteriemia neonatal asintomática y se inicia o continúa tratamiento antibiótico, para disminuir el riesgo de desarrollo de sepsis y/o meningitis vertical.
Estas recomendaciones no avalan una pauta única de comportamiento. Otras pautas alternativas para la prevención de la infección perinatal por EGB pueden ser también adecuadas de acuerdo con las circunstancias particulares de cada centro asistencial y del juicio clínico de los médicos implicados en la atención de cada caso.
Dr. Juan Ignacio Alós Cortés. SEIMC. Servicio de Microbiología. Hospital de Getafe. Madrid.
Dra. Antonia Andreu Domingo. SEIMC. Servicio de Microbiología. Hospital Vall d’Hebron. Barcelona.
Dr. Lorenzo Arribas Mir. SEMFYC. Centro Salud La Chana. Granada.
Dr. Luis Cabero Roura. SEGO. Servicio de Obstetricia y Ginecología. Hospital Vall d’Hebron. Barcelona.
Dra. Marina Cueto López. SEIMC. Servicio de Microbiología. Hospital Virgen de la Macarena. Sevilla.
Dr. José López Sastre. SEN. Servicio de Neonatología. Hospital Central de Asturias. Oviedo.
Dr. Juan Carlos Melchor Marcos. SEGO. Servicio de Obstetricia y Ginecología. Hospital de Cruces. Vizcaya.
Dr. Alberto Puertas Prieto. SEGO. Servicio de Obstetricia y Ginecología. Hospital Virgen de las Nieves. Granada.
Dr. Manuel de la Rosa Fraile. SEQ. Secretario de Redacción. Hospital Virgen de las Nieves. Granada.
Dr. Salvador Salcedo Abizanda. SEN. Servicio de Neonatología. Hospital Vall d’Hebron. Barcelona.
Dr. Manuel Sánchez Luna. SEN. Hospital Gregorio Marañón. Madrid.
Dra. María José Sánchez Pérez. Escuela Andaluza de Salud Pública. CIBER de Epidemiologia y Salud Pública. Granada.
Dr. Rafael Torrejón Cardoso. SEGO. Servicio de Obstetricia y Ginecología. Hospital Virgen del Rocío. Sevilla.