Los patógenos gramnegativos se han señalado en la literatura como los principales causantes de infecciones asociadas a la atención a la salud.
Material y métodosAnalizamos los resultados en cuanto a resistencia antimicrobiana de los principales patógenos gramnegativos obtenidos por diversos métodos de cultivo recabados mediante un sistema de vigilancia epidemiológica de control de las infecciones asociadas a la atención a la salud durante todo el 2006 para compararlos con los obtenidos en el 2012.
ResultadosIdentificamos 10 patógenos gramnegativos que sumaron un total de 387 aislamientos, con una prevalencia mayor en el 2012 (0.37) vs. 2006 (0.36). Destacaron 4 patógenos, en orden de importancia: Klebsiella pneumoniae (113-29.1%), Escherichia coli (88-22.7%), Enterobacter cloacae (65-16.7%) y Pseudomonas aeruginosa (63-16.2%). Hubo otros con menos aislamientos, pero que en conjunto estaban dentro del grupo de patógenos «ESKAPE-E» (Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa y Enterobacter sp.). Estos son causantes de infecciones asociadas a la atención de la salud desde el 2006, pero en menor proporción de eventos y con mejor susceptibilidad antimicrobiana. A diferencia del 2012 donde las resistencias a la mayoría de los antibióticos aumentó en poco más del 20%. Hubo alerta de multirresistencia sobre todo para Klebsiella pneumoniae, Escherichia coli y Klebsiella oxytoca. Pocos antibióticos (imipenem, meropenem, gentamicina y amikacina) mantuvieron su perfil de actividad en ambos periodos, y otros como ertapenem y quinolonas que no se usaban en el 2006, se mostraron con buena susceptibilidad antimicrobiana en el 2012.
ConclusionesLos patógenos «ESKAPE-E» son un problema real de salud pública y la multirresistencia antibiótica les permite evadir muchas de las opciones terapéuticas disponibles. Aunado al hecho de que no hay nuevos antimicrobianos, el realizar estudios y creas mapas de resistencias bacterianas en nuestras instituciones nos puede ayudar a tomar mejores decisiones al iniciar una terapéutica empírica.
Gram-negative pathogens have been shown in the literature to be the main cause of healthcare-associated infections.
Material and methodsAn analyse is performed on the results of the antimicrobial resistance of the main gram-negative pathogens obtained by different cultivation methods collected by means of an healthcare-associated infections epidemiological surveillance control system during the year 2006, in order to compare them with those obtained in the year 2012.
ResultsA total of 10 organisms Gram-negative organisms were identified from a total of 387 isolations, with a higher prevalence in 2012 (0.37) vs 2006 (0.36). The 4 most important pathogens were: Klebsiella pneumoniae (113, 29.1%), Escherichia coli (88, 22.7%), Enterobacter cloacae (65, 16.7%), and Pseudomonas aeruginosa (63, 16.2%). There were others with less frequent isolations, but were on the whole within the “ESKAPE-E” (Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa, and Enterobacter species) group of pathogens. These are causes of healthcare-associated infections since 2006, but in a lower proportion of events and with better antimicrobial susceptibility. In contrast to 2012, when the resistances to most of antibiotics increased by little more than 20%. There were multi-drug-resistant alerts especially for Klebsiella pneumoniae, Escherichia coli, and Klebsiella oxytoca. Few antibiotics (imipenem, meropenem, gentamycin and amikacin) maintained their activity profile in both periods, and others like ertapenem and quinolones that were not used in 2006, appeared in 2012 with good antimicrobial susceptibility.
ConclusionsThe “ESKAPE-E” pathogens are a real problem for public health and the multidrug antibiotic resistance allows them to evade many of the available therapeutic options. In addition to the fact of there are no new antimicrobials to perform studies and create maps of bacterial resistances in our institutions, it would help us to make better decisions on having initiated empirical therapies.
Sin lugar a dudas a principios de los años 40, con el advenimiento de los antibióticos, el área de la medicina se llenó de un gran entusiasmo, sobre todo por los logros alcanzados en curar una serie de enfermedades que eran una amenaza para la vida y productividad de un enfermo, que en ese entonces eran más de índole comunitario. Sin embargo con el paso del tiempo tanto los antibióticos como los gérmenes causantes de enfermedades infecciosas han evolucionado a la par, ejemplo; la primera β-lactamasa contra la penicilina apareció en 1940. Hacia 1965 se describe el desarrollo de una β-lactamasa que es transmitida por plásmidos en una cepa de Escherichia coli (E. coli), que es llamada TEM-1. En 1971 se describe una cefalosporinasa generada por Klebsiella que es llamada SHV-1. En la actualidad la gran mayoría de las β-lactamasas (que ya exceden las 300) derivan de mutaciones de TEM-1 y de SHV-1. Conforme avanza el tiempo las bacterias han generado además de diversas β-lactamasas, las β-lactamasas de espectro extendido, las β-lactamasas de espectro ampliado a las carbapenemasas y no tan recientemente (1991) a las métalo-β-lactamasas1,2.
Siendo tal que casi 80 años después nos enfrentamos a un futuro incierto, ello por la resistencia que estos patógenos han generado contra una amplia serie de antibióticos en la actualidad, condicionando así que de nuevo encaremos nuevos retos de tratamiento para evitar el curso natural de la enfermedad que pueda terminar con la vida del paciente. Hecho que nos preocupa grandemente porque esta resistencia antibiótica no solo la vemos en patógenos comunitarios, sino que es más marcada en aquellos que son adquiridos intrahospitalariamente3,4.
Sabemos que prácticamente desde que se conoció la primera bacteria se supo que mostraba ciertos mecanismos de protección contra los antibióticos, ya fuese a través de mutaciones o por adquisición de material genético. Al paso del tiempo, las bacterias han desarrollado estrategias variadas que les han permitido generar resistencia incluso tanto a antibióticos a los cuales ya se había expuesto anteriormente y que eran susceptibles, como a aquellos a los que no se había expuesto la bacteria. Esto ha crecido de manera alarmante y ha permitido el desarrollo de infecciones graves con elevada prevalencia y alta morbilidad en el ámbito de las infecciones adquiridas de forma nosocomial o como tal derivadas de la propia atención a la salud, denominadas actualmente infecciones asociadas a la atención a la salud (IAAS)5,6.
Sabemos que entre los agentes causales de las IAAS participan hongos, virus, parásitos y bacterias. De estas últimas, los patógenos gramnegativos, en particular el grupo de las enterobacterias, son los que representan la principal causa de infección, destacando Klebsiella pneumoniae (K. pneumoniae), E. coli y Enterobacter spp. entre otras7–9. Ciertamente las bacterias gramnegativas son las que predominan en la literatura como causantes de IAAS, sin embargo para los fines de este artículo solo mencionaremos las más relevantes en cuanto a ser causantes de infección nosocomial. Dado lo anterior, el objetivo de este reporte es describir la prevalencia e incidencia de patógenos nosocomiales del tipo de los gramnegativos identificados durante la vigilancia epidemiológica en 2 periodos de tiempo (2006 y 2012), y sobre todo aquellos del grupo denominado ESKAPE (Enterococcus faecium, Staphylococcus aureus, K. pneumoniae, Acinetobacter baumannii [A. baumannii], Pseudomonas aeruginosa [P. aeruginosa], Enterobacter spp.), o ESKAPEE (que incluye además a E. coli), e identificar cuál ha sido la tendencia en cuanto a su resistencia antimicrobiana. No se hará referencia en esta revisión de los patógenos cocos grampositivos, los cuales serán motivo de otro análisis. Cabe señalar que hay otra nomenclatura (ESCAPE) que incluye a C: Clostridium difficile, el cual tampoco se incluye en este trabajo10,11.
Material y métodosEl Departamento de Epidemiología del Hospital Infantil de México Federico Gómez (tercer nivel de atención), como parte de su sistema de vigilancia de infecciones nosocomiales registra mediante formatos de reporte de infecciones nosocomiales los casos relacionados, y por igual en esos formatos se anotan los patógenos identificados en cada evento considerado como IAAS. Se captura cuál es su susceptibilidad antibiótica y cuál su resistencia a los diferentes antibióticos testados en su momento; de tal manera que para los propósitos de este estudio se analizaron todos los resultados de patógenos identificados por medio de los diversos métodos de cultivos (hemocultivo, urocultivo, cultivo punta de catéter, cultivo líquido cefalorraquídeo, etc.), registrados en esos formatos durante 2 periodos de tiempo (enero a diciembre del 2006 y enero a diciembre del 2012). El objetivo de describir la frecuencia y prevalencia de los principales patógenos nosocomiales gramnegativos identificados en esta vigilancia ocurrida durante 2006 y compararlos con los identificados en el 2012 es evaluar si en el contexto de integración de hospital (no por servicio ni por sitio de infección) ha habido cambios o las tendencias en cuanto a su resistencia antimicrobiana son las mismas. Los formatos de registro se concentran en el departamento de epidemiología del Hospital Infantil de México Federico Gómez. Cabe señalar que todos los patógenos identificados como causantes de IAAS se correlacionaron con la libreta de reportes microbiológicos del departamento de bacteriología, del cual se rescatan las susceptibilidades antibióticas. Dicho departamento identifica las cepas bacterianas mediante pruebas manuales básicas, la morfología colonial, tinción de Gram, y el procedimiento de identificación mediante el sistema automatizado Vitek 2XL (bio-Mérieux), mismo sistema empleado para pruebas de susceptibilidad antibiótica acorde con los lineamientos del Instituto de Estándares de Laboratorio Clínico (CLSI)12,13.
Análisis estadísticoSe realizó un análisis descriptivo de 2 periodos de tiempo para determinar la frecuencia y prevalencia de los principales patógenos identificados durante el 2006 y compararlos con los del 2012, empleando, medidas de tendencia central y dispersión. En la comparación entre ambos periodos de tiempo analizados se calcularon frecuencias simples y acumuladas, al igual que porcentajes. Con base en los porcentajes de concordancia para detectar las concentraciones mínimas inhibitorias de susceptibilidad vs. resistencia microbiológica, se construyó un mapa microbiológico en cuanto a los patrones de actividad (sensible, resistente e intermedio) de los diferentes antibióticos analizados14–17, considerando para nuestro hospital un porcentaje de susceptibilidad entre 66-80%,>80% y<66%.
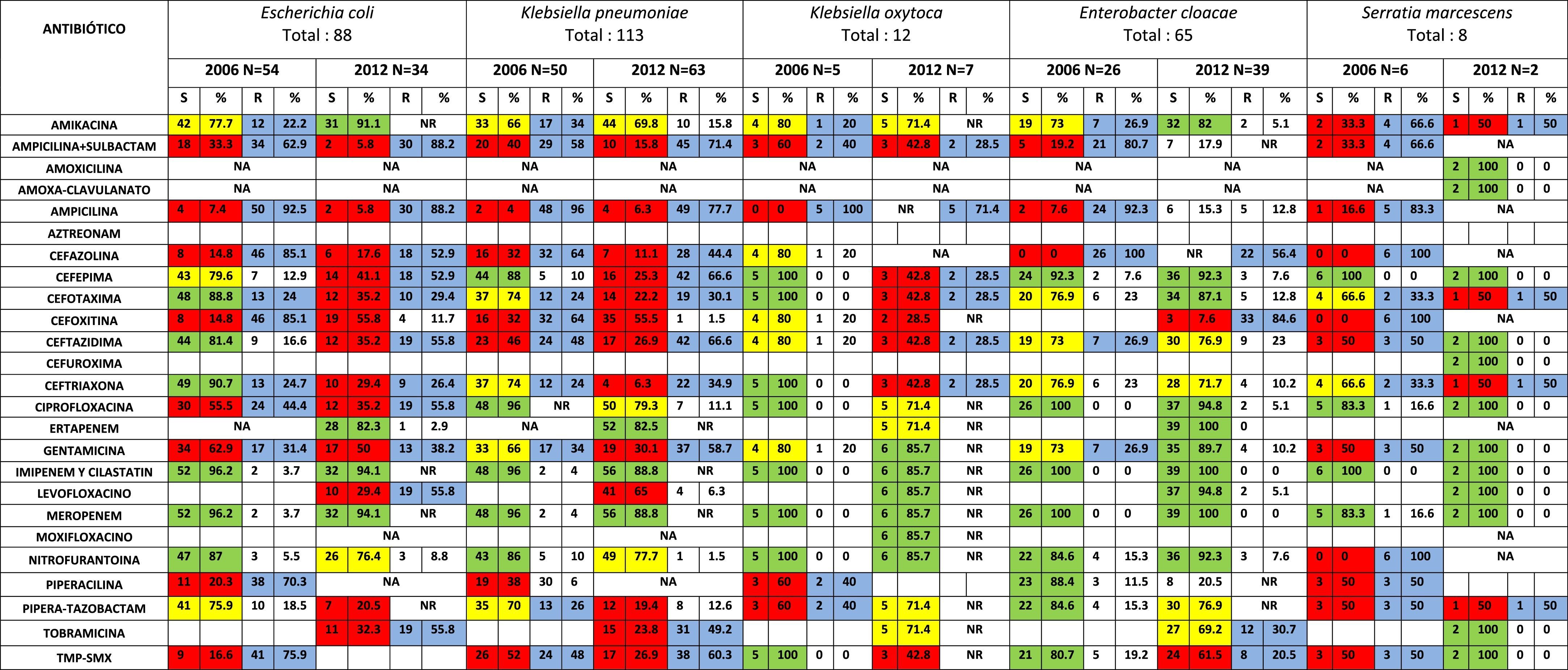
ResultadosEn el global (2006 y 2012) consideramos importante dividir los microorganismos con base en sus características de fermentar o no hidratos de carbono independientemente de si son solo bacilos gramnegativos (BGN) y/o si son de la familia Enterobacteriacea. Se encontraron en primer lugar las enterobacterias fermentadoras de lactosa (EFL), de las cuales se aislaron 5 diferentes patógenos que destacaron en ambos periodos, correspondiendo a un total de 286 BGN-EFL; 141 en el 2006 y 145 en el 2012. De estos, K. pneumoniae ocupó el primer lugar con 113 aislamientos (42.1% de N=286), correspondiendo 63 (55.7% de N=113) aislamientos en el 2012 y 50 (44.2% de N=113) en el 2006. Seguida de E. coli con 88 aislamientos (30.7% de N=286); correspondiendo 54 aislamientos (61.3 de N=88) en el 2006 y solo 34 (38.6% de N=88) en el 2012. En tercer lugar encontramos a Enterobacter cloacae (E. cloacae) con 65 aislamientos (22.7% de N=286); predominando en el 2012 con 39 aislamientos (60% de N=65) y solo 26 (40% de N=65) en el 2006. Otros menos frecuentes pero de relativa importancia dentro de las IAASH fueron: Klebsiella oxytoca (K. oxytoca) y Serratia marcescens (S. marcescens) con 12 (4.1% de N=286) y 8 (2.7% de N=286) aislamientos respectivamente (tabla 1)
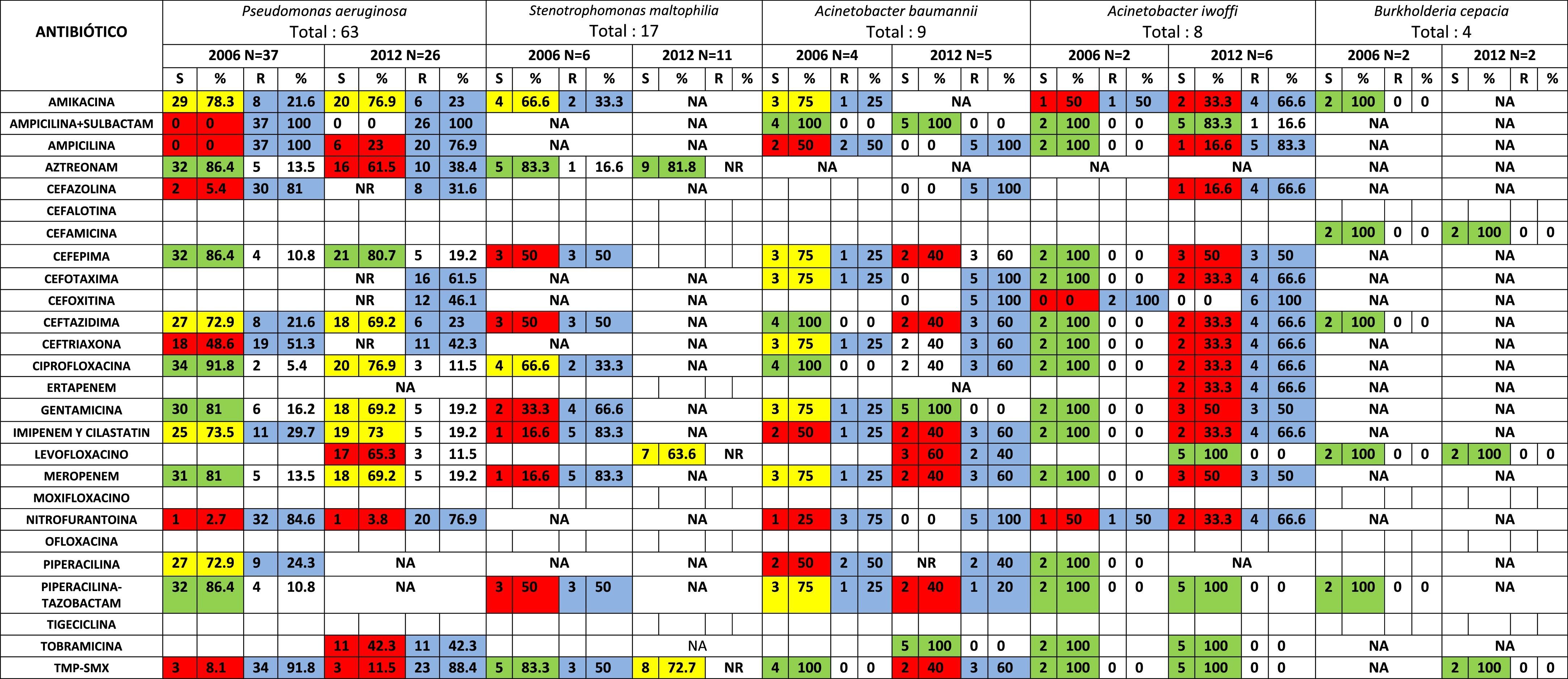
Les siguen los bacilos gramnegativos no fermentadores de glucosa (BGN-NFG), de los cuales también hubo 5 principales microorganismos (N=101) que destacaron en estos periodos analizados. Resaltó P. aeruginosa con 88 aislamientos (87.1% de N=101); correspondiendo 37 (42% de N=88) al 2006 y 26 (29.5% de N=88) al 2012. El segundo lugar lo ocupó Stenotrophomonas maltophilia (S. maltophilia) con 17 (16.8% de N=101) aislamientos, de los cuales 11 (64.7%) de N=17) fueron en el 2012 y 6 (35.3% de N=17) en el 2006. Acinetobacter baumannii ocupó el tercer lugar con tan solo 9 (8.9% de N=101) aislamientos; 5 (55.5% de N=9) en el 2012 y 4 en el 2006 (44.5% de N=9). En menor frecuencia se aisló Acinetobacter iwoffi (A. iwoffi) 8/101 (7.9%) y Burkholderia cepacia (B. cepacia) 4/101 (3.9%)(tabla 2).
Cabe señalar que hubo en total otros 10 aislamientos de 4 diferentes tipos de microorganismos identificados del tipo de enterobacterias no fermentadoras de lactosa, los cuales por ser en menor número no se analizaron. Estos fueron: Proteus mirabilis con 6 aislamientos (3 por periodo), Proteus vulgaris (2 en el 2006), Morganella morganii (uno en el 2012) y Aeromona hydrophila (un aislamiento en el 2006).
En cuanto a las susceptibilidades antimicrobianas de los principales patógenos asociados con IAAS, los patrones de resistencia se consideraron en base a la utilidad de empleo: susceptibilidad entre el 66-80% (puede emplearse con reserva); susceptibilidad>del 80% (amplio uso) y susceptibilidad<66% (no usar más).
En la tabla 1 podemos observar los 3 principales patógenos correspondientes al grupo de BGN-EFL, donde podemos ver que E. coli mostró cambios importantes relativos a mostrar resistencia a antibióticos para los cuales en el 2006 tenía una adecuada susceptibilidad, tal es el caso para cefotaxima, ceftriaxona, ceftazidima, y cefepima, en donde los patrones de resistencia fueron del 29.4,26.4,55.8 y 52.9% respectivamente. Mantuvo excelentes porcentajes de susceptibilidad en ambas temporadas a carbapenémicos, tales como: imipenem-cilastatin (96.2 vs. 94.1%) y meropenem (96.2 vs. 94.1%) e incluso ertapenem en el 2012 del 82.3%. Este último no se usó en el 2006. Mejoro su patrón de susceptibilidad a amikacina del 77.7% en el 2006 al 91.1% en el 2012, y lo mantuvo con nitrofurantoína del 87 vs. 76.4% respectivamente entre 2006 y 2012. En cuanto a K. pneumoniae, no hubo cambios importantes en sus patrones de resistencia y susceptibilidad entre 2006 y 2012 a los diferentes antibióticos probados; salvo cefepima que en el 2006 era activo (88%) contra este patógeno, para el 2012 su susceptibilidad bajó al 25.3% con una resistencia del 66.6%, al igual que piperacilina-tazobactam cuya actividad del 70% en 2006, bajo al 19.4% para 2012. Las susceptibilidades se mantuvieron en ambos periodos tanto para amikacina, imipenem-cilastatina y meropenem; e incluso ertapenem que no se empleó en el 2006 mostró actividad del 82.5% contra este patógeno. El tercero en importancia fue E. cloacae, que se mantuvo sin cambios en cuanto a excelentes patrones de susceptibilidad entre 2006 y 2012 para la mayoría de los antibióticos retados, tales como: amikacina, gentamicina, ceftriaxona, ceftazidima, cefepima, ciprofloxacina, imipenem-cilastatina, meropenem, nitrofurantoína y piperacilina-tazobactam. Y los redujo solo en cefotaxima y TMP-SMX. Igualmente mostró excelente actividad a antibióticos no empleados en el 2006, como levofloxacino (94.8%), similar a ciprofloxacina, y a ertapenem (100%), igual que los otros 2 carbapenémicos.
En los otros 2 en menor frecuencia de aislamiento (K. oxytoca y S. marcescens) observamos una excelente actividad antimicrobiana de los diversos antibióticos probados, sobre todo hacia S. marcescens, cuya susceptibilidad para el 2012 fue del 100%. Aunque para K. oxytoca en el 2006 sus susceptibilidades antibióticas se mantuvieron entre el 80-100%; en el 2012 para ciertos antibióticos bajó su actividad de porcentajes de 71.4 al 85.7%, y mostró resistencia a ceftriaxona, cefotaxima y cefepima del 42.8% respectivamente (tabla 1).
En cuanto a los BGN-NFG, de los 5 de mayor aislamiento (tabla 2) observamos que destacaron 2, P. aeruginosa y S. maltophilia, llamando la atención que con relación a P. aeruginosa los patrones de resistencia se presentaron por igual en el 2006 y en el 2012 para la mayoría de los antibióticos analizados, y que solo cefepima mantuvo excelente actividad en ambos periodos de tiempo, 86.4 vs. 80.7% respectivamente. En cuanto a S. maltophilia, en el 2006 observamos que solo aztreonam y TMP-SMX mostraron excelente actividad (83.3%), así como amikacina y ciprofloxacina tuvieron igual buena actividad (66.6%). Lamentablemente para el 2012 se redujo la actividad de TPM-SMX al 72.7%, pero se mantuvo la de aztreonam (81.8%) y antibióticos nuevos (en esa época) se mostraron activos, como levofloxacino con el 63.6%.
De los otros 3 patógenos encontrados, observamos que ambos Acinetobacter (baumannii e iwoffi) incrementaron sus patrones de resistencia del 2006 al 2012 a antibióticos que inicialmente eran incluso 100% activos y que se convirtieron en resistentes, con porcentajes que variaron del 25-100% en A. baumannii y del 50-100% para A. iwoffi; salvo ampicilina-sulbactam que mantuvo actividad del 100 vs. 100% para A. baumannii y del 100 vs. 83.3% para A. iwoffi respectivamente en ambos periodos analizados. Igualmente para este patógeno, antibióticos como piperacilina-tazobactam, tobramicina y TMP-SMX se mantuvieron activos al 100% tanto en 2006 como en 2012. Cabe señalar que para el 2012 gentamicina y tobramicina mostraron excelente actividad (100%) para A. baumannii, así como levofloxacino (100%) para A. iwoffi. Finalmente, para B. cepacia encontramos que solo se retó en el 2006 a: amikacina, cefamicina, cefoxitina, levofloxacino y piperacilina-tazobactam, fue susceptible a todos ellos en el 100%; pero para el 2012 de estos 5 antibióticos solo se testó contra cefamicina y levofloxacino, a la vez que para TMP-SMX, encontrando para estos el 100% de actividad (tabla 2).
AnálisisEn este estudio observamos que la incidencia total de patógenos gramnegativos identificados en ambos periodos fue de 387, con una mayor prevalencia de BGN-EFL sobre los BGN-NFG, sobre todo en el 2012; ya que para el 2006 hubo 141 aislamientos con una prevalencia de 0.36, que correspondió a 36 aislamientos por cada 100 cultivos tomados, y para el 2012 fueron 145 aislamientos; su prevalencia fue de 0.37, que correspondió a 37 aislamientos por cada 100 cultivos tomados.
En cuanto a los BGN-NFG su incidencia fue de 101 aislamientos, siendo aquí la prevalencia mayor para el 2006 vs. 2012. Esto porque en el 2006 se identificaron 51 patógenos, lo que correspondió a una prevalencia de 0.13, o sea 13 aislamientos por cada 100 cultivos, y para el 2012 solo 50 patógenos NFG fueron identificados dando una prevalencia de 0.12 (12 aislamientos por 100 cultivos analizados).
A pesar de que hubo una mayor prevalencia de BGN-EFL en el 2012, la proporción de estos en el 2006, fue mayor solo para 2 de ellos: E. coli (54/88) y S. marcescens (6/8), correspondiendo al 0.61 (61%) y 0.75 (75%) respectivamente. Resaltar que en el global 2006 y 2012 K. pneumoniae fue el patógeno predominante, con 113 aislamientos, con una prevalencia y proporción global de 0.29 y 29.1% respectivamente (tablas 1 y 3)
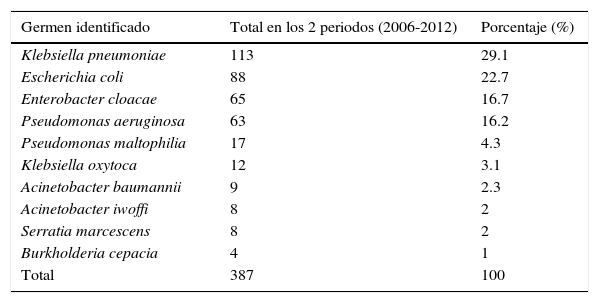
Frecuencia global de patógenos identificados
| Germen identificado | Total en los 2 periodos (2006-2012) | Porcentaje (%) |
|---|---|---|
| Klebsiella pneumoniae | 113 | 29.1 |
| Escherichia coli | 88 | 22.7 |
| Enterobacter cloacae | 65 | 16.7 |
| Pseudomonas aeruginosa | 63 | 16.2 |
| Pseudomonas maltophilia | 17 | 4.3 |
| Klebsiella oxytoca | 12 | 3.1 |
| Acinetobacter baumannii | 9 | 2.3 |
| Acinetobacter iwoffi | 8 | 2 |
| Serratia marcescens | 8 | 2 |
| Burkholderia cepacia | 4 | 1 |
| Total | 387 | 100 |
Respecto a los BGN-NFG, ciertamente su prevalencia fue relativamente elevada en el 2012, no obstante su incidencia en cuanto a número de aislamientos fue igual en ambos periodos, solo para B. cepacia con 2 aislamientos respectivamente, pero la proporción de P. aeruginosa fue mayor en el 2006 (37/63), correspondiendo al 0.58 (58.7%) (tablas 2 y 3.)
En la tabla 3 se enlistan en orden de frecuencia los microorganismo identificados en ambos periodos analizados, encontrando que si los consideramos como patógenos ESKAPE o ESKAPE-E (sin incluir a S. aureus) tenemos que 4 de ellos (K: K. pneumoniae–E: E. coli–E: E. cloacae y P: P. aeruginosa) destacan entre los aislamientos identificados tanto en el 2006 como en el 2012. El otro de ellos A: A. baumannii, que se ha convertido recientemente en uno de los principales patógenos multifarmacorresistentes, afortunadamente no mostró una prevalencia ni frecuencia elevadas (0.02 y 2.3% respectivamente).
Respecto a las susceptibilidades antimicrobianas de los principales BGN-EFL podemos decir que sí hubo un incremento en 6 años en cuanto a mayor número de antibióticos resistentes sobre todo para K. pneumoniae y E. coli así como también para K. oxytoca, incluso antibióticos con excelente actividad del 100% para estos patógenos disminuyeron su susceptibilidad sin dejar de estar dentro del rango de continuar siendo empleados como primera opción. Cabe resaltar que patógenos como S. marcescens y E. cloacae continuaron mostrando el mismo patrón de susceptibilidad antimicrobiana e incluso mejoraron su porcentaje de actividad para algunos otros antibióticos. Al respecto también es importante señalar que antibióticos con los que no se contaba antes en el arsenal terapéutico, como ertapenem, tuvieron excelente actividad contra estos 5 patógenos BGN-EFL (tabla 1).
En cuanto a la susceptibilidad mostrada de los BGN-NFG, llama fuertemente la atención que A. iwoffi a diferencia de A. baumannii incrementó significativamente su resistencia a más antibióticos que A. baumannii, el cual también se vio afectado ya que se volvió resistente a antibióticos a los que inicialmente era activo regularmente. P. aeruginosa bajó sus porcentajes de actividad para algunos antibióticos, sin dejar de estar dentro del rango de utilidad. Resalta en este grupo de BGN que tobramicina en el 2012 resultó ser un antibiótico con excelente actividad (100%) contra A. baumannii, A. iwoffi y B. cepacia; asimismo con igual actividad, levofloxacino para A. iwoffi (tabla 2).
ConclusionesEn este estudio podemos observar que al igual que lo que se ha reportado sobre la epidemiología global e incluso local, las bacterias gramnegativas incluidas la enterobacterias desempeñan un papel importante como causantes de IAAS8,18–20 En este análisis comparativo de 6 años podemos decir que en nuestro hospital en el 2006 estos patógenos no representaban ni una causa seria de infecciones adquiridas dentro del hospital (192 eventos identificados) ni mucho menos un problema importante de resistencia bacteriana; pero para el 2012, a pesar de que el número de eventos o aislamientos asociados con IAAS no se incrementó significativamente (195 eventos identificados), el patrón de resistencia antimicrobiana sí lo hizo de forma importante. Podemos observar que los patógenos ESKAPE o ESKAPE-E han estado presentes en todo este tiempo y a la par de que surgió la primera nomenclatura (en el 2008 por Rice10) donde empezaron a considerarse como bacterias superpoderosas o malas por su resistencia a varios antimicrobianos; de igual manera se globalizó y nos alcanzó, como vemos en las tablas 1 y 2 en los comparativos de susceptibilidad vs. resistencia antibiótica. Como tal en estas observamos la resistencia mostrada ya para el 2012 tanto para cefalosporinas de segunda, tercera e incluso hasta de cuarta generación como a ureidopenicilinas, tanto de enterobacterias como BGN-NFG, lo cual nos traduce que son bacterias productoras de β-lactamasas de espectro extendido. La resistencia observada o la disminución en su actividad hacia algunas bacterias como Acinetobacter y Pseudomonas de los carbapenémicos nos hace pensar en que son productores de carbapenemasas tipo OXA en Acinetobacter y metalo-β-lactamasas principalmente en Pseudomonas. A pesar de que solo A. iwoffi y S. marcescens se mostraron con resistencia a aminoglucósidos, los otros microorganismos únicamente evidenciaron disminución de su actividad. Estos resultados observados en nuestro estudio por igual nos alertan sobre la problemática de la multifarmacorresistencia, como ya señalaban incluso Falagas et al. desde el 200719. Y sin lugar a dudas en el momento actual la multifarmacorresistencia asociada a los patógenos ESKAPE-E se ha convertido en uno de los principales problemas de salud pública en el ámbito de las IAAS, gracias a que ellos han logrado adquirir una gran variedad de mecanismos de resistencia a múltiples antibióticos que les permiten evadir prácticamente la mayoría de las opciones terapéuticas disponibles en la actualidad, aunado ello a otro problema que es el que no haya nuevos fármacos con potencial actividad para estos microorganismos. No obstante, los programas de vigilancia epidemiológica y creación de mapas sobre la resistencia vs. susceptibilidad bacteriana en cada institución nos ayudan a determinar la magnitud del problema, esclarecer si ha habido o no aumento de esta (como lo fue nuestro caso), detectar tipos de resistencia anteriormente no conocidas y determinar si algún tipo en particular de resistencia está extendida o asociada con algún brote. Al igual que favorecen que se puedan tomar las mejores decisiones en cuanto al inicio de una terapéutica empírica en el paciente con una IAAS. Cabe señalar que en estas tablas se enmarcan los porcentajes de resistencias significativos acorde a los lineamientos de que antibióticos con≥20% de resistencia deben ser vigilados más estrechamente17,21,22. Asimismo con base en ello este análisis servirá de referencia para hacer otro corte en otro periodo igual de tiempo y ver el comportamiento del mapa.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses; asimismo, que no hay relaciones financieras, laborales o de otra índole, respecto del presente trabajo, que tengan un particular interés en los resultados de la investigación.