La otitis media crónica (OMC) activa (mucosa) es una enfermedad infecciosa frecuente de la infancia, tanto en los países en vías de desarrollo como en los indus-trializados1-3. Produce una morbilidad considerable y es una causa general importante de trastornos auditivos en el niño. Además, puede originar graves complicaciones intra y extracraneales, como mastoiditis y meningitis4-8. Por lo tanto, es importante adoptar una conducta activa en el tratamiento de la OMC6. No se conoce bien cuál es el tratamiento médico o quirúrgico más eficaz en la OMC, pues se han efectuado pocos ensayos controlados de distribución aleatoria y, además, los criterios de inclusión, los parámetros valorados en la evolución y el seguimiento varían considerablemente en los distintos estudios9-16.
El trimetoprim-sulfametoxazol (TMP-SMX) se ha utilizado durante muchos años en el tratamiento de las infecciones de las vías respiratorias altas en el niño, al ser un antimicrobiano económico y bien tolerado. Se ha demostrado su eficacia profiláctica en la otitis media aguda recurrente17,18. Un análisis retrospectivo de niños con OMC que se trataron con TMP-SMX en nuestro hospital durante un período prolongado mostró unos resultados prometedores. Así pues, se inició un ensayo de distribución aleatoria, controlado con placebo, sobre la administración oral de TMP-SMX durante 6 a 12 semanas, además de una corta tanda de gotas óticas con esteroides y antibióticos, en niños con otitis media crónica activa en quienes había fracasado el tratamiento convencional con medicamentos tópicos y/o antibióticos sistémicos a corto plazo. Se informa aquí sobre la eficacia clínica y los hallazgos bacteriológicos observados en dicho ensayo clínico.
MATERIAL Y MÉTODOSPacientesSe llevó a cabo un ensayo de distribución aleatoria, controlado con placebo, entre febrero de 2003 y junio de 2006. Otorrinolaringólogos y pediatras de toda Holanda remitieron a los potenciales participantes, es decir, niños con OMC en quienes había fracasado el tratamiento convencional con medicamentos tópicos y/o antibióticos sistémicos a corto plazo, al departamento de otorrinolaringología infantil del University Medical Center Utrecht. Los criterios de inclusión fueron: edad 1 a 12 años y una historia documentada de, al menos, 3 meses de otorrea continua a través de una perforación timpánica o un tubo de timpanostomía. Se excluyó a los niños con (1) colesteatoma, (2) déficit inmunológicos conocidos, excepto los de las subclases IgA o IgG, (3) síndrome de Down, (4) anomalías craneofaciales, fibrosis quística, (6) discinesia ciliar primaria, (7) alergia alTMP-SMX y (8) uso continuado de antibióticos durante más de 6 semanas en los últimos 6 meses. El comité de ética del University Medical Center Utrecht aprobó el protocolo del estudio.
Distribución aleatoriaCon el consentimiento informado de los progenitores, se distribuyó aleatoriamente a los niños para recibir TMP-SMX oral (18 mg/kg 2 veces al día) o un placebo durante 6 a 12 semanas. Un colaborador independiente elaboró una lista aleatoria, generada por ordenador, que se remitió al farmacéutico del hospital, quien proporcionó frascos numerados con una suspensión de TMP-SMX o placebo. El sabor de ambas suspensiones y el aspecto del frasco y del líquido eran similares en ambos casos. Al ingresar en el estudio, el investigador encargado entregaba la suspensión que correspondía al número siguiente de la distribución aleatoria. Los investigadores desconocieron la distribución de los pacientes hasta el final del estudio.
En la primera visita de control a las 6 semanas, si persistía la otorrea en uno u otro oído se proseguía con la medicación durante otras 6 semanas. Se suspendía la medicación si ambos oídos se hallaban libres de otorrea y los padres confirmaban que no la habían observado durante la semana anterior. Se indicó a los padres que reanudaran el tratamiento si los síntomas de otorrea reaparecían entre las visitas de control de las 6 y 12 semanas. A su ingreso en el estudio, y también si la otorrea estaba presente a las 6 y 12 semanas, se prescribieron en ambos grupos gotas óticas de hidrocortisona-bacitracina-colistina (Baci-coline-B) durante 7 a 10 días, además de la medicación del estudio. Se eligieron estas gotas óticas debido a que se emplean profusamente en Holanda y se consideran en general como inocuas6. A partir de julio de 2004 se prescribieron gotas óticas de hidrocortisona-neomicina-polimixina B (Otosporin), debido a que la anterior combinación ya no se hallaba disponible en Holanda. Durante las 12 primeras semanas se permitió que los otorrinolaringólogos y los pediatras locales prescribieran a los participantes la medicación adicional que acostumbraran a emplear, a excepción de TMP-SMX. Después de la segunda visita de control a las 12 semanas, se suspendió la medicación de estudio, independientemente de la presencia o ausencia de otorrea. En ese momento se remitió a los niños a su médico. Un investigador independiente abrió el código e informó por carta a los padres y a los médicos locales acerca del tratamiento que se había seguido. En la carta se incluía también una recomendación de tratamiento en el caso de que persistiera o reapareciera la otorrea: TMP-SMX (2 veces al día 18 mg/kg durante 6 a 12 semanas) en el grupo placebo, y azitromicina (1 vez al día 5 mg/kg durante 6 a 12 semanas) en el grupo TMP-SMX. En esa fase, los otorrinolaringólogos y los pediatras locales podían seguir esta recomendación o tratar los síntomas de otorrea según su práctica habitual.
Inclusión y seguimientoEn el momento de la inclusión se cumplimentaron formularios específicos para recoger información sobre los potenciales factores de riesgo para las afecciones óticas, la duración de la otorrea antes de ingresar en el estudio y los tratamientos que se habían empleado. En el momento de la inclusión y en las tres visitas de control a las 6 y 12 semanas y al año, los padres cumplimentaron 1 cuestionario genérico y 2 cuestionarios específicos sobre la calidad de vida en relación con el estado de salud: child health questionnaire parental form19 (CHQpf50), cuestionario de 6 ítems sobre la otitis media20 (OM-6) y una escala analógica visual para medir la calidad de vida en relación con la patología ótica20. En estas visitas se examinaron los oídos con el otomicroscopio y se registraron las siguientes características: tubo de timpanostomía, perforación timpánica, otorrea y exudado del oído medio. En caso de otorrea se practicaba un frotis del exudado antes de proceder a la aspiración de limpieza. Para investigar las reacciones adversas a la medicación del estudio, al ingreso y a las 6 y 12 semanas se tomaron muestras de sangre venosa para practicar un hemograma completo y pruebas funcionales hepáticas (AST, ALT, -GT) y renales (urea, creatinina). En los niños mayores de 3 años se practicaron audiometrías de tonos puros a las frecuencias de 500, 1.000, 2.000 y 4.000 Hz.
Los padres cumplimentaban un diario donde anotaban la medicación del estudio y otros medicamentos empleados, incluidas las gotas óticas. Estos datos se recogieron en las visitas de control. En estas visitas se registraron los efectos adversos de la medicación y se pesaron los frascos de suspensión para averiguar el grado de cumplimiento de las prescripciones.
Examen bacteriológicoEn el momento de la inclusión y en las visitas de control, los médicos de la investigación tomaron muestras del exudado mediante escobillones estériles flexibles con punta de rayón (Medical Wire & Equipment Co.). Las muestras se guardaron de inmediato a temperatura ambiente en el medio de transporte Stuart, se remitieron al laboratorio de microbiología y en el plazo de 18 horas se sembraron en placas con agar-sangre de carnero (5%), agar Haemophilus y agar de Mac Conkey, para aislar los potenciales gérmenes aerobios. Las placas de cultivo se incubaron aeróbicamente a 37 °C (agar de Mac Conkey) y atmósfera con < 5% de dióxido de carbono (agar-sangre y agar Haemophilus), y se examinaron a las 24 y 48 horas. Las colonias sospechosas de Streptococcus pneumoniae, Haemophilus influenzae, Moraxella catarrhalis, Staphylococcus aureus, Streptococcus pyogenes o bacterias gramnegativas aerobias se identificaron con los métodos descritos previamente21.
Parámetros valorados en la evoluciónEl parámetro primario estuvo constituido por los signos otomicroscópicos de otorrea en presencia de un tubo de timpanostomía o de una perforación timpánica, en las visitas de las 6 y 12 semanas y de 1 año. Los parámetros secundarios fueron: uso de medicación ótica diferente a la del estudio; efectos adversos de la medicación del estudio; operaciones ORL practicadas; calidad de vida en relación con el estado de salud, niveles auditivos con tonos puros y hallazgos bacteriológicos en las muestras de otorrea.
Aspectos estadísticosAsumiendo un porcentaje de recuperaciones espontáneas del 25% y un efecto del TMP-SMX del 50% (según los datos recogidos en un estudio retrospectivo de niños tratados con TMPSMX por OMC en nuestro hospital), y aceptando un valor = 0,05 y una potencia de 0,80, se calculó que cada grupo debería estar constituido por 50 niños.
Las diferencias de tasas y los intervalos de confianza del 95% se calcularon en las tres visitas de control para comparar ambos grupos con respecto a: resultados otomicroscópicos, empleo de medicación ótica diferente a la del estudio y efectos adversos de la medicación del estudio. Para detectar la posible modificación de los efectos se realizaron análisis de subgrupos según la edad ( 3/> 3 años) y la duración de la otorrea antes de ingresar en el estudio ( 6/> 6 meses), según se especificaba previamente en el protocolo del ensayo. Las puntuaciones de la calidad de vida en relación con la salud se transformaron linealmente en escalas de 0-100. La diferencia entre las puntuaciones en las visitas de control y al ingreso en el estudio se calcularon y se presentaron por campos. Las diferencias entre los grupos en las puntuaciones por campos a las 0, 6, 12 semanas y 1 año se analizaron con la prueba de la U de Mann-Whitney, al no seguir una distribución normal. Se utilizaron diagramas de caja y patillas para comparar los niveles auditivos de tonos puros (conducción aérea a 500, 1.000, 2.000 y 4.000 Hz) entre los dos grupos. En los hallazgos bacteriológicos se calcularon las diferencias de porcentajes y de intervalos de confianza del 95%. Todos los análisis se realizaron según el principio de la intención de tratar.
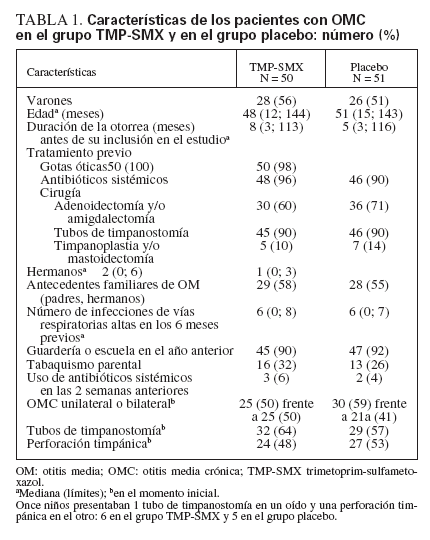
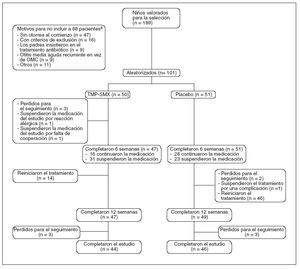
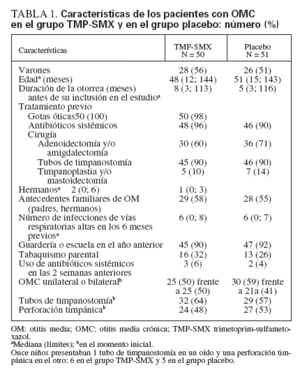
RESULTADOSGrupo de estudioEntre febrero de 2003 y noviembre de 2005 se incluyó a 101 niños: 50 al grupo TMP-SMX y 51 al grupo placebo. En la figura 1 se observa el flujo de los participantes a lo largo del ensayo. En el momento inicial, las características clínicas no diferían significativamente entre los dos grupos (tabla 1). La edad mediana de los participantes era de 50 meses (RIC 55). Los niveles de cooperación fueron buenos en ambos grupos, pues se consumió más del 90% de la medicación prescrita.
Fig. 1. Flujo de participantes durante el estudio. OMC: otitis media crónica; TMP-SMX: trimetoprim-sulfametoxazol. aEl número es > 87 debido a existir más de 1 motivo; bla medicación del estudio se suspendió si ambos oídos se hallaban sin otorrea y los padres confirmaban que no habían observado signos de otorrea durante la semana anterior.
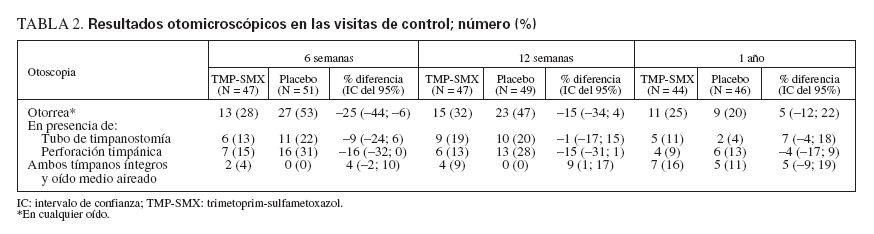
Parámetros valorados en la evoluciónEn el control realizado a las 6 semanas se observó otorrea en el 28% de los niños del grupo TMP-SMX y en el 53% del grupo placebo (DT –25 [IC del 95% –44; –6], número necesario para tratar [NNT] 4) (tabla 2). A las 12 semanas, la diferencia de tasas era todavía de –15 (IC del 95% –34; 4) (NNT 7) a favor del grupo TMPSMX. En el control al cabo de 1 año no había diferencia entre los dos grupos (DT 5 [IC del 95% –12; 22]).
TABLA 1. Características de los pacientes con OMC en el grupo TMP-SMX y en el grupo placebo: número (%)
TABLA 2. Resultados otomicroscópicos en las visitas de control; número (%)
En los controles a las 6 y 12 semanas y al año, hubo más niños del grupo TMP-SMX con integridad timpánica y aireación del oído medio, en comparación con el grupo placebo.
Los resultados otomicroscópicos se analizaron también según la edad y la duración de la otorrea antes de incorporarse al estudio. A las 6 semanas existía aún otorrea en 8 (29%) niños con más de 6 meses de otorrea antes del estudio que se trataron con TMP-SMX, y en 14 (67%) tratados con placebo (DT –38 [IC del 95% –64; –12]) (NNT 3). En los niños con otorrea previa de 3 a 6 meses, estos porcentajes fueron de 5 (26%) frente a 13 (43%) (DT –17 [IC del 95% –44; 10]) (NNT 6). A las 12 semanas, las cifras fueron de 11 (39%) frente a 15 (71%) (DT –32 [–59; –5]) (NNT 3) y 4 (21%) frente a 8 (29%) (DT –8 [–33; 17]) (NNT 13), respectivamente. Al cabo de 1 año, el efecto del tratamiento ya no se vio influido por la duración de la otorrea antes de ingresar en el estudio. La edad no influyó en la eficacia del TMPSMX.
Durante las primeras 6 semanas, 38 (83%) niños del grupo TMP-SMX y 39 (77%) del grupo placebo utilizaron gotas óticas con antibiótico (DT 6 [IC del 95% –10; 22]). Después de las 6 semanas, estas gotas óticas se utilizaron algo más en el grupo placebo: 21 (55%) en el grupo TMP-SMX y 26 (67%) en el grupo placebo (DT –12 [IC del 95% –34; 10]) las utilizaron entre las semanas 6 y 12. Entre las 12 semanas y el año, estas cifras fueron de 78% y 82% (DT –4 [IC del 95% –22; 14]), respectivamente. Los antibióticos sistémicos diferentes de la medicación del estudio (principalmente amoxicilina) se utilizaron en 4 (11%) niños del grupo TMP-SMX y en 7 (18%) del grupo placebo entre el momento de la inclusión y las 12 semanas (DT –7 [IC del 95% –23; 9]). Entre las 12 semanas y el año, estas cifras fueron de 23 (62%) y 18 (47%), respectivamente (DT 15 [IC del 95% –7; 37]); se utilizaron principalmente TMP-SMX y azitromicina. La cirugía ORL (inserción o extracción de tubos de timpanostomía [N = 13], amigdaloadenoidectomía [N = 7], timpanomastoidectomía y/o timpanoplastia [N = 5]) se realizó en un número similar de niños de ambos grupos entre las 12 semanas y el año: 13 (30%) en el grupo TMP-SMX y 11 (24%) en el grupo placebo (DT 6 [IC del 95% –12; 24]).
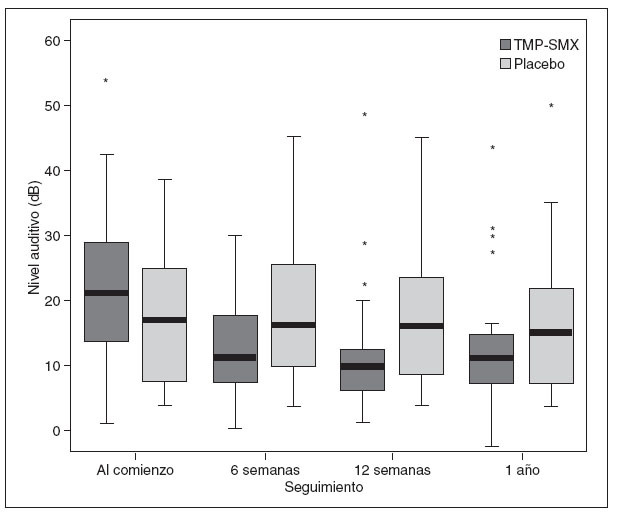
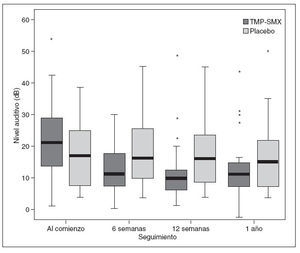
En la figura 2 se muestran diagramas de caja y patillas para los niveles auditivos de los niños mayores de 3 años. Se pudieron determinar los niveles de conducción aérea de tonos puros a 500, 1.000, 2.000 y 4.000 Hz en 20 niños del grupo TMP-SMX y 18 del grupo placebo. Aunque los niveles auditivos mejoraron generalmente, no se hallaron diferencias entre ambos grupos.
Fig. 2. Diagramas de caja y patillas22 del nivel medio de conducción aérea a 500, 1.000, 2.000 y 4.000 Hz al comienzo y a las 6 y 12 semanas y 1 año de seguimiento. Los valores se expresan en forma de mediana (línea horizontal de cada caja) y cuartiles (límites superior e inferior de cada caja); se excluyen los valores fuera del límite (*es decir, > 1,5 veces el rango intercuartílico más allá del cuartil). TMP-SMX: trimetoprim-sulfametoxazol.
Durante el estudio mejoraron sustancialmente las puntuaciones de la calidad de vida en relación con la salud en los dos grupos (datos no mostrados). Las puntuaciones medias de ambos grupos en las pruebas OM-6, CHQ y EAV fueron iguales en todas las visitas.
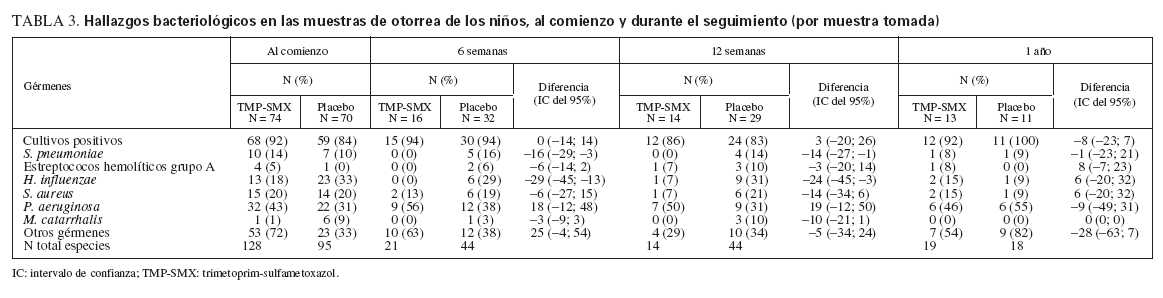
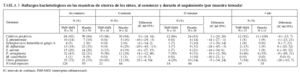
La tabla 3 muestra que a las 6 y 12 semanas y al año no había diferencia en las proporciones de cultivos positivos de muestras de otorrea entre uno y otro grupo: DT 0 (IC del 95% –14; 14) a las 6 semanas, DT 3 (IC del 95% –20; 26) a las 12 semanas, y DT –8 (IC del 95% –23; 7) al año. A las 6 y 12 semanas, Pseudomonas aeruginosa fue el germen aislado con más frecuencia en los dos grupos y, a diferencia de los demás gérmenes, se halló con mayor frecuencia en el grupo TMP-SMX que en el grupo placebo: 9 (56%) frente a 12 (38%) a las 6 semanas (DT 18 IC del 95% [–12; 48]) y 7 (50%) frente a 9 (31%) a las 12 semanas (DT 19 IC del 95% [–12; 50]), respectivamente. Al cabo de 1 año no se hallaron diferencias entre los dos grupos.
TABLA 3. Hallazgos bacteriológicos en las muestras de otorrea de los niños, al comienzo y durante el seguimiento (por muestra tomada)
Efectos adversosDurante las 6 primeras semanas se observaron vómitos
o diarrea, como efectos adversos potenciales de la medicación estudiada, en el 9% del grupo TMP-SMX y el 2% del grupo placebo (DT 7 IC del 95% [–2; 16]; número necesario para dañar [NND] 14). Entre las 6 y las 12 semanas no se hallaron diferencias entre los grupos. Un niño del grupo TMP-SMX desarrolló un exantema; se trató con cetirizina y se suspendió la medicación del estudio, tras lo cual desapareció el exantema. El tratamiento de la OMC se continuó con azitromicina. El hemograma completo y las pruebas funcionales hepáticas y renales al ingreso y a las 6 y 12 semanas no mostraron ninguna anomalía en ambos grupos. Dos niños desarrollaron una mastoiditis durante las 12 primeras semanas, e inmediatamente se abrió el código de tratamiento. Uno de ellos había recibido TMP-SMX; se trató con mastoidectomía y amoxicilina-ácido clavulánico IV durante 7 días, y oral durante 14 días. El otro niño se había incluido en el grupo placebo; se trató con amoxicilina-ácido clavulánico IV durante 7 días, y luego con TMP-SMX durante 6 semanas. Los dos niños se recuperaron bien con esta pauta.
DISCUSIÓNEl presente estudio es el primer ensayo de distribución aleatoria, controlado con placebo, de un tratamiento antibiótico sistémico en pacientes con OMC. En el mismo se observa que, con una tanda de 6 a 12 semanas con altas dosis de TMP-SMX, además de una tanda breve de gotas óticas con esteroide y antibiótico, se logró una tasa de curaciones del 68% a las 12 semanas y fue clínicamente más eficaz que el placebo en niños con OMC en quienes había fracasado el tratamiento convencional con medicamentos tópicos o antibióticos sistémicos a corto plazo. El efecto del tratamiento fue más pronunciado durante las 6 primeras semanas. Los niños con una historia de otorrea durante más de 6 meses se beneficiaron más del tratamiento con TMP-SMX que aquellos otros cuya historia de otorrea era más breve. La edad no influyó en la eficacia del TMP-SMX. Los niveles auditivos de tonos puros y la calidad de vida en relación con la salud mejoraron durante el estudio, pero no difirieron entre ambos grupos.
El efecto del tratamiento con TMP-SMX en la OMC se ha estudiado en un ensayo anterior: una tanda de 2 semanas de TMP-SMX se comparó con una tanda de antibióticos basada en los resultados de los cultivos9. Después de un período máximo de sólo 14 días de seguimiento, la otorrea se resolvió en el 75% del grupo TMP-SMX y en el 85% del grupo tratado con antibióticos según el cultivo. En otros estudios con diversos antibióticos sistémicos para la OMC se hallaron unos porcentajes similares de éxitos, aproximadamente del 10%10-14,16. Los criterios de inclusión y de los parámetros valorados, la vía de administración de los fármacos y el seguimiento variaron considerablemente entre estos estudios, y ninguno de ellos se controló con un placebo2.
Nuestros resultados deben interpretarse a la luz de varias limitaciones. En primer lugar, los niños presentaban síntomas persistentes de OMC a pesar del tratamiento convencional con medicación tópica, tandas breves de antibióticos sistémicos y/o cirugía ótica previa. Dado que la mayoría de los casos de otorrea que acuden a un médico general responde bien al tratamiento convencional, nuestros resultados deben aplicarse a los pacientes con OMC complicada de un modo similar.
En segundo lugar, dado que en Holanda se sigue una política restrictiva en cuanto al tratamiento antibiótico sistémico para la otitis media, es posible que antes de ingresar en el estudio los participantes hubieran recibido menos antibióticos sistémicos y más antibióticos tópicos, en comparación con lo que sería de esperar en otros países. Sin embargo, un meta-análisis efectuado por Macfadyen et al16 mostró que los antibióticos tópicos, como los utilizados por nuestros participantes antes de incluirlos en el estudio, eran más eficaces que las tandas breves de antibióticos sistémicos para resolver la otorrea. Por lo tanto, creemos que nuestros resultados pueden extrapolarse también a los países que utilizan con más frecuencia tandas breves de antibióticos sistémicos en el tratamiento de la OMC.
En tercer lugar, en todos nuestros pacientes con otorrea se practicó una aspiración de limpieza y se aplicó un tratamiento tópico, además de la medicación del estudio. Las gotas óticas antibióticas se utilizaron con una frecuencia ligeramente mayor en el grupo placebo que en el grupo TMP-SMX entre las 6 y 12 semanas. Ello podría haber influido en la alta tasa de curaciones observada en el grupo placebo a las 12 semanas y, por lo tanto, se podría haber subestimado el efecto real del tratamiento con TMP-SMX. Otros factores importantes para el escaso efecto del tratamiento en la tanda más prolongada pueden haber sido el curso natural de la OMC y la regresión a la media.
En cuarto lugar, a las 12 semanas se informó a los padres y al otorrinolaringólogo o pediatra locales sobre el tratamiento asignado, y los médicos podían tratar los síntomas ulteriores de OMC siguiendo nuestros consejos, con una tanda de 6 semanas de antibióticos, o según su criterio habitual. Nuestros datos de seguimiento revelaron que 10 niños del grupo placebo y 7 del grupo TMPSMX requirieron de hecho una tanda prolongada de antibióticos después de las 12 semanas. Ello podría haber contribuido a diluir el efecto después de dicho período.
En quinto lugar, la elección de TMP-SMX en la OMC podría cuestionarse, dado que Pseudomonas aeruginosa, que es el germen más común en la OMC y se hallaba presente en el momento inicial en 54 (38%) de las muestras de otorrea, es resistente al TMP-SMX. Ello se reflejó en los resultados de nuestros cultivos durante el tratamiento con TMP-SMX, pues no cambió la proporción de cultivos positivos a P. aeruginosa, mientras que disminuyó la proporción de gérmenes que no son intrínsecamente resistentes al TMP-SMX, como Haemophilus influenzae y Streptococcus pneumoniae. Dado que el TMP-SMX fue eficaz durante las primeras 6 a 12 semanas, P. aeruginosa parece ser un microorganismo secundario en la OMC, en vez de ser un germen causal.
CONCLUSIONESEn conclusión, una tanda de 6 a 12 semanas con altas dosis de trimetoprim-sulfametoxazol por vía oral es beneficiosa en los niños con otitis media crónica activa. El efecto del tratamiento es más pronunciado con la tanda más corta y desaparece si se suspende la medicación.
AGRADECIMIENTOSDamos las gracias a A. McArthur-Noom por los exámenes microbiológicos practicados, y a P.M. van Eden por su concienzuda labor de secretaría.
Ayuda económica: el estudio fue subvencionado con una beca del Health Care Insurance Council, Holanda (proyecto 01235).
Correspondencia: Erwin L. van der Veen, MD, Department of Otorhinolaryngology (KE04.140.5), Wilhelmina Children’s Hospital, University Medical Center Utrecht, PO Box 85090, 3508 AB Utrecht, Holanda.
Correo electrónico: e.l.vanderveen@umcutrecht.nl