Ziconotida es un nuevo fármaco no opioide indicado para el tratamiento del dolor crónico grave. Se trata de un péptido extraído de una toxina paralizante que produce el caracol acuáticoConus magus, que habita en el mar de las islas filipinas. Este conopéptido tiene la propiedad de bloquear de forma selectiva los canales del calcio tipo N, mecanismo al que se debe su actividad analgésica
El dolor es difícil de medir y se define como crónico si supera los seis meses de duración. En la actualidad afecta a uno de cada cinco adultos en Europa, pero tradicionalmente se ha diagnosticado y tratado de manera insuficiente. Su etiología es muy diversa: artritis, fracaso de la cirugía vertebral, lesiones, cáncer, sida, etc.
La base del tratamiento del dolor crónico son los opiáceos como la morfina por vía oral, sistémica o intratecal, pero un porcentaje significativo de pacientes no responde de un modo eficaz o experimenta efectos adversos graves. Este tipo de dolor afecta de un modo importante a la calidad de vida del paciente y de su familia.
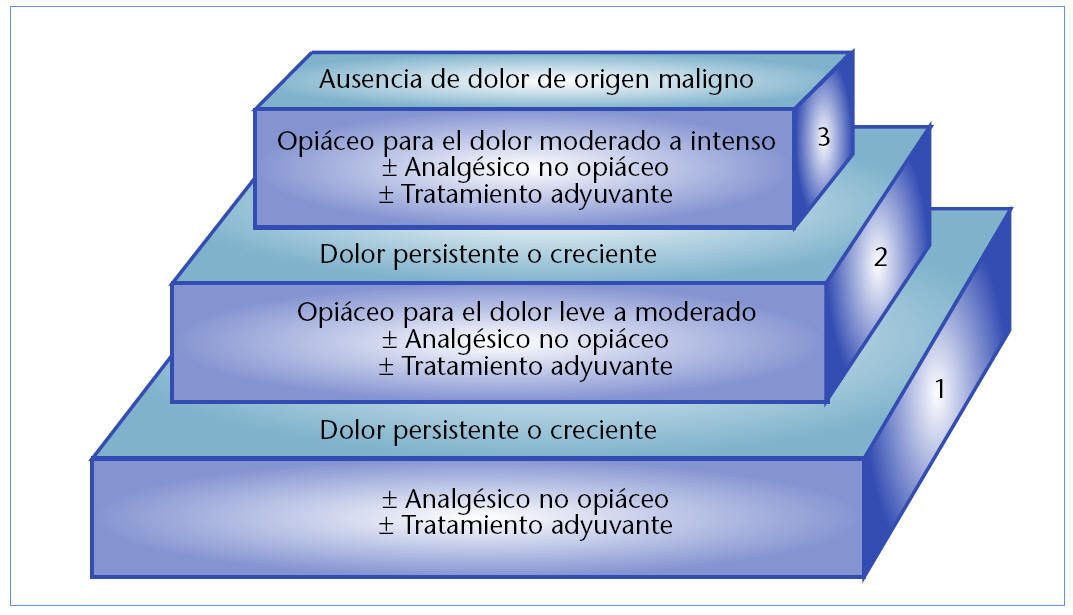
La Organización Mundial de la Salud (OMS) ha desarrollado una «escalera analgésica» de tres peldaños con recomendaciones para su tratamiento farmacológico (fig. 1). Los pacientes con dolor crónico intenso suelen avanzar al nivel 3, a menudo utilizando una combinación de opiáceos, analgésicos no opiáceos y tratamientos adyuvantes para aliviar el dolor.
Fig. 1. Escalera de la Organización Mundial de la Salud para el alivio del dolor.
La mayoría de los pacientes responde a la terapia convencional, pero una minoría no obtiene una analgesia satisfactoria o padece efectos secundarios importantes. Estos pueden beneficiarse de técnicas alternativas, como es el tratamiento intratecal (IT). Los candidatos a este tratamiento deben cumplir los siguientes criterios:
• No haber respondido a tratamientos conservadores.
• No haber podido conseguir un balance favorable entre la analgesia y los efectos secundarios del tratamiento con opiáceos orales.
• Haber superado una evaluación multifactorial para el tratamiento IT.
La disponibilidad de un tratamiento analgésico no opiáceo intratecal representa una opción terapéutica importante para algunos pacientes.
Ziconotida
Aproximadamente 500 especies de caracoles del género conos viven en los océanos tropicales de las islas filipinas. En una variedad, Conus magus, se halló un péptido presente en sus toxinas que demostró la capacidad de bloquear los canales del calcio de tipo N. Nuevos estudios condujeron al desarrollo de la ziconotida, la forma sintética de este conopéptido.
Mecanismo de acción
Ziconotida está considerado un tipo diferente de antagonista del calcio y, por tanto, un analgésico no opiáceo diferente. Es el primer antagonista de los canales del calcio de tipo N para uso intratecal en el dolor crónico intenso.
Los canales de calcio de tipo N se expresan densamente en las terminaciones nerviosas sensoriales en las láminas medulares I y II (láminas superficiales del asta dorsal). Allí modulan la entrada de calcio inducida por la despolarización necesaria para la liberación de los neurotransmisores desde las terminaciones aferentes nociceptivas primarias. Los resultados en animales indican que la ziconotida ejerce sus efectos analgésicos por medio del bloqueo directo de los canales del calcio de tipo N presinápticos. Inhibe la transmisión de las señales del dolor desde las neuronas aferentes a las neuronas del asta dorsal de la médula espinal. Todavía no se ha determinado el mecanismo de acción de la ziconotida en el ser humano.
La acción de unión de ziconotida es diferente a la de los opiáceos. A diferencia de los analgésicos opiáceos, como la morfina, que se unen a los receptores mu, delta o kappa, la ziconotida no se une a los receptores para opiáceos y sus efectos farmacológicos no son bloqueados por los antagonistas de los opiáceos.
El dolor agudo o dolor nociceptivo (somático) responde a los analgésicos tradicionales (AINE y opiáceos) y responde menos a los adyuvantes analgésicos, como son los antidepresivos tricíclicos y los fármacos antiepilépticos, que han demostrado tener un efecto beneficioso para el tratamiento del dolor crónico.
Se cree que el dolor crónico representa una sensibilización central, un proceso mediante el cual las terminaciones aferentes primarias se hacen más sensibles a los estímulos nociceptivos (hiperalgesia) o producen una respuesta nociceptiva a estímulos normalmente no nociceptivos (alodinia). Los datos no clínicos indican que la supresión de la sensibilización central interviene en el alivio del dolor crónico resistente al tratamiento.
Farmacodinamia
Los resultados de estudios clínicos en modelos animales y humanos demuestran que la ziconotida es un fármaco eficaz, no se une a los receptores opioides y sus efectos farmacológicos no son bloqueados por los antagonistas de los opiáceos.
A diferencia de la morfina, la ziconotida tiene un efecto antonociceptivo uniforme en la neuropatía periférica dolorosa y no produce tolerancia cuando se administran crónicamente dosis analgésicas.
Farmacocinética
La farmacocinética de la ziconotida se ha estudiado en el líquido cefalorraquídeo y sus características farmacocinéticas son predecibles y homogéneas. La eliminación tiene lugar por flujo masivo de LCR y las cantidades detectadas en el plasma se degradan con rapidez.
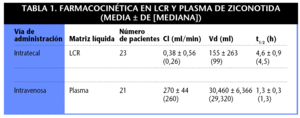
Se han estudiado las propiedades farmacocinéticas de la ziconotida en LCR tras infusiones IT de una h de 1-10 microgramos de ziconotida en pacientes con dolor crónico. También se estudió la farmacocinética en plasma tras dosis intravenosas de de 0,3-10 microgramos/kg/24 h (tabla 1)
Tras la administración IT durante una h, los valores de la exposición acumulada y de la exposición máxima fueron variables y dependientes de la dosis. Las concentraciones plasmáticas tras la infusión continua parecen ser relativamente bajas y, por lo general, indetectables (cerca del 80% de las muestras de plasma recogidas de pacientes con dolor no contienen cantidades cuantificables de ziconotida). No se ha observado acumulación de ziconotida en plasma tras la administración IT a largo plazo.
La mediana del volumen de distribución de ziconotida en el LCR se sitúa entre el volumen de LCR en la médula espinal y el volumen total de LCR. Al parecer, la ziconotida se distribuye principalmente en el LCR hasta el paso a la circulación general. Una vez en ella, parece que experimenta una distribución más extensa según el volumen de distribución plasmática de unos 30 l y solo presenta una unión inespecífica a las proteínas plasmáticas del 53%.
La ziconotida es un péptido formado por 25 aminoácidos y no parece experimentar un metabolismo apreciable en LCR. Cuando pasa a la circulación general tiene lugar una escisión proteolítica por varias peptidasas/ptoteasas y será degradada a fragmentos peptídicos y aminoácidos libres cuya actividad biológica no es significativa.
La eliminación de ziconotida del LCR se realiza principalmente por flujo masivo del LCR hacia fuera del SNC a través de las vellosidades aracnoideas con el paso posterior a la circulación general. La vida media de eliminación plasmática es de 1,3 h.
Tras la infusión intravenosa sólo se recuperan en la orina cantidades mínimas de ziconotida.