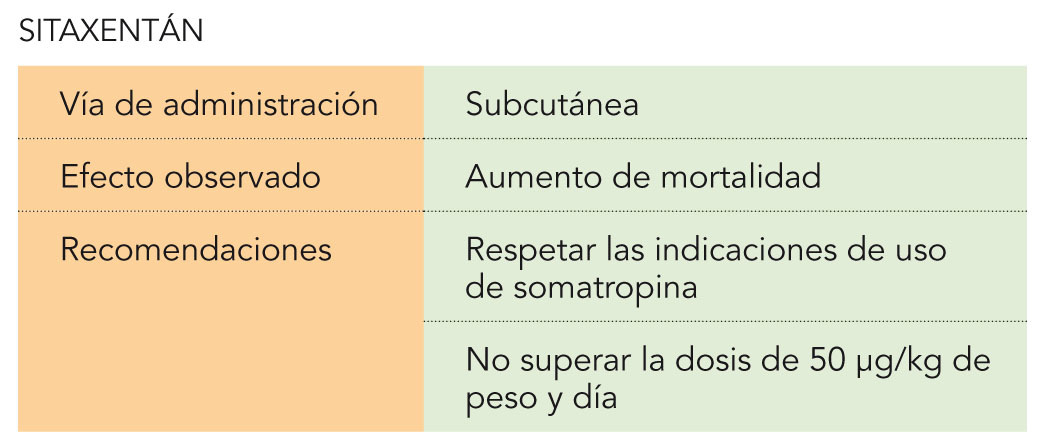
La somatropina es la hormona del crecimiento humana obtenida por tecnología de ADN recombinante. Actúa como agente anabólico y anticatabólico, estimulando el crecimiento de los huesos largos e incrementando el número y tamaño de las células musculares en niños con deficiencia en hormona del crecimiento. Con ello, se consigue un aumento de la talla final del paciente.
Está indicado en adultos con déficit de la hormona de crecimiento, en niños con síndrome de Prader Willi o en el retraso en el crecimiento de niños y adolescentes asociado a déficit de hormona de crecimiento congénita, genética, adquirida o idiopática, síndrome de Turner o insuficiencia renal crónica.
Recientemente se ha llevado a cabo un estudio epidemiológico en Francia, denominado Santé Adulte GH Enfant (SAG-hE) diseñado para mejorar el conocimiento sobre la hormona de crecimiento recombinante y la evaluación de la salud de los jóvenes tratados en la infancia con los fármacos que contienen esta hormona.
El estudio a largo plazo, que se inició en octubre del 2004, identificó a 10.000 tratados con la hormona del crecimiento entre 1985 y 1996, de los cuales se pudo cubrir en el estudio a alrededor de 7.000.
La FDA y la EMA informaron al público de que los resultados preliminares del estudio francés señalan que los pacientes con cierto tipo de enfermedades asociadas con baja estatura (deficiencia de la hormona de crecimiento y baja estatura gestacional idiopáticas) que fueron tratados con GH durante su infancia y se les hizo seguimiento durante un período largo tuvieron un riesgo incrementado de muerte cuando se compararon con individuos de la población general francesa.
Sin embargo, ninguna de las dos agencias define la magnitud del incremento en el riesgo. Ambas agencias, en la actualidad, no han considerado necesario tomar medidas regulatorias pero han comenzado una revisión del balance riesgo/ beneficio del producto.
La AEMPS informa de que, en tanto no concluya el proceso de evaluación iniciado, los prescriptores deberán seguir las indicaciones terapéuticas y dosis que han sido autorizadas para estos medicamentos. Se recuerda que la dosis máxima de somatropina es de 50 μg/kg de peso y día y no debe superarse.
Por su parte, la FDA, con los datos disponibles hoy día, cree justificada la relación beneficio-riesgo de dicha medicación.
BIBLIOGRAFÍA GENERAL
Ficha técnica de somatropina. Disponible en https://sinaem4.agemed.es/consaem/especialidad.do?metodo=verFichaWordPdf&codigo=70642&formato=pdf&formulario=FICHAS
Medwatch, FDA Recombinant Human Growth Hormone (somatropin): Ongoing Safety Review - Possible Increased Risk of Death. Disponible en http://www.fda.gov/Safety/MedWatch/SafetyInformation/SafetyAlertsforHumanMedicalProducts/ucm237969.htm
Nota informativa de la Agencia Española del Medicamento: inicio de la evaluación en Europa del perfil de seguridad de somatropina ref MUH (FV)/17/2010. Disponible en www.agemed.es