Metabolismo y acción biológica
Los polifenoles son unos componentes químicos que están presentes en muchos productos naturales. Recientemente se ha sistematizado parte del estudio de estos compuestos y se han analizado sus aspectos positivos y negativos. Los autores ponen de manifiesto en este trabajo las características de los polifenoles, con especial atención a su metabolismo, su acción biológica y su aplicación en farmacia.
Los polifenoles son los componentes químicos mayoritarios de un grupo de plantas naturales de uso habitual, como el café, el té, el mate o el cacao, y de bebidas de gran consumo, como el vino. Simultáneamente, asociado a su consumo, se detecta un aumento de la capacidad antioxidante en el organismo, lo que induce a un grupo numeroso de investigadores a estudiar su papel en el proceso antienvejecimiento.
Pretendemos poner de manifiesto, junto al conocimiento de sus estructuras, su interés en farmacia, así como las líneas de investigación abiertas en torno a ellos.
De modo especial nos centraremos en los flavonoides, tanto por su extensión (más de 4.000 sustancias), como por la cantidad de procesos en los que pueden intervenir.
Flavonoides
Entre las sustancias de carácter fenólico, los que han sido objeto de estudios más profundos son los flavonoides. Comprenden un gran grupo de metabolitos secundarios que derivan de subunidades que provienen de las rutas metabólicas del acetato y del shikimato. Se encuentran casi exclusivamente en plantas superiores, y se presentan de dos modos muy característicos: enlazados a unidades glucídicas (flavonoides glucósidos), o libres (flavonoides agliconas), como es el caso de las flavanonas (catequinas y proantocianidinas).
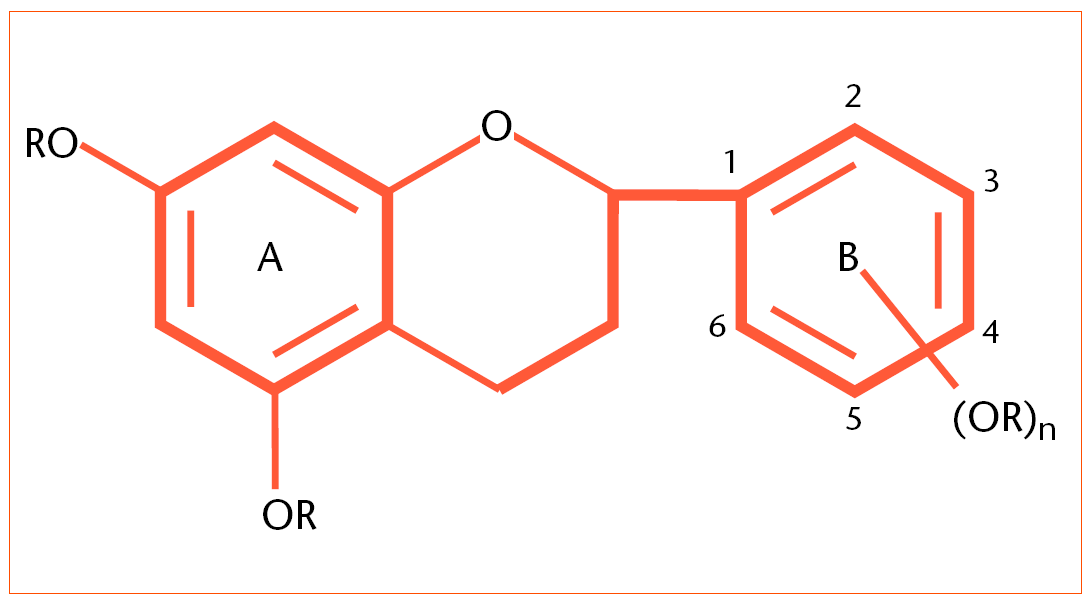
Invariablemente, tienen una unidad C15, como se muestra en la figura 1; la subunidad ArC3 (anillo B) deriva del shikimato y el otro anillo aromático A proviene de un policétido.
Fig. 1. Fórmula estructural de los flavonoides.
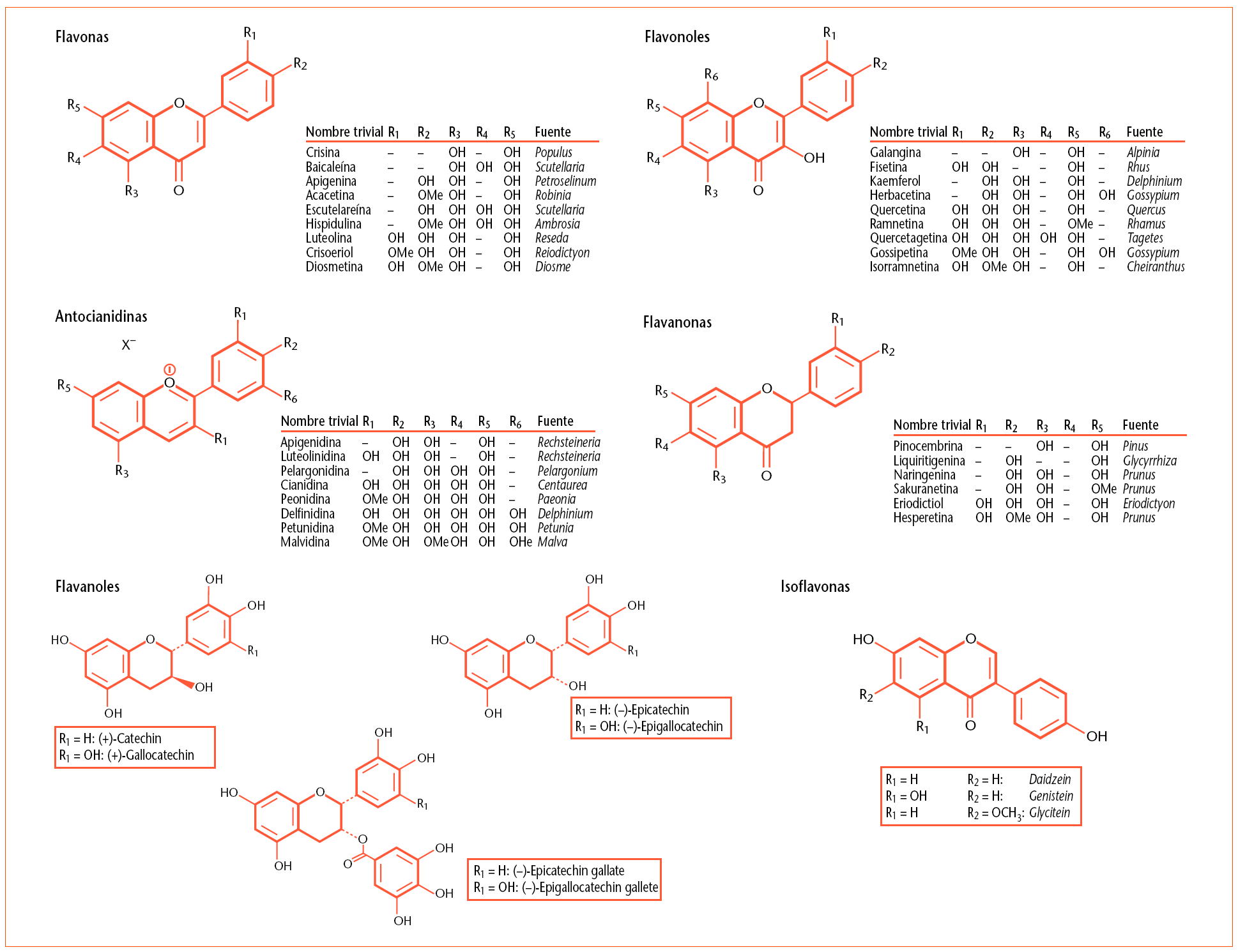
El anillo A tiene, normalmente, dos grupos alcóxidos (en posición relativa meta) y el anillo B puede presentar grupos 4-hidroxi, 3,4-dihidroxi o 3,4,5-trihidroxi (en posición relativa para y orto). Además, la posterior oxidación, reducción y alquiler de este esqueleto básico origina estructuras adicionales. La fenilalanina (y no la tirosina) es precursora de la subunidad p-cumarilo, que se condensa con tres unidades C2 (malonilcoenzima A) para dar chalconas en un proceso catalizado por la chalconasintetasa. A partir de las chalconas se forman casi todos los demás derivados, flavononas mediante la chalconaisomerasa, flavononoles, flavonoles, antocianinas y flavonas (fig. 2).
Fig. 2. Derivados de los flavonoides.
El procedimiento biogenético se podría describir como:
* Paso 1. Condensación tipo Claisen.
* Paso 2. Formación de un anillo aromático previa reacción de un metileno activado sobre el grupo carbonilo de un éster como en el paso 1 y aromatización.
* Paso 3. Ataque de un anión fenóxido a un doble enlace y formación de una benzo-2,3-dihidropirona-4 o flavona.
* Paso 4. Reacción de hidroxilación en el carbono 3.
* Pasos 5 y 6. Flavanonoles a flavonoles y después a antocianinas. Oxidaciones sucesivas de una 2,3-dihidropirona-4 a sal de pirilio.
* Paso 7. Flavononas a Flavonas. Reacción de oxidación.
* Todos los pasos estarían catalizados por la enzima correspondiente.
Nomenclatura y tipos
Los flavonoides se clasifican en varias clases, de acuerdo con las variantes estructurales que presenta la cadena central C3. La mayoría de agliconas flavonoides tienen nombres triviales con la terminación INA u OL. La quercetina es un flavonol y corresponde al 5,7,3',4'-tetrahidroxiflavonol. La naringenina es una flavanona y corresponde a la 5,7,4'-trihidroxiflavanona.
En el caso de los glicósidos flavonoides, es muy común nombrarlos con relación al nombre trivial de la aglicona. Por ejemplo, la apigenina corresponde a la 5,7,4'-trihidroxiflavona y la vitexina corresponde al 8-C-D-glucopiranósido de apigenina.
Acción biológica
Desde hace muchos años se les han reconocido a los polifenoles una serie de acciones beneficiosas para la salud. Tal es el caso de la citrina, que fue el primer flavonoide al que se le atribuyó una actividad biológica bien definida sobre la permeabilidad vascular, recibiendo por ello el nombre de vitamina P. La citrina es una mezcla de glucósidos flavonoides, principalmente quercetina, rutina, hesperidina y eriodictina.
Acción antioxidante
Dentro de esta acción, destaca su capacidad protectora sobre las proteínas LDL. Entre los detalles estructurales que pueden refrendar su potencial antioxidante podemos destacar la presencia y localización de dobles enlaces, y los propios grupos fenólicos, que según su número y posición pueden actuar como dadores de protones y reductores, además de ser capaces de establecer puentes de hidrógeno. De esta manera, se puede explicar su pluralidad de acciones, ya sea como antioxidantes primarios antirradicalarios o como sustancias reductoras, como agentes sinérgicos, o como quelantes de metales de transición.
Acción quelante
Los iones, de metales como hierro y cobre, pueden catalizar la producción de radicales libres. La capacidad quelante de los flavonoides sobre ellos parece contribuir a su actividad antioxidante in vitro. En organismos vivos, la mayoría del hierro y el cobre están enlazados a las proteínas, limitando su participación en las reacciones que producen radicales libres. Aunque las actividades metalquelantes de los flavonoides pueden ser beneficiosas en condiciones patológicas de exceso de hierro o de cobre, los estudios realizados hasta ahora no detallan aún la incidencia de los flavonoides como quelantes eficaces in vivo.
Efectos sobre el sistema de señalización celular
Estas vías regulan numerosos procesos en la célula, incluyendo el crecimiento, la proliferación y la muerte celular (apoptosis). Incluyen a los receptores de membrana (de superficie e intracelulares), las proteínas cinasas y las proteínas fosfatasas.
Muchos de los efectos biológicos de los flavonoides están relacionados con su capacidad de modular estas vías. Las concentraciones intracelulares de los flavonoides, requeridas para afectar a las vías celulares, son considerablemente más bajas que las necesarias para modular la capacidad antioxidante en la célula. Los flavonoides pueden alterar el factor de crecimiento en la señalización, inhibiendo la fosforilación del receptor o bloqueando su enlace. También se les asocia cierta capacidad inhibitoria sobre las proteínas cinasas.
Acción termogénica
Un estudio de Dullo et al ha demostrado la eficacia del extracto de té verde, rico en polifenoles y cafeína, que incrementa el gasto energético y la oxidación grasa en humanos. El estudio se realizó en tres grupos de pacientes sanos, con placebo, cafeína y té verde, valorando durante 24 h el gasto energético, cociente respiratorio y oxidación metabólica de grasas, hidratos de carbono y proteínas. Se demostró que el té verde tiene propiedades termogénicas y promotoras de la oxidación de grasas superiores a las de la cafeína sola, a través de un mecanismo de acción que haría prolongar la vida de la noradrenalina (al inhibir el efecto de la enzima que la degrada: la catecol-ortometiltransferasa [COMT]) entre otras acciones, con un mínimo efecto cardiovascular.
Acción mutagénica y cancerígena
En los polifenoles con estructuras derivadas del flavonol, como la quercetina, la miricetina y el camferol, han dado resultados positivos de mutageneidad con el test de Ames (desarrollado sobre Salmonella typhymurium). Para esta actividad mutagénica, parece esencial que el flavonoide disponga en su estructura de un doble enlace en posición 2,3 y de un hidroxilo en la posición 3.
En cambio, para la actividad cancerígena se han implicado sus intermediarios quinónicos, capaces de formar aductos con el ADN. Por su carácter electrófilo, estas quinonas son muy reactivas y pueden participar en el ciclo de producción de los radicales superóxidos y peróxidos, lo que explicaría sus propiedades mutagénicas y cancerígenas. No obstante, está descrita la fuerte incidencia de tumores digestivos que ha sido relacionada con estos compuestos, lo que parece estar relacionado también con la actividad de la población microbiana intestinal, que es muy activa en la metabolización de los flavonoides.
Acción anticáncerígena
La acción anticancerígena de los flavonoides destacaría a través de cinco procesos:
* Estimulación de la desintoxicación enzimática de la fase II. Los flavonoides serían agonistas de las enzimas de desintoxicación de la fase II que catalizan las reacciones que promueven la excreción de productos químicos potencialmente tóxicos o carcinógenos.
* Preservación de la regulación normal del ciclo celular. Activando los caminos que conduce a la muerte de la célula (apoptosis) si el daño en la replicación del ADN ha sido irremediable.
* Inhibición de la proliferación y activación de la apoptosis.
* Inhibición de la invasión del tumor y de la angiogénesis. Los tumores invasores deben desarrollarse en los vasos sanguíneos nuevos por un proceso conocido como angiogénesis para aprovisionarse de nutrientes en su rápido crecimiento. Los flavonoides evitarían que las células cancerosas invadan el tejido normal (proceso conducido por las enzimas llamadas metaloproteinasas).
* Disminución de la inflamación. Ésta puede dar lugar a una producción local y creciente de radicales libres por las enzimas inflamatorias, así como el lanzamiento de los mediadores que promueven la proliferación y la angiogénesis de la célula, y que simultáneamente inhiben la apoptosis.
Actuaciones específicas de los polifenoles
Los flavonoides se han aislado de muchas drogas vegetales debido a que son productos naturales muy comunes. A sus polifenoles se les ha atribuido una cantidad de acciones que van desde actividades inhibidoras de enzimas (hidrolasas, ciclooxigenasas, fosfatasa alcalina, cAMP fosfodiesterasas, ATP-asas, liasas, hidroxilasas, transferasas, oxidorreductasas y cinasas), hasta acción antiinflamatoria, anticancerígena, antibacteriana y antiviral.
Hay algunas evidencias de que los consumidores de vinos tintos presentan baja mortalidad por enfermedad coronaria, y que ello se debe, al parecer, a sus compuestos fenólicos, entre los que están flavonoides catequina, epicatequina y quercetina
Los taninos presentes en las habas, plátanos, cacao, etc., se caracterizan por combinarse con las proteínas e interferir en su posterior utilización digestiva, sobre todo cuando se oxidan y pasan de estructuras polifenólicas a las de quinonas.
La crisina se encuentra en el álamo (Populus sp.) y en la cereza salvaje (Prunus sp.), la apigenina en el perejil, el kaemferol en el sen, y la liquiritigenina en el regaliz. La rutina presente en la cáscara de los cítricos fue alguna vez considerada como vitamina P, pero actualmente no se le reconoce como tal. Su uso para el tratamiento de la fragilidad capilar es motivo de controversia, pero sin embargo se utiliza para el tratamiento de la hipertensión y en geriatría.
Las flores de saúco (Sambucus niger), usadas para el tratamiento de resfriados, gripe y reumatismo, contienen varios glicósidos flavonoides. Una cantidad de isoflavonas (derivados de la 3-fenil-cromona), poseen actividad estrogénica y producen esterilidad en las ovejas que consumen trébol. La silibina y la silimarina son flavolignanos constituyentes del cardosanto (Silybum marianum), que se utiliza mucho en Alemania como hepatoprotector. Algunos dímeros flavonoides (biflavonoides), como el diinsininol, tienen acción antiinflamatoria. La quercetina y la rutina tienen efectos anticancerígenos potenciales. También hay algunas evidencias de que los consumidores de vinos tintos presentan baja mortalidad por enfermedad coronaria, y que ello se debe, al parecer, a sus compuestos fenólicos, entre los que están flavonoides catequina, epicatequina y quercetina. Las procianidinas presentes en las uvas tienen uso potencial en isquemias cardíacas.
También se han descrito flavonoides que inhiben la agregación plaquetaria, con acción vasodilatadora (naringenina, eriodictyol y luteolina), con acción antiarrítmica, chalconas, así como con acción antimicótica y antibacteriana. La 3-ramnosilquercetina presenta actividad antidiarreica, y otras isoflavanquinonas poseen potente actividad antiinflamatoria y antialérgica. Hay flavonoles con actividad antiespasmolítica, mientras que isoflavonas y flavanonas poseen propiedades antimicóticas. Hay isoflavanos antimicrobianos y flavanos con actividad leishmanicida. Las antocianinas, por sus características, se han sugerido como colorantes de alimentos. Además, se ha descrito el uso potencial de ciertos flavonoides en cosméticos.
Metabolismo
La mayoría de flavonoides se degradan en condiciones alcalinas fuertes (como por ejemplo, en el tracto gastrointestinal), y se rompen por el anillo C (enlace éster).
Incluso después de cocinarse, la mayoría de los glucósidos y agliconas flavonoides alcanzan el intestino delgado intactos, donde se metabolizan rápidamente a la forma metilada, glucoronizada o sulfatada de los metabolitos. Los flavonoides que alcanzan el colon pueden metabolizarse más a fondo por las enzimas de la flora bacteriana que ahí coloniza, favoreciendo su absorción.
En general, su biodisponibilidad es relativamente baja debido a su limitada absorción y a su rápida eliminación. Además, los flavonoides se metabolizan rápida y extensamente, aunque su actividad biológica no es siempre igual a la del compuesto precursor.
En seres humanos, las concentraciones máximas en plasma de las isoflavonas de la soja y de los flavanones de cítricos no han sido superiores a 10 µmol/l después de su consumo oral, mientras que las obtenidas tras la ingestión de antocianinas, flavanoles y flavonoles (incluyendo los del té) han sido generalmente inferiores a un µmol/l.
Todas las clases de flavonoides experimentan un metabolismo extenso en el yeyuno y el íleon del intestino delgado y entran en la vena porta, donde tienen un metabolismo adicional en el hígado. La microflora que coloniza el colon degrada los flavonoides a ácidos fenólicos más pequeños, que también serían absorbidos. El destino de la mayoría de estos metabolitos será la excreción renal. Sin embargo, el grado en el que estos compuestos entran en las células y en los tejidos aún está por descubrirse.
Bibliografía general
Alena F, Jimbow K, Ito S. Melanocytotoxicity and antimelanoma effects of phenolic amine compounds in mice in vivo. Cancer Res. 1990;50:3743-7.
Bae EA, Han MJ, Kim DH. Planta Med. 1999;65(5):442-3.
Ballesteros P, Claramunt RM. Química orgánica avanzada. Madrid: UNED; 2001.
Bello J. Ciencia de la bromatología. Madrid: Díaz de Santos; 2000.
Beltrán I. Polifnoles y xantinas: su aplicación en obesidad. Actividad Dietética. 2003;19:10-6.
Buciumeanu E, Grecu C, Bejan C. La teneur en polyphènols chez les vignestteintes des maladies virales. Polyphènols Actualités. 1994;11:69.
Capasso R. Biotechnology and ecotoxicology of the polyphenols naturally occurring in vegetable wastes. Current Topics in Phytochemistry. 1997;1:145-56.
Díaz J, Fernández MT, Paredes F. Aspectos básicos de bioquímica clínica. Madrid: Díaz de Santos; 1996.
Dullo AG, et al. American Journal Clinical Nutrition. 1999;70:1040-5.
Frankel EN, Waterhouse AL, Teissedre PL. Principal phenolic phytochemicals in selected California wines and their antioxidant activity in inhibiting oxidation of human low-density lipoproteins. J Agric Food Chem. 1995;43:890-4.
Fuhrman B, Aviram M. Flavonoids protect LDL from oxidation and attenuate atherosclerosis. Curr Opin Lipidol. 2001;12:41-8.
Fuhrman B, Lavy A, Aviram M. Consumption of red wine with meals reduces the susceptibility of human plasma and low-density lipoprotein to lipid peroxidation. Am J Clin Nutr. 1995;61:549-54.
Ghiselli A, Nardini M, Baldi A, Scaccini C. antioxidant activity of different phenolic fractions separated from an Italian red wine. J Agric Food Chem. 1998;46:361-7.
Hernández M, Prieto EA. Plantas que contienen polifenoles. Antioxidantes dentro del estilo de vida. Rev Cubana Invest Biomed. 1999;18(1):12-4.
Marimon JM, Bujanda L, Gutiérrez Stampa MA, et al. Am J Gastroenterol. 1998;93(8):1392.
Masquelier J. La vigne, plante médicinale, naissance et essor d'une thérapeutique. Bull de l'Oiv. 1992;65:177-96.
Mitjavila S, Fernández Y. Les polyphenos dans la protection contre l'agression oxydante. II Simposio Internacional Uva, Vino y Salud. Buenos Aires, 1991.
Nigdikar SV, Williams NR, Griffin BA, Howard AN. Consumption of red wine polyphenols reduces the susceptibility of low-density lipoproteins to oxidation in vivo. Am J Clin Nutr. 1998;68:258-65.
Rice-Evans CA, Miller NJ, Paganga G. Antioxidant properties of phenolic compounds. Trends in Plant Science. 1997;2:152-9.
Slowing K, Padilla E, Serrano C, et al. Efectos del vino y diversos polifenoles en cultivos celulares y reactividad vascular. Resúmenes del II Congreso de Fitoterapia.