A través de una declaración hecha pública en el congreso anual celebrado en Niza
La FIP respalda la formación continuada de los farmacéuticos
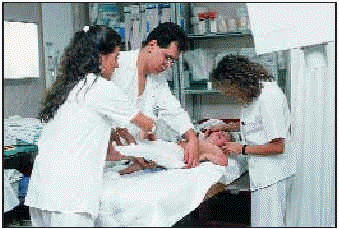
Entre los días 31 de agosto y 5 de septiembre se celebró en Niza (Francia) el LXII Congreso Internacional de la Federación Farmacéutica Internacional (FIP). La seguridad del paciente en el uso de medicamentos, el papel del farmacéutico en el uso racional del medicamento, las donaciones de fármacos y la atención farmacéutica han sido algunos de los temas más relevantes. Además, la FIP hizo pública una declaración de respaldo al desarrollo de la formación continuada en la profesión farmacéutica.
La representación española expuso en la FIP su experiencia en formación continuada farmacéutica.
Conscientes de que la formación continuada de los farmacéuticos es imprescindible para garantizar el mejor servicio al ciudadano, los dirigentes farmacéuticos reunidos en Niza aprobaron por unanimidad una Declaración sobre Estándares Profesionales en la Formación Continuada. «Mantener la competencia a lo largo de la carrera, en la cual se encontrarán nuevas y desafiantes responsabilidades profesionales, es un requisito ético fundamental para todos los profesionales sanitarios», dice la introducción de la declaración, que defiende que «el desarrollo profesional continuado debe ser un compromiso para todos los farmacéuticos en ejercicio durante toda su vida».
Precisamente, los planteamientos incluidos en esta declaración están recogidos en uno de los pósters que el Consejo General de COF de España presentó en el Congreso, que esquematizaba el papel a desempeñar por las organizaciones farmacéuticas nacionales en este campo. En 1997, el máximo órgano de representación de los farmacéuticos españoles puso en marcha el Plan Nacional de Formación Continuada, cuyos objetivos son, en buena parte, los que ahora se han marcado desde la FIP.
Junto al póster dedicado a la formación continuada, la representación de la farmacia española presentó otros tres pósters: el primero sobre Portalfarma, para trasladar a los farmacéuticos de otros países la experiencia de este portal entre la estructura colegial, los farmacéuticos y las empresas e instituciones del sector; el segundo para destacar el papel del farmacéutico como asesor en protección solar, y el tercero sobre la nueva Base de Datos del Conocimiento Sanitario, que para Capilla es «una herramienta imprescindible para el desarrollo definitivo de la atención farmacéutica en España».
Propuestas
En el consejo de clausura el presidente de la Organización Profesional de Farmacéuticos de Alemania (ABDA), Hans Gunter Friese, apoyado por el presidente del Consejo General de COF, Pedro Capilla, solicitaron que en el próximo congreso de la FIP se debata ampliamente el papel del farmacéutico en la sanidad y su relación con otros profesionales de la salud. Además, como consecuencia de la posible influencia de Internet en la profesión farmacéutica, pidieron que se perfile el papel actual del farmacéutico, así como el que desempeñará en un futuro.
La cita ha servido también para elegir al nuevo presidente de la FIP, el francés Jean Parrot, a su vez presidente de la Orden de Farmacéuticos de Francia. Como nueva vicepresidenta fue nombrada Linda Stone, del Reino Unido.
LA AEM podrá requerir a los laboratorios información sobre medicamentos que ya están en el mercado
Un nuevo real decreto regula la farmacovigilancia de medicamentos de uso humano
El Real Decreto 711/2002 de Farmacovigilancia aprobado desarrolla el Capítulo VI de la Ley del Medicamento e incorpora al ordenamiento jurídico nacional la Directiva 2000/38/CE de la Comisión sobre esta misma materia. La Agencia Española del Medicamento tendrá capacidad para solicitar en cualquier momento al titular de la autorización de comercialización de un producto un informe actualizado de evaluación de la relación beneficio/riesgo del producto.
A partir del nuevo real decreto se otorga un papel relevante al Comité de Seguridad de Medicamentos de Uso Humano, órgano consultivo de la Agencia Española del Medicamento (AEM).
La norma aprobada, que viene a definir las obligaciones de cada uno de los agentes implicados (administraciones sanitarias, industria farmacéutica y profesionales sanitarios), teniendo en cuenta la estructura administrativa del Estado y la pertenencia a la Unión Europea, deberá ser tomada como referencia por las comunidades autónomas para desarrollar una normativa específica que regule dichos estudios en su ámbito competencial.
En concordancia con lo previsto en la Ley del Medicamento, el real decreto dedica un capítulo al Sistema Español de Farmacovigilancia de medicamentos de uso humano, definido como «la estructura descentralizada bajo la que se integran las actividades que las Administraciones Sanitarias realizan para recoger y elaborar la información sobre reacciones adversas a los medicamentos (RAM) y que es coordinado por el Ministerio de Sanidad y Consumo, a través de la Agencia Española del Medicamento». De esta forma, se establecen las funciones atribuibles en esta materia, por un lado a la AEM y, por otro, a los órganos competentes en materia de farmacovigilancia de las comunidades autónomas. Asimismo, se definen las obligaciones de los laboratorios farmacéuticos titulares de una autorización de comercialización. A este respecto, el decreto establece que el titular debe notificar las sospechas de reacciones adversas graves de forma simultánea a la AEM y al órgano competente en materia de farmacovigilancia de la comunidad autónoma donde se haya producido la reacción. De igual forma, establece que «el titular queda obligado a incorporar al expediente de registro toda nueva información relevante para la seguridad de un medicamento». Todo ello al tiempo que se reitera el deber de los profesionales sanitarios de notificar toda sospecha de RAM a un paciente cuando tenga conocimiento de ella.
Seguridad y calidad
El subdirector general de Seguridad del Medicamento, Ramón Palop, ha explicado que «se trata de una iniciativa que permitirá a la industria colaborar con la Administración sanitaria a la hora de tener en el mercado medicamentos más seguros, más eficaces y de mejor calidad; al tiempo que reitera la obligación de los profesionales sanitarios de comunicar toda reacción adversa, independientemente de su gravedad, a través de la tarjeta amarilla». Según Palop, por primera vez se aborda en un texto normativo jurídico los estudios postautorización, para los que ya se había emitido una circular, y que deberán tener como finalidad «complementar la información obtenida durante el desarrollo clínico de los medicamentos previo a su autorización». En este sentido, el real decreto subraya que no se planificarán, realizarán o financiarán estudios postautorización con el objetivo de promover la prescripción de los medicamentos. La autorización de estos estudios, que serán evaluados por los comités de ética hospitalarios, se traslada a las comunidades autónomas, «a las que corresponderá establecer una fundamentación jurídica específica dentro de su ámbito territorial», añadió Palop.
M.ª Purificación Neira presidirá la Agencia Española de Seguridad Alimentaria
M.ª Purificación Neira González fue nombrada por real decreto, el pasado 30 de agosto, presidenta de la recientemente creada Agencia Española de Seguridad Alimentaria. Neira, hasta ese momento responsable del Departamento de Prevención, Control y Erradicación de Enfermedades Infecciosas de la OMS en Ginebra, es licenciada en Medicina y Cirugía por la Facultad de Oviedo y máster en Salud Pública por la Universidad Pierre y Marie Curie de París (Francia).
Entre otros cargos, la máxima responsable de la Agencia Española de Seguridad Alimentaria ha sido asistente médico en el Hospital Necker y Saint Louis de París, coordinadora médico de Médicos Sin Fronteras en Ruanda, directora en funciones del Hospital de Tete (Mozambique) y coordinadora del Grupo de Trabajo Mundial de la Lucha contra el Cólera y otras Enfermedades Epidémicas de la OMS.
El crecimiento acumulado del gasto farmacéutico de enero hasta julio es del 10,12%
El incremento del gasto farmacéutico en el primer semestre del año supera las previsiones del Gobierno
Según se desprende de una respuesta parlamentaria a la diputada de CiU Maria Zoila Riera, el crecimiento acumulado del gasto farmacéutico de enero hasta julio es del 10,12%, 6 décimas por encima de la tasa máxima aceptable para el conjunto del año que maneja el Gobierno.
El Gobierno confía en la moderación del incremento del gasto farmacéutico.
Según señalaron fuentes de la Administración, esta tasa «se sitúa en torno a los tres puntos por encima del crecimiento del PIB nominal, por lo que se podría señalar un crecimiento del 9,5% como tasa máxima aceptable. A pesar de estas cifras, que están 6 décimas por encima de esa aceptabilidad, el Gobierno, que achaca este crecimiento del gasto farmacéutico al aumento del número de recetas, confía en una normalización de este incremento del gasto hasta fin de año.
El Ejecutivo explica el aumento del número de recetas por el aumento de la población protegida, así como por el incremento de actividad de las consultas como consecuencia de las políticas de captación de pacientes y la detección precoz de patologías realizado por los servicios de salud. También lo achaca a la incidencia de la epidemia de gripe o a los efectos producidos en el mes anterior de la entrada en vigor de una orden de precios de referencia.
Previsiones
En cuanto a las previsiones sobre la evolución del gasto público en medicamentos para lo que resta del ejercicio 2002, el Gobierno asegura que este crecimiento comenzó a moderarse en el mes de mayo, ya que en los períodos enero-febrero y enero-abril las tasas de crecimiento fueron del 10,47% y del 9,12%, respectivamente. De este modo, según los responsables de Sanidad, la previsión apunta a una progresiva normalización del incremento del número de recetas en lo que queda de año.
Las fuentes gubernamentales resaltaron que «es necesario destacar la favorable tendencia experimentada por el gasto medio por receta, cuyo incremento se sitúa en el 2,87% en el período enero-mayo, cifra que se encuentra por debajo del incremento del IPC». Así, teniendo en cuenta la entrada en vigor de la nueva orden sobre precios de referencia, «puede aventurarse que el comportamiento del gasto farmacéutico en lo que resta de 2002 alcanzará el objetivo de situar su crecimiento por debajo del 9,5%».
En marcha la elaboración del Manual del Farmacéutico de Atención Primaria
Hasta el 15 de enero de 2003 permanecerá abierto el plazo de recepción de trabajos para el Manual de Farmacéuticos de Atención Primaria que prepara la Sociedad Española de Farmacéuticos de Atención Primaria (SEFAP), que patrocina laboratorios Almirall Prodesfarma y edita Drug Farma.
Según datos de la SEFAP, más de un centenar de profesionales de las distintas comunidades autónomas tomarán parte en esta iniciativa, en la que pueden tomar parte todos los farmacéuticos de atención primaria. Una comisión evaluadora, constituida por miembros de la SEFAP, se cerciorará de que los trabajos presenten una línea homogénea en sus contenidos, se ajusten a los capítulos propuestos y estén en consonancia con los criterios fijados en las normas.
Con este manual, que verá la luz el 15 de junio de 2003, la SEFAP pretende crear una herramienta de consulta práctica y eficaz para todos sus asociados. El documento incluye 12 temas estructurados en 60 capítulos a través de los que se abordarán aspectos relacionados con los medicamentos, como información y formación, selección y evaluación de su utilización; la docencia e investigación; o estrategias de intervención en la atención primaria, entre otros. Igualmente, se tratarán también materias relativas a su labor profesional: gestión de stocks de medicamentos y material sanitario, farmacovigilancia, educación para la salud, coordinación entre niveles asistenciales, asesoría técnica a las distintas estructuras sanitarias y garantía de calidad en atención primaria y atención farmacéutica.
Tras la compra de Pharmacia
Pfizer controlará el 11% del mercado farmacéutico mundial
Laboratorios Pfizer, líder del mercado de medicamentos, con el 8% de las ventas, ha comprado recientemente Pharmacia, una de las compañías medianas (algo más del 3% del total). Como consecuencia Pfizer controlará el 11% del mercado mundial farmacéutico. La nueva compañía tiene garantizada su presencia en las principales áreas de negocio, desde la oncología a la oftalmología.
Henry A. McKinnell, director general de Pfizer.
Con esta compra, por primera vez, una empresa controlará una cuota del mercado de medicamentos superior al 10%. Además, hay quien afirma que todas las personas de más de 50 años comprarán alguno de sus productos. Según se recoge en The Wall Street Journal, «la fusión está diseñada para aumentar la potencia de Pfizer en el mercado y reforzar sus posibilidades de que las biotecnológicas y las compañías farmacéuticas especializadas les otorguen las licencias de sus moléculas más prometedoras».
Mientras Pfizer aporta a la nueva empresa productos para el colesterol, la depresión, el sida, la disfunción eréctil y la alergia, Pharmacia, con aproximadamente la mitad de beneficios que su compradora, tiene una cartera de 11 fármacos con más de 1.000 millones de dólares de venta cuya patente no expira hasta 2010. Entre ambas empresas generan unos 48.000 millones de euros de beneficios y disponen de más de 7.000 euros para investigación y desarrollo. Pfizer asegura que confía en comercializar una veintena de nuevos medicamentos durante los próximos 5 años, más la cartera de productos en fase experimental de Pharmacia.
Según han señalado los analistas, con esta operación, sólo en fármacos para combatir la incontinencia urinaria y en el desarrollo de medicamentos para tratar el enfisema, se produce una duplicación de productos entre ambas compañías. Los analistas han advertido que las fusiones no resolverán la falta de nuevos productos y las pobres expectativas con las que se afrontan los próximos años, principales puntos débiles del sector. La concentración del mercado en la última década no ha evitado que la FDA sólo haya recibido dos peticiones para la aprobación de fármacos durante los cinco primeros meses de 2002; 24 en 2001 o 53 en 1996.
Según datos de la SEFH, los mayores de 50 años son el grupo más afectado
Los antibióticos son los fármacos más implicados en las RAM hospitalarias
Según la memoria de las notificaciones recibidas en la unidad de farmacovigilancia de la Sociedad Española de Farmacia Hospitalaria (SEFH), los antibióticos continúan siendo el grupo farmacológico más implicado en las reacciones adversas a medicamentos (RAM), por delante de los inmunosupresores selectivos y los antiinflamatorios. Desde la implantación del sistema de notificación de RAM a la SEFH, los antibióticos figuran en primer lugar.
Los antibióticos causan la mayoría de las RAM hospitalarias.
Entre 1999 y 2002, la SEFH recibió 306 tarjetas amarillas, de las que se han estudiado 287, con un total de 454 RAM comunicadas. De ellas, 85 han sido originadas por antibióticos y vacunas (18,72%), 74 por inmunosupresores selectivos (16,31%) y 47 por antiinflamatorios y antirreumáticos (10,35%). Según Víctor Napal, jefe del Servicio de Farmacia Hospitalaria del Hospital de Navarra y miembro de la SEFH, la entrada de los antiinflamatorios entre los más vinculados a las RAM se debe «al aumento de especialidades comercializadas de este grupo terapéutico».
En cuanto a las reacciones, Napal explica que «los antibióticos y las vacunas son el grupo de fármacos más relacionado con las reacciones de tipo dermatológico, que son las más frecuentes». Además de la piel, el aparato digestivo ha sido el órgano más afectado, siendo la hemorragia gastrointestinal, la erupción cutánea y prurito las RAM que se han notificado en mayor proporción.
Finalidad
Según explica el Dr. Napal, «la finalidad del informe es promocionar y recordar a los profesionales farmacéuticos la importancia de su colaboración en farmacovigilancia». Actualmente, el número de RAM de las que tiene conocimiento la SEFH a través de este registro es inferior al número de RAM notificadas al Servicio Español de Farmacovigilancia, aunque este especialista valora el sistema de comunicación de sospecha de reacciones adversas como «muy eficaz y eficiente en el conocimiento del perfil de toxicidad de los medicamentos». Por ello, añade que la SEFH también desea potenciar y mejorar la utilización de la información obtenida de dosis unitarias, monitorización de fármacos alertantes, monitorización de diagnósticos alertantes, monitorización de alergias, el uso de datos de laboratorio para la detección de RAM y la utilización de los informes al alta a través del análisis y seguimiento del Conjunto Mínimo Básico de Datos.
Guillermo Tena, nuevo presidente de AESEG
Guillemo Tena.
El pasado 12 de septiembre, la Asociación Española de fabricantes de Sustancias y Especialidades farmacéuticas Genéricas (AESEG) eligió nueva Junta Directiva, nombrando a Guillermo Tena, de Mabofarma, como nuevo presidente de la entidad. Asimismo, se nombraron tres nuevos vicepresidentes: Montserrat Almirall, de Bayvit; Pablo Sancho, de Kern Pharma, y José Luis Stampa, de Medichem. El tesorero será Luis Fernández, de Química Sintética, y continuará en su cargo de secretario general José Zamarriego.
Los objetivos principales de la nueva Junta Directiva se centrarán en impulsar y dinamizar el mercado de los medicamentos genéricos en España. «Tenemos por delante retos importantes en el sector si queremos conseguir desarrollar una verdadera cultura del genérico en nuestro país», declaró Guillermo Tena tras asumir su nuevo cargo.
Constituida en 1998, AESEG es una organización de ámbito nacional, sin ánimo de lucro, que pretende impulsar la implantación efectiva de las EFG en España y fomentar un desarrollo sostenido que equipare a nuestro país con los países de su entorno en el campo de los medicamentos genéricos.
Anteproyecto de Ley Autonómica de Ordenación Farmacéutica
Las farmacias canarias tendrán que estar abiertas bajo la misma titularidad durante dos décadas
Las 63 oficinas que comenzarán a abrirse en los próximos meses en Canarias estarán sujetas a la normativa referente a la transmisión, que recoge el anteproyecto de Ley Autonómica de Ordenación Farmacéutica presentado por el Servicio Canario de Salud. Un anteproyecto que establece que las nuevas oficinas de farmacia de las islas tendrán que permanecer abiertas bajo la misma titularidad al menos 20 años para poder ser transmitidas.
José Luis Mola.
La medida del Gobierno canario se desliga de la línea general seguida por la mayoría de las normativas autonómicas: 3 años (en Cataluña son 6) y del extremo opuesto (la prohibición establecida en Castilla-La Mancha, Extremadura y Galicia).
Aunque, en general, tanto los colegios farmacéuticos como las asociaciones empresariales consideran positivo el anteproyecto, han presentado alegaciones por considerar abusiva la limitación fijada. El presidente de la Asociación Empresarial de Farmacéuticos de Canarias, Tomás García Armas, afirmó que «aunque entendemos que es para evitar especulaciones, sería suficiente con 10 años». Para los representantes colegiales, el límite debería bajarse todavía más. Así, mientras que el presidente del COF de Tenerife, Elviro Hernández, apunta que «lo ideal son 5 o 6 años», su homólogo de Las Palmas, José Luis Mola, defiende la situación actual, que fija 5 años.
Por otro lado, se mantienen los parámetros de planificación que se venían aplicando y que coinciden con los de la normativa básica estatal: 2.800 habitantes por oficina y 250 metros de distancia entre ellas y respecto a un centro de salud. Para la asociación empresarial de Canarias no estaría de más aumentar la ratio a 3.000 habitantes «para favorecer la viabilidad económica de la farmacia canaria, que debido a las características geográficas del archipiélago tiene más dificultades en el abastecimiento de medicamentos, las farmacias tienen que duplicar o triplicar stocks y eso supone un coste añadido».
Otra de las peculiaridades que presenta el anteproyecto canario respecto a las ordenaciones ya existentes es el proceso para abrir una farmacia. Previo al concurso de nuevas autorizaciones se convoca otro de traslados. Su ventaja, según destacan los colegios farmacéuticos, es que permite a los titulares de zonas rurales que lo deseen mejorar su situación. Las vacantes generadas en esta parte del proceso se incorporarán a la oferta de nuevas autorizaciones, en cuyo proceso sólo podrán participar aquellos farmacéuticos que no sean titulares de una oficina ni lo hayan sido en los tres años anteriores.
Se publica la Lista Modelo OMS de Medicamentos Esenciales
La OMS ha publicado recientemente una guía mundial de referencia para garantizar un uso eficaz de los 325 fármacos que actualmente se encuentran en la lista de medicamentos esenciales. El documento elaborado por la OMS, que lleva por título Lista Modelo OMS de Medicamentos Esenciales, especifica en cada caso las indicaciones terapéuticas, la posología, los efectos adversos, las contraindicaciones y las advertencias pertinentes de cada uno de los 325 fármacos. La OMS considera que «el empleo correcto de este instrumento permitirá mejorar la seguridad de los pacientes y limitar el gasto superfluo en medicamentos».
La OMS espera que el nuevo formulario sirva a los gobiernos e instituciones nacionales de modelo para la elaboración de sus propios formularios nacionales. También considera que puede resultar particularmente útil en el caso de los países en desarrollo, donde las publicaciones comerciales y de promoción a menudo constituyen la única fuente de información sobre los medicamentos a la que tienen acceso el personal de salud; los prescriptores de medicamentos, y los pacientes. Según estimaciones de la OMS, en los países en desarrollo sólo dos terceras partes de la población tiene algún tipo de acceso a los medicamentos esenciales. En esos países, los productos farmacéuticos pueden llegar a acaparar un 40% del presupuesto nacional de salud.
Como consecuencia del pacto firmado por estas comunidades autónomas en materia sanitaria
Extremadura, las dos Castillas y Madrid quieren negociar un concierto propio con las farmacias
Las cuatros comunidades del centro que firmaron un acuerdo de colaboración en materia sanitaria tras recibir las transferencias (Extremadura, Castilla y León, Castilla-La Mancha y Madrid) rechazan el concierto actual del INSALUD con las oficinas de farmacia y quieren negociar uno propio. Una medida que, en algunos casos va contra la voluntad de los colegios farmacéuticos de estas comunidades.
Alberto Sáez.
El eje de los nuevos conciertos farmacéuticos podría ser común en las comunidades autónomas de Extremadura, Castilla y León, Castilla-La Mancha y Madrid, siguiendo su política de sentar bases comunes de colaboración en materia farmacéutica. Así, los once puntos que ha planteado la Administración sanitaria extremeña a los representantes colegiales y que presentará su homóloga castellanoleonesa a los de su autonomía, recogen como eje la fijación de precios máximos para los productos de dietoterapia y nutrición enteral, para «evitar abusos y garantizar equidad en el acceso a estos productos», según ha señalado el presidente del COF de Badajoz, Cecilio Venegas, así como el planteamiento de, al menos, un acuerdo sobre la prescripción por principio activo.
En Extremadura, la Consejería de Salud ya ha hablado a los farmacéuticos de establecer un pacto «de dobles precios de referencia, de dispensación de medicamentos genéricos más baratos o como se quiera, pero un modelo como el andaluz», según ha explicado Cecilio Venegas.
Por su parte, desde el Servicio de Salud de Castilla y León se ha quitado importancia a la decisión de denunciar el concierto, pues, a juicio de la directora de Farmacia de esta autonomía, Nieves Martín, «la denuncia es una cuestión formal por el cambio que se ha producido con las transferencias tanto a nivel de organización farmacéutica como sanitaria». Sin embargo, desde el Consejo de COF de Castilla y León, su presidente, Alberto Sáez, ha apuntado que «la Consejería debe querer incluir alguna novedad si ha preferido negociar un concierto desde cero». Una novedad que, «en ningún caso --señala Sáiz-- podría ir encaminada a establecer descuentos sobre la facturación o empeorar la fecha de pago». Los farmacéuticos de Castilla y León confiaban en prorrogar el concierto actual, al menos un año, adaptando sólo lo que fuera imprescindible.
El TSJA obliga a las farmacias andaluzas a dispensar la píldora del día siguiente
El Tribunal Superior de Justicia de Andalucía (TSJA) ha dictado una sentencia que obliga a los farmacéuticos andaluces a disponer de la píldora del día siguiente, porque la considera «un anticonceptivo y no un abortivo». Esta sentencia viene a respaldar el decreto del Gobierno andaluz. Un decreto que Manuel Guillén Pascual, un boticario que no ejerce, recurrió para proteger lo que él consideraba su derecho a la objeción de conciencia.
A finales de 2001, el TSJA dictó, y luego anuló, un auto en el que suspendía cautelarmente la dispensación obligatoria de la píldora poscoital por considerarla un abortivo. En la última sentencia dictada la sala varía su postura inicial y admite que la píldora del día siguiente es un anticonceptivo, tal y como establece la Agencia Española del Medicamento, el Tribunal Europeo de Derechos Humanos y la OMS.
La sentencia dictada ahora por el TSJA también deslegitima al recurrente para interponer el escrito de impugnación, porque «no tiene la condición de titular o cotitular de oficina de farmacia en el territorio autonómico andaluz; ni ejerce cargo de responsabilidad alguna en el almacén farmacéutico de distribución; ni ha presentado facturación alguna por las recetas oficiales dispensadas» y, por último, porque «aunque se encuentra colegiado como farmacéutico en el Colegio de Jaén, aparece en la modalidad de no ejerciente». Por tanto, «no está legitimado para recurrir una orden de la Consejería de Salud que incluye los preservativos y los progestágenos como productos de los que deben disponer las oficinas de farmacias y almacenes farmacéuticos de distribución».
Ejercerá un mayor control sobre los visitadores médicos
La Comunidad de Madrid regulará las actividades de promoción de medicamentos en los centros de salud
La Comunidad de Madrid (CAM) ha dado luz verde a una iniciativa de su Consejería de Sanidad que ordena las actividades de promoción de medicamentos en los centros sanitarios públicos de la región y establece la forma en que va a ser controlada esta actividad, en particular la visita médica en hospitales y centros de salud.
Los prescriptores madrileños estarán más controlados.
Con esta iniciativa, la Consejería de Sanidad de Madrid persigue que la información científico-técnica que se facilita a los profesionales tenga los deseables niveles de calidad, transparencia y ética profesional. La Dirección General de Farmacia y Productos Sanitarios de la Consejería de Sanidad de Madrid también considera que la forma en que se viene informando a los médicos sobre los medicamentos no es la correcta, por lo que estima que todos los implicados deben tomar cartas en el asunto.
Por este motivo, la Consejería ha realizado una amplia consulta entre las diferentes asociaciones y sociedades que representan a los médicos, así como a los representantes de los visitadores médicos y a la propia Farmaindustria para elaborar esta medida. Sanidad pretende una actuación coordinada entre Farmaindustria y la Administración para que los profesionales sanitarios reciban una información acerca de los medicamentos con todas las garantías éticas y de calidad.
Supervisor
El borrador elaborado por la CAM establece los estándares de lugar, tiempo, duración de la visita médica y de frecuencia para los impactos informativos que permitan a los responsables de los centros una organización razonable de la información sobre productos médicos. Asimismo, la norma establece un procedimiento simplificado para la autorización previa de los planes de promoción de los laboratorios, en el que se contempla la colaboración de Farmaindustria, y se ordena el procedimiento para la realización de actividades formativas en los centros con el patrocinio de los laboratorios, así como la colaboración de la industria en la asistencia a cursos y congresos.
Para garantizar la eficacia de las actuaciones y controlar el cumplimiento de la normativa, se introduce la figura del supervisor general de promoción de los medicamentos. Una figura que tendrá asignadas, entre otras, las funciones de: evaluar la idoneidad del material promocional, hacer un seguimiento permanente de estas prácticas de promoción, canalizar las informaciones que se le hagan llegar desde las gerencias de los centros y desde los propios profesionales sobre posibles infracciones de la norma, coordinar actuaciones con la comisión deontológica de la industria farmacéutica implantada en España y con las comisiones deontológicas de los colegios oficiales de médicos y de farmacéuticos de Madrid, autorizar los planes de visita médica y proponer las sanciones que procedan en su caso.
El 20% de los jóvenes españoles se automedica
Según un estudio del Instituto de la Juventud (Injuve), el 22,2% de los jóvenes españoles recurre a la automedicación. Para los responsables del estudio, esta proporción tenderá a aumentar a medida que se incremente el nivel educativo y socioeconómico de los jóvenes.
El estudio publicado por el Injuve revela que el 51,1% de los jóvenes acude a la consulta médica «ante cualquier tipo de dolor»; el 22,2% se automedica y el 11,1% de éstos consulta a familiares; por último, el 11,1% hace una autovaloración del tipo de dolencia. Lo más insólito del estudio es que sólo el 4,4% de los encuestados decide pedir ayuda al farmacéutico.
En los últimos 3 meses se ha producido una mayor incidencia de la automedicación entre los jóvenes, ya que sólo el 7% de los encuestados no había tomado medicina alguna por voluntad propia. En cuanto al tipo de especialidades consumidas, el 78% había tomado Aspirina y/o paracetamol; el 17,8%, vitaminas y minerales, y el 17,8, antibióticos. Un 18% había consumido cuatro o más medicamentos. Durante 2002, el 80% de los jóvenes encuestados ha tomado medicamentos sin receta, mientras que el 86,8% adquirió medicamentos con receta. Según el informe, los antibióticos son los medicamentos más usados con receta.
Con la presencia de la ministra de Sanidad y Consumo
Presentada la Fundación Farmaindustria
La Fundación Farmaindustria es una entidad privada que centrará toda su actividad en la promoción de la investigación biomédica y farmacéutica en España. Durante la presentación de la Fundación Farmaindustria, la ministra de Sanidad y Consumo, Ana María Pastor, manifestó al presidente de Farmaindustria, Jesús Acebillo, su apuesta por el actual sistema público y de financiación de los medicamentos.
La ministra calificó de «buena noticia» la creación de la Fundación Farmaindustria, una entidad privada que centrará toda su actividad en la promoción de la investigación biomédica y farmacéutica en España, porque, a su juicio, «debe suponer el compromiso de participación de la iniciativa privada en la investigación y en el interés general». Según explicó Jesús Acebillo, la Fundación nace con vocación de «contribuir a la mejora de la sanidad española, promoviendo la formación de los profesionales sanitarios, así como el uso racional del medicamento».
Por su parte, Ana María Pastor se manifestó partidaria de la creación de un «marco de cooperación entre la Administración sanitaria y la industria farmacéutica, en un entorno de transparencia, definido por la ética, el rigor y la profesionalidad», así como por «la necesaria estabilidad presupuestaria» que, a su juicio, «debe garantizar la Administración a los ciudadanos, protegiendo su sistema de prestaciones sanitarias, mediante una adecuada gestión de los recursos públicos». En este sentido, la ministra señaló que «el uso adecuado de los medicamentos es la única garantía de éxito que puede avalar los recursos invertidos en investigación y desarrollo».
Finalmente, el presidente de Farmaindustria recordó que el sector farmacéutico dedica el 8,9% de su facturación a investigación y desarrollo, y ha multiplicado sus gastos en un 2,3%. También subrayó la necesidad de «contar con un entorno estable». A este respecto, indicó que «el desarrollo de un fármaco requiere 10 años» y que la industria española «ha de competir con la de Estados Unidos, que lo hace en condiciones más favorables».
El 23% de los jóvenes españoles sigue adoptando conductas de riesgo sexual
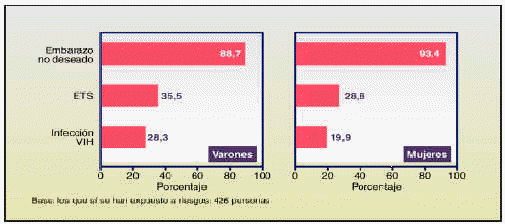
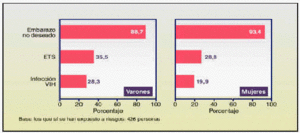
Porcentaje de las conductas de riesgo sexual a las que se exponen los jóvenes españoles.
Según la Primera Encuesta Schering sobre Sexualidad y Anticoncepción en la Juventud Española, presentada en Barcelona el pasado 18 de septiembre, aunque la gran mayoría de los jóvenes españoles son conscientes de los riesgos que conlleva una relación sexual sin protección (embarazo, VIH y enfermedades de transmisión sexual), un 23% sigue adoptando conductas de riesgo.
Tal y como destacan los miembros del Equipo Daphne, entre las principales conclusiones de la encuesta resalta el alto número de jóvenes españolas que están en riesgo de embarazo no deseado «por no usar métodos anticonceptivos o por usarlos de forma inadecuada (preservativos)». Otro aspecto destacable --añaden-- es «el alto grado de satisfacción de los jóvenes con la píldora anticonceptiva (muy superior a la del preservativo)».
En cuanto a las principales causas de riesgo sexual, son las siguientes: no haber empleado preservativo (81% de los varones y 75% de las mujeres), no haber empleado un método anticonceptivo en general (24% de los varones y 34% de las mujeres), lo imprevisto de la relación (19% de los varones y 18% de las mujeres), y el estado de euforia provocado por el consumo de alcohol o drogas ilegales (17% de los varones y 11% de las mujeres).
Un nuevo índice de protección solar armonizará la medición de los riesgos de exposición a los rayos ultravioleta
Página web de la OMS que informa sobre el nuevo índice de protección solar.
A fin de armonizar a nivel internacional la medición de los riesgos de exposición a los rayos ultravioleta y aumentar la prevención del cáncer del piel y las cataratas, la OMS ha diseñado un nuevo índice de protección solar.
Según datos de este organismo, cada año se producen entre 2 y 3 millones de casos de cáncer cutáneo, de los cuales 132.000 se agravan en forma de melanoma cutáneo. Además, la OMS recuerda que se ha producido un aumento en la incidencia de cáncer a partir de los años setenta debido a los cambios en el modo de vida, con una mayor exposición al sol unida al deterioro de la capa de ozono.
Aun así, aunque numerosos países promueven la protección solar publicando los índices en los boletines meteorológicos de los medios de comunicación, según la OMS, a menudo utilizan símbolos, códigos y colores distintos que provocan «confusión». A fin de acabar con esta situación, esta organización ha publicado un modelo de índice común: Global Solar UV Index, a practical guide, un documento que clasifica los índices y valores de radiación solar en distintas categorías de exposición (leve, moderada, fuerte, muy fuerte y extrema). La información está elaborada a base de pictogramas simples que señalan la actitud que se ha de tomar ante el sol, dependiendo del índice de radiación. Una información que se puede consultar en el sitio web de la OMS (www.who. int/peh-uv).
Con la presencia del rector de la UIB
El COF de Baleares clausura el Curso de Especialista Universitario en Educación Nutricional
Mesa de clausura.
El presidente y la vicepresidenta de la Fundación de Ciencias Farmacéuticas de les Islas Baleares, Antoni Real, e Isabel Llompart, respectivamente, acompañados del profesor de Ciencias de la Actividad Física de la Universidad de las Islas Baleares (UIB), Josep Tur; el rector de la UIB, Llorenç Huguet, y el director general de Evaluación y Acreditación de la Conselleria de Salut del Gobierno balear, Vicenç Mateu, clausuraron en Palma de Mallorca el Curso de Especialista Universitario en Educación Nutricional, organizado por la mencionada Fundación y la UIB. La ceremonia de clausura contó además con la presencia de la mayoría de los alumnos que, durante los últimos 10 meses, han participado en esta iniciativa formativa.
Durante el acto, Antoni Real destacó la importancia de una iniciativa de estas características «tanto por la importancia objetiva de la materia objeto de estudio como por el hecho de reafirmar una alianza con la Universidad balear en la búsqueda de nuevos caminos formativos para el conjunto de los profesionales sanitarios de las Islas Baleares».
Colaboración
Por su parte, Llorenç Huguet expresó su satisfacción por el trabajo conjunto realizado por ambas instituciones, al tiempo que reiteró su disposición a seguir colaborando con el colectivo farmacéutico «en proyectos que a priori resulten interesantes para ambas partes». Finalmente, Vicenç Mateu destacó la función que llevan a cabo instituciones como los colegios profesionales en la promoción y formación de sus colegiados.
Desarrollado por la SEFH en colaboración con el Ministerio de Sanidad y Consumo
Un programa informático mejora el uso de los medicamentos en los hospitales
El pasado 19 de septiembre se presentó, en el marco del XLVII Congreso Nacional de la Sociedad Española de Farmacia Hospitalaria (SEFH), los objetivos y primeros resultados del Proyecto GRDOSIS, basado en la determinación de los estándares españoles de coste por GRD (grupos relacionados por el diagnóstico) y de utilización de medicamentos por patología.
En 1998, el Ministerio de Sanidad estableció con la SEFH, con el patrocinio de Laboratorios Esteve, un acuerdo de colaboración técnica en un proyecto basado en la distribución gratuita del programa informático GRDOSIS a los servicios de farmacia de los 25 hospitales que participan en el proyecto.
En una primera fase se llevó a cabo un estudio piloto en el que se han analizado los datos de 7 de los 25 hospitales participantes en el proyecto, que han podido establecer comparaciones con sus propios datos y determinar las estrategias de racionalización y optimización de tiempo y recursos destinados a cada GRD. En esta primera fase de implantación del programa se detectó un ahorro de casi 400.000 euros en el estudio de 538 GRD. Asimismo, se pudo saber que 27 patologías representan el 50% del coste del conjunto total de episodios, siendo la quimioterapia la que mayor gasto ha supuesto.
Este programa lleva a cabo un cruce de información entre los grupos de pacientes, agrupados por primera vez por GRD con estándares españoles, y la base de datos de los medicamentos que han recibido durante su hospitalización.
Ventajas
El programa GRDOSIS permite conocer el coste real de cada patología; los perfiles de utilización de medicamentos para cada GRD; las dosis, duración de tratamiento y frecuencias de administración; localizar y agrupar pacientes a los que, dentro de un mismo GRD se les haya prescrito un determinado medicamento para compararlo con otros tratados con un medicamento alternativo, y analizar la información por centros asistenciales, hasta llegar al nivel de un paciente concreto.
La aplicación GRDOSIS confirma la correcta utilización de los medicamentos, de acuerdo con los criterios establecidos para la implantación de medidas correctoras en caso de mal uso generalizado.