La rabia es una zoonosis de etiología viral que cuando afecta al hombre le produce una encefalomielitis aguda, siempre mortal. Ocupa el décimo lugar entre las enfermedades infecciosas mortales. En el presente trabajo se aborda la etiología, patogenia, epidemiología, diagnóstico, medidas profilácticas y tratamiento de la rabia.
La rabia se transmite a través de mordedura o contacto directo de mucosas o heridas con saliva del animal infectado. También se ha demostrado su adquisición a través de trasplante corneal de donador muerto infectado por el virus y no diagnosticado. No obstante, no se ha documentado su transmisión por mordedura de humano a humano, pero se ha aislado de la saliva de los pacientes afectados de rabia. Este virus también se ha identificado en sangre, leche y orina. No se ha documentado transmisión transplacentaria.
La rabia fue descrita por Aristóteles y por Celso, y no fue hasta 1885 cuando Pasteur consiguió la primera vacuna antirrábica, salvando al niño Joseph Meister de una muerte segura tras sufrir múltiples mordeduras de un perro rabioso.
A pesar de la eficacia y la inocuidad del tratamiento actual, entre 35.000 y 50.000 personas mueren cada año de rabia debido a que no son tratadas. La rabia ocupa el décimo lugar entre las enfermedades infecciosas mortales.
Estructura
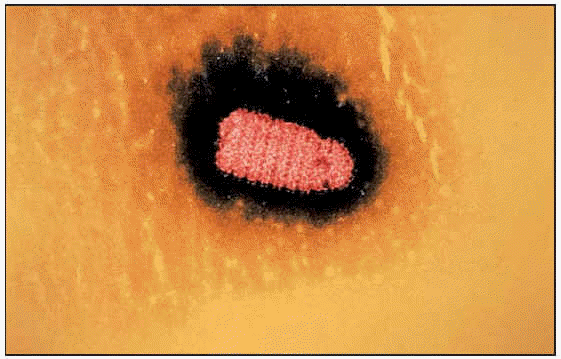
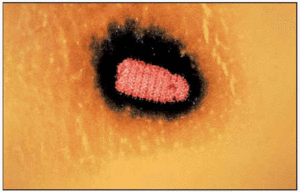
El virus de la rabia pertenece a la familia Rhabdoviridae, género Lyssavirus. Es un rhabdovirus de 180 nm de longitud por 75 nm de anchura con forma de bala de fusil o de proyectil cilíndrico. Tiene una extremidad redondeada y la otra plana con una muesca como el talón de una flecha. Asimismo, posee una nucleocápside y envoltura. Esta última es una doble capa bilipídica perfectamente definida.
Patogenia
La mordedura o arañazo de un animal rabioso trae como consecuencia la presencia de saliva infectada con virus rábico en la musculatura estriada. Éste se multiplica en los miocitos hasta lograr una concentración infectante necesaria para alcanzar las terminaciones nerviosas sensitivas y las placas neuromusculares motoras. Se une a los receptores de acetilcolina, penetrando en las fibras nerviosas periféricas, donde es descapsidado, y comienza así el proceso de replicación viral.
Epidemiología
La rabia es una zoonosis de distribución mundial (excepto en Australia, Reino Unido, Japón y Nueva Zelanda), y se calculan alrededor de 15.000 casos anuales. El principal reservorio de los virus son los animales salvajes, a partir de los cuales la infección se extiende a otros animales salvajes y a los domésticos. Todos los seres de sangre caliente pueden experimentar el virus rábico.
Los principales reservorios dependen del área geográfica: en Europa son los zorros y los lobos; en América, la mofeta, el zorro y el mapache; en África, la mangosta y el chacal, y en Asia, el lobo y el chacal. Mención especial requieren los murciélagos, que muerden y chupan la sangre de bóvidos y équidos durante la noche, transmitiéndoles la rabia. En América existen vampiros portadores del virus que hacen que se les consideren los verdaderos reservorios de la enfermedad. En Europa Central y Occidental es el zorro rojo o común la causa principal de la propagación de la rabia.
En cuanto a la rabia urbana, los animales domésticos son la principal fuente de infección. El perro es, en el 90% de los casos, el principal atacante del hombre, principalmente el perro vagabundo. Los gatos, de vida mucho más incontrolada, transmiten la enfermedad por múltiples arañazos y su peligro de transmisión es más alto.
Diagnóstico
El diagnóstico de la rabia puede realizarse en el hombre o en el animal mordedor. Estamos ante una enfermedad mortal la mayor parte de las veces. Por esta razón, es necesario realizar el diagnóstico durante el período de incubación, circunstancia sólo posible en el animal mordedor. Por ello, en el hombre tiene poco interés en el diagnóstico. No obstante, se puede establecer directamente por la demostración del virus a partir de la saliva, esputo, exudados traqueal y nasal, orina y LCR.
En otras ocasiones se pueden detectar antígenos virales, por inmunofluorescencia, en células del epitelio corneal y piel de la herida. Finalmente, post mortem, el aislamiento, la investigación de antígenos y la búsqueda de corpúsculos de Negri pueden realizarse en el tejido cerebral.
La detección de anticuerpos tiene poco interés en los casos de período de incubación corto. Si, por el contrario, éste es largo, pueden aparecer anticuerpos en sangre y en el LCR al iniciarse el cuadro clínico. Se detectan mediante reacciones de fijación del complemento, inmunoflurescencia indirecta y pruebas de neutralización. Recientemente se han empleado también las de inhibición de la fluorescencia y el test de reducción de placas.
El principal reservorio de los virus son los animales salvajes, a partir de los cuales la infección se extiende a otros animales salvajes y a los domésticos
Vacunación antirrábica
Vacunas avianizadas
Como la vacuna VEP (vacuna de embrión de pato), que se obtiene por cultivo en embrión de pato y cuya inactivación se hace con betapropiolactona. Es muy empleada en Estados Unidos.
Vacunas obtenidas de tejido cerebral de animales inmaduros
Vacuna de fuenzalida. Se obtiene del cerebro del ratón lactante y la posterior inactivación con rayos ultravioleta. Es muy inmunógena. Se recomienda una dosis diaria durante 14 días con dosis de 0,5 ml en niños menores de 3 años, y de 1,0 ml en adultos por vía subcutánea en la región periumbilical interescapulovertebral. Las reacciones secundarias generalmente son locales, como dolor, eritema e induración en el sitio de la aplicación. Se calcula que 1 de cada 8.000 receptores de vacunas pueden presentar alguna complicación neurológica como encefalitis, mielitis transversa, neuropatías periféricas y neuritis. Las complicaciones están en relación directa con el número de dosis de vacunas y la edad del paciente. En caso de presentarse cualquiera de estas reacciones adversas, debe suspenderse este tipo de vacuna y continuar con la de células diploides.
Vacuna de Rossi. Se obtiene del cerebro del carnero y la posterior emulsión en solución salina mertiolada y fenolada.
Vacuna de Gispen. Se obtiene del cerebro del conejo lactante.
Vacunas obtenidas de cultivos tisulares
No presentan las complicaciones encefalíticas de hipersensibilidad a la mielina que aparece en las vacunas obtenidas a partir de tejido cerebral. Existen muchas vacunas de este tipo, a saber:
Vacuna de Abelseth. En células de riñón de cerdo.
Vacuna de Atanasiu. Células BHK/21.
Vacunas en células diploides. Como la WI38 del Instituto Wistar de Filadelfia y la vacuna VCDH (vacuna de células diploides humanas) del Instituto Merieux de Lyon). En el caso de la vacuna VCDH se administran 4 o 5 dosis de 1 ml por vía intramuscular los días 1, 3, 7 y 14 (el día 28 es opcional).
Profilaxis
Es posible distinguir tres estrategias de vacunación diferentes:
En áreas libres de rabia, se recomienda la inmunización preexposición a los sujetos de alto riesgo por motivos laborales.
En los países desarrollados con rabia salvaje, hay que evitar la transmisión de la rabia mediante la vacunación y otras medidas de control de los perros. El tratamiento preexposición se aplica como en las áreas libres de rabia y el tratamiento postexposición se aplica rara vez.
En los países en vías de desarrollo con rabia urbana es prioritaria la inmunización canina y la erradicación de animales callejeros. El tratamiento postexposición es frecuente, pero las vacunas disponibles son poco inmunógenas y provocan graves reacciones adversas.
Profilaxis preexposición
La OMS ha establecido algunas recomendaciones sobre la profilaxis preexposición. Tres dosis de 2,5 U administradas por cualquier vía generan niveles de anticuerpos neutralizantes casi en el 100% de los individuos. Si se emplean vacunas celulares, la inmunización consiste en la aplicación por vía intramuscular de 3 dosis de 1 ml en los días 0, 7, 21 y 28. En zonas donde las limitaciones económicas dificultan la disponibilidad de vacunas se pueden inocular por vía intradérmica 3 dosis de 0,1 ml en los días 0, 7, 21 y 28.
Muchas autoridades sanitarias, incluidas las de la OMS, recomiendan una serología de 2-4 semanas después de la última inyección para asegurar una seroconversión satisfactoria. Es fundamental realizar este control en individuos que tienen un elevado riesgo de contraer la rabia, en los sometidos a tratamiento inmunosupresor y en los que reciben múltiples vacunas simultáneamente. Si existe una exposición continua al virus de la rabia se deben efectuar determinaciones de anticuerpos neutralizantes cada 6-12 meses y administrar dosis de recuerdo si los títulos son inferiores a 0,5 U/ml.
En cuanto a las indicaciones de la profilaxis preexposición, queda restringida a aquellos individuos que tienen un elevado riesgo de exposición: personal de laboratorio, veterinarios, granjeros, manipuladores de animales y personas que viajan a zonas endémicas. Especial interés presenta el estudio de la profilaxis preexposición en los viajeros.
La vacunación preexposición elimina la necesidad de administrar inmunoglobulina y reduce el número de dosis de vacuna postexposición, pero no elimina la necesidad de tratamiento postexposición, sólo lo simplifica
La vacunación antirrábica no es un requisito obligatorio para entrar en ningún país, pero aquellas personas que viajan a países donde la rabia es endémica deben ser informadas del riesgo de contraer esta enfermedad y de la conducta que deben seguir en caso de mordedura. Se recomienda el tratamiento preexposición para aquellos que viven o visiten durante más de 30 días zonas endémicas de rabia en las que no es posible obtener un tratamiento óptimo para una mordedura. Estas zonas incluyen casi todos los países de América central y Sudamérica, la India, el sureste asiático y la mayor parte de África. Sin embargo, un grupo de expertos recientemente ha desaconsejado la profilaxis preexposición para los que viajen a zonas endémicas durante largo tiempo. Según este grupo de trabajo, la vacunación previa debe limitarse a individuos sometidos a un elevado riesgo de exposición y a niños incapaces de comprender la necesidad de evitar los animales o de comunicar un contacto con éstos.
Finalmente, decir que la vacunación preexposición elimina la necesidad de administrar inmunoglobulina y reduce el número de dosis de vacuna postexposición, pero no elimina la necesidad de tratamiento postexposición, sólo lo simplifica.
Profilaxis postexposición
Es muy efectiva si se combinan el tratamiento local de la herida, la inmunización pasiva y la vacunación de forma correcta.
Sólo está indicada si ha existido exposición realmente. Así, las caricias a animales rabiosos o el contacto con sangre, orina o heces de un animal con rabia no se considera exposición.
El mayor riesgo corresponde a mordeduras en zonas ricas en terminales nerviosas o próximas al SNC. Sin embargo, la localización de la mordedura no debería influir en la decisión de iniciar el tratamiento.
Las exposiciones que no son mordeduras rara vez provocan rabia. El mayor riesgo se corre cuando ha existido exposición a grandes cantidades de aerosoles que contienen virus de la rabia, en trasplantes de órganos y por arañazos de animales rabiosos. Se han descrito casos en trasplantes de córnea. No se han descrito casos de transmisión digestiva, transplacentaria, ni mediada por artrópodos.
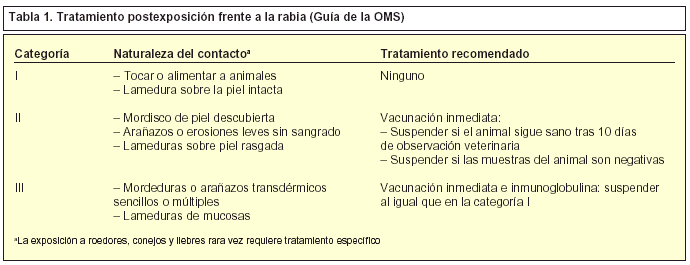
La OMS ha establecido tres categorías en función del grado de exposición (tabla 1). Se ha sugerido una cuarta categoría que incluye a aquellos pacientes que han sufrido mordeduras graves en la cara, la cabeza, los brazos y las manos, casos en los que puede ser inadecuado el volumen de inmunoglobulina recomendado.
El objetivo de la infiltración de la herida con inmunoglobulina es neutralizar el virus antes de que penetre en las terminaciones nerviosas periféricas y estimular la respuesta de linfocitos T
Tratamiento local de la herida
La herida debe lavarse inmediatamente con agua y una solución jabonosa al 20% para evitar contraer la rabia. En la actualidad no se aconseja el uso de ácido nítrico o los derivados de amonio cuaternario, porque su efectividad es inferior a la solución de jabón al 20%.
La sutura primaria de la herida sin infiltración previa de inmunoglobulina puede provocar la entrada del virus en las terminaciones nerviosas. Por ello debe evitarse la sutura primaria, y se hará siempre después de la limpieza e infiltración con inmunoglobulina. La sutura secundaria podría hacerse 2 semanas después, cuando el paciente dispone de anticuerpos neutralizantes.
Inmunización pasiva
La inmunoglobulina antirrábica está indicada en todos los contactos de la categoría III de la OMS y se inoculará si es posible en las primeras 24 horas. La inmunización siempre debe ir acompañada de una pauta vacunal completa.
Las inmunoglobulinas antirrábicas homólogas aprobadas por la FDA de Estados Unidos se obtienen por fraccionamiento con etanol frío a partir de plasma de donantes hiperinmunizados.
La dosis recomendada por la OMS es de 20 U/kg de peso corporal de inmunoglobulina humana y de 40 U/kg de peso corporal de inmunoglobulina equina. Se administrará la mayor cantidad posible localmente alrededor de la herida, siempre que sea posible. El resto se administrará en la región glútea. El objetivo de la infiltración de la herida con inmunoglobulina es neutralizar el virus antes de que penetre en las terminaciones nerviosas periféricas y estimular la respuesta de linfocitos T.
Cuando el volumen de inmunoglobulina es insuficiente para infiltrar todas las heridas (categoría IV), existen dos posibilidades: administrar la dosis calculada alrededor de heridas más graves o incrementar la dosis. Pero existen evidencias de que un incremento de la dosis suprime la producción de anticuerpos. Por ello se ha considerado adecuado diluir la inmunoglobulina en suero salino hasta disponer de un volumen suficiente para infiltrar todas las heridas.
Tras la administración de inmunoglobulinas de origen humano puede presentarse dolor local y fiebre. La inmunoglobulina heteróloga se ha asociado a edema angioneurótico, síndrome nefrótico y anafilaxia. Las preparaciones de origen equino se asocian con frecuencia a la enfermedad del suero, pero las usadas hoy día son inocuas.
La inmunoglobulina humana, en dosis de 20 U/kg, apenas interfiere en la producción de anticuerpos inducidos por la vacuna de células diploides humanas. Un incremento en la dosis de inmunoglobulina o su asociación con otras pautas vacunales pueden provocar fenómenos de interferencias.
Inmunización activa
La OMS desaconseja las vacunas de tejido nervioso y no da la recomendación sobre la pauta vacunal que se debe seguir.
El régimen de vacunación postexposición más usado en los países desarrollados incluye la administración por vía intramuscular de 5 dosis de 1 ml de vacuna de células diploides humanas o de vacuna purificada de embrión de pato. La primera dosis puede administrarse después de la exposición; las restantes en los días 3, 7, 14, y 30 posteriores a la primera dosis. Para evitar interferencias, la vacuna no será inoculada con la misma jeringuilla o en la misma localización que la inmunoglobulina. Los lactantes y niños pequeños deben recibir la misma cantidad y dosis vacunales que los adultos. Durante el embarazo la vacuna no está contraindicada. Por su elevada eficacia no se recomienda la comprobación de marcadores posvacunales, excepto en inmunocomprometidos.
Asimismo, si el paciente ha recibido profilaxis preexposición y/o existe constancia de una adecuada respuesta de anticuerpos, el tratamiento postexposición consistirá en la inoculación de dos dosis de refuerzo los días 0 y 3.
Para terminar, decir que la combinación del tratamiento local de la herida, junto con la inmunización pasiva y activa, asegura una protección adecuada contra la rabia.
Conclusiones
Estas enfermedades mantienen una prevalencia considerable y ocupa el décimo lugar entre las enfermedades infecciosas mortales.
La labor del farmaceútico es importante en la prevención y el adecuado tratamiento de las heridas que puedan comportar una infección por Lyssavirus. Su consejo y conocimiento farmacológico harán que en cada momento pueda decidir sobre la prioridad o no de administrar inmunoglobulinas, sueros o vacunas, así como las más adecuadas.
Bibliografía general
Anderson LJ, Winkler WG. Aqueous quaternary ammonium compounds and rabies treatment. J infect Dis 1979;139:494-5.
Bernard KW, Fishbein DB, Miller KD, Parker RA, et al. Preexposure rabies immunization with human diploid cell rabies vaccine: decreased antibody responses in persons immunized in developing countries. Am J Trop Med Hyg 1985;34:633-47.
CDC. Rabies prevention-United States, 1991. Recommendations of the Immunizations Practices Advisory Committee MMWR 1991;40(RR-3):1-19.
Comité de expertos de la OMS sobre la rabia. Serie de informes técnicos 824. Ginebra: OMS, 1992;1-88.
Dean DJ. Pathogenesis and prophylasis of rabies in man. N Y State J Med 1963;63:3507-13.
Helmick CG, Johnstone C, Summer J, Winkler WG, Fager S. A clinical study of Merieux human rabies immune globulin. J Biol Stand 1982;10: 357-67.
Hemachudha T. Rabies. En: Vinken PJ, Bruyn GW, Klawans HL, editors. Handbook of clinical neurology. Amsterdam: Elsevier, 1989;383-404.
Karliner JS, Belaval G. Incidence of adverse reactions following administration of antirabies serum: a study of 562 cases. JAMA 1965;193:359.
Medicina preventiva de la rabia. Medicina Militar 1996;4:183.
National Advisory Committee on Immunization. Canadian Inmunization Guide. 4.ª ed. National Health and Welfare of Canada, 1993.
Nicholson KG. Rabies. Lancet 1990;335: 1201-5.
Pumarola A, Rodríguez-Torres A, García-Rodríguez JA, Piédrola-Angulo G. Microbiología y parasitología médica. Madrid: Salvat, 1990;697-702.
Vdopija I, Sureau P, Smerdel S, Lafon M, et al. Comparative study of two human diploid rabies vaccines administered with antirabies globulin. Vaccine 1988;6:489-90.
Verger G. Enfermedades infecciosas. Barcelona: Doyma, 1988.
www.lafacu.com/apuntes/medicina/salud_la_rabia/default.htm