En la sexualidad humana, la capacidad para controlar el tiempo de eyaculación es una característica primordial de la salud sexual de la pareja. Por ello, las alteraciones en el control de la eyaculación pueden tener un impacto psicológico negativo en el individuo afectado. La aparición de una novedad farmacológica en este terreno, la dapoxetina, propicia la presente revisión.
La incapacidad de ejercer un control voluntario sobre el reflejo eyaculatorio es una de las disfunciones sexuales más comunes entre los varones adultos, pero puede ser tratada. Hasta ahora no se disponía de un fármaco indicado para el tratamiento de la eyaculación precoz, por lo que varios enfoques farmacológicos se han venido utilizando fuera de la indicación (off label), pero recientemente la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) y la Agencia Europea del Medicamento (EMA) han aprobado la comercialización de dapoxetina, un inhibidor selectivo de la recaptación de serotonina (ISRS) de acción corta, para tratar esta alteración. Dapoxetina es un medicamento bien tolerado, con una baja incidencia de reacciones adversas graves, y no se asocia con eventos adversos relacionados con los ISRS en el estado de ánimo o de ansiedad o con síndrome de discontinuación de ISRS.
EYACULACIÓN: CONTROL DEL SISTEMA NERVIOSO CENTRAL
El proceso de la eyaculación humana consta de dos fases principales: la emisión y la expulsión del semen. La vía de la eyaculación se origina en un centro reflejo medular mediado por el tronco encefálico, en el que inicialmente influyen algunos núcleos del encéfalo (núcleo preóptico medial y núcleo paraventricular). Las vesículas seminales producen alrededor del 40-80% del volumen total de la eyaculación, la contribución de la próstata es de aproximadamente un 10-30%, y el bulbo uretral y las glándulas uretrales secretan una pequeña cantidad de moco que se corresponde con un 2-5% del volumen total del eyaculado.
Durante la fase de emisión, las secreciones de las glándulas periuretrales, de las vesículas seminales y de la próstata, junto con el esperma de los vasos deferentes, se depositan en la uretra posterior y drenan en la uretra anterior, mientras que el cuello de la vejiga permanece cerrado. La emisión, así como el cierre del cuello de la vejiga, son principalmente reflejos simpáticos toracolumbares, con una intensa modulación supraespinal. La fase de emisión está precedida por la fase de erección, también como resultado de la inervación simpática del pene. Durante la fase de expulsión, el músculo bulbocavernoso, que forma parte integrante del esfínter anal externo, desempeña un papel primordial, junto con otros músculos, como el isquiocavernoso y los perineales transversales. Todos ellos están inervados por el nervio pudendo, es decir, por las motoneuronas del núcleo de Onuf (motoneuronas que ocupan una posición intermedia entre las motoneuronas somáticas y las motoneuronas autónomas), y su contracción de forma coordinada provoca la expulsión del semen.
Las motoneuronas involucradas en la eyaculación son las motoneuronas preganglionares simpáticas en la parte superior de la médula espinal lumbar y las mencionadas motoneuronas del núcleo de Onuf, ubicado en la médula sacra superior. El primer grupo está involucrado en la fase de emisión y el segundo en la fase de expulsión. Ambos grupos reciben aferencias de las interneuronas premotoras (células intermediomediales) que se encuentran casi al mismo nivel que las propias motoneuronas. Estos grupos de células premotoras representan los generadores del patrón central espinal de la eyaculación.
El área tegmental ventral y el cerebelo parecen activarse durante la eyaculación, mientras que la región de la amígdala se desactiva, no sólo durante la eyaculación sino también durante el estímulo y la erección. La actividad de la amígdala es crucial para la supervivencia del individuo que constantemente supervisa los estímulos ambientales para proteger al organismo del daño. Sin embargo, en el contexto del comportamiento sexual, tal vigilancia podría bloquear fácilmente el acto sexual, conduciendo a una reproducción fracasada. Es posible que, para prevenir tal interrupción, las estructuras del cerebro implicadas en el comportamiento sexual disminuyan la vigilancia inhibiendo la actividad de la amígdala. Al parecer, es necesaria la ausencia general de la reacción del miedo para que este proceso se produzca con éxito.
A PESAR DE LA ELEVADA PREVALENCIA DE LA EP, SE DISPONE DE ESCASAS INVESTIGACIONES SOBRE SU ETIOLOGÍA, A LA QUE PUEDEN CONTRIBUIR TANTO FACTORES BIOLÓGICOS COMO PSICOLÓGICOS
EYACULACIÓN PRECOZ
La eyaculación precoz (EP) es la disfunción sexual masculina más común y afecta a varones de todas las edades. Ejerce efectos significativos sobre la calidad de vida tanto del individuo afectado como de su pareja y, por tanto, constituye un problema sexual importante. Su prevalencia se estima en torno al 5-20%. La EP puede ser primaria, es decir, presente desde el comienzo de la actividad sexual, o secundaria, debido a razones desconocidas u otras condiciones orgánicas como prostatitis crónica, disfunción eréctil, diabetes mellitus o hipertiroidismo.
A pesar de la elevada prevalencia de la EP, se dispone de escasas investigaciones sobre su etiología, a la que pueden contribuir tanto factores biológicos como psicológicos. Entre los factores biológicos cabe destacar: hipersensibilidad del pene, reflejo eyaculatorio hiperexcitable, incremento en la excitación sexual, posible endocrinopatía, predisposición genética y disfunción de los receptores de serotonina (5-hidroxitriptamina, 5-HT). La EP se ha asociado a diversos factores psicológicos como ansiedad, fobia social, problemas de pareja, relaciones sexuales infrecuentes y falta de experiencia sexual.
El diagnóstico de la EP se ha visto dificultado por la falta de una definición estándar que, además, abarque el amplio rango de prevalencia estimada. La definición que se ha utilizado frecuentemente es la del Manual Estadístico y Diagnóstico de los Trastornos Mentales (Diagnostic and Statistical Manual of Mental Disorders Fourth Edition, text revision [DSM-IV-TR]): «eyaculación persistente y recurrente con estimulación sexual mínima antes, en, o poco después de la penetración, antes de que la persona lo desee». Dada la ausencia de datos clínicos, esta definición se basó en la opinión de expertos. Los ensayos clínicos más recientes han utilizado la definición basada en la evidencia de EP primaria propuesta en 2008 por la Sociedad Internacional de Medicina Sexual (ISSM) en respuesta a la variabilidad de definiciones y a la necesidad de una definición estándar universal: «disfunción sexual masculina caracterizada por la eyaculación que siempre o casi siempre tiene lugar antes o en el período de un minuto tras la penetración vaginal, y por la incapacidad para retrasar la eyaculación en todas o casi todas las penetraciones vaginales, y las consecuencias personales negativas como estrés, molestia, frustración, y el impedimento de la intimidad sexual». En síntesis, la PE implica tres características específicas: tiempo de latencia eyaculatoria intravaginal breve, falta de control e insatisfacción sexual.
En la práctica, el tiempo de latencia eyaculatoria intravaginal (TLEI) es un parámetro estándar que se utiliza para la cuantificación de la respuesta a un tratamiento determinado, así como para la comparación de tratamientos en ensayos clínicos. El TLEI se define como el tiempo que transcurre desde la intromisión vaginal hasta la eyaculación intravaginal.
Las terapias cognitiva y comportamental no se han asociado con mejoras a largo plazo de los pacientes con eyaculación precoz. A continuación se describen los agentes farmacológicos que se utilizan off label, así como la dapoxetina, hasta la fecha, único fármaco autorizado para tal indicación.
PAROXETINA, SERTRALINA Y FLUOXETINA HAN SIDO EVALUADAS EN PACIENTES CON EP, Y SE HA ENCONTRADO QUE LA PAROXETINA PRESENTA UNA EFICACIA MUCHO MAYOR, SEGUIDA DE SERTRALINA Y FLUOXETINA
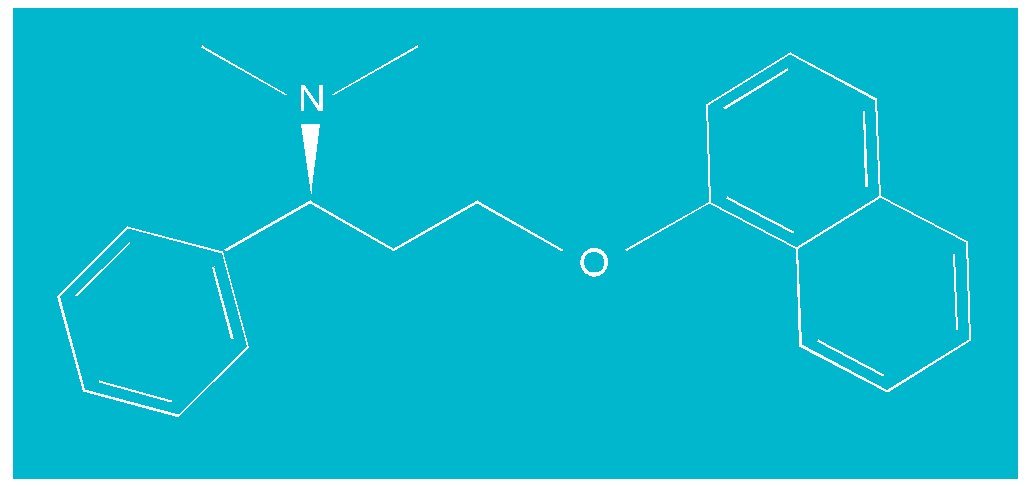
Fig. 1. Estructura química de dapoxetina.
AGENTES FARMACOLÓGICOS
ANESTÉSICOS LOCALES DE ADMINISTRACIÓN TÓPICA
La hipersensibilidad del pene en varones con EP puede proporcionar una justificación del uso de agentes desensibilizantes, como los anestésicos locales. Los agentes de administración tópica resultan atractivos ya que pueden ser utilizados según las necesidades, y los efectos secundarios sistémicos tienden a ser mínimos. Aunque causan con frecuencia efectos adversos locales, se ha descrito que son muy eficaces. Sin embargo, se dispone de pocos estudios que avalen su eficacia y seguridad.
La crema de lidocaína-prilocaína es una emulsión que en fase oleosa contiene una mezcla eutéctica de dos anestésicos locales, lidocaína (2,5%) y prilocaína (2,5%), que proporcionan analgesia dérmica. La anestesia de la piel se produce por medio de la liberación de lidocaína y prilocaína a las capas epidérmica y dérmica, produciéndose acumulación de estos anestésicos locales en la vecindad de los receptores del dolor y terminaciones nerviosas cercanas. Lidocaína y prilocaína estabilizan las membranas neuronales inhibiendo el flujo iónico que se requiere para la iniciación y conducción de impulsos. La calidad de la anestesia depende del tiempo de aplicación y de la dosis. Los ensayos con esta crema en varones con EP son escasos. En un estudio de 42 individuos de los cuales sólo 29 completaron la investigación, el TLEI aumentó de 1,49 a 8,45 min después de dos meses de uso. Sin embargo, en este estudio se ha descrito hipoestesia genital en ambos sexos.
El aerosol de lidocaína-prilocaína es una formulación de lidocaína y prilocaína que libera en cada dosis 7,5 mg de lidocaína y 2,5 mg de prilocaína. Se aplica cinco minutos antes del coito. Es de acción rápida y ha mostrado eficacia en estudios pequeños. No atraviesa el epitelio queratinizado por lo que sólo anestesia el glande, sin embargo causa cierta hipoestesia asociada al uso. En un ensayo de fase II de 56 pacientes, el TLEI alcanzado con el aerosol fue 2,4 veces superior al placebo. En un estudio multicéntrico de fase III de 300 pacientes, el aerosol incrementó el TLEI de 0,6 a 3,8 min y fue bien tolerado por los pacientes y sus respectivas parejas, además de ser calificado como bueno o excelente en un 66% de los pacientes tratados. Aunque la hipoestesia no ha sido un problema detectado en la mujer, ha habido un pequeño número de ellas que han experimentado sensación de ardor durante el coito.
La diclonina es un anestésico local, de uso en odontología, que se combina con el vasodilatador alprostadilo para tratar la EP. El producto se aplica en la región del meato del pene. En un estudio piloto se han obtenido resultados positivos con esta combinación, sin embargo, los datos son limitados y no se pueden emprender nuevos estudios antes de sacar conclusiones sobre esta combinación.
TERAPIAS SISTÉMICAS
Tramadol
Es un analgésico opiáceo de acción central. Su mecanismo de acción en la EP no está del todo esclarecido, sin embargo parece estar relacionado con su acción sobre los receptores μ, lo que podría reducir la sensibilidad del pene, y con la inhibición de la recaptación de serotonina, que retrasaría la eyaculación. Se han realizado dos ensayos clínicos pequeños y ambos han mostrado un aumento significativo del TLEI en comparación con el placebo. Un estudio cruzado simple ciego de 60 sujetos en el que se comparaba tramadol (25 mg) con placebo mostró que el tramadol aumentó el TLEI de 1,17 a 7,37 min. Con tramadol se consiguió un mayor control de la eyaculación y de la satisfacción sexual. Un estudio controlado de más de 64 varones en el que se comparó tramadol (50 mg) con placebo mostró un aumento de la TLEI de 19 s a más de 4 min. Los resultados de estos estudios parecen alentadores.
LA RELEVANCIA CLÍNICA DE LOS EFECTOS DEL TRATAMIENTO CON DAPOXETINA NO SE LIMITA AL AUMENTO DEL TIEMPO DE LATENCIA EYACULATORIA INTRAVAGINAL (TLEI) SINO QUE INCLUYE ADEMÁS LAS MEJORA DE LA SATISFACCIÓN CON LA EXPERIENCIA SEXUAL
Clomipramina
La clomipramina es un antidepresivo tricíclico que inhibe la recaptación de noradrenalina y serotonina. Los estudios han utilizado tanto dosis múltiples como dosis única, y muestran un aumento significativo mayor en el TLEI en el primer caso. La administración de clomipramina de 4 a 6 h antes del coito es eficaz y bien tolerada, sin embargo, se asocia con un menor retraso en la eyaculación a diferencia del tratamiento diario. En un metanálisis de evaluación de tratamientos sistémicos de la EP, entre los que se encuentran la clomipramina, en particular en administración continua, los resultados de ésta fueron comparables a los inhibidores selectivos de la recaptación de serotonina (ISRS) en sus efectos. Sin embargo los pacientes experimentaron una alta incidencia de reacciones adversas.
Inhibidores selectivos de la recaptación de serotonina
Los antidepresivos que son ISRS se han utilizado para retrasar la eyaculación, y de hecho pueden prolongar el TLEI durante varios minutos. En el tratamiento de la depresión se observaba que uno de los efectos secundarios comunes de los ISRS era la eyaculación retardada. En el tratamiento de la EP, los ISRS se suelen utilizar a dosis más bajas que para el tratamiento de la depresión. Las reacciones adversas de estos fármacos incluyen sequedad de boca, somnolencia, náuseas y disminución de la libido, así como disfunción eréctil. Actualmente se utilizan cuatro ISRS en el tratamiento de la EP: fluoxetina, paroxetina, sertralina y citalopram.
Se han identificado tres subtipos de receptores de serotonina con un papel en la eyaculación: 5-HT1A, 5-HT1B y 5-HT2C. La activación de receptores 5-HT1A provoca un efecto proeyaculatorio, sin embargo, la activación de los 5-HT1B y 5-HT2C retrasa la eyaculación. Para evitar la sobreestimulación de los receptores 5-HT postsinápticos, los transportadores de serotonina recaptan inmediatamente la serotonina de la hendidura sináptica. El bloqueo de los mecanismos de transporte de serotonina por los ISRS aumenta la concentración de serotonina en la sinapsis. Esto a su vez activa los receptores 5-HT1A y 5-HT1B, lo que resulta en la inhibición de la liberación de serotonina en la hendidura sináptica. A partir de ahí se produce una estimulación moderada de todos los receptores postsinápticos. Tras varios días o semanas de tratamiento con ISRS, los receptores presinápticos se desensibilizan y, como consecuencia, aumenta la liberación de serotonina en la sinapsis. La activación de receptores 5-HT2C retrasa la eyaculación, sin embargo, la extensión del TLEI depende de varios factores, como el tipo, la dosis y la frecuencia de administración de ISRS, así como el umbral eyaculatorio determinado genéticamente.
Paroxetina, sertralina y fluoxetina han sido evaluadas en pacientes con EP, y se ha encontrado que la paroxetina presenta una eficacia mucho mayor, seguida de sertralina y fluoxetina. El tratamiento diario con 20 a 40 mg de paroxetina aumenta el TLEI alrededor de 8,8 veces en comparación con placebo. Desafortunadamente, estos fármacos provocan otras reacciones adversas, como la disminución de la libido, anorgasmia, disfunción eréctil, además de insomnio, fatiga, estreñimiento, náuseas y pérdida del apetito. La cesación o retirada brusca de la terapia con ISRS puede estar asociada con un síndrome de discontinuación, cuyos síntomas incluyen mareos, náuseas o vómitos, fatiga, dolores de cabeza, ataxia, letargo, ansiedad, agitación e insomnio. Los síntomas comienzan tras 24 a 72 h de la interrupción y pueden prolongarse más allá de una semana. Es importante mencionar que la administración diaria de un ISRS se asocia con los mejores aumentos de TLEI en comparación con la administración de varias horas antes del acto sexual. Se ha postulado que el tratamiento de la EP según demanda con los ISRS convencionales sólo tiene éxito si éstos se combinan con un antagonista del receptor 5-HT1A o algún otro tratamiento que estimule de forma aguda la liberación de serotonina. Antagonistas del receptor 5-HT1A han demostrado retrasar la eyaculación cuando se han utilizado de forma concomitante y de forma aguda con un ISRS, sin embargo, no fueron eficaces en retrasar la eyaculación cuando se utilizaron en monoterapia. Esto es muy prometedor, sin embargo, se requieren estudios adicionales que permitan extraer conclusiones acerca de esta combinación.
Aunque los ISRS tienen un papel importante en el tratamiento de la EP, se deben utilizar con precaución y los pacientes deben ser advertidos de que existe riesgo de ideación suicida asociado al uso.
DAPOXETINA
Dapoxetina es un ISRS de acción muy rápida y corta que ejerce una potente inhibición del transportador de recaptación de serotonina, con una mínima actividad sobre la recaptación de dopamina y de noradrenalina. Actúa a nivel supraespinal inhibiendo el reflejo de expulsión eyaculatoria. Se ha demostrado en ratas que dapoxetina modula el reflejo eyaculador prolongando la latencia de la descarga refleja de la neurona motora pudenda (DRNP) y reduciendo su duración.
Las características farmacocinéticas de dapoxetina favorecen una dosificación adecuada según demanda o necesidad antes de la relación sexual, y conllevan un mejor perfil de reac ciones adversas en comparación con los ISRS estándar, por la menor exposición al fármaco en comparación con los regímenes de dosificación diaria, y por la reducción significativa en la acumulación de metabolitos.
LA EFICACIA DE DAPOXETINA EN EL TRATAMIENTO DE LA EP HA SIDO PROBADA EN 5 ENSAYOS CLÍNICOS DOBLE CIEGO Y CONTROLADOS CON PLACEBO, EN LOS QUE FUERON ALEATORIZADAS 6.081 PERSONAS DE 32 PAÍSES
ENSAYOS CLÍNICOS
La eficacia de dapoxetina en el tratamiento de la EP ha sido probada en 5 ensayos clínicos doble ciego y controlados con placebo, en los que fueron aleatorizadas 6.081 personas de 32 países. Los criterios de inclusión fueron los siguientes: varones heterosexuales (y sus parejas) de 18 años de edad en adelante con antecedentes de EP en la mayor parte de las relaciones sexuales monógamas en el período de 6 meses previo al reclutamiento. En todos los estudios fueron excluidos los pacientes que presentaban otras formas de disfunción sexual como disfunción eréctil o que usaban otras formas de farmacoterapia para el tratamiento de la EP. El período de tratamiento osciló entre 9 y 24 semanas. En 4 estudios, el criterio de valoración principal del TLEI promedio se midió con un cronómetro durante cada episodio de relaciones sexuales. Los resultados de todos los estudios aleatorizados fueron similares. En un estudio representativo con la máxima duración del tratamiento (24 semanas) fueron aleatorizados 1.162 varones, 385 a placebo, 388 a 30 mg de dapoxetina en función de las necesidades y 389 a 60 mg de dapoxetina en función de la demanda. Los aumentos del TLEI medio en la evaluación de la semana 24 fueron estadísticamente significativos (p < 0,001) en los dos grupos de dapoxetina en comparación con placebo. La magnitud de la prolongación del TPEI estuvo relacionada con el TPEI basal y fue variable entre los pacientes.
La relevancia clínica de los efectos del tratamiento con dapoxetina no se limita al aumento del tiempo de latencia eyaculatoria intravaginal sino que incluye además la mejora de la satisfacción con la experiencia sexual y una reducción de las consecuencias psicológicas, como angustia, estrés personal o dificultades interpersonales, tanto para el varón afectado como para su pareja.
Los resultados de eficacia fueron similares en cada uno de los ensayos individuales, lo que indica que dapoxetina es siempre más eficaz que el placebo, independientemente de las características demográficas, la región geográfica, o la raza.
A diferencia de otros ISRS utilizados en el tratamiento de la depresión, dapoxetina se ha asociado con bajas tasas de disfunción sexual. La mayoría de los acontecimientos adversos se producen generalmente en las primeras 4 semanas de tratamiento, a menudo con la primera dosis, lo que permite evaluar la tolerancia individual al inicio del curso del tratamiento. Los acontecimientos adversos graves fueron infrecuentes en los ensayos. El uso de ISRS en pacientes con trastornos psiquiátricos como depresión o trastorno obsesivo-compulsivo está asociado con ciertos riesgos de seguridad, como ansiedad, acatisia, cambios de humor y tendencias suicidas (en adolescentes). El tratamiento con dapoxetina no ha mostrado cambios clínicamente relevantes en el estado de ánimo, y ninguna evidencia de ansiedad o acatisia, respectivamente. Tampoco ha mostrado ninguna evidencia de tendencias suicidas. Los efectos secundarios más comunes incluyeron náuseas, mareos y dolor de cabeza.
Los efectos de la retirada tras la interrupción repentina del tratamiento se midieron con la escala de Signos y Síntomas Emergentes de Discontinuación (SSED). Los acontecimientos adversos mostraron pocos indicios de síntomas de abstinencia. Se observaron resultados parecidos en un segundo ensayo clínico doble ciego con una fase de tratamiento de 24 semanas de duración con las dosis de 30 y 60 mg en función de las necesidades, seguida por un período de evaluación de la abstinencia de una semana de duración.
La administración de dapoxetina a metabolizadores lentos para el CYP2D6 requiere de especial precaución cuando se administran, de forma concomitante, otros medicamentos que pueden inhibir el metabolismo de dapoxetina, como inhibidores potentes y moderados del CYP3A4.
En conclusión, dapoxetina es generalmente bien tolerada, con una baja incidencia de reacciones adversas graves, y no se asocia con eventos adversos relacionados con los ISRS en el estado de ánimo o de ansiedad o con síndrome de discontinuación de ISRS. En la población tan diversa estudiada en estos cinco ensayos clínicos, dapoxetina mejoró significativamente todos los aspectos de la EP.
PROPIEDADES FARMACOCINÉTICAS
La dapoxetina se absorbe rápidamente, y alcanza concentraciones plasmáticas máximas (Cmax) en 1-2 h tras la administración oral (comprimidos). La biodisponibilidad absoluta es del 42% (rango 15-76%). La unión de dapoxetina a las proteínas plasmáticas es del 99% y la del metabolito activo desmetildapoxetina (DMD), de un 98,5%. Dapoxetina tiene una distribución rápida con un volumen de distribución en el estado de equilibrio de 162 l. Tras su administración por vía intravenosa a seres humanos, las vidas medias estimadas inicial, intermedia y terminal de dapoxetina fueron de 0,10, 2,19 y 19,3 h, respectivamente. Dapoxetina se metaboliza por varios sistemas enzimáticos en hígado y riñón, principalmente CYP2D6, CYP3A4 y flavina monooxigenasa (FMO1). Tras la administración oral, dapoxetina es ampliamente metabolizada a múltiples metabolitos a través de las siguientes vías de biotransformación: N-oxidación, N-desmetilación, naftil hidroxilación, glucuronidación y sulfatación. La dapoxetina intacta y el N-óxido de dapoxetina son los principales metabolitos circulantes en plasma. Como metabolitos adicionales se incluyen desmetildapoxetina y didesmetildapoxetina, que suponen menos de un 3% del material circulante en relación con el fármaco original. Los estudios de unión in vitro indican que la DMD es equipotencial a la dapoxetina y que la didesmetildapoxetina tiene aproximadamente un 50% de la potencia de la dapoxetina. La dapoxetina se elimina principalmente por orina, sobre todo en forma de metabolitos conjugados. La eliminación es rápida ya que 24 h después de la administración, la concentración plasmática se reduce a menos del 5% de la Cmax. Se produce una mínima acumulación de dapoxetina tras la administración diaria. La vida media terminal tras la administración por vía oral es de 19 h. No se han encontrado diferencias significativas en los parámetros farmacocinéticos (Cmax, biodisponibilidad, Tmax) entre varones ancianos sanos y varones adultos jóvenes sanos. No se ha observado una correlación entre el aclaramiento de creatinina y la Cmax o la biodisponibilidad de dapoxetina en pacientes con insuficiencia renal leve, moderada y grave. La farmacocinética de dapoxetina en pacientes que necesitan diálisis renal aún no se ha evaluado. Los datos sobre pacientes con insuficiencia renal grave son limitados. La farmacocinética de dapoxetina y DMD permanece inalterada en pacientes con insuficiencia hepática leve.
A DIFERENCIA DE OTROS ISRS UTILIZADOS EN EL TRATAMIENTO DE LA DEPRESIÓN, DAPOXETINA SE HA ASOCIADO CON BAJAS TASAS DE DISFUNCIÓN SEXUAL
INHIBIDORES DE FOSFODIESTERASA 5
Muchos varones con EP también tienen disfunción eréctil (DE) concomitante. El hombre con EP puede desarrollar disfunción eréctil secundaria debido a la ansiedad con respecto a su EP, o puede eyacular con disfunción eréctil temprana durante las relaciones sexuales antes de su erección. La EP causada por la DE puede resolverse si la DE es tratada con éxito. Los fármacos para el tratamiento de la DE son inhibidores de fosfodiesterasa 5: sildenafilo, vardenafilo, tadalafilo y alprostadilo. Los estudios no han demostrado un aumento significativo del TLEI con sildenafilo, sin embargo, vardenafilo en comparación con placebo o sertralina en un estudio aleatorizado, prospectivo cruzado, en varones con EP, sí mostró un aumento significativo del TLEI. Dos estudios pequeños han mostrado que la combinación de paroxetina y sildenafilo proporcina mejoras significativas en el TLEI en comparación con paroxetina sola, sin embargo, hubo una mayor incidencia de reacciones adversas con el tratamiento combinado.
BIBLIOGRAFÍA GENERAL
Agencia Española de Medicamentos y Productos Sanitarios. Fecha de la revisión del texto: febrero 2010. Ficha técnica o resumen de las características del producto Priligy (comprimidos, 30 y 60 mg dapoxetina, respectivamente). Titular de la autorización de comercialización: Janssen-Cilag, S.A.
Cardona W. Definición actual y tratamiento de la eyaculación precoz. Arch. Esp. Urol. 2010;63(1):53-5.
Hellstrom WJ. Available and future therapies for premature ejaculation. Drugs Today. 2010;46(7):507-52.
Holstege G. Central nervous system control of ejaculation. World J. Urol. 2005;23:109-14.
Linton K, Wylie K. Recent advances in the treatment of premature ejaculation. 2010. Drug Des. Devel. Ther. 4:1-6.
McMahon C, Althof S, Kaufman J, buvat J, Levine S, Aquilina J, Tesfaye F, Rothman M, Rivas D, Porst H. Efficacy and safety of dapoxetine for the treatment of premature ejaculation: integrated analysis of results from five phase 3 trials. J. Sex Med. Doi: 10.1111/j.1743-6109. 2010.02097.x.