La infección por VIH, que en un principio supuso una enfermedad focalizada en ciertos subgrupos de población, ha llegado a tomar consideración de pandemia, provocando unas cargas inmensas, tanto sanitarias como económicas. La prevención de nuevos casos de infección supone el primer paso frente a la enfermedad. El farmacéutico puede colaborar activamente en dichos programas obteniendo unos magníficos resultados clínicos y farmacoeconómicos.
Se estima que a finales de 1999 había en todo el mundo unos 53,1 millones de personas infectadas con el virus de inmunodeficiencia humana (VIH). De éstas, 18,8 millones moriría antes de acabar el año, y los 34,4 millones restantes sobrevivirían. De todos los casos existentes, casi el 90% se producían en países en desarrollo1. Un año antes, a principios de 1998, se estimaba en 42 millones el número de personas que estaban infectadas por el VIH, de los cuales 11,7 millones de ellos habrían muerto debido a patologías asociadas con el sida. Los 30,6 millones restantes, de los cuales 29,5 millones eran adultos y 1,1 millones, niños, permanecían vivos2.
Se ve claramente que el número de nuevas personas infectadas sigue creciendo, si bien en los países ricos se ha alcanzado una estabilidad del crecimiento debido al establecimiento de las terapias antirretrovirales de combinación, lo que ha producido igualmente que la tasa de mortalidad descienda, especialmente en estos países. Se había estimado que en el año 2000 habría unos 60 millones de personas infectadas, de las cuales el 92% corresponderían a países subdesarrollados.
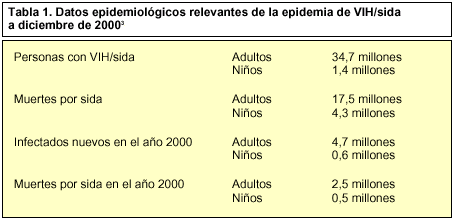
Observando a las personas que vivían infectadas por VIH, se constata que el 90% lo hace en países subdesarrollados, siendo el África subsahariana la región más afectada, con el 66% del total de infecciones. América en su conjunto ocupa el tercer puesto, con las tres grandes bolsas de HIV: Latinoamérica, Norteamérica y el Caribe. Europa, principalmente los países orientales, es otro gran foco de la infección. La zona occidental, al igual que en Estados Unidos, está estabilizada, si bien los países del este continúan incrementando el número de casos3 (tabla 1).
Los datos ofrecidos reflejan que nos hallamos ante una pandemia de graves consecuencias sanitarias, que continúa aumentando en los países pobres, pero que incluso en los países ricos supone una enorme carga sanitaria de inmensas repercusiones económicas.
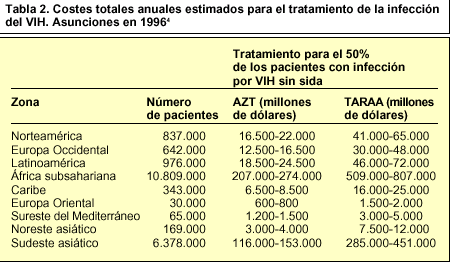
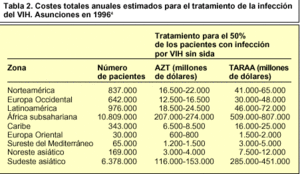
La estimación del coste total anual de la terapia del VIH/sida ofrece datos muy variables en función de cada país. Se ha hecho una estimación del coste total que representaría tratar al 50 y al 100% de los pacientes con infección por VIH, pero no con sida, en 1996 (tabla 2)4.
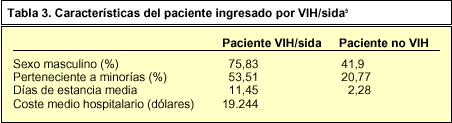
Las hospitalizaciones de los pacientes suponen un enorme montante en la cifra final de los costes. Se ha estimado que en 1994 se produjeron aproximadamente 188.506 admisiones por pacientes con VIH/sida en los hospitales de Estados Unidos, lo que originó un coste hospitalario cifrado en 36.300 millones de dólares5. Comparado con los pacientes no infectados con VIH, los pacientes con VIH/sida tienen unas características diferentes (tabla 3).
Prevención de nuevos casos
Como hemos indicado, los costes de la enfermedad son tan elevados que el primer frente de lucha se halla en la prevención de nuevos casos de la epidemia. Como se observará, mediante esta prevención se consiguen unos muy favorables ratios coste/efectividad, expresados normalmente como cantidad de recursos económicos por cada año de vida ajustado a calidad (AVAC) que se evita.
La prevención se centrará inicialmente en los mecanismos de transmisión de la enfermedad. A nivel mundial, estas formas de transmisión de esta enfermedad infecciosa son:
Contacto sexual, hetero y homosexual.
Compartir agujas y jeringas en drogadictos.
Perinatal, de madre a hijo.
Transfusiones de sangre.
Accidentes con material infectado.
El grado en que esta infección se propaga a través de la población general depende de su tasa reproductiva, es decir, la cantidad de personas susceptibles de ser infectadas por alguien que padece ya la enfermedad, así como del tiempo en que esa persona permanece infectada y del número de nuevas parejas que tenga. Factores de tipo biológico, de comportamiento y económicos influyen en estas variables.
La evaluación farmacoeconómica de la prevención del VIH/sida ofrecerá mejores o peores parámetros de coste/efectividad en función de si el programa realizado evita o no costes asociados. Los tratamientos actuales son más efectivos pero también más costosos, lo que puede hacer que las intervenciones preventivas presenten unas u otras medidas de eficiencia6.
Si bien las medidas profilácticas no producen siempre ahorros en los costes, al menos deberían poseer unos ratios farmacoeconómicos favorables7. Debido a lo expuesto, el objetivo primordial sería la prevención de la enfermedad, con el fin de minimizar el número de nuevas infecciones y producir un ahorro en los costes.
Para obtener unas mejores medidas de coste/efectividad, el primer paso sería focalizar las intervenciones que se realicen sobre los individuos que tengan una mayor probabilidad de transmitir la infección. Ello implica la identificación previa de las poblaciones de alto riesgo, para recoger posteriormente información sobre la prevalencia y sus características de comportamiento. Por ello, aquellas personas con muchos compañeros sexuales o que comparten agujas y/o jeringas para inyectarse drogas de abuso, serían el primer grupo sobre el que actuar.
Transmisión a través de sexo y drogas
Los programas de intervención más favorables farmacoeconómicamente estarían encaminados hacia la disminución del riesgo asumido por estos grupos: la promoción del uso del preservativo, el intercambio de jeringas estériles, o la educación sanitaria. Se han realizado, en este sentido, acciones dirigidas hacia la disminución del riesgo, como los programas dirigidos a prostitutas, en los que se realizaba una promoción del uso habitual del profiláctico, explicando las ventajas de su uso y el enorme peligro que originaba su no utilización. La evaluación farmacoeconómica realizada en programas en los que se informaba durante 5 sesiones a dicho grupo de población obtuvo un ratio de 2.000 dólares por cada AVAC ganado8.
Respecto a las acciones dirigidas hacia los usuarios de drogas intravenosas (UDI), se ha evaluado el impacto económico que supondría su acceso a jeringas y agujas estériles. Se estimó que dicho programa costaría 423 millones de dólares anuales en la población de UDI en Estados Unidos, pero presentaría un coste/efectividad de 34.278 dólares por infección de VIH evitada9.
En Edmonton (Canadá) se ha realizado un programa centrado en la facilitación e intercambio de jeringas nuevas que evite su uso compartido10. El estudio estaba dirigido a un grupo de personas en los que el VIH puede ser ampliamente transmitido. Analizan el comportamiento y los resultados obtenidos en dos grupos de población homogéneos, en los que se implementa el programa en uno de ellos, dejando al otro la estrategia de no hacer nada. Las características principales del estudio se indican en la tabla 4.
El coste anual de dicho programa de intercambio de jeringas alcanzó unos 195.000 dólares, y en el primer año hubo 10,1 infecciones con el programa y 30,4 sin él, por lo que la efectividad estimada fue de 20,3 casos evitados. Con estos resultados, el coste/efectividad incremental estimado se calculó en 9.500 dólares por cada caso evitado de infección por VIH. Extendiendo este ahorro de costes al tiempo medio de supervivencia de este tipo de pacientes, el programa tendría un coste actualizado de 116.000 dólares, el cual es inferior al inicialmente estimado de 150.000 por cada tratamiento. Además, el programa realizado produjo un beneficio neto positivo en forma de un menor número de casos de sida, por lo que dicha estrategia es dominante.
Otro programa de prevención de la transmisión del VIH se ha dirigido hacia la facilitación de un tratamiento de mantenimiento de metadona en usuarios de drogas intravenosas. El análisis económico de dicho programa reflejó que se obtenía desde 8.200 dólares/AVAC ganado para una prevalencia de infección por VIH del 40% en esta población de adictos, hasta 10.900 dólares/AVAC para una prevalencia del 5%11.
Transmisión perinatal
Por otro lado, se desarrollan programas dirigidos a la prevención de la transmisión vertical de la enfermedad, de madre a hijo, la cual, en países ricos, alcanza la cifra del 6%. Esta profilaxis se ha realizado administrando a la madre AZT durante el embarazo y el parto, y al niño, durante 6 semanas, consiguiéndose una reducción de la transmisión del 67%. No obstante, en países sin desarrollar este tratamiento preventivo es caro, por lo que se ha ensayado un tratamiento en una dosis única, a madre y a hijo, de nevirapina, siendo esta alternativa la que presenta mejor ratio coste/efectividad12 frente a otras ensayadas, como ciclos cortos de ZDV.
Obviamente, el tratamiento preventivo estará dirigido a aquellas madres que sean VIH positivas, para lo cual se hace preciso la detección previa de la infección, lo cual incrementa los costes. Se ha analizado el coste/efectividad del screening rutinario posnatal para VIH en mujeres embarazadas y sus recién nacidos en Estados Unidos. De esta forma, aumentando el control anual en 1,1 millones de mujeres, se identificarían 527 madres VIH positivas adicionalmente, lo que evitaría 150 infecciones en recién nacidos, obteniéndose un ratio de 8.900 dólares por año de vida ganado. El screening rutinario en recién nacidos alcanzaría hasta los 3,9 millones de niños anualmente, identificándose 1.061 madres infectadas, y evitándose 266 infecciones en los niños, con un coste/efectividad de 7.000 dólares por año de vida ganado13.
Para prevenir la transmisión de la enfermedad de madre a hijo se ha analizado igualmente la posibilidad de realizar los partos por cesárea, desde la perspectiva de costes y resultados, comparándolo con el parto vaginal, resultando que la cesárea, en mujeres con tratamiento profiláctico de zidovudina presentó un coste/efectividad de 1.131 dólares por caso evitado; si recibían terapia de combinación antirretroviral, el ratio ascendía a 112.693 dólares por caso evitado. Si no habían recibido tratamiento alguno durante el embarazo, la cesárea producía ahorro de costes14 (ratio coste/beneficio de 2,23).
Accidentes con material infectado
Con el aumento del número de pacientes infectados, la probabilidad de contraer la infección a través de accidentes fortuitos con material infectado aumenta.
Los programas de prevención de la infección mediante este tipo de transmisión pasan por la administración profiláctica de AZT durante 4 semanas después del accidente, estimándose un coste de 420 dólares, a lo que hay que sumar un test de VIH para el diagnóstico del contagio y otro para observar el resultado de la infección. Se ha realizado un análisis coste/efectividad de este tipo de profilaxis, comparando la administración sistemática de AZT y proseguir o no el tratamiento en función del resultado del primer test (realizado a las 72 horas), frente al tratamiento exclusivamente de los que dieran positivo en el test. El resultado indica que el coste por cada 100 trabajadores sanitarios sería de 47.910 y 38.849 dólares canadienses respectivamente, lo que implica un coste/efectividad incremental de 300.140 dólares canadienses por cada caso prevenido15.
Se ha recomendado también el tratamiento profiláctico con una terapia de triple combinación, mediante la administración de AZT, lamivudina e indinavir durante 4 semanas, con un coste estimado de 792 dólares. La evaluación farmacoeconómica de las dos posibilidades profilácticas citadas estimó que la profilaxis con AZT prevenía 53 casos de infecciones por cada 100.000 exposiciones, con un coste para la sociedad de 2,0 millones de dólares por cada infección prevenida, y un valor de 175.222 dólares por cada año de vida ajustado a calidad (AVAC); la prevención con terapia triple prevendría 66 seroconversiones por cada 100.000 exposiciones, con un coste para la sociedad de 2,2 millones de dólares por caso evitado, y 190.392 dólares por AVAC16.
A la vista de los datos expuestos, el tratamiento dirigido a personas en las que se ha determinado que son HIV positivos y/o al tratamiento de las exposiciones severas serían unas alternativas con mucho mejor ratio coste/efectividad.
Actuación farmacéutica
El farmacéutico colabora activamente en diferentes programas de prevención mencionados. Las dos participaciones más importantes, tanto clínica como económicamente, se realizan a través de la promoción del uso del preservativo, no sólo facilitando su uso (reducción del precio, dispensación de envases de capacidad reducida, disposición de máquinas automáticas, etc.), sino a través de la cotidiana y permanente labor de educación sanitaria acerca de su correcto uso, así como de las ventajas de su utilización.
El otro gran papel lo realiza el farmacéutico mediante la actuación sobre los UDI, especialmente en el plan de dispensación de metadona, en el que los ahorros económicos que se consiguen por la disminución del número de nuevos casos de infección por VIH son muy grandes. Las actuaciones en las que se facilitan jeringas y agujas estériles para evitar que se compartan y se transmita el virus obtienen unos inmejorables parámetros coste/efectividad.
La evaluación farmacoeconómica de los programas de prevención de la infección por VIH realizados en España por las oficinas de farmacia pondría de relevancia el inmenso ahorro en costes que la sociedad y el sistema proveedor de servicios de salud obtienen de las actuaciones farmacéuticas. *