Los costes del tratamiento del VIH son muy elevados, pero pueden incrementarse notablemente si disminuye el objetivo terapéutico deseado. Esta reducción se manifiesta, en parte, debido a la adquisición de resistencias a los fármacos, lo que provoca el cambio hacia tratamientos más complejos, encareciendo aún más la terapéutica antirretroviral.
Una estrategia adecuada que podría mejorar el resultado clínico sería el análisis del virus mediante la determinación de la secuencia genotípica, para determinar las cepas resistentes a los fármacos, lo que podría guiar la elección de la terapia, disminuyendo así la tasa de resistencias. El inconveniente es el elevado precio del test (400-500 dólares), por lo que se realizó una evaluación farmacoeconómica para determinar el coste/efectividad de la acción mencionada a partir de los resultados de un ensayo clínico. Al cabo de un año de seguimiento, en el grupo de cuidado estándar, los costes totales por paciente y año ascendieron a 20.412 dólares, mientras que en el grupo en el que el tratamiento se guió mediante el análisis de genotipos fueron de 18.484 dólares. Del total de costes, el 55% correspondió a medicamentos, pero a pesar del incremento en costes la aplicación del análisis ahorró costes finales en base a una disminución del uso de inhibidores de la proteasa1.
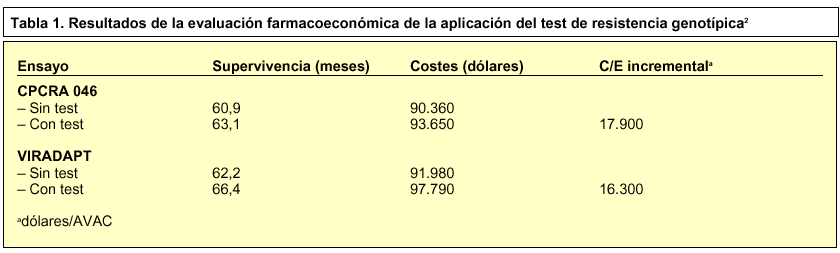
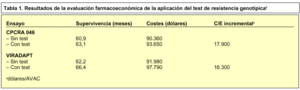
Se ha evaluado esta alternativa a más largo plazo2 mediante un modelo de simulación con los datos de los ensayos clínicos realizados. Cuando se realizaba el test después de producirse el fracaso terapéutico de la administración de la TARAA, se obtuvieron los datos que se muestran en la tabla 1, en los que se evidencian buenos parámetros farmacoeconómicos mediante la implementación del análisis genotípico, de lo que se puede deducir que, una vez que se ha producido el fracaso terapéutico por resistencia secundaria, es adecuada la utilización rutinaria del test. Para obtener un buen ratio coste/efectividad en su utilización en resistencia primaria, su prevalencia debería ser al menos del 4-5%2.
La aplicación de la terapia de observación directa colabora en la obtención de mejores resultados mediante el aumento de la adherencia
Adherencia al tratamiento
El cumplimiento terapéutico del paciente en patologías crónicas alcanza habitualmente una tasa pobre en el tiempo, aproximadamente del 50%. En el tratamiento del VIH se precisa de una alta tasa de adherencia, que se calcula en el 95% o más, para obtener buenos resultados3. Se ha estudiado el grado de cumplimiento al tratamiento del VIH, preguntando a los pacientes sobre su autoadministración en la semana anterior al cuestionario, observándose unas adherencias deficientes4: el 28% de los pacientes tomó menos del 80% del tratamiento diario, el 23% tomó entre el 80 y el 99%, y sólo el 50% de los pacientes evaluados consiguió el cumplimiento total. Finalmente, la adherencia al tratamiento se correlacionó directamente con la reducción plasmática de las concentraciones de ARN del VIH.
Terapia de observación directa
La terapia TARAA es efectiva y farmacoeconómicamente muy favorable, pero exige un cumplimiento muy fuerte. Las posologías actuales, menos frecuentes por las más largas vidas medias de los nuevos fármacos, así como el uso de menores dosis de ritonavir y otros inhibidores de la proteasa, han hecho pensar, en analogía con el tratamiento de la tuberculosis pulmonar (TP), que se podría realizar igualmente terapias de observación directa (TOD), es decir, que cada dosis prescrita sea directamente supervisada en su administración. En contraste con la TP, la infección por VIH es actualmente incurable, con lo que la observación de la administración, una o dos veces al día y durante un tiempo indefinido, no es fácilmente realizable, obteniéndose entonces un método de TOD modificado (TODM).
El fin del programa TOD en el VIH, de prevenir la aparición de cepas resistentes, es menos consistente que en la TP. Los pacientes que tienen un elevado cumplimiento terapéutico alcanzan una supresión total de la carga viral, lo que obvia el desarrollo de resistencias. Por su parte, aquellos que presentan una pobre adherencia puede que no desarrollen tampoco resistencias, puesto que no ha habido una exposición selectiva suficiente. Por este modo, los pacientes que presentan una adherencia media son los más propensos a desarrollarlas. Esto haría que un programa TOD que no pudiera cubrir nada más que una fracción del tratamiento podría promover la aparición de resistencias, cambiando radicalmente el signo de los parámetros farmacoeconómicos obtenidos por el TOD5.
A pesar de ello, se ha constatado una correlación entre la progresión de la enfermedad clínica y la adherencia al tratamiento. En un estudio de 13 meses de seguimiento, los pacientes que tuvieron más del 90% de adherencia no presentaron nuevos diagnósticos de sida; los que cumplieron el 50-89% tuvieron un 8% de riesgo, y aquellos con una adherencia menor del 50% presentaron un riesgo de diagnóstico de sida del 38%6.
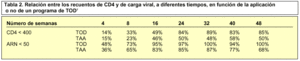
Vemos entonces que la aplicación de la terapia de observación directa colabora en la obtención de mejores resultados mediante el aumento de la adherencia. En distintos estudios se ha evidenciado una disminución más eficaz de los recuentos de CD4 (hasta valores menores de 400 cel/ml) y de la carga inicial viral (hasta cifras de 50 células/ml o menores) cuando se compara con la autoadministración del tratamiento7,8 (tabla 2).
Una iniciativa innovadora es la realizada en el Tacoma Departament of Health, donde han realizado un programa TOD mediante la instalación de un videoteléfono que posee una cámara de televisión en el lugar donde acuden los participantes. Los datos de adherencia conseguidos en los pacientes adscritos alcanzan el 95%. De esta forma, una enfermera puede observar directamente, a través de una pantalla de televisión, la administración de cada dosis, obteniéndose el objetivo del programa, pero con un ahorro en costes de 268 horas de tiempo de personal de enfermería, así como 8.830 millas de desplazamientos con respecto a la implementación de un programa TOD domiciliario5.
Infecciones oportunistas
El coste del paciente ingresado durante largo tiempo por infecciones oportunistas es muy elevado, especialmente cuando se trata de retinitis por citomegalovirus (CMV) o toxoplasmosis. La primera de ellas se había evidenciado como la complicación más costosa, con un coste mensual medio de 7.825 dólares en los 6 meses transcurridos tras su diagnóstico9.
Existen diversas opciones para la profilaxis de las infecciones oportunistas asociadas con el sida. Sin embargo, debido a las diferencias en su prevalencia, así como a la eficacia de los fármacos empleados y por los costes que se originan, el efecto actual de la profilaxis es incierto10,11,12.
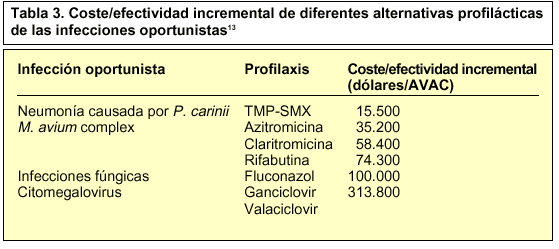
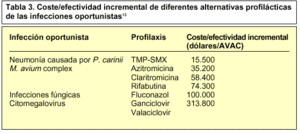
Se ha desarrollado un modelo de Markov13 para evaluar farmacoeconómicamente las diferentes estrategias de la profilaxis frente a la neumonía causada por Pneumocystis carinii (NPC), toxoplasmosis (TXP), infección causada por Mycobacterium avium complex (MAC), infecciones fúngicas y citomegalovirus (CMV). Para pacientes con recuentos de CD4+ de 200-300 células/ml, que no recibieron profilaxis, se proyectó una esperanza de vida ajustada a calidad de 39,08 meses y un coste total de 40.288 dólares. La profilaxis para la NPC y TXP con trimetroprim-sulfametoxazol en pacientes con recuentos de CD4+ de 200 células/ml o menores, el incremento de esperanza de vida fue de 42,56 meses. La profilaxis para la infección por MAC, en pacientes con 50 células CD4+/ml o menos, produjo menores incrementos en la esperanza de vida. La prevención de la infección por CMV ofreció, sin embargo, unos parámetros farmacoeconómicos muy desfavorables (tabla 3).
Los resultados que ofrecen estos estudios se muestran muy sensibles al riesgo de prevalencia de las infecciones oportunistas. La aparición de la TARAA ha reducido su prevalencia, por lo que se ha planteado el cese en la implantación rutinaria de este tipo de profilaxis, permaneciendo exclusivamente en pacientes en los que haya fallado la respuesta antiviral. Así, se han analizado las consecuencias de la discontinuación de la profilaxis primaria y secundaria de algunas infecciones oportunistas, observándose que puede ser intentada sin riesgo para el paciente que responde favorablemente al tratamiento antiviral14.
Comorbilidades asociadas
Existen otros procesos diferentes, pero asociados a la infección por VIH, como es el caso de la demencia del sida, los cuales representan un incremento muy grande en los costes de la enfermedad. En pacientes con recuento de CD4+ mayor de 500 células/ml, el 35% de los costes totales fueron debidos a trastornos psiquiátricos9.
Muchos de los pacientes con enfermedad avanzada buscan cuidados médicos en el servicio de urgencias en vez de acudir a su centro de atención primaria para los síntomas comunes de la infección por VIH. En Estados Unidos se ha observado que los afroamericanos, los indigentes y los pacientes con problemas psicológicos son los que mayor predisposición tienen a acudir a dichos servicios de urgencias, lo que repercute aún más en los costes asociados al VIH/sida15.
Hay una importante comorbilidad asociada a la infección por VIH en adultos, como epilepsia, reflujo gastroesofágico, cáncer de próstata, depresión, diabetes, etc. Todo ello contribuye al incremento en costes, por lo que las medidas dirigidas hacia estos fines no sólo conseguiría reducir en parte el consumo de recursos, sino que aumentaría la calidad de vida de estos pacientes16,17.
Actuación farmacéutica
El farmacéutico tiene un inmenso campo ante sí con los pacientes afectados por el VIH/sida. Se ha hecho alguna iniciativa en España al respecto18, con buen resultado y satisfacción para el farmacéutico y el paciente. Se realizan de forma habitual los programas de dispensación de metadona a pacientes con VIH y otros, así como actuaciones en el intercambio de jeringas para administración intravenosa de drogas. Pero el farmacéutico podría involucrarse mucho más activamente en esta patología. La Administración sanitaria otorgó hace unos años a los servicios de farmacia de los centros hospitalarios la dispensación de antirretrovirales a pacientes ambulatorios.
Otras posibles actuaciones del farmacéutico en esta enfermedad serían:
La implementación de programas de atención farmacéutica focalizados en escenarios específicos19, en subgrupos de pacientes tales como embarazadas y niños, que pueden tener un mayor riesgo de alteración de parámetros farmacocinéticos, obteniéndose concentraciones subterapéuticas, individuos que responden bien al tratamiento pero que desean comenzar un régimen nutracéutico.
La participación en programas de prevención de la transmisión de la infección, como la promoción sanitaria del uso del profiláctico, la participación en programas de educación sanitaria, etc., que contribuiría igualmente a la obtención de mejores resultados clínicos, además de la consecución de una disminución de costes.
La implementación de programas de terapia de observación directa, una vez realizada la dispensación de forma rutinaria, lo que contribuiría muy eficazmente a rebajar la tasa de resistencias con el consiguiente descenso notable de los costes por nuevos retratamientos.
La implementación de estos y más programas20,21 de atención farmacéutica, que fueran debidamente diseñados y que tuvieran como uno de los objetivos la cuantificación de la efectividad clínica de los tratamientos del VIH/sida, así como de los costes en que se incurre, pondría de relieve el potencial descenso en los costes que el sistema proveedor de servicios de salud obtendría y el aumento en la calidad de la asistencia sanitaria del sistema. Potencial descenso en los costes que podría revelarse como superior al ahorro que en estos momentos obtiene el sistema, al evitarse el margen profesional de la oficina de farmacia con la dispensación ambulatoria en hospitales.